5.8:5.8 Desglose de ácidos grasos
- Page ID
- 52956
La lipasa sensible a hormonas en el tejido adiposo hidroliza la grasa almacenada en esas células en glicerol y ácidos grasos. El glicerol puede ingresar al ciclo glicolítico a través de la conversión a fosfato de dihidroxiacetona (una conversión de dos pasos usando glicerol quinasa y glicerol-3-fosfato deshidrogenasa). Los ácidos grasos son secretados de las células adiposas al torrente sanguíneo donde se unen a una proteína portadora, la albúmina. Este complejo puede entonces ser llevado al interior de otras células por endocitosis, donde se pueden descomponer como fuente de energía.
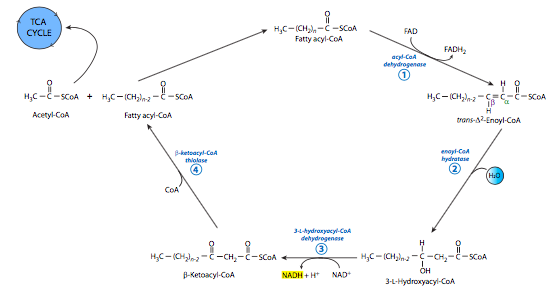
La descomposición de los ácidos grasos ocurre por β-oxidación dentro de la matriz mitocondrial (Figura\(\PageIndex{14}\)).
Dado que la membrana mitocondrial interna es impermeable a los ácidos grasos libres de cadena larga, primero deben activarse a acil-CoA grasos y unirse a carnitina, un derivado de aminoácido sintetizado a partir de metionina y lisina (ver Figura\(\PageIndex{15}\)). El primer paso lo realiza una de una familia de enzimas conocidas como acil-CoA sintetasas o tiocinasas, y requiere hidrólisis de Coenzima A y ATP. Estas reacciones ocurren ya sea en la superficie cytoplásmica de la membrana externa mitocondrial o en el retículo endoplásmico, donde se incrustan acil-CoA sintetasas. En la segunda reacción, la carnitina palmitoil- transferasa I en el exterior de la membrana mitocondrial interna une la cadena de acilo a la carnitina, liberando CoA. La acil-carnitina se transporta a la matriz mitocondrial donde la carnitina palmitoiltransferasa II libera la cadena de acilo graso de la carnitina y la vuelve a unir a una molécula de CoA.
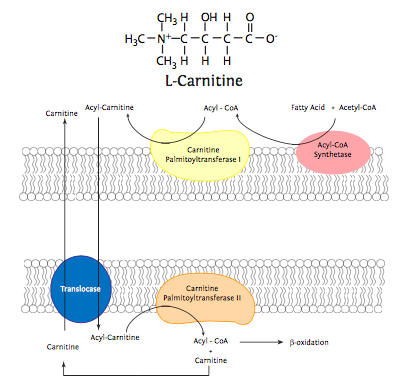
Los síndromes de deficiencia de carnitina pueden ocurrir cuando existe una mutación disfuncional de carnitina palmitoiltransferasa o una deficiencia grave de carnitina intracelular. Dado que la mayor parte de la carnitina en el cuerpo se encuentra en el músculo cardíaco y voluntario, los síntomas habituales son debilidad muscular y arritmias cardíacas, así como hipocetosis. En los neonatos, las arritmias pueden llevar a la muerte. La suplementación con carnitina es un tratamiento exitoso en la deficiencia sistémica de carnitina debido a una baja ingesta de carnitina o defectos en el transportador de carnitina incrustado en las membranas celulares. Sin embargo, si el defecto está en la palmitoiltransferasa, la suplementación no tendrá éxito.
La carnitina se vende ampliamente como un suplemento dietético para aumentar la pérdida de peso al potenciar el catabolismo de las grasas. La idea básica es obvia: la carnitina es necesaria para la descomposición de ácidos grasos de cadena larga, por lo que más carnitina = más grasa quemada. Sin embargo, eso solo es cierto si los niveles de carnitina están por debajo de los niveles de saturación para las palmitoiltransferasas. Debido a que el 75% de la carnitina en el organismo debe ser ingerida (solo se sintetiza el 25%), esta es una posibilidad leve, dependiendo de la dieta. Actualmente, la comunidad biomédica no ha llegado a un consenso sobre la eficacia de la suplementación de carnitina sobre la oxidación de ácidos grasos en personas suficientes de carnitina.
En la matriz mitocondrial, la β-oxidación ocurre en cuatro etapas para producir una cadena acil-CoA que se acorta en dos carbonos, y una acetil-CoA que luego puede ingresar al TCA. El β se refiere al segundo carbono más cercano al unido a CoA. El enlace que se romperá es el enlace entre los carbonos α y β. Por lo tanto, todos los ácidos grasos de número par, completamente saturados, pueden oxidarse completamente. La presencia de dobles enlaces en los ácidos grasos no saturados introduce complicaciones a este proceso que deben abordarse utilizando enzimas adicionales que mueven el doble enlace o lo eliminan.
La mayoría de los animales y plantas generan ácidos grasos pares; sin embargo, algunos animales marinos (por ejemplo, fundición, salmonete) y algunas plantas y bacterias también sintetizan ácidos grasos de cadena impar. Las mismas enzimas responsables de la oxidación β de ácidos grasos pares también pueden manejar ácidos grasos impares, excepto que la degradación final produce propionil-CoA en lugar de acetil-CoA.
La propionil-CoA se convierte en succinil-CoA a través de una serie de tres enzimas: propionil-CoA carboxilasa, metilmalonil-CoA racemasa y metilmalonil-CoA mutasa. El succinil-CoA teóricamente podría entrar en el ciclo de TCA, pero recuerde que el succinil-CoA simplemente se recicla y nunca se consume realmente por el ciclo de TCA. Así, para que la succinil-CoA contribuya a las necesidades energéticas de la célula, primero debe convertirse en malato (etapas 6-8 del ciclo TCA), que luego se convierte en piruvato por la enzima málica, también conocida como malato descarboxilante deshidrogenasa. El piruvato puede entonces entrar y ser consumido por el ciclo de TCA.
La vitamina B 12, o 5'-desoxiadenosilcobalamina, es un componente coenzimático de la metilmalonil-CoA mutasa, pero no es producida por plantas ni animales. Sólo lo hacen ciertas bacterias, algunas de las cuales viven en los tractos intestinales de los herbívoros. Los herbívoros absorben así el B 12 para su uso, y los carnívoros obtienen su B 12 al comer herbívoros. Los defectos en la metilmalonil-CoA mutasa o la deficiencia grave de vitamina B 12 (con mayor frecuencia en vegetarianos) pueden llevar a metimalonil aciduria/acidemia, que puede ser fatal en lactantes no tratados por acidosis. Sin embargo, dependiendo de la causa, puede tratarse con altas dosis de B 12 y/o evitando grasas dietéticas de cadena impar y proteínas ricas en isoleucina, leucina o metionina, que también catabolizan a propionil-CoA. La anemia perniciosa, en la que generalmente los pacientes de edad avanzada presentan niveles muy bajos de glóbulos rojos y hemoglobina, así como neurodegeneración, también se relaciona con B 12. Sin embargo, no suele deberse a una deficiencia vitamínica, sino a la insuficiente secreción de factor intrínseco, que se une al B 12 en el estómago y luego se introduce en las células intestinales por endocitosis mediada por receptores.
Además de la oxidación en las mitocondrias, los ácidos grasos también sufren β-oxidación en peroxisomas. Sin embargo, generalmente, la oxidación en los peroxisomas es limitada, y el propósito es acortar los ácidos grasos largos en preparación para la degradación final en las mitocondrias.
Además de los ácidos grasos monocatenarios más comunes, las células también se encontrarán con ácidos grasos ramificados, que bloquean β-oxidación es el grupo alquilo está en el carbono β. En estos casos, el ácido fitánico por ejemplo, es necesaria una oxidación para generar un intermedio con el grupo alquilo en el carbono a. A esto le sigue la β-oxidación hasta su finalización.
Por último (con respecto al catabolismo de ácidos grasos), hay que señalar que en el hígado especialmente, gran parte del acetil-CoA generado por la oxidación de los ácidos grasos no entra en el ciclo de TCA. En cambio, se convierte en acetoacetato o D-β-hidroxibutirato, que junto con la acetona, son conocidos, algo extrañamente, como cuerpos cetónicos. Estas moléculas son solubles en agua, y se transportan a través del torrente sanguíneo como fuentes de energía para una variedad de tejidos, incluso el cerebro, que normalmente solo usa glucosa como combustible ya que los ácidos grasos no pueden pasar a través de la barrera hematoencefálica. Sin embargo, los cuerpos cetónicos pueden penetrar y son utilizados por las células cerebrales en condiciones de inanición.
La cetoacidosis es una afección en la que los cuerpos cetónicos se están produciendo mucho más rápido de lo que se usan. Esto lleva a una acumulación de las moléculas en el torrente sanguíneo, lo que disminuye el pH, ya que las moléculas son ácidas. Un diagnóstico fácil de cetoacidosis es un olor dulce algo afrutado (de acetona) en la respiración. Esta afección puede ser un indicio de diabetes, pero también puede ocurrir cuando una persona está consumiendo una dieta alta en grasas/bajas en carbohidratos. Cuando el metabolismo del cuerpo no está usando glucosa/carbohidratos como fuente principal de alimento por cualquier razón, se usa grasa en su lugar, aumentando la producción de cuerpos cetónicos. Si no se trata, la cetoacidosis grave puede provocar daño celular a medida que la sangre se acidifica, y la compensación por el aumento de la exhalación de dióxido de carbono y provocar insuficiencia respiratoria en individuos susceptibles.

