11.6: Transporte vesicular
- Page ID
- 53122
Además del procesamiento de proteínas, la sala de urgencias y el Golgi también se encargan de algunos tipos de transporte de proteínas. Las vesículas (burbujas unidas a la membrana, esencialmente) se pellizcan de la sala de urgencias, Golgi y otros orgánulos membranosos, llevando consigo las moléculas solubles que estaban dentro del fluido que estaba encerrado, así como cualquier molécula incrustada en esa sección de la membrana. Estas vesículas luego capturan un paseo en un motor molecular como la cinesina o la miosina, y viajan a lo largo del citoesqueleto hasta que se acoplan en el destino apropiado y se fusionan con la membrana u orgánulo diana. En general, las vesículas se mueven de la sala de urgencias al cis de Golgi, del cis al Golgi medial, del Golgi medial al trans, y del Golgi trans a la membrana plasmática u otros compartimentos. Aunque la mayor parte del movimiento es en esta dirección, también hay vesículas que retroceden del Golgi a la sala de urgencias, portando proteínas que se suponía que permanecerían en la sala de urgencias (p. ej. PDI) y que se recogían accidentalmente dentro de una vesícula.
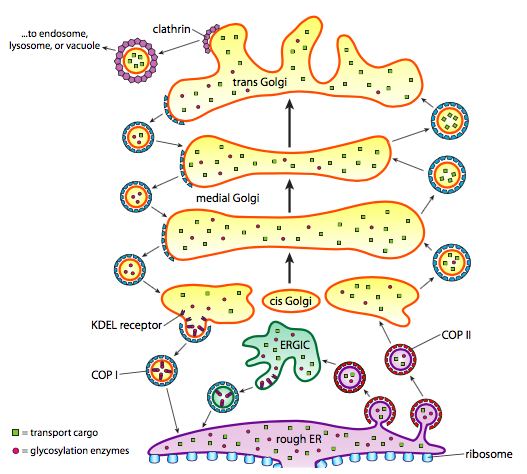
La formación de vesículas depende de proteínas de cubierta que, en condiciones adecuadas, se autoensamblarán en jaulas esféricas. Cuando se asocian con proteínas transmembrana, también pueden tirar de la membrana unida en una forma esférica. Los principales tipos de proteínas de cubierta utilizadas en la formación de vesículas son COPII, COPI y clatrina.
Las proteínas de la cubierta COPII forman las vesículas que se mueven de ER a Golgi. Las proteínas de la cubierta COPI se utilizan entre partes del aparato de Golgi así como para formar vesículas que van desde el Golgi de regreso a la sala de urgencias. Finalmente, la clatrina se utiliza para formar vesículas que salen del Golgi para la membrana plasmática así como para vesículas formadas a partir de la membrana plasmática para endocitosis.
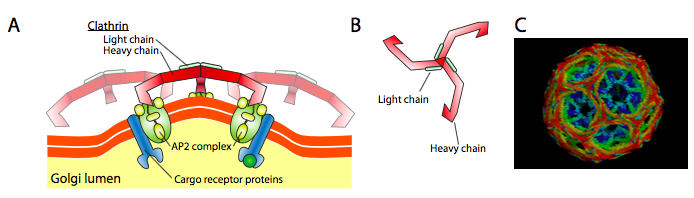
La clatrina (Figura\(\PageIndex{17}\)) es la mejor descrita de las tres, y las capas vesiculares están hechas de arreglos de triskelions de clatrina (del griego, que significa tres patas). Cada triskelion está compuesto por tres cadenas pesadas unidas en el extremo C y tres cadenas ligeras, una asociada con cada cadena pesada. Las cadenas pesadas de diferentes triskelions interactúan a lo largo de su cadena pesada “patas” para crear una construcción muy robusta. Las cadenas ligeras son innecesarias para la formación de vesículas y se cree que ayudan a prevenir interacciones accidentales de moléculas de clatrina en el citoplasma.
Existe una similitud significativa entre los mecanismos de formación de vesículas utilizando estas diferentes proteínas de la cubierta, comenzando con el reclutamiento de ARF1 (ARF significa factor de ribosilación ADP, que no tiene nada que ver con su función aquí) a la membrana. Esto requiere el intercambio facilitado por ARNO de un GTP por GDP (ARNO es un abridor de sitios de unión a nucleótidos ARF). Una vez que ARF1 se ha unido a GTP, el cambio conformacional revela un grupo miristoílo N-terminal que se inserta en la membrana. Tanto la COPI como las vesículas recubiertas de clatrina usan ARF1 y ARNO, pero COPI usa proteínas similares llamadas Sar1p y Sec12p.
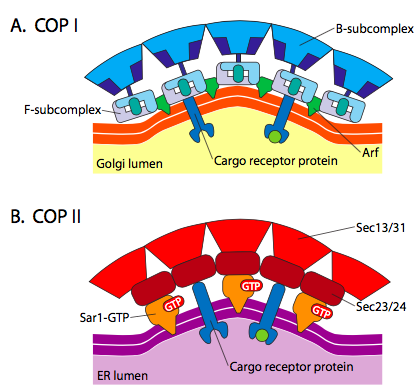
Figura\(\PageIndex{18}\). Vesículas recubiertas de COP
El ARF1 (o SAR1p) se usa para reclutar proteínas adaptadoras que se unen al extremo de la “cola” de las proteínas receptoras unidas a la membrana. El extremo comercial de estos receptores se une a las moléculas car- go que necesitan ser empaquetadas en la vesícula. Las proteínas adaptadoras actúan como enlace entre la membrana (a través de los receptores) y las proteínas de la cubierta. Para la clatrina, las proteínas adaptadoras son AP1 para vesículas derivadas de trans-Golgi y AP2 para vesículas encíticas. Para las vesículas de COPI, los homólogos aproximados son los COPs β-, γ-, δ- y-, mientras que el sistema COPI utiliza Sec23p y Sec24p.
Finalmente, los adaptadores se vinculan a las proteínas reales de la cubierta: clatrina, α- o ε- COP, Sec13p y Sec31p. Lo que todas estas proteínas tienen en común es que espontáneamente (es decir, sin ningún requisito de gasto energético), se autoensamblan en estructuras esféricas tipo jaula. Bajo el microscopio electrónico, las vesículas recubiertas de clatrina están más definidas y las formas hexagonales y pentagonales delimitadas por las subunidades de clatrina le dan a la vesícula un aspecto de “balón de fútbol”. Las vesículas recubiertas con recubrimiento COP son mucho más borrosas en apariencia bajo EM.
Los tres tipos de proteínas de la cubierta vesicular tienen la capacidad de asociarse espontáneamente en un constructo esférico, pero solo la vesícula recubierta con COPI y COPI también “pellizca” espontáneamente la membrana para liberar la vesícula de su membrana de origen. Las vesículas recubiertas de clatrina requieren un mecanismo externo para liberar la vesícula (Figura\(\PageIndex{19}\)).
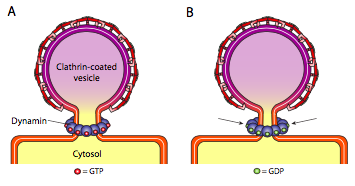
Una vez que la vesícula casi se ha completado, todavía hay un pequeño tallo o cuello de membrana que conecta la vesícula con la membrana. Alrededor de este tallo, las moléculas dinámicas de GTP se agregan en una construcción anillo/espiral. Las moléculas de dinamina son GTPasas globulares que se contraen tras la hidrólisis de GTP. Cuando se asocian alrededor del tallo de la vesícula, cada proteína de dinamina se contrae, con el efecto combinado de estrechar el tallo lo suficiente como para que la membrana se pellizque, sellando y liberando la vesícula de la membrana originaria.
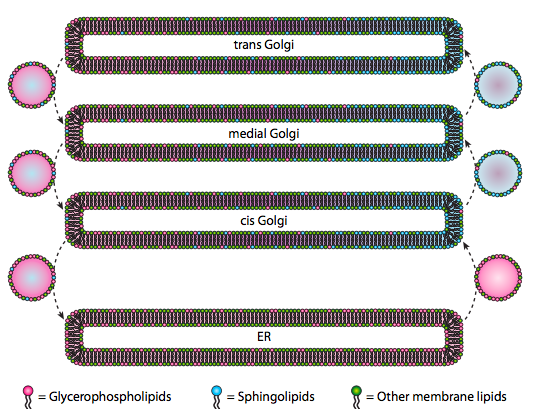
Aunque los lípidos y las membranas se discutieron en el capítulo 4, se descuidó discutir la ubicación de sus síntesis en eucariotas. Como\(\PageIndex{20}\) indica la Figura, la síntesis de ciertos tipos de lípidos es segregada y exclusiva. Los glicerofosfolípidos se forman principalmente en el retículo endoplásmico, aunque también se hacen en mitocondrias y peroxisomas. En contraste, los esfingolípidos no se elaboran en la sala de urgencias (aunque sus precursores de ceramida lo son) en mamíferos, las enzimas necesarias se encuentran en la luz del Golgi cis y medial. Existe evidencia de tráfico vesicular anterógrado y retrógrado entre los diversos compartimentos de Golgi y ER, lo que teóricamente indicaría una redistribución de los tipos de lípidos. Sin embargo, los esfingolípidos tienden a agregarse en balsas lipídicas y parecen estar más concentrados en vesículas en movimiento de anterogrado.
Las proteínas de la cubierta se desprenden poco después de la liberación vesicular. Para la clatrina, el proceso involucra Hsc70, una ATPasa. Sin embargo, para vesículas recubiertas con COPI o COPII, la hidrólisis del GTP en Arf/Sar1p parece debilitar la afinidad de la proteína de la cubierta por los adaptadores e inicia el desrecubrimiento. El activador de GTPasa es ARF GAP (o Sec23p) y es una parte integral de la capa de COP I (o II).
Las vesículas portan dos categorías de carga: proteínas solubles y proteínas transmembrana. De las proteínas solubles, algunas son absorbidas en la vesícula en virtud de estar unidas a un receptor. Otras proteínas simplemente están en las cercanías y se recogen a medida que se forma la vesícula. Ocasionalmente, se toma una proteína que no se suponía que fuera; por ejemplo, el PDI puede estar encerrado en una vesícula que se forma a partir de la sala de emergencia. Tiene poca función en el Golgi, y se necesita en la sala de urgencias, entonces, ¿qué le pasa? Afortunadamente, PDI y muchas otras proteínas ER tienen una secuencia señal C-terminal, KDEL (Lisina-Ácido Aspártico-Ácido Glutámico-Leucina), que grita “Pertenezco a la ER”. Esta secuencia es reconocida por los receptores KDEL dentro del Golgi, y la unión de las proteínas KDEL a los receptores desencadena la formación de vesículas para enviarlas de vuelta al ER.
Las vesículas secretoras tienen un problema especial con la carga soluble. Si la vesícula dependiera simplemente de encerrar proteínas dentro de ella durante el proceso de formación, sería difícil obtener altas concentraciones de esas proteínas. Muchas proteínas secretadas son necesarias por el organismo rápidamente y en cantidades significativas, por lo que existe un mecanismo en el Golgi trans para agregar proteínas secretoras. El mecanismo utiliza proteínas agregantes como la secretogranina II y la cromogranina B que reúnen las proteínas diana en gránulos concentrados grandes. Estos graninos funcionan mejor en el medio trans Golgi de pH bajo y alto Ca 2+, por lo que cuando la vesícula libera su contenido fuera de la célula, el pH más alto y menor Ca 2+ rompe los agregados para liberar las proteínas individuales.
Hay un cambio de pH consistente durante la maduración del Golgi, de manera que a medida que pasamos de ER a Golgi, cada compartimento tiene un pH luminal progresivamente más bajo (más ácido).
Por último, está la cuestión de la focalización de las vesículas. Las vesículas son mucho menos útiles si se lanzan en un tren de carga molecular y se dejan al azar. Por lo tanto, existe un mecanismo de acoplamiento que requiere una coincidencia de la proteína V-snare en la superficie citoplasmática de la vesícula y la trampa T en la superficie citoplásmica de la membrana diana. La fusión de la vesícula a la membrana solo procede si hay una coincidencia. De lo contrario, la vesícula no puede fusionarse, y se adherirá a otro motor molecular para dirigirse a otro destino, ojalá sea correcto. Este proceso es ayudado por la unión de proteínas que inicialmente hacen contacto con una vesícula entrante y la acercan lo suficiente a la diana para probar la interacción de la proteína SNARE. Otras proteínas en la vesícula y las membranas diana interactúan entonces y si las SNares coinciden, pueden ayudar a “cabrestante” la vesícula en la membrana objetivo, con lo cual las membranas se fusionan. Una regla general importante para entender la fusión vesicular y también la direccionalidad de las proteínas y lípidos de membrana, es que el lado de una membrana que mira al citoplasma siempre va a estar frente al citoplasma. Por lo tanto, una proteína que finalmente se encuentra en la superficie externa de la membrana celular se habrá insertado en la superficie luminal de la membrana del ER para empezar.
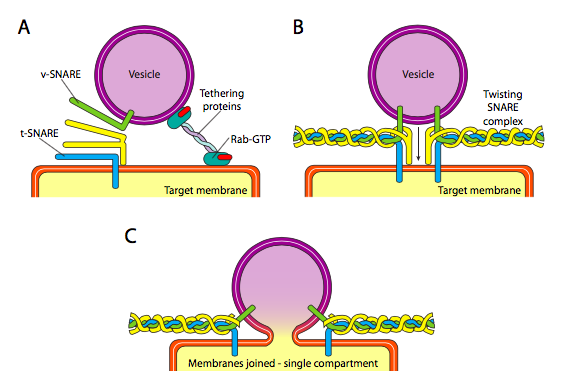
Más específicamente, a medida que una vesícula se acerca a la membrana diana, la proteína de fijación Rab-GTP, que se une a la membrana diana a través de una doble cola lipídica de geranilgeranilo, se asocia flojamente con la vesícula y la mantiene cerca de la membrana diana para dar a las SNARES una oportunidad de funcionar. Los V-snares y T-snares ahora tienen la oportunidad de interactuar y probar para un partido. Recientemente, los SNares han sido renombrados R-Snares y Q-Snares, respectivamente, basados en restos conservados de arginina y glutamina. Además de estas dos SNAR primarias, al menos otra SNARE está involucrada, formando juntas un haz de cuatro hélices α-( cuatro, no tres, porque al menos en el mejor ejemplo estudiado, una de las SNAR está doblada alrededor de manera que dos de sus dominios alfa-helicoidales participan en la interacción. Las cuatro hélices se envuelven entre sí y se piensa que a medida que lo hacen, juntan la vesícula y la membrana diana.
La toxina tetánica, tetanoespasmina, que es liberada por la bacteria Clostridium tetani, provoca espasmos al actuar sobre las células nerviosas, y prevenir la liberación de neurotransmisores. El mecanismo para ello es que escinde la sinaptobrevina, una proteína SNARE, de manera que las vesículas sinápticas no pueden fusionarse con la membrana celular. La toxina botulínica, de Clostridium botulinum, también actúa sobre SNARes para prevenir la fusión de vesículas y la liberación de neurotransmisores, aunque se dirige a diferentes neuronas y así tiene el efecto contrario: el tétanos es causado por la prevención de la liberación de neurotransmisores inhibidores, mientras que el botulismo es causado por prevenir la liberación de neurotransmisores excitatorios.


