16.2: Ciclos de Vida Virales
- Page ID
- 53239
Ciclo lítico de “vida” de los virus
Los virus pueden interactuar con sus huéspedes de dos maneras distintas: la vía lítica y la vía lisogénica. Algunos virus son capaces de cambiar entre las dos vías mientras que otros solo usan una. La característica distintiva del ciclo de vida lítico es la muerte catastrófica de la célula hospedadora por lisis y liberación simultánea de partículas virales. En la Figura\(\PageIndex{2}\), se representan las etapas de la vía lítica. En este caso, se usa como ejemplo un bacteriófago T4 (el término “fago” se usa para virus bacterianos). En el paso 1, el virus se adhiere a la pared celular. En el paso 2, el virus inyecta su material genético (ADNds) en el citoplasma de la bacteria. En el paso 3, el ADN viral se está replicando y los genes en el ADN viral están siendo transcritos y traducidos en proteínas virales. Se detiene la expresión del ADN genómico del huésped. En el paso 4, los virus se ensamblan a partir de las proteínas y el ADN. Y por último, una vez que la fábrica viral ha agotado la energía y los recursos materiales de la célula para hacer más virus, realiza un último golpe de gracia, ya que la célula se destruye para liberar a los virus para que salgan y encuentren más células hospedadoras. El fago T4 utilizado en este ejemplo solo experimenta esta vía y no la vía lisogénica.
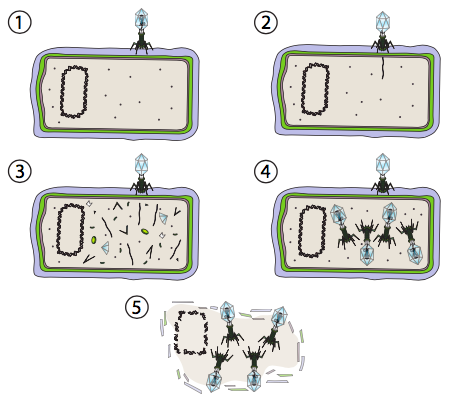
En los eucariotas, el mecanismo es un poco más complicado por el núcleo. El ADN se transporta al núcleo, donde se lleva a cabo la transcripción y replicación. Aunque el ARNm viral se transporta al citoplasma para su traducción como se esperaba, las proteínas de la cápside resultantes se importan de nuevo al núcleo, donde se ensamblan las partículas del virión. Los virus líticos de plantas y animales con genomas de ARN pueden eludir el núcleo por completo, y la replicación del genoma, la síntesis de proteínas y el ensamblaje de partículas ocurren en el citoplasma.
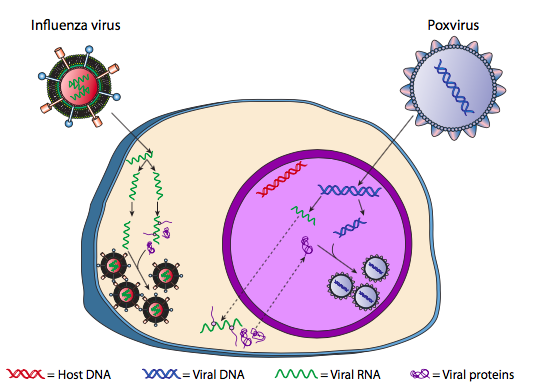
La vía lítica puede producir una gran cantidad de partículas virales entre la infección y la lisis, hasta varias decenas de miles, por ejemplo a partir de una célula infectada con rabia. Por lo tanto, esta vía es muy adecuada para condiciones en las que las células hospedadoras potenciales son abundantes. Por otro lado, esto es un desperdicio de recursos si hay relativamente pocos anfitriones potenciales. Imagínese algunas bacterias que han flotado fuera de la colonia: si un fago infectara a una bacteria en la colonia principal, comandándola para crear miles de partículas virales, la mayoría de esas partículas infectarían nuevos huéspedes y convertirían a muchos miles de soldados más en este ejército viral. Pero si el virus infectó a una de las bacterias separadoras, entonces una vez que mató a su huésped por lisis, las partículas virales tendrían pocos, si los hay, otros huéspedes potenciales, y eventualmente todas las partículas virales simplemente se descomponen de diversas condiciones ambientales. ¿Cuál sería una mejor estrategia de supervivencia para el virus en tal situación?
La vía lisogénica
Una mejor opción para algunos virus bacterianos se llama vía lisogénica. Los bacteriófagos que tienen esta opción, así como una vía lítica, se conocen como fagos templados. En esta vía, el virus entra en latencia integrándose en el genoma del huésped, y permaneciendo transcripcionalmente quiescente hasta que las condiciones ambientales cambien y reflejen una probabilidad de que más células hospedadoras infecten (Figura\(\PageIndex{4}\)).
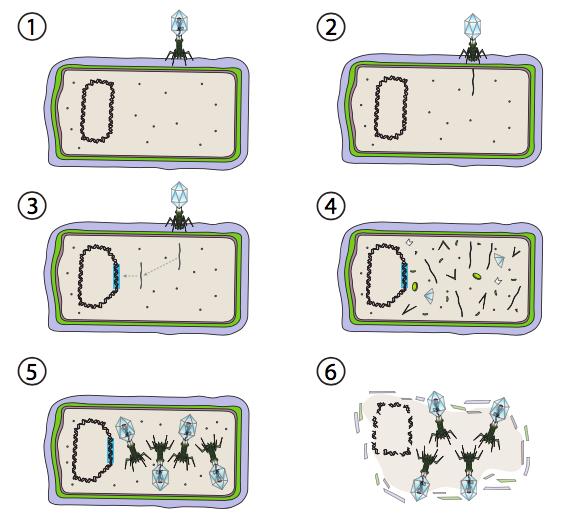
Lambda (λ) es un ejemplo de bacteriófago templado. Las etapas iniciales de infección e inyección genómica son las mismas que las del ciclo lítico, pero bajo condiciones que fomentan la lisogenia, el genoma viral se integra en el genoma del huésped en el paso 3. En la integración λ en E. coli, esto ocurre por recombinación recíproca en una secuencia de 15 pares de bases conocida como el sitio att λ y es facilitado por el producto génico Int. Mientras las condiciones ambientales no sean propicias para la reproducción bacteriana (y por lo tanto un número limitado de posibles células hospedadoras), el genoma viral permanece mayormente oculto e inactivo. La única excepción significativa es un gen que codifica un represor λ que impide el siguiente paso y mantiene el virus latente.
Ese siguiente paso es la escisión del ADN del fago λ del cromosoma huésped, y la posterior replicación y transcripción del ADN viral (Figura\(\PageIndex{4}\), Etapa 4). Entonces, como antes, los pasos finales son el ensamblaje y acumulación de viriones, y eventual ruptura de la estructura celular y liberación de las partículas virales.
Para empaquetar en las limitaciones de espacio reducido que ofrecen las cápsidas, los genomas virales deben ser altamente económicos. Por ejemplo, el genoma del VIH (Figura\(\PageIndex{6}\)) tiene varios genes que se superponen.
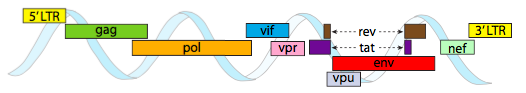
O, en el caso de los curtovirus, los virus vegetales ssDNA (por ejemplo, el virus de la parte superior rizada de la remolacha), el genoma no solo tiene genes superlapeantes Rep, sino que incluso es bidireccional (Figura\(\PageIndex{7}\)) que codifica productos génicos en ambas cadenas de ADN después de que el ADNss se haya convertido en ADNds.
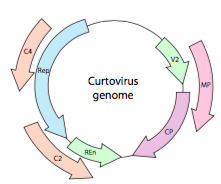
Ante la necesidad de economía, ¿qué genes se encuentran en los virus? Uno de los genomas virales más estudiados, el bacteriófago λ, contiene genes que codifican cinco proteínas de control transcripcional (cuáles se expresan depende de si el fago está en modo lisogénico o lítico), una proteína de unión que controla la degradación de un activador transcripcional, 17 proteínas de la cápsida, una excisionasa que controla la escisión e inserción del genoma del fago en el genoma del huésped, una proteína de integración que inserta el genoma del fago en el huésped, y 3 genes que participan en la lisis de la célula hospedadora.
El genoma del VIH descrito anteriormente es mucho más pequeño que λ, con alrededor de 9 kilobases en comparación con 48 kb, pero nuevamente, el tema es usar proteínas celulares cuando sea posible, y codificar genes virales si es necesario. Entonces, gag codifica proteínas de la cápside, pol codifica transcriptasa inversa, integrasa y proteasa del VIH (que escinde los productos génicos gag y pol en sus proteínas funcionales), vif actúa contra una enzima antiviral de célula huésped común, vpr regula la importación nuclear, tat aumenta fuertemente la transcripción de los genes del VIH, rev exporta ARN viral del núcleo, vpu es necesario para la brotación de partículas del huésped, env codifica glicoproteínas de la envoltura viral y nef promueve la supervivencia de las células infectadas. Las regiones LTR son promotores muy fuertes para impulsar la alta expresión de estos genes.
Aunque no se le conoce como lisogenia, algunos virus animales pueden comportarse de manera similar. El ejemplo más destacado son los virus Baltimore Clase VI -comúnmente conocidos como retrovirus, uno de los cuales es el VIH. La ruta de un retrovirus a través de una célula hospedadora eucariota se representa a continuación (g. 5).
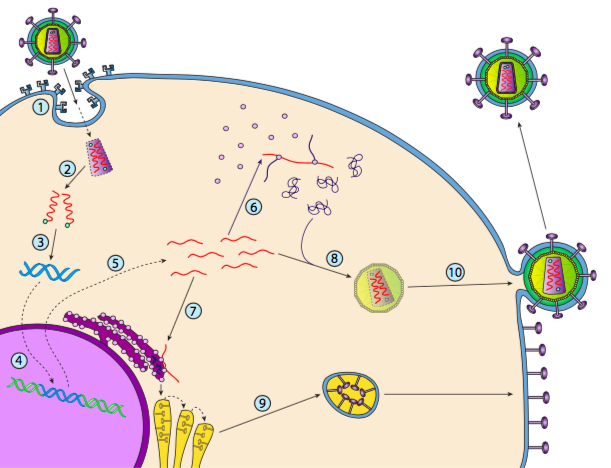
El VIH tiene una envoltura, la cual está tachonada de proteínas transmembrana que son reconocidas por la célula hospedadora, uniendo el virus a la superficie celular e iniciando endocitosis mediada por receptores (1). Después de la endocitosis, la envoltura de membrana del virión y la membrana vesicular se fusionan para liberar la cápside y su contenido (2). Después de que la cápside se disocia en el citoplasma, se liberan las dos cadenas de ARN viral junto con una polimerasa especial: la transcriptasa inversa, que lee un molde de ARN y sintetiza ADN. La transcriptasa inversa también utiliza ese nuevo ADN para sintetizar una cadena de ADN complementaria para que finalmente produzca una versión de ADN bicatenario del genoma viral (3). Este ADNds viral se transporta al núcleo donde se integra en el genoma del huésped utilizando otra proteína viral, la integrasa
(4). El ADN viral integrado se llama provirus. El provirus puede permanecer latente, pero si se activa, entonces se transcribe y el ARN viral resultante se transporta fuera del núcleo (5). Parte del ARN viral codifica enzimas como transcriptasa inversa e integrasa, o proteínas de la cápside, todas las cuales se producen en el citoplasma (6), pero algunas codifican glicoproteínas unidas a membrana, que se translocan al RE (7) y finalmente se procesan a través del Golgi e incorporadas a la membrana plasmática (9). Una vez ensamblado el virión (8), se une a las proteínas transmembrana virales, nucleando una “vesícula” exocítica (10) que es el virión completo con envoltura viral.
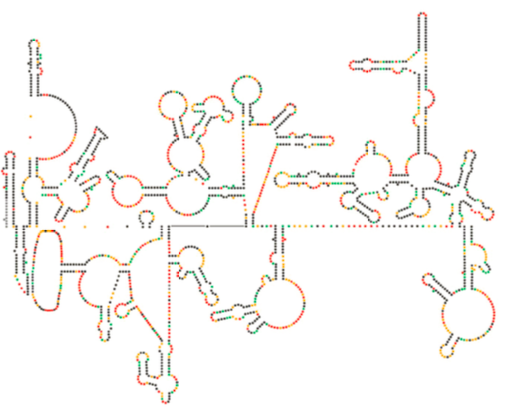
El reciente examen estructural del genoma del VIH sugiere que la estructura del ARN del VIH en sí puede desempeñar un papel significativo en su propagación dentro de las células hospedadoras. La figura\(\PageIndex{8}\), de Watts et al, Nature 460:711-716, 2009, muestra una estructura secundaria predicha del genoma. Los autores sugieren que la estructura del ARN en realidad puede interactuar con la elongación ribosómica para controlar el plegamiento de las proteínas virales. También postulan la extensión de este argumento para incluir información genética importante codificada no solo en la secuencia de nucleótidos, sino la estructura secundaria y estructura terciaria de cualquier virus ARN.
Al considerar los virus con respecto al resto de este capítulo integrador, hay dos ideas primordiales a tener en cuenta. Primero, la supervivencia viral se basa en números: necesita hacer un gran número de sus componentes para lanzar una red lo más amplia posible para nuevas células hospedadoras. Para ello, los promotores virales suelen ser mucho más fuertes que los promotores de células hospedadoras, impulsando simultáneamente más expresión génica viral al tiempo que previenen la expresión del gen huésped (dedicando recursos celulares a la producción de virus). Segundo, debido a los rápidos tiempos de generación, la tasa de mutación y evolución viral es mucho más rápida que los genomas eucariotas normales. Además, si el virus usa su propia polimerasa (como la transcriptasa inversa o la ARN replicasa), la tasa de mutación aumenta aún más porque no hay verificación de errores por las polimerasas virales.


