2.2: Agua
- Page ID
- 54100
¿Alguna vez te has preguntado por qué los científicos pasan tiempo buscando agua en otros planetas? Es porque el agua es esencial para la vida; incluso las huellas diminutas de ella en otro planeta pueden indicar que la vida podría o existió en ese planeta. El agua es una de las moléculas más abundantes en las células vivas y la más crítica para la vida tal como la conocemos. Aproximadamente el 60—70 por ciento de tu cuerpo está compuesto por agua. Sin ella, la vida simplemente no existiría.
El agua es polar
Los átomos de hidrógeno y oxígeno dentro de las moléculas de agua forman enlaces covalentes polares. Los electrones compartidos pasan más tiempo asociados con el átomo de oxígeno que con los átomos de hidrógeno. No hay carga general a una molécula de agua, pero hay una ligera carga positiva en cada átomo de hidrógeno y una ligera carga negativa en el átomo de oxígeno. Debido a estas cargas, los átomos de hidrógeno ligeramente positivos se repelen entre sí y forman la forma única que se ve en la Figura 2.1.6. Cada molécula de agua atrae a otras moléculas de agua debido a las cargas positivas y negativas en las diferentes partes de la molécula. El agua también atrae a otras moléculas polares (como los azúcares), formando enlaces de hidrógeno. Cuando una sustancia forma fácilmente enlaces de hidrógeno con el agua, puede disolverse en agua y se la conoce como hidrófila (“amante del agua”). Los enlaces de hidrógeno no se forman fácilmente con sustancias no polares como aceites y grasas (Figura\(\PageIndex{1}\)). Estos compuestos no polares son hidrófobos (“temerosos del agua”) y no se disolverán en el agua.

El agua estabiliza la temperatura
Los enlaces de hidrógeno en el agua le permiten absorber y liberar energía térmica más lentamente que muchas otras sustancias. La temperatura es una medida del movimiento (energía cinética) de las moléculas. A medida que aumenta el movimiento, la energía es mayor y por lo tanto la temperatura es mayor. El agua absorbe una gran cantidad de energía antes de que suba su temperatura. El aumento de la energía interrumpe los enlaces de hidrógeno entre las moléculas de agua. Debido a que estos enlaces se pueden crear e interrumpir rápidamente, el agua absorbe un aumento en la energía y los cambios de temperatura solo mínimamente. Esto significa que el agua modera los cambios de temperatura dentro de los organismos y en sus ambientes. A medida que la entrada de energía continúa, el equilibrio entre la formación de enlaces de hidrógeno y la destrucción oscila hacia el lado de la destrucción. Se rompen más lazos de los que se forman. Este proceso da como resultado la liberación de moléculas de agua individuales en la superficie del líquido (como un cuerpo de agua, las hojas de una planta o la piel de un organismo) en un proceso llamado evaporación. La evaporación del sudor, que es 90 por ciento de agua, permite el enfriamiento de un organismo, porque romper los enlaces de hidrógeno requiere un aporte de energía y quita el calor del cuerpo.
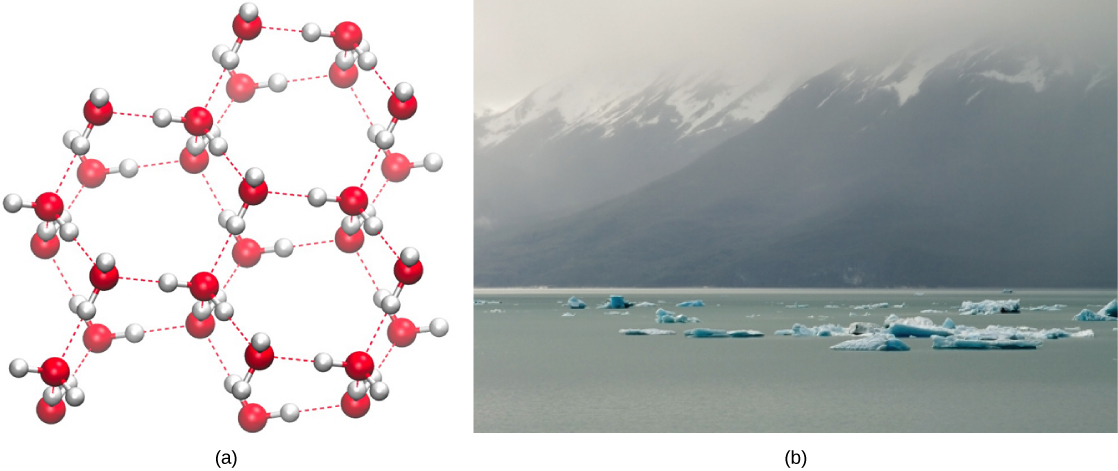
Por el contrario, a medida que el movimiento molecular disminuye y las temperaturas disminuyen, hay menos energía presente para romper los enlaces de hidrógeno entre las moléculas de agua. Estos enlaces permanecen intactos y comienzan a formar una estructura rígida similar a una celosía (por ejemplo, hielo) (Figura\(\PageIndex{2}\) a). Cuando se congela, el hielo es menos denso que el agua líquida (las moléculas están más separadas). Esto significa que el hielo flota en la superficie de un cuerpo de agua (Figura\(\PageIndex{2}\) b). En lagos, estanques y océanos, se formará hielo en la superficie del agua, creando una barrera aislante para proteger la vida animal y vegetal debajo de la congelación en el agua. Si esto no sucediera, las plantas y animales que viven en el agua se congelarían en un bloque de hielo y no podrían moverse libremente, haciendo que la vida en temperaturas frías sea difícil o imposible.
El agua es un excelente solvente
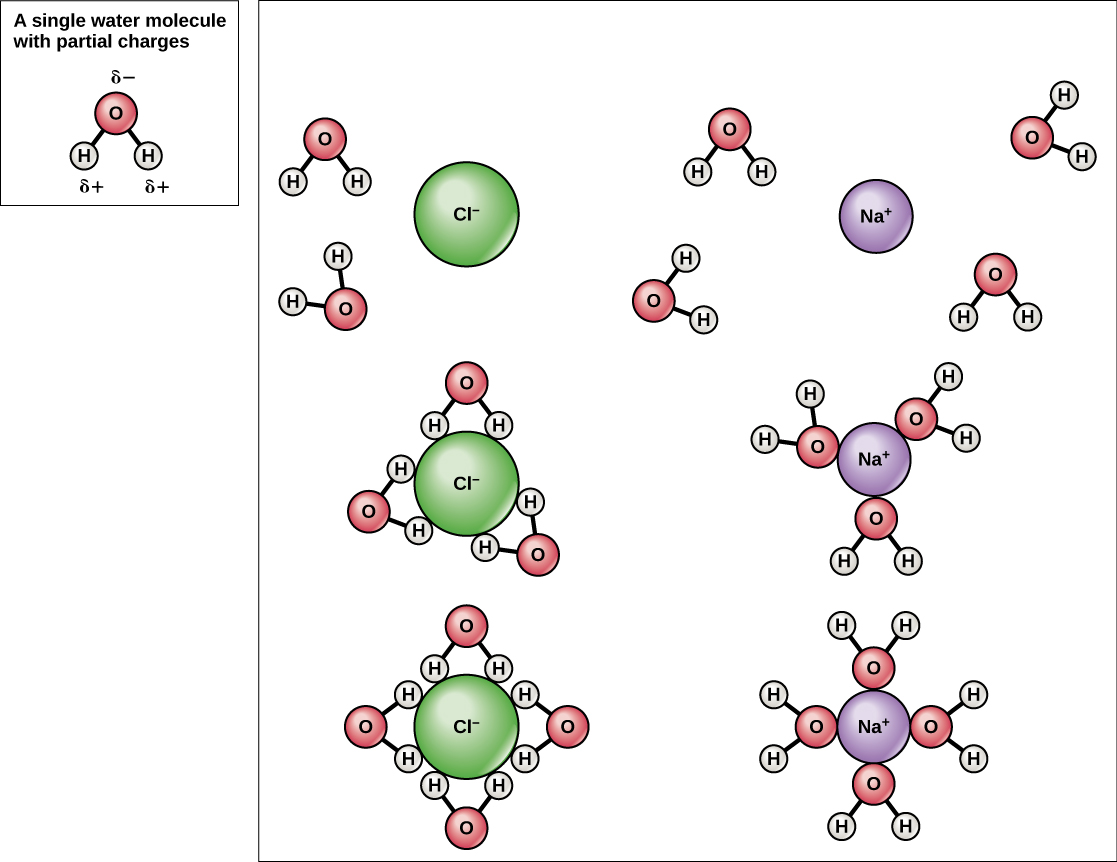
Debido a que el agua es polar, con ligeras cargas positivas y negativas, los compuestos iónicos y las moléculas polares pueden disolverse fácilmente en ella. El agua es, por lo tanto, lo que se denomina disolvente, una sustancia capaz de disolver otra sustancia. Las partículas cargadas formarán enlaces de hidrógeno con una capa circundante de moléculas de agua. Esto se conoce como una esfera de hidratación y sirve para mantener las partículas separadas o dispersas en el agua. En el caso de la sal de mesa (NaCl) mezclada en agua (Figura\(\PageIndex{3}\)), los iones sodio y cloruro se separan, o se disocian, en el agua, y se forman esferas de hidratación alrededor de los iones. Un ion de sodio cargado positivamente está rodeado por las cargas parcialmente negativas de los átomos de oxígeno en las moléculas de agua. Un ion cloruro cargado negativamente está rodeado por las cargas parcialmente positivas de los átomos de hidrógeno en las moléculas de agua. Estas esferas de hidratación también se denominan conchas de hidratación. La polaridad de la molécula de agua la convierte en un solvente efectivo y es importante en sus múltiples roles en los sistemas vivos.
El agua es cohesiva
¿Alguna vez has llenado un vaso de agua hasta la parte superior y luego lentamente agregaste algunas gotas más? Antes de que se desborde, el agua en realidad forma una forma de cúpula sobre el borde del vidrio. Esta agua puede permanecer por encima del cristal debido a la propiedad de cohesión. En cohesión, las moléculas de agua son atraídas entre sí (debido a los enlaces de hidrógeno), manteniendo las moléculas juntas en la interfaz líquido-aire (gas), aunque no hay más espacio en el vidrio. La cohesión da lugar a la tensión superficial, la capacidad de una sustancia para soportar la ruptura cuando se coloca bajo tensión o tensión. Cuando se deja caer un pequeño trozo de papel sobre una gotita de agua, el papel flota sobre la gotita de agua, aunque el objeto es más denso (más pesado) que el agua. Esto ocurre debido a la tensión superficial que crean las moléculas de agua. La cohesión y la tensión superficial mantienen intactas las moléculas de agua y el artículo flotando en la parte superior. Incluso es posible “flotar” una aguja de acero sobre un vaso de agua si la colocas suavemente, sin romper la tensión superficial (Figura\(\PageIndex{4}\)).

Estas fuerzas cohesivas también están relacionadas con la propiedad de adhesión del agua, o la atracción entre las moléculas de agua y otras moléculas. Esto se observa cuando el agua “sube” por una pajita colocada en un vaso de agua. Notarás que el agua parece estar más alta en los lados de la paja que en el medio. Esto se debe a que las moléculas de agua son atraídas por la paja y por lo tanto se adhieren a ella.
Las fuerzas cohesivas y adhesivas son importantes para mantener la vida útil. Por ejemplo, debido a estas fuerzas, el agua puede fluir desde las raíces hasta la parte superior de las plantas para alimentar a la planta.
CONCEPT EN ACCIÓN
Para conocer más sobre el agua, visite el Servicio Geológico de Estados Unidos Ciencia del agua para escuelas: ¡Todo sobre el agua! sitio web.
Tampones, pH, ácidos y bases
El pH de una solución es una medida de su acidez o alcalinidad. Probablemente hayas usado papel tornasol, papel que ha sido tratado con un tinte natural soluble en agua por lo que se puede usar como indicador de pH, para probar cuánto ácido o base (alcalinidad) existe en una solución. Incluso podría haber usado algunos para asegurarse de que el agua de una piscina al aire libre esté tratada adecuadamente. En ambos casos, esta prueba de pH mide la cantidad de iones hidrógeno que existe en una solución dada. Las altas concentraciones de iones hidrógeno producen un pH bajo, mientras que los niveles bajos de iones de hidrógeno dan como resultado un pH alto. La concentración global de iones hidrógeno está inversamente relacionada con su pH y se puede medir en la escala de pH (Figura\(\PageIndex{5}\)). Por lo tanto, cuantos más iones hidrógeno estén presentes, menor será el pH; a la inversa, cuanto menos iones hidrógeno, mayor será el pH.
La escala de pH oscila entre 0 y 14. Un cambio de una unidad en la escala de pH representa un cambio en la concentración de iones hidrógeno por un factor de 10, un cambio en dos unidades representa un cambio en la concentración de iones hidrógeno por un factor de 100. Así, pequeños cambios en el pH representan grandes cambios en las concentraciones de iones hidrógeno. El agua pura es neutra. No es ni ácida ni básica, y tiene un pH de 7.0. Cualquier cosa por debajo de 7.0 (que va de 0.0 a 6.9) es ácida, y cualquier cosa por encima de 7.0 (de 7.1 a 14.0) es alcalina. La sangre en tus venas es ligeramente alcalina (pH = 7.4). El ambiente en tu estómago es altamente ácido (pH = 1 a 2). El jugo de naranja es ligeramente ácido (pH = aproximadamente 3.5), mientras que el bicarbonato de sodio es básico (pH = 9.0).

Los ácidos son sustancias que proporcionan iones hidrógeno (H +) y pH más bajo, mientras que las bases proporcionan iones hidróxido (OH —) y elevan el pH. Cuanto más fuerte es el ácido, más fácilmente dona H +. Por ejemplo, el ácido clorhídrico y el jugo de limón son muy ácidos y renuncian fácilmente al H + cuando se agregan al agua. Por el contrario, las bases son aquellas sustancias que donan fácilmente OH —. Los iones OH — se combinan con H + para producir agua, lo que eleva el pH de una sustancia. El hidróxido de sodio y muchos limpiadores domésticos son muy alcalinos y abandonan el OH, rápidamente cuando se colocan en agua, elevando así el pH.
La mayoría de las células en nuestro cuerpo operan dentro de una ventana muy estrecha de la escala de pH, típicamente que varía solo de 7.2 a 7.6. Si el pH del cuerpo está fuera de este rango, el sistema respiratorio funciona mal, al igual que otros órganos del cuerpo. Las células ya no funcionan correctamente y las proteínas se descomponen. La desviación fuera del rango de pH puede inducir coma o incluso causar la muerte.
Entonces, ¿cómo es que podemos ingerir o inhalar sustancias ácidas o básicas y no morir? Los búferes son la clave. Los búferesabsorben fácilmente el exceso de H + u OH —, manteniendo el pH del cuerpo cuidadosamente mantenido en el rango estrecho mencionado anteriormente. El dióxido de carbono es parte de un sistema tampón prominente en el cuerpo humano; mantiene el pH dentro del rango adecuado. Este sistema tampón involucra ácido carbónico (H 2 CO 3) y anión bicarbonato (HCO 3 —). Si entra demasiado H + al cuerpo, el bicarbonato se combinará con el H + para crear ácido carbónico y limitar la disminución del pH. De igual manera, si se introduce demasiado OH — en el sistema, el ácido carbónico se disociará rápidamente en bicarbonato e iones H +. Los iones H + pueden combinarse con los iones OH —, limitando el aumento del pH. Si bien el ácido carbónico es un producto importante en esta reacción, su presencia es fugaz porque el ácido carbónico se libera del cuerpo como gas dióxido de carbono cada vez que respiramos. Sin este sistema tampón, el pH en nuestros cuerpos fluctuaría demasiado y no lograríamos sobrevivir.
Resumen
El agua tiene muchas propiedades que son críticas para mantener la vida. Es polar, permitiendo la formación de enlaces de hidrógeno, que permiten que los iones y otras moléculas polares se disuelvan en el agua. Por lo tanto, el agua es un excelente solvente. Los enlaces de hidrógeno entre las moléculas de agua le dan al agua la capacidad de retener el calor mejor que muchas otras sustancias. A medida que aumenta la temperatura, los enlaces de hidrógeno entre el agua se rompen y se reforman continuamente, permitiendo que la temperatura general permanezca estable, aunque se agrega mayor energía al sistema. Las fuerzas cohesivas del agua permiten la propiedad de la tensión superficial. Todas estas propiedades únicas del agua son importantes en la química de los organismos vivos.
El pH de una solución es una medida de la concentración de iones hidrógeno en la solución. Una solución con un alto número de iones hidrógeno es ácida y tiene un valor de pH bajo. Una solución con un alto número de iones hidróxido es básica y tiene un alto valor de pH. La escala de pH oscila entre 0 y 14, siendo neutro un pH de 7. Los tampones son soluciones que moderan los cambios de pH cuando se agrega un ácido o una base al sistema tampón. Los tampones son importantes en los sistemas biológicos debido a su capacidad para mantener condiciones de pH constantes.
Notas al pie
- 1 Humphrey, W., Dalke, A. y Schulten, K., “VM—Dinámica Molecular Visual”, J. Molec. Gráficos, 1996, vol. 14, pp. 33-38. http://www.ks.uiuc.edu/Research/vmd/
Glosario
- ácido
- una sustancia que dona iones de hidrógeno y por lo tanto disminuye el pH
- adhesión
- la atracción entre moléculas de agua y moléculas de una sustancia diferente
- base
- una sustancia que absorbe iones de hidrógeno y por lo tanto eleva el pH
- búfer
- una solución que resiste un cambio en el pH absorbiendo o liberando iones de hidrógeno o hidróxido
- cohesión
- las fuerzas intermoleculares entre las moléculas de agua causadas por la naturaleza polar del agua; crea tensión superficial
- evaporación
- la liberación de moléculas de agua del agua líquida para formar vapor de agua
- hidrofílico
- describe una sustancia que se disuelve en el agua; amante del agua
- hidrofóbico
- describe una sustancia que no se disuelve en agua; temeroso del agua
- papel tornasol
- papel de filtro que ha sido tratado con un tinte natural soluble en agua para que pueda usarse como indicador de pH
- Escala de pH
- una escala que va de 0 a 14 que mide la concentración aproximada de iones hidrógeno de una sustancia
- solvente
- una sustancia capaz de disolver otra sustancia
- tensión superficial
- la fuerza cohesiva en la superficie de un cuerpo de líquido que impide que las moléculas se separen
- temperatura
- una medida de movimiento molecular



