6.2: Ciclo del ácido cítrico y vías relacionadas
- Page ID
- 53246
Fuente: BiochemFFA_6_2.pdf. Todo el libro de texto está disponible de forma gratuita de los autores en http://biochem.science.oregonstate.edu/content/biochemistry-free-and-easy
Ciclo del ácido cítrico
La vía catabólica primaria en el cuerpo es el ciclo del ácido cítrico porque es aquí donde se produce la oxidación a dióxido de carbono para los productos de descomposición de los principales bloques de construcción de la célula: azúcares, ácidos grasos y aminoácidos. La ruta es cíclica (Figura 6.63) y, por lo tanto, no tiene realmente un punto inicial o final. Todas las reacciones ocurren en las mitocondrias, aunque una enzima está incrustada en la membrana interna del orgánulo. A medida que cambian las necesidades, las células pueden usar un subconjunto de las reacciones del ciclo para producir una molécula deseada en lugar de ejecutar todo el ciclo (ver AQUÍ).
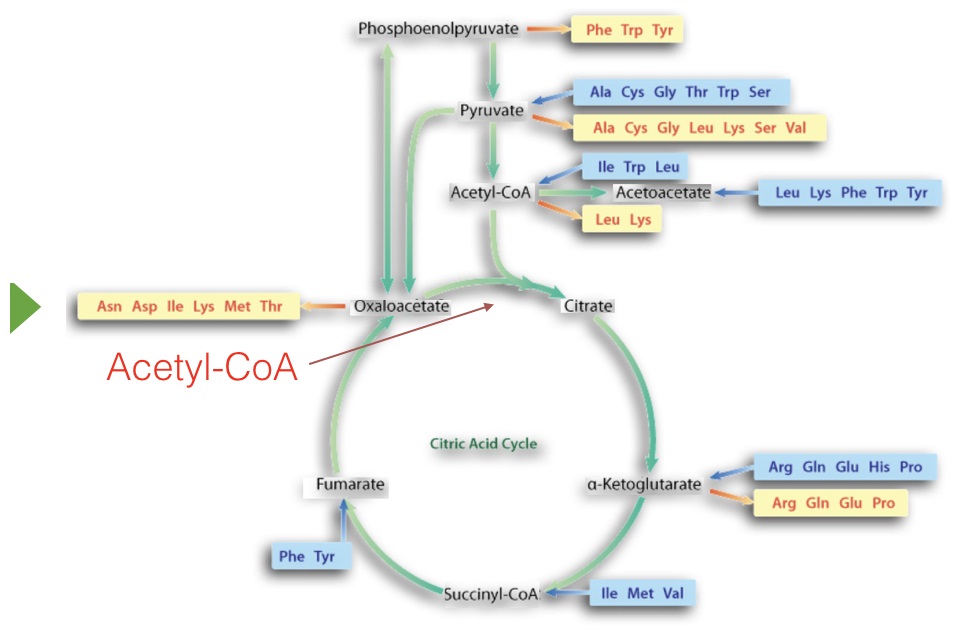
Acetil-CoA
La molécula que “alimenta” el ciclo del ácido cítrico es acetil-CoA y se puede obtener del piruvato (de la glucólisis), de la β-oxidación de ácidos grasos, de cuerpos cetónicos y del metabolismo de aminoácidos. Las moléculas de otras vías que se alimentan al ciclo del ácido cítrico para catabolismo hacen que el ciclo del ácido cítrico sea “cataplerótico”. Vale la pena señalar que el acetil-CoA tiene destinos muy diferentes, dependiendo del estado/necesidades energéticas de la célula (ver AQUÍ). La siguiente descripción describe la oxidación (catabolismo) en el ciclo del ácido cítrico.
Anabólicamente, la acetil-CoA también es muy importante para proporcionar bloques de construcción para la síntesis de ácidos grasos, cuerpos cetónicos, aminoácidos y colesterol. Otros intermedios del ciclo del ácido cítrico también son importantes en el metabolismo de aminoácidos (Figura 6.63), la síntesis de hemo, el transporte de electrones y el transporte de acetil-CoA a través de la membrana interna mitocondrial. La capacidad del ciclo del ácido cítrico para suministrar intermedios a las vías da lugar al término 'anaplerótico'. Significa 'llenar'. Antes de discutir el ciclo del ácido cítrico, es importante describir primero un complejo enzimático importante que es una fuente importante de acetil-CoA para el ciclo.
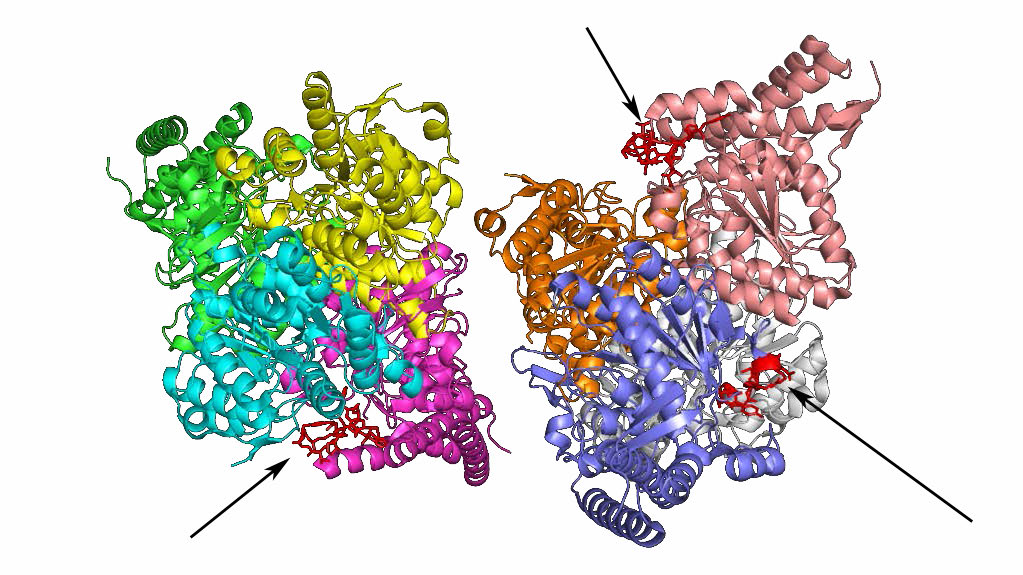
Figura 6.64 - Subunidad E1 de piruvato deshidrogenasa. Wikipedia
Descarboxilación de piruvato
La enzima piruvato deshidrogenasa es un complejo de múltiples copias de tres subunidades que catalizan la descarboxilación del piruvato para formar acetil-CoA. El mecanismo de reacción requiere el uso de cinco coenzimas. La piruvato deshidrogenasa es un enorme complejo en mamíferos con un tamaño cinco veces mayor que los ribosomas.
Subunidades
Las tres subunidades son designadas por E1, E2 y E3. E2 también se conoce como dihidrolipoamida acetiltransferasa y E3 se llama más precisamente dihidrolipoil deshidrogenasa. La confusión surge con el nombre de E1. Algunos lo llaman piruvato deshidrogenasa y otros le dan el nombre piruvato descarboxilasa. Utilizaremos piruvato descarboxilasa únicamente para referirnos a E1 y piruvato deshidrogenasa solo para referirse al complejo de E1, E2 y E3.
Las acciones catalíticas de la piruvato deshidrogenasa pueden dividirse en tres etapas, cada una teniendo lugar en una de las subunidades. Las etapas, que ocurren secuencialmente en E1, E2 y E3, son 1) descarboxilación del piruvato; 2) oxidación del producto descarboxilado; y 3) transferencia de electrones para finalmente formar NADH (Figura 6.65).
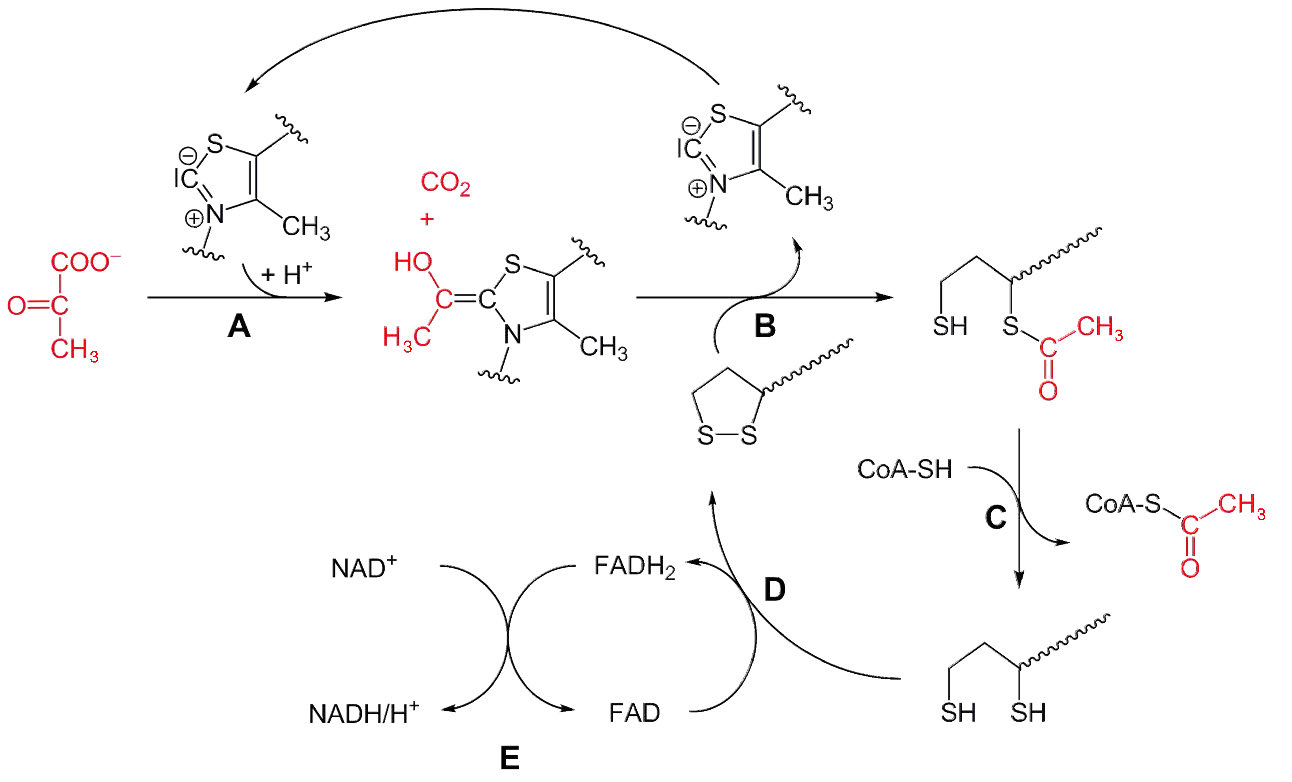
Figura 6.65 - Mecanismo de acción de la descarboxilación y oxidación de piruvato por piruvato deshidrogenasa.
Catálisis
El proceso catalítico comienza después de la unión del sustrato de piruvato con la activación de la coenzima pirofosfato de tiamina a través de la formación de un intermedio iluro. El carbanión nucleófilo del iluro ataca el carbono de cetona electrófila sobre el piruvato, liberando dióxido de carbono y creando un enol que pierde un protón sobre el carbono para convertirse en un dipolo 1,3 que incluye el nitrógeno cargado positivamente de la tiamina. La reacción (etapa A en la Figura 6.65) es una descarboxilación no oxidativa. La oxidación de la unidad hidroxietilo de dos carbonos ocurre en la transferencia a la lipoamida.
Acetilación reductora
La acetilación reductora ocurre a continuación (Etapa B) a medida que la unidad de hidroxietilo de 2 carbonos se transfiere a lipoamida en E2. (Lipoamida es el nombre de una molécula de ácido lipoico unida covalentemente a una cadena lateral de lisina en la subunidad E2). En procariotas en ausencia de oxígeno, el grupo hidroxietilo no se pasa a la lipoamida, sino que se libera como acetaldehído libre, que puede aceptar electrones del NADH (catalizado por la alcohol deshidrogenasa) y convertirse en etanol en proceso de fermentación. En presencia de oxígeno en casi todos los organismos aeróbicos, el proceso continúa con la transferencia de la unidad de hidroxietilo a E2 y continuación del ciclo a continuación.
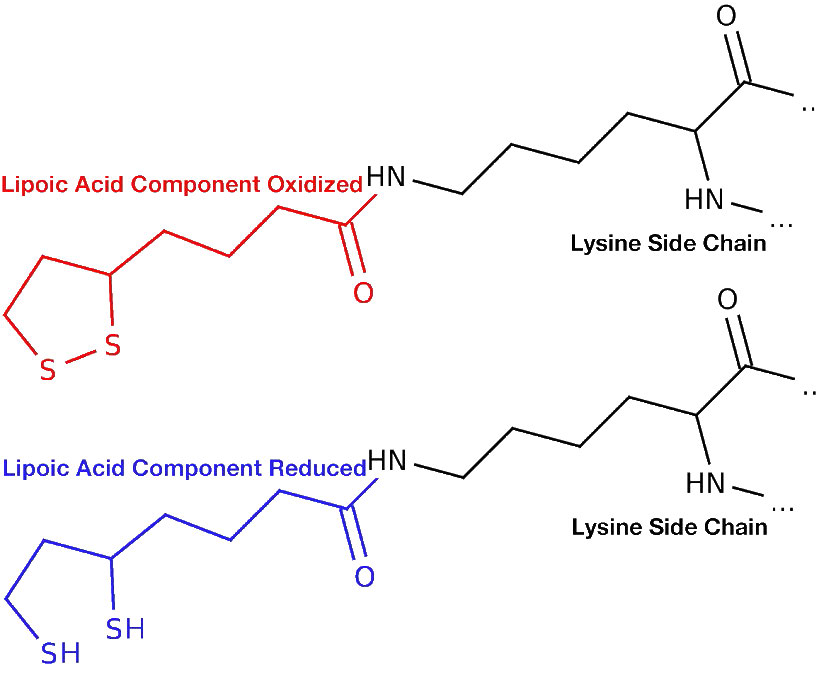
Etapa de oxidación
La transferencia del grupo hidroxietilo de E1 a la coenzima lipoamida en E2 es una oxidación, con transferencia de electrones del grupo hidroxietilo al disulfuro de lipoamida (reduciéndolo) y formación sobre la lipoamida de un acetil-tioéster (oxidándolo).
El grupo acetilo se transfiere luego de la lipoamida a la coenzima A en E2 (Etapa C en la Figura 6.65), formando acetil-CoA, que se libera y deja sulfhidrilos reducidos en la lipoamida. Para que la enzima vuelva a su estado original, se debe volver a formar el enlace disulfuro en la lipoamida. Esto ocurre con la transferencia de electrones de lipoamida reducida a un FAD unido covalentemente a E3 (Etapa D). Esto reduce el FAD a FADH2.
Formación de NADH
En el último paso del proceso, los electrones de FADH2 se transfieren al NAD+ externo, formando NADH (Paso E) y completando el ciclo general. Entonces la enzima puede entonces comenzar otra ronda catalítica uniéndose a un piruvato.
Regulación de piruvato deshidrogenasa
La piruvato dehidrogenasa está regulada tanto alostéricamente como por modificación covalente: fosforilación/desfosforilación. La regulación de la piruvato deshidrogenasa, ya sea por mecanismos alostéricos o covalentes, tiene la misma estrategia. Los indicadores de alta energía apagan la enzima, mientras que los indicadores de baja energía la estimulan. Para la regulación alostérica, los indicadores de alta energía que afectan a la enzima son ATP, acetil-CoA, NADH y ácidos grasos, que la inhiben. AMP, Coenzima A, NAD+ y calcio, por otro lado, lo estimulan (Figura 6.67).
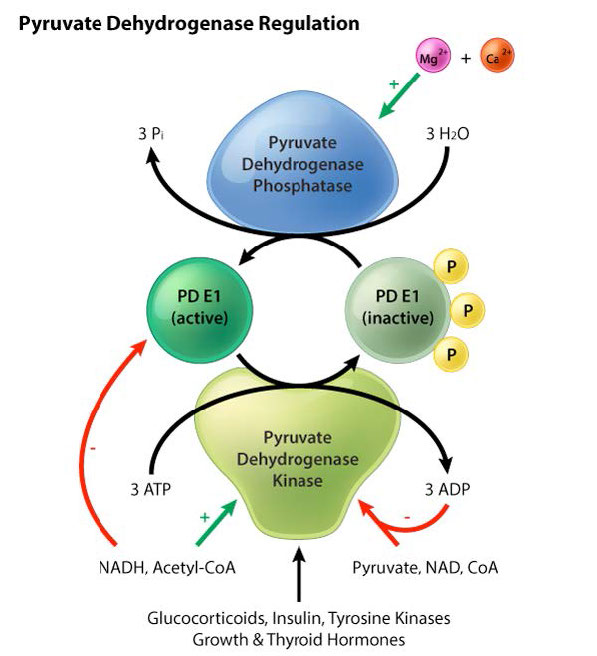
Modificación covalente
La regulación por modificación covalente de la piruvato deshidrogenasa es un poco más complicada. Ocurre como resultado de la fosforilación por piruvato deshidrogenasa quinasa (PDK - Figura 6.67) o desfosforilación por piruvato deshidrogenasa fosfatasa (PDP).
PDK pone fosfato en uno cualquiera de los tres residuos de serina en la subunidad E1, lo que hace que la piruvato quinasa no pueda realizar su primer paso de catálisis: la descarboxilación del piruvato. El PDP puede eliminar esos fosfatos. La PDK se activa alostéricamente en la matriz mitocondrial cuando aumentan las concentraciones de NADH y acetil-CoA.
Inhibición del producto
Así, los productos de la reacción de piruvato deshidrogenasa inhiben la producción de más productos favoreciendo su fosforilación por PDK. El piruvato, un sustrato de piruvato deshidrogenasa, inhibe la PDK, por lo que las concentraciones crecientes de sustrato activan la piruvato deshidrogenasa al reducir su fosforilación por PDK. A medida que disminuyen las concentraciones de NADH y acetil-CoA, la PDP se asocia con piruvato quinasa y elimina el fosfato de la serina en la subunidad E1.
Las concentraciones bajas de NADH y acetil-CoA son necesarias para que la PDP permanezca en la enzima. Cuando esas concentraciones aumentan, PDP se disocia y PDK obtiene acceso a la serina para fosforilación. La insulina y el calcio también pueden activar el PDP. Esto es muy importante en el tejido muscular, ya que el calcio es una señal para la contracción muscular, lo que requiere energía. La insulina también activa la piruvato quinasa y la vía de la glucólisis para usar glucosa internalizada. Cabe señalar que la cascada de fosforilación de cAMP del receptor β-adrenérgico no tiene ningún efecto sobre la piruvato quinasa, aunque la cascada de insulina, de hecho, afecta a la PDP y a la piruvato quinasa.
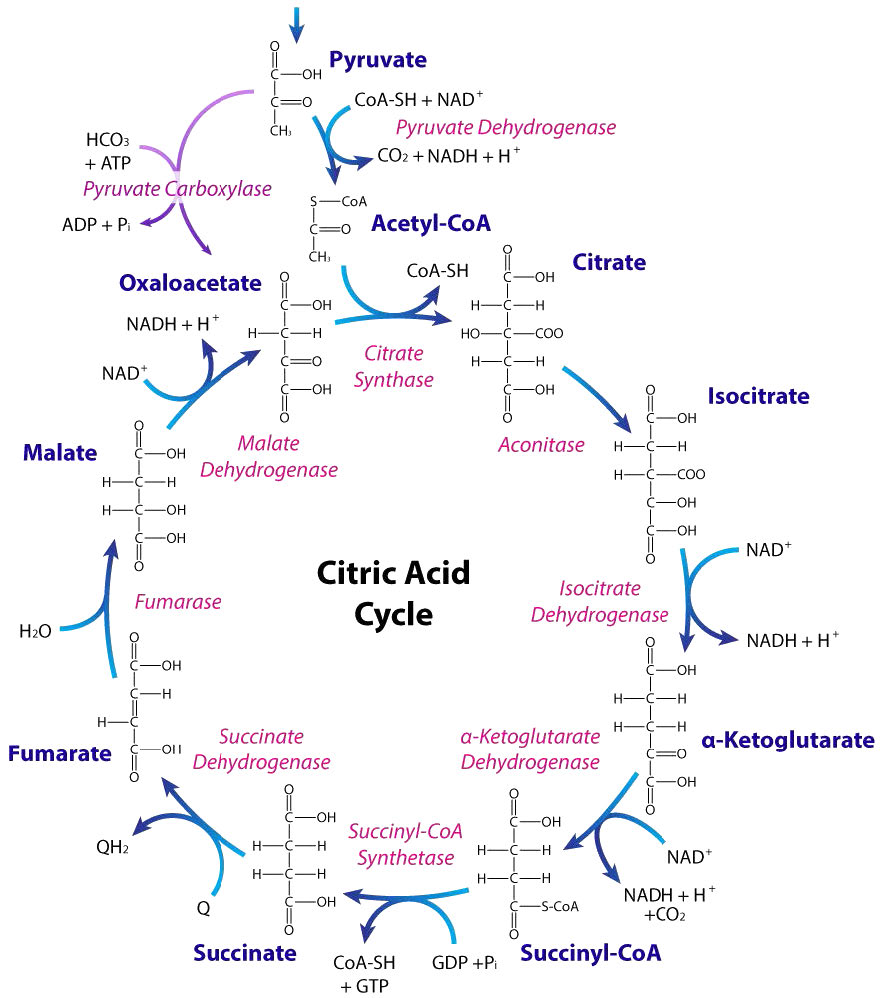
Reacciones del ciclo del ácido cítrico
Centrándose en la propia vía (Figura 6.69), el punto habitual para iniciar la discusión es la adición de acetil-CoA al oxaloacetato (OAA) para formar citrato.
La acetil-CoA para la vía puede provenir de una variedad de fuentes. La reacción que lo une a OAA es catalizada por citrato sintasa y el ∆G°' es bastante negativo. Esto, a su vez, ayuda a “tirar” de la reacción de malato deshidrogenasa que la precede en el ciclo.
En la siguiente reacción, el citrato se isomeriza a isocitrato por acción de la enzima llamada aconitasa.
El isocitrato es un punto de ramificación en plantas y bacterias para el ciclo del glioxilato (ver AQUÍ). La descarboxilación oxidativa de isocitrato por isocitrato deshidrogenasa produce el primer NADH y produce α-cetoglutarato.
Este intermedio de cinco carbonos es un punto de ramificación para la síntesis del aminoácido glutamato. Además, el glutamato también se puede convertir fácilmente en este intermedio en la reacción inversa. La descarboxilación de α-cetoglutarato produce succinil-CoA y es catalizada por α-cetoglutarato deshidrogenasa.
La enzima α-cetoglutarato deshidrogenasa es estructuralmente muy similar a la piruvato deshidrogenasa y emplea las mismas cinco coenzimas: NAD+, FAD, CoA-SH, pirofosfato de tiamina y lipoamida.
Regeneración de oxaloacetato
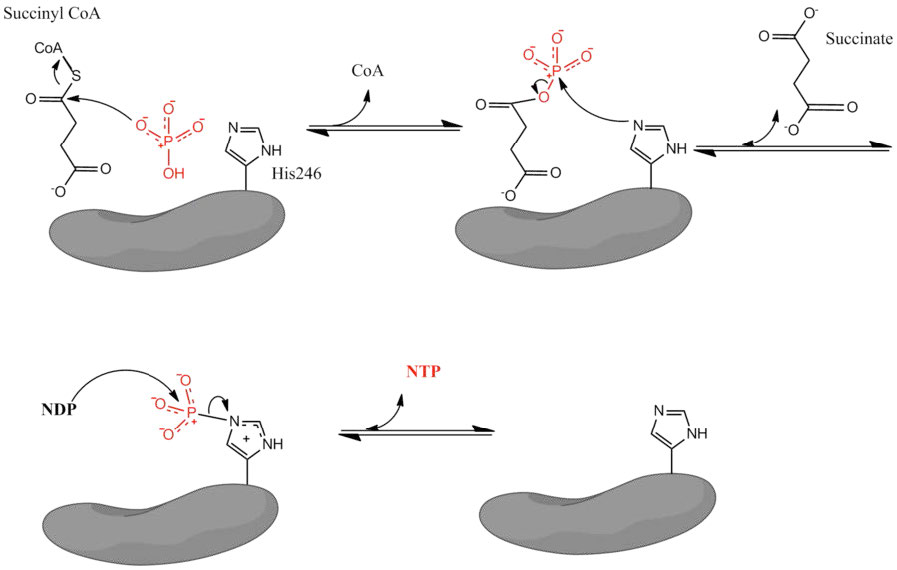
El resto del ciclo del ácido cítrico implica la conversión del succinil-CoA de cuatro carbonos en oxaloacetato. La succinil-CoA es un punto de ramificación para la síntesis de hemo (ver AQUÍ). La succinil-CoA se convierte en succinato en una reacción catalizada por succinil-CoA sintetasa (llamada así por la reacción inversa) y también se produce un GTP, el único nivel de fosforilación de sustrato en el ciclo.
La energía para la síntesis del GTP proviene de la hidrólisis del enlace tioéster de alta energía entre el succinato y el CoA-SH. La evidencia de la alta energía de un enlace tioéster también es evidente en la reacción de citrato sintasa, que también es muy favorable energéticamente. El succinato también se produce por el metabolismo de los ácidos grasos de cadena impar (ver AQUÍ).
Oxidación de succinato
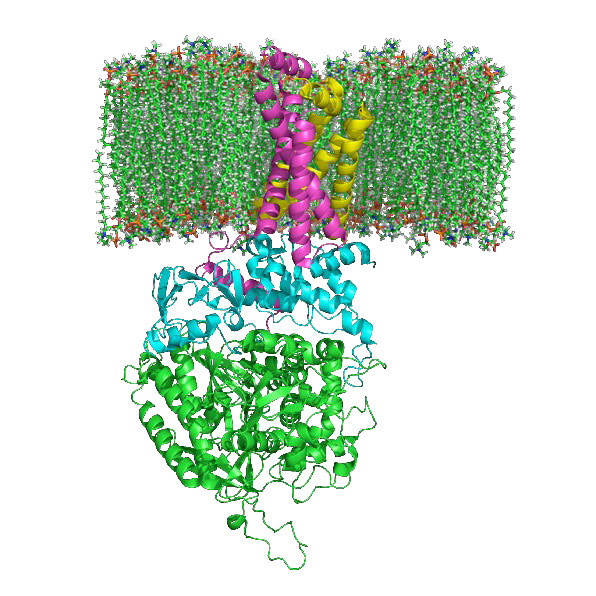
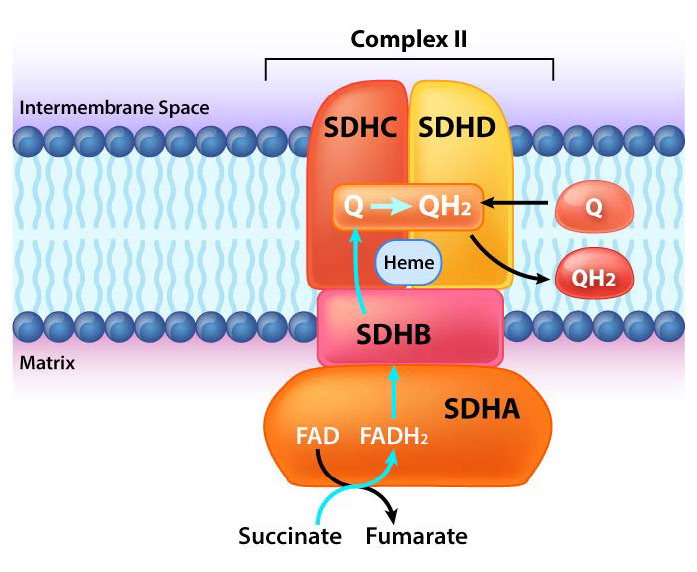
La oxidación del succinato ocurre en la siguiente etapa, catalizada por la succinato deshidrogenasa. Esta interesante enzima cataliza esta reacción y participa en el sistema de transporte de electrones, canalizando electrones del FADH2 que gana en la reacción a la coenzima Q. El producto de la reacción, fumarato, gana un agua a través de su doble enlace trans en la siguiente reacción, catalizada por fumarasa para formar malato.
El fumarato también es un subproducto del metabolismo de los nucleótidos y del ciclo de la urea. El malato es importante también para transportar electrones a través de las membranas en la lanzadera de malato-aspartato (ver AQUÍ) y para transportar dióxido de carbono desde las células mesófilas a las células de vaina agrupadas en plantas C4 (ver AQUÍ).
Oxidación rara
La conversión de malato a oxaloacetato por malato deshidrogenasa es una rara oxidación biológica que tiene un ∆G°' con un valor positivo (29.7 kJ/mol).
La reacción es 'arrastrada' por la conversión energéticamente favorable de oxaloacetato en citrato en la reacción de citrato sintasa descrita anteriormente. El oxaloacetato cruza otras vías importantes, incluyendo el metabolismo de los aminoácidos (fácilmente convertido en ácido aspártico), la transaminación (movimiento del nitrógeno) y la gluconeogénesis.
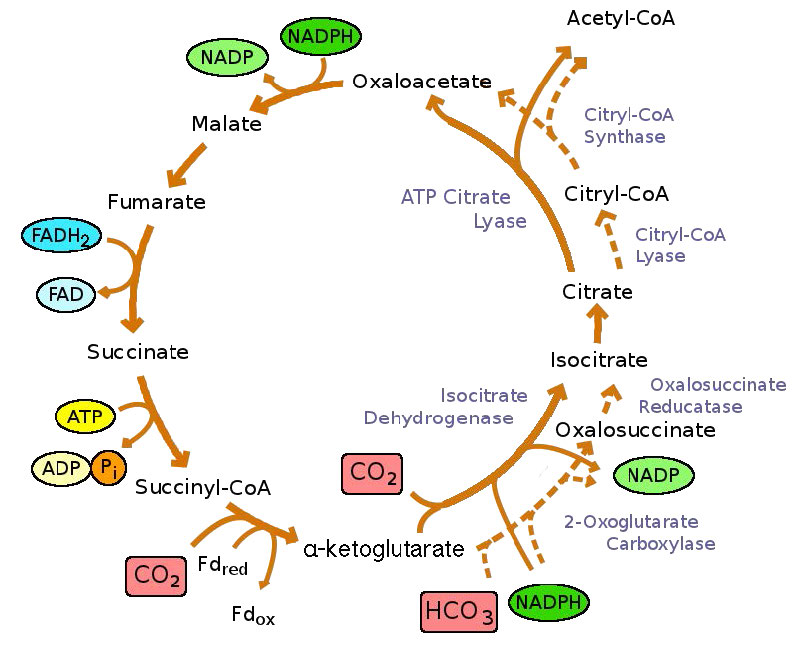
Vale la pena señalar que la inversión del ciclo del ácido cítrico teóricamente proporciona un mecanismo para asimilar CO2. De hecho, esta inversión se ha observado tanto en bacterias anaerobias como microaerobias, donde se denomina ciclo Arnon-Buchanan (Figura 6.73).
Regulación del ciclo del ácido cítrico
La regulación alostérica del ciclo del ácido cítrico es bastante sencilla. Las moléculas involucradas son todos sustratos/productos de la ruta o moléculas involucradas en la transferencia de energía. Los sustratos/productos que regulan o afectan la vía incluyen acetil-CoA y succinil-CoA.
Inhibidores y activadores
Los indicadores moleculares de alta energía, como ATP y NADH, tenderán a inhibir el ciclo y los indicadores de baja energía (NAD+, AMP y ADP) tenderán a activar el ciclo. La piruvato deshidrogenasa, que cataliza la formación de acetil-CoA para la entrada al ciclo, es inhibida alostéricamente por su producto (acetil-CoA), así como por NADH y ATP.
Enzimas reguladas
Las enzimas reguladas en el ciclo incluyen citrato sintasa (inhibida por NADH, ATP y succinil-CoA), isocitrato deshidrogenasa (inhibida por ATP, activada por ADP y NAD+) y α-cetoglutarato deshidrogenasa (inhibida por NADH y succinil-CoA y activada por AMP).
Vía anaplerótica/cataplerótica
El ciclo del ácido cítrico es una importante vía catabólica que oxida acetil-CoA en CO2 y genera ATP, pero también es una fuente importante de moléculas que necesitan las células y un mecanismo para extraer energía de aminoácidos en la descomposición de proteínas y otros productos de descomposición. Esta capacidad del ciclo del ácido cítrico para suministrar moléculas según sea necesario y para absorber subproductos metabólicos da una gran flexibilidad a las células. Cuando se toman intermedios del ciclo del ácido cítrico de la vía para hacer otras moléculas, el término utilizado para describirlo es cataplerótico, mientras que cuando se agregan moléculas a la ruta, el proceso se describe como anaplerótico.
Moléculas catapleróticas
Las moléculas catapleróticas primarias del ciclo del ácido cítrico incluyen α-cetoglutarato, succinil-CoA y oxaloacetato. La transaminación de α-cetoglutarato y oxaloacetato produce los aminoácidos glutamato y ácido aspártico, respectivamente. El oxaloacetato es importante para la producción de glucosa en la gluconeogénesis.
El glutamato juega un papel muy importante en el movimiento del nitrógeno a través de las células a través de la glutamina y otras moléculas y también es necesario para la síntesis de purinas. El aspartato es un precursor de otros aminoácidos y para la producción de nucleótidos de pirimidina. La succinil-CoA es necesaria para la síntesis de porfirinas, como los grupos hemo en hemoglobina, mioglobina y citocromos.
El citrato es una fuente importante de acetil-CoA para la elaboración de ácidos grasos. Cuando la concentración de citrato es alta (como cuando el ciclo del ácido cítrico se mueve lentamente o se detiene), se traslada a través de la membrana mitocondrial hacia el citoplasma y se descompone por la enzima citrato liasa a oxaloacetato y acetil-CoA. Este último es un precursor para la síntesis de ácidos grasos en el citoplasma.
Moléculas anapleróticas
Las moléculas anapleróticas que reponen los intermedios del ciclo del ácido cítrico incluyen acetil-CoA (hecho en muchas vías, incluida la oxidación de ácidos grasos, descarboxilación de piruvato, catabolismo de aminoácidos y descomposición de cuerpos cetónicos), α-cetoglutarato (del metabolismo de aminoácidos), succinil-CoA (del metabolismo del ácido propiónico ), fumarato (del ciclo de la urea y metabolismo de la purina), malato (carboxilación de PEP en plantas) y oxaloacetato (muchas fuentes, incluyendo el catabolismo de aminoácidos y la acción de la piruvato carboxilasa sobre el piruvato en la gluconeogénesis)
Ciclo de glioxilato
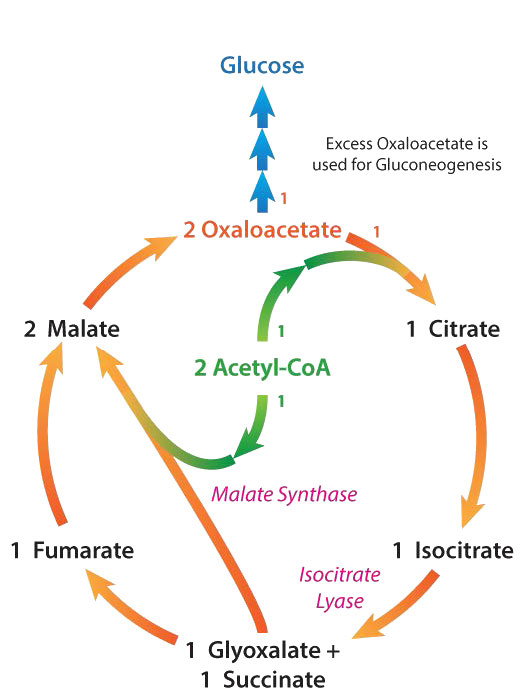
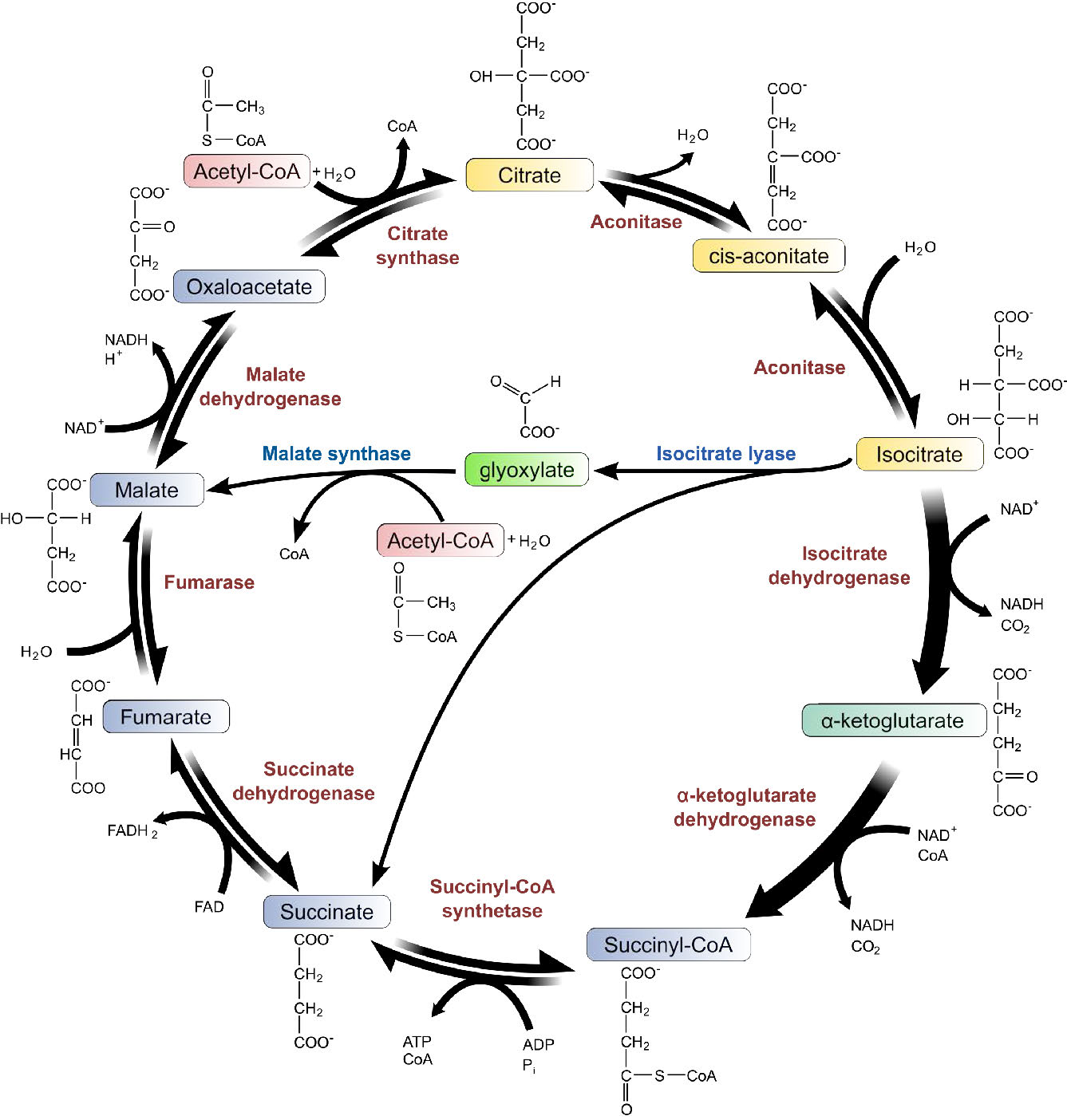
Una vía relacionada con el ciclo del ácido cítrico que solo se encuentra en plantas y bacterias es el ciclo del glioxilato (Figuras 6.74 y 6.75). El ciclo del glioxilato, que elude las reacciones de descarboxilación mientras usa la mayoría de las reacciones de no descarboxilación del ciclo del ácido cítrico, no opera en animales, porque carecen de dos enzimas necesarias para ello: la isocitrato liasa y la malato sintasa. El ciclo ocurre en peroxisomas vegetales especializados llamados glioxisomas. La isocitrato liasa cataliza la conversión de isocitrato en succinato y glioxilato. Debido a esto, los seis carbonos del ciclo del ácido cítrico sobreviven a cada giro del ciclo y no terminan como dióxido de carbono.
El succinato continúa a través de las reacciones restantes para producir oxaloacetato. El glioxilato se combina con otro acetil-CoA (se utilizó un acetil-CoA para iniciar el ciclo) para crear malato (catalizado por malato sintasa). El malato puede, a su vez, oxidarse a oxaloacetato.
Es en este punto que el contraste de la vía del glioxilato con el ciclo del ácido cítrico es evidente. Después de una vuelta del ciclo del ácido cítrico, se produce un solo oxaloacetato y equilibra el único utilizado en la primera reacción del ciclo. Así, en el ciclo del ácido cítrico, no hay producción neta de oxaloacetato en cada giro del ciclo.
Producción neta de oxaloacetato
Por otro lado, gracias a la asimilación de carbonos de dos moléculas de acetil-CoA, cada giro del ciclo del glioxilato da como resultado la producción de dos oxaloacetatos, después de comenzar con uno. El oxaloacetato extra del ciclo del glioxilato se puede utilizar para elaborar otras moléculas, incluyendo la glucosa en la gluconeogénesis. Esto es particularmente importante para la germinación de semillas de plantas (Figura 6.76), ya que la plántula no está expuesta a la luz solar. Con el ciclo del glioxilato, las semillas pueden producir glucosa a partir de los lípidos almacenados.
Debido a que los animales no ejecutan el ciclo del glioxilato, no pueden producir glucosa a partir de acetil-CoA en cantidades netas, pero las plantas y las bacterias sí pueden. Como resultado, las plantas y las bacterias pueden convertir acetil-CoA de grasa en glucosa, mientras que los animales no pueden. Pasar por alto las descarboxilaciones oxidativas (y la fosforilación a nivel de sustrato) tiene costos de energía, pero también hay beneficios. Cada giro del ciclo del glioxilato produce un FADH2 y un NADH en lugar de los tres NADH, un FADH2 y un GTP hechos en cada giro del ciclo del ácido cítrico.

Necesidades de carbohidratos
Los organismos que producen paredes celulares, como plantas, hongos y bacterias, necesitan grandes cantidades de carbohidratos a medida que crecen para apoyar la biosíntesis de los complejos polisacáridos estructurales de las paredes. Estos incluyen celulosa, glucanos y quitina. Notablemente, cada uno de los organismos puede operar el ciclo del glioxilato usando acetil-CoA a partir de β-oxidación.
Coordinación del ciclo del glioxilato y del ciclo del ácido cítrico
El ciclo del ácido cítrico es una vía catabólica importante que produce una cantidad considerable de energía para las células, mientras que la función principal del ciclo del glioxilato es anabólica, para permitir la producción de glucosa a partir de ácidos grasos en plantas y bacterias. Las dos vías están físicamente separadas entre sí (ciclo de glioxilato en glioxisomas/ciclo del ácido cítrico en mitocondrias), pero sin embargo una regulación coordinada de las mismas es importante.
La enzima que parece proporcionar controles para el ciclo es la isocitrato deshidrogenasa. En plantas y bacterias, la enzima puede ser inactivada por fosforilación por una quinasa que se encuentra únicamente en esas células. La inactivación hace que el isocitrato se acumule en la mitocondria y cuando esto sucede, se deriva a los glioxisomas, favoreciendo el ciclo del glioxilato. La eliminación del fosfato de la isocitrato deshidrogenasa es catalizada por una fosfoproteína fosfatasa específica de isocitrato deshidrogneasa y restaura la actividad de la enzima.
Cuando esto sucede, la oxidación del isocitrato se reanuda en la mitocondria junto con el resto de las reacciones del ciclo del ácido cítrico. En bacterias, donde las enzimas para ambos ciclos están presentes juntas en el citoplasma, la acumulación de intermedios del ciclo del ácido cítrico y los intermedios de glucólisis tenderán a favorecer el ciclo del ácido cítrico activando la fosfatasa, mientras que las condiciones de alta energía tenderán a favorecer el ciclo del glioxilato al inhibiéndola.
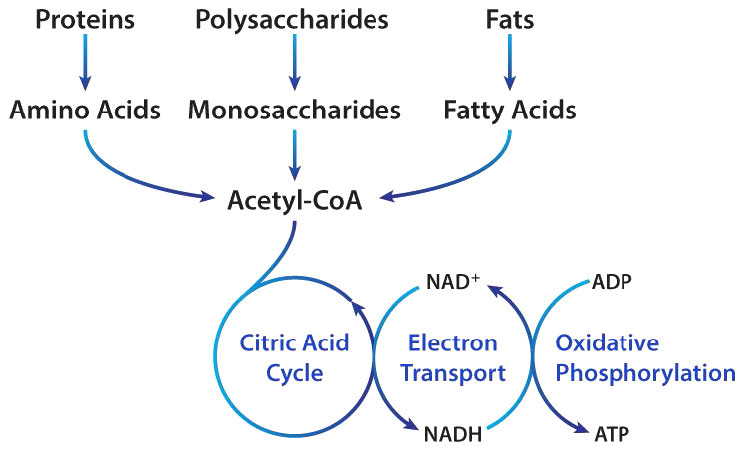
Metabolismo acetil-CoA
El acetil-CoA es uno de los metabolitos más “conectados” en la bioquímica, apareciendo en la oxidación/síntesis de ácidos grasos, la oxidación del piruvato, el ciclo del ácido cítrico, el anabolismo/catabolismo de aminoácidos, el metabolismo del cuerpo cetónico, la síntesis de esteroides/ácidos biliares y (por extensión del metabolismo de los ácidos grasos) la síntesis de prostaglandinas . La mayoría de estas vías se tratarán por separado. Aquí cubriremos el metabolismo del cuerpo cetónico.
Metabolismo corporal cetónico
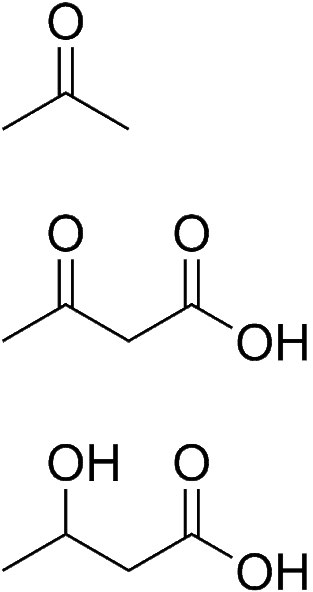
Los cuerpos cetónicos son moléculas que se producen cuando los niveles de glucosa en sangre caen muy bajos. Los cuerpos cetónicos pueden convertirse en acetil-CoA invirtiendo la reacción de la vía que los produce (Figura 6.78). El acetil CoA, por supuesto, se puede usar para la síntesis de ATP a través del ciclo del ácido cítrico. Las personas que son muy hipoglucémicas (incluyendo algunos diabéticos) producirán cuerpos cetónicos (Figura 6.79) y estos suelen ser detectados primero por el olor a acetona en su aliento.
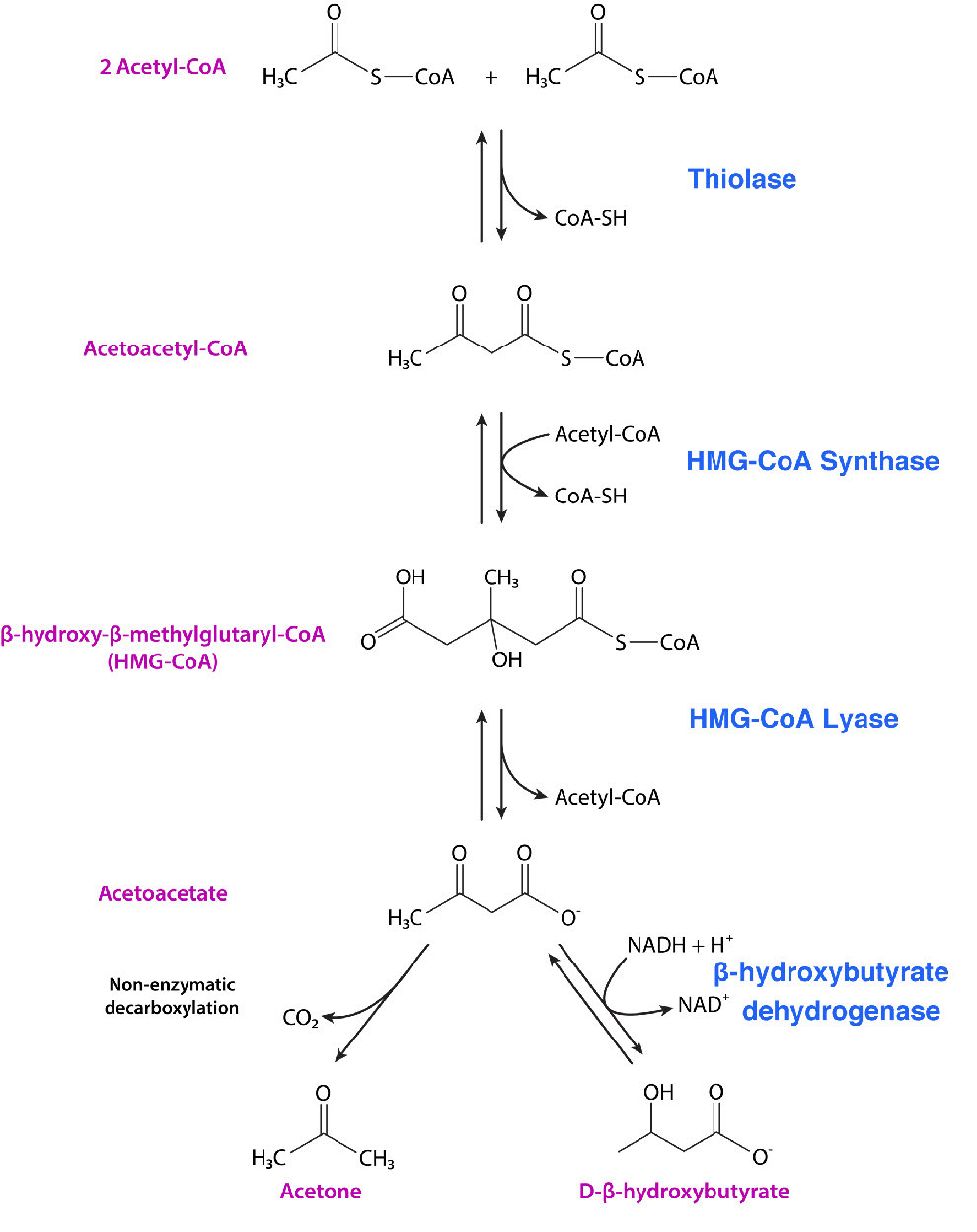
Vías superpuestas
Las vías para la síntesis de cuerpos cetónicos y la biosíntesis de colesterol (Figura 6.80 y ver AQUÍ) se superponen al principio. Cada uno de estos comienza combinando dos acetil-CoA juntos para hacer acetoacetil-CoA. No casualmente, ese es el último producto de la β-oxidación de ácidos grasos con números pares de carbonos (ver AQUÍ para la oxidación de ácidos grasos). De hecho, la enzima que cataliza la unión es la misma que la que cataliza su rotura en la oxidación de ácidos grasos —la tiolasa—. Así, estas vías comienzan por revertir el último paso de la última ronda de oxidación de ácidos grasos.
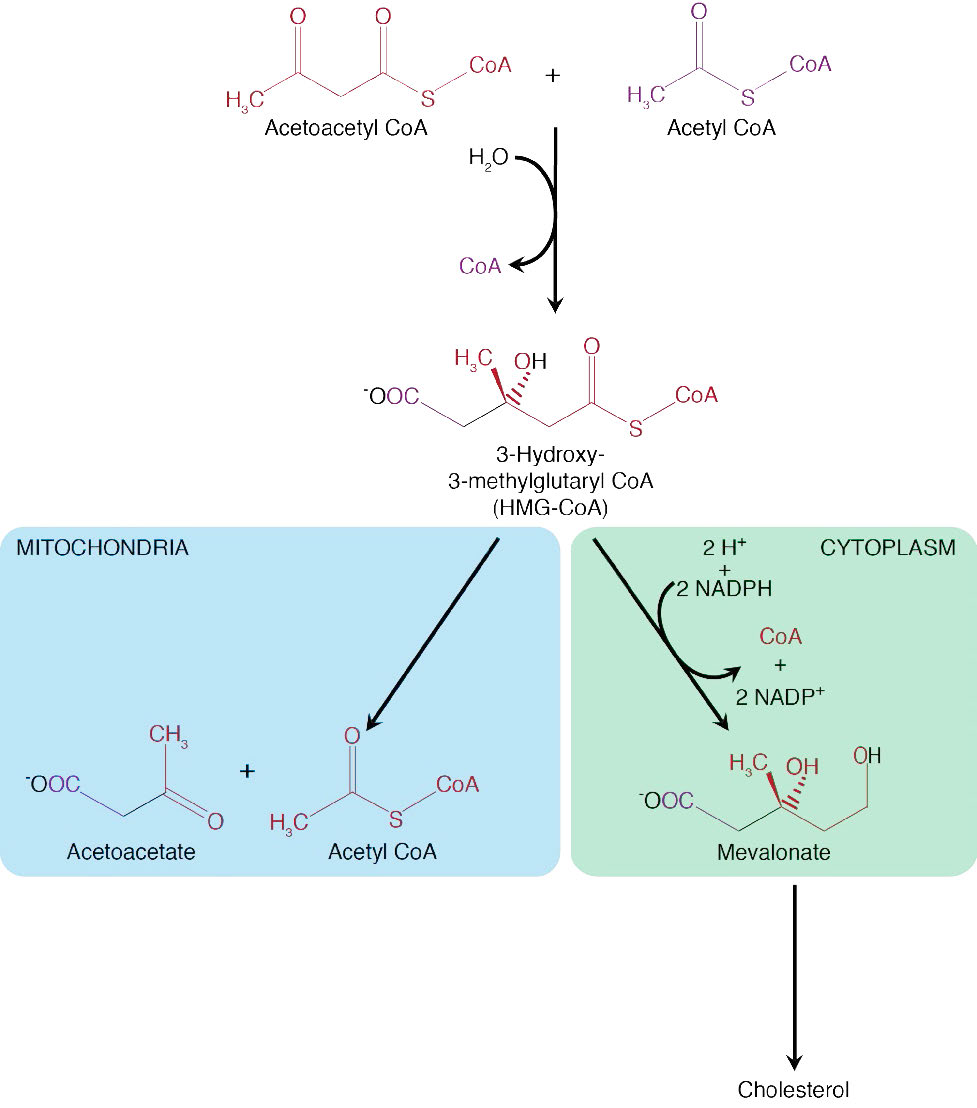
Formación de HMG-CoA
Ambas vías también incluyen la adición de dos carbonos más a acetoacetil-CoA a partir de un tercer acetil-CoA para formar hidroxi-metil-glutaril-CoA, o HMG-CoA, como se conoce más comúnmente. Es en este punto que los dos caminos divergen. HMG-CoA es un punto de ramificación entre las dos vías y puede llegar a convertirse en colesterol o cuerpos cetónicos. En esta última vía, la HMG-CoA se descompone en acetil-CoA y acetoacetato.
El acetoacetato es en sí mismo un cuerpo cetónico y se puede reducir para formar otro, el D-β-hidroxibutirato (aunque en realidad no es una cetona). Alternativamente, el acetoacetato se puede convertir en acetona. Esta última reacción puede ocurrir ya sea espontáneamente o vía catálisis por acetoacetato descarboxilasa. La acetona se puede convertir en piruvato y el piruvato se puede convertir en glucosa.
El D-β-hidroxibutirato viaja fácilmente en la sangre y cruza la barrera hematoencefálica. Se puede oxidar de nuevo a acetoacetato, convertirse en acetoacetil-CoA, y luego descomponer en dos moléculas de acetil-CoA para la oxidación en el ciclo del ácido cítrico.
Cetosis
Cuando un cuerpo está produciendo cuerpos cetónicos por su energía, este estado en el cuerpo se conoce como cetosis. La formación de cuerpos cetónicos en el hígado es crítica. Normalmente la glucosa es la fuente de energía primaria del cuerpo. Proviene de la dieta, de la descomposición de los carbohidratos de almacenamiento, como el glucógeno, o de la síntesis de glucosa (gluconeogénesis). Dado que las reservas primarias de glucógeno se encuentran en los músculos y el hígado y dado que la gluconeogénesis ocurre solo en hígado, riñón y gametos, cuando se interrumpe el suministro de glucosa por cualquier motivo, el hígado debe suministrar una fuente de energía alternativa.
De la descomposición de ácidos grasos
A diferencia de la glucosa, los cuerpos cetónicos pueden elaborarse en animales a partir de la descomposición de grasas/ácidos grasos. La mayoría de las células del cuerpo pueden usar cuerpos cetónicos como fuentes de energía. La cetosis puede surgir del ayuno, una dieta muy baja en carbohidratos o, en algunos casos, la diabetes.
Acidosis
El término acidosis se refiere a afecciones en el cuerpo donde el pH de la sangre arterial cae por debajo de 7.35. Es lo opuesto a la condición de alcalosis, donde el pH de la sangre arterial se eleva por encima de 7.45. Normalmente, el pH de la sangre permanece en este estrecho rango de pH. Los valores de pH de la sangre inferiores a 6.8 o superiores a 7.8 pueden causar daños irreversibles y pueden ser fatales. La acidosis puede tener raíces en el metabolismo (acidosis metabólica) o en la respiración (acidosis respiratoria).
Existen varias causas de acidosis. En la acidosis metabólica, la producción de exceso de ácido láctico o la falla de los riñones para excretar ácido puede hacer que el pH de la sangre baje. El ácido láctico se produce en el organismo cuando el oxígeno es limitante, por lo que cualquier cosa que interfiera con el suministro de oxígeno puede crear condiciones que favorezcan la producción de exceso de ácido láctico. Estos pueden incluir restricciones en el movimiento de la sangre hacia los tejidos diana, dando como resultado hipoxia (condiciones de bajo oxígeno) o disminuciones en el volumen sanguíneo. Los problemas con el movimiento de la sangre pueden ser el resultado de problemas cardíacos, presión arterial baja o hemorragia.
El ejercicio extenuante también puede resultar en la producción de ácido láctico debido a la incapacidad del suministro de sangre para entregar oxígeno tan rápido como lo requieran los tejidos (shock hipovolémico). Sin embargo, al final del ejercicio, el suministro de oxígeno a través del sistema sanguíneo se pone al día rápidamente.
La acidosis respiratoria surge de la acumulación de dióxido de carbono en la sangre. Las causas incluyen hipoventilación, problemas pulmonares, enfisema, asma y neumonía grave.
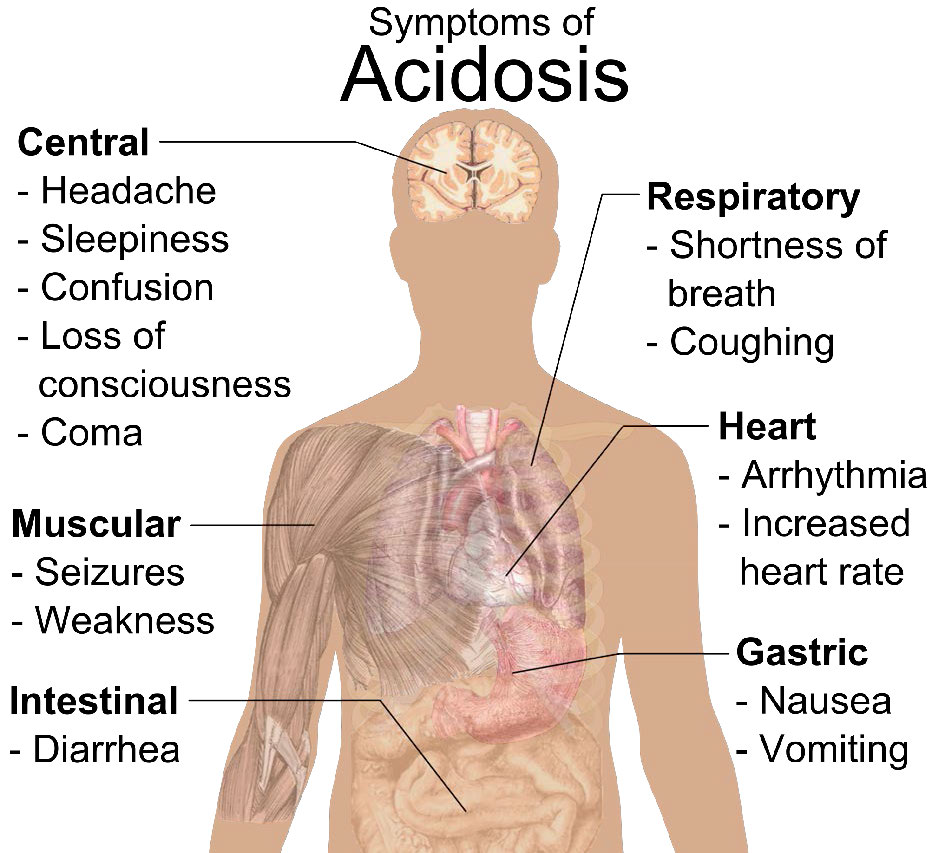
Figura 6.81 - Síntomas de acidosis


