7.3: Replicación de ADN
- Page ID
- 52992
Fuente: BiochemFFA_7_2.pdf. Todo el libro de texto está disponible gratuitamente de los autores en http://biochem.science.oregonstate.edu/content/biochemistry-free-and-easy
Instrucciones para copiar
La única manera de hacer nuevas células es mediante la división de células preexistentes. Los organismos unicelulares experimentan división para producir más células como ellos mismos, mientras que los organismos multicelulares surgen a través de la división de una sola célula, generalmente el óvulo fertilizado. Cada vez que una célula se divide, todo su ADN debe copiarse fielmente para que una copia de esta información pueda transmitirse a la célula hija. Este proceso se llama replicación del ADN. Es el medio por el cual la información genética puede transmitirse a través de generaciones de células, y asegura que cada nueva célula tenga una copia completa del genoma. En la siguiente sección, examinaremos el proceso por el cual se copia completa y con precisión el ADN de una célula.
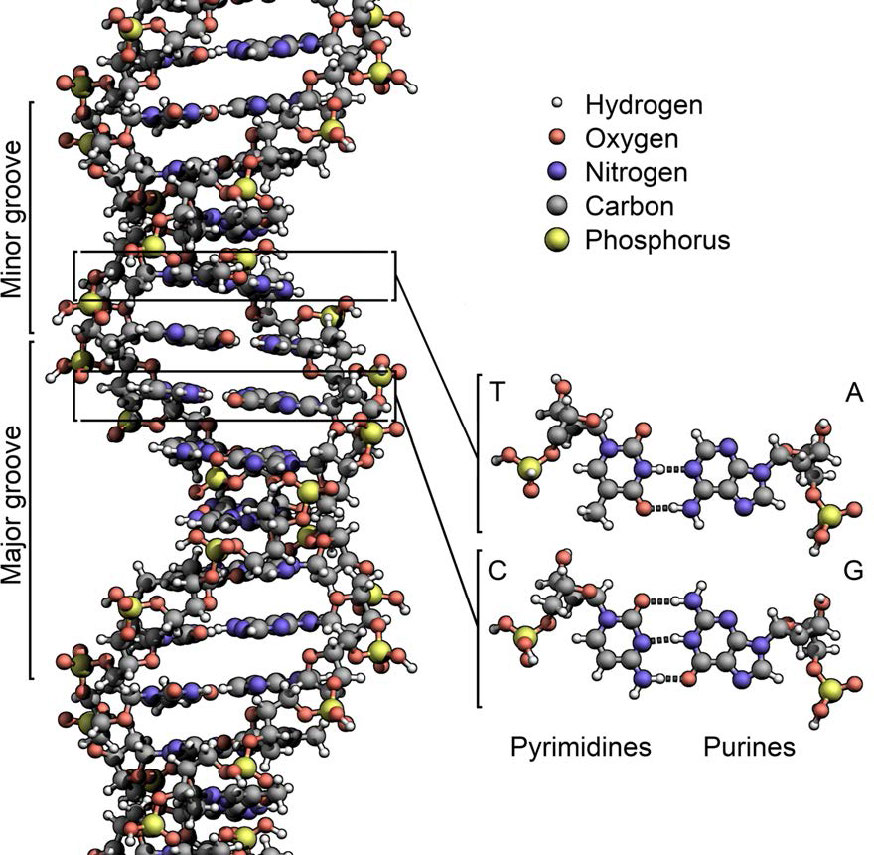
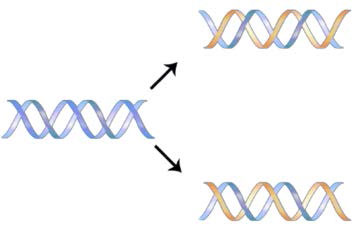
La estructura del ADN dilucidada por Watson y Crick en 1953 sugirió inmediatamente un mecanismo por el cual el ADN bicatenario podría copiarse para dar dos copias idénticas del ADN. Propusieron que las dos cadenas de la molécula de ADN, que se mantienen unidas por enlaces de hidrógeno entre los nucleótidos pares de bases, se separarían y cada una serviría como molde sobre el que podría ensamblarse una cadena complementaria (Figura 7.8). Las reglas de emparejamiento de bases asegurarían que este proceso resultaría en la producción de dos moléculas de ADN idénticas. Se demostró que la hermosa simplicidad de este esquema era correcta en experimentos posteriores de Meselson y Stahl, que demostraron que la replicación del ADN era semiconservadora, es decir, que después de la replicación, cada una de las dos moléculas de ADN resultantes estaba compuesta por una hebra vieja y una nueva hebra que había sido ensamblado a través de él (Figura 7.9).
Materiales de construcción
¿Cuáles son los ingredientes necesarios para construir una nueva molécula de ADN? Como se señaló anteriormente, la molécula de ADN original o parental sirve como molde. Las nuevas moléculas de ADN se ensamblan a través de cada molde uniendo nucleótidos de ADN libres según lo dirigido por las reglas de emparejamiento de bases, con As frente a Ts y Gs a través de Cs.
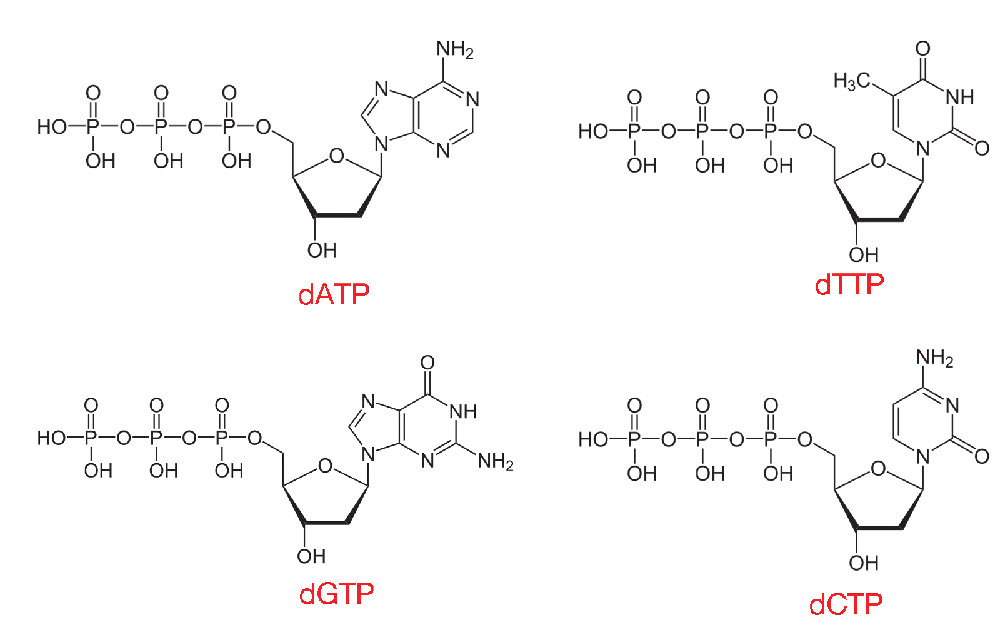
Los nucleótidos utilizados en la síntesis de ADN son desoxirribonucleósido trifosfatos o dNTPs. Como se puede deducir de su nombre, dichos nucleótidos tienen un azúcar desoxirribosa y tres fosfatos, además de una de las cuatro bases de ADN, A, T, C o G (Figura 7.10).
Cuando se agregan dNTP a una cadena de ADN en crecimiento, dos de esos fosfatos se escindirán, como se describe más adelante, dejando los nucleótidos en una molécula de ADN con solo un fosfato por nucleótido. Esta reacción es catalizada por enzimas conocidas como ADN polimerasas, que crean enlaces fosfodiéster entre un nucleótido y el siguiente.
Desafíos
Antes de examinar el proceso real de replicación del ADN, es útil pensar en lo que se necesita para lograr esta tarea con éxito. Considere los desafíos que enfrenta una célula en este proceso:
- El gran número de nucleótidos a copiar es enorme: e.g., en células humanas, del orden de varios miles de millones.
- Se debe desenrollar una molécula de ADN parental de doble hélice para exponer cadenas individuales de ADN que puedan servir como moldes para la síntesis de nuevas cadenas de ADN.
- El desenrollado debe realizarse sin introducir distorsión topológica en la molécula.
- Se debe evitar que las cadenas individuales desenrolladas de ADN se vuelvan a unir el tiempo suficiente para que las nuevas cadenas sean sintetizadas.
- Las ADN polimerasas no pueden comenzar la síntesis de una nueva cadena de ADN de novo y requieren un OH 3' libre al que pueden agregar desoxinucleótidos.
- Las ADN polimerasas solo pueden extender una cadena en la dirección 5' a 3'. El crecimiento de 5' a 3' de ambas nuevas hebras significa que una de las hebras está hecha en trozos.
- El uso de cebadores de ARN requiere que los nucleótidos de ARN se eliminen y reemplacen con nucleótidos de ADN y se deben unir los fragmentos de ADN resultantes.
- La copia de todo el ADN parental debe ser precisa, para que no se introduzcan mutaciones en el ADN recién hecho.
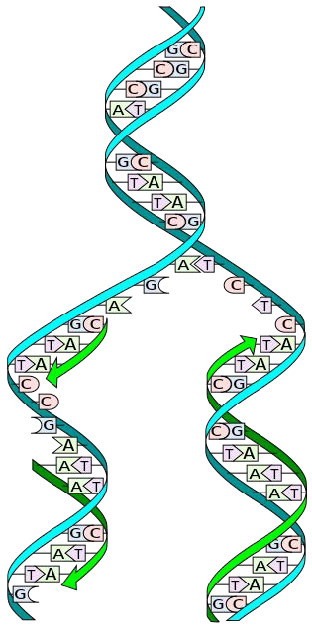

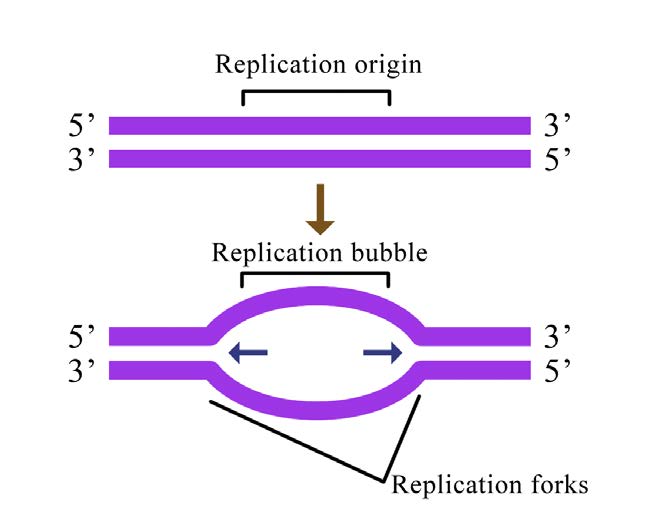
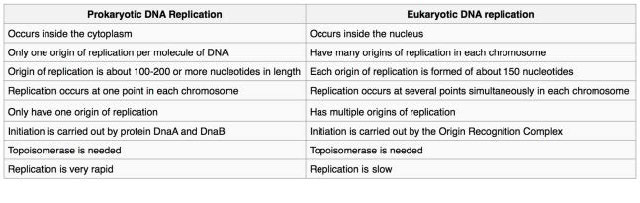
Figura 7.14 - Replicación de ADN procariota vs. eucariota - Wikipedia, la
Abordar desafíos
Con esto en mente, podemos comenzar a examinar cómo las células afrontan cada uno de estos desafíos. Nuestra comprensión del proceso de replicación del ADN se deriva de estudios que utilizan bacterias, levaduras y otros sistemas. Estas investigaciones han revelado que la replicación del ADN se lleva a cabo por la acción de un gran número de proteínas que actúan juntas como una compleja máquina proteica. Numerosas proteínas involucradas en la replicación han sido identificadas y caracterizadas, incluyendo múltiples ADN polimerasas diferentes tanto en procariotas como eucariotas. Aunque las proteínas específicas involucradas son diferentes en bacterias y eucariotas, es útil comprender las consideraciones básicas que son relevantes en todas las células. A continuación se presenta un relato generalizado de los pasos en la replicación del ADN, enfocado en los desafíos mencionados anteriormente.
- El gran número de nucleótidos a copiar es enorme: e.g., en células humanas, del orden de varios miles de millones.
Las células, ya sean bacterianas o eucariotas, tienen que replicar todo su ADN antes de que puedan dividirse. En células como la nuestra, la gran cantidad de ADN se descompone en muchos cromosomas, cada uno de los cuales está compuesto por una cadena lineal de ADN (Figura 7.12). En células como las de E. coli, hay un solo cromosoma circular.
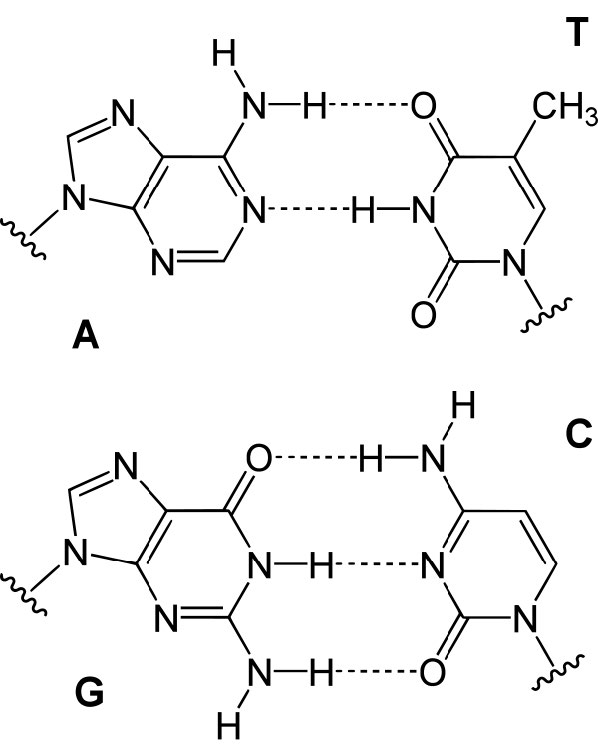
En cualquier situación, la replicación del ADN se inicia en sitios llamados orígenes de replicación. Estas son regiones de la molécula de ADN que son reconocidas por proteínas especiales llamadas proteínas iniciadoras que se unen al ADN. En E. coli, los orígenes tienen pequeñas regiones de secuencias ricas en A-T que se “funden” para separar las cadenas, cuando las proteínas iniciadoras se unen al origen o replicación. Como recordará, los pares de bases A-T, que tienen dos enlaces de hidrógeno entre ellos, se rompen más fácilmente que los pares de bases G-C que tienen tres cada uno (Figura 7.15).
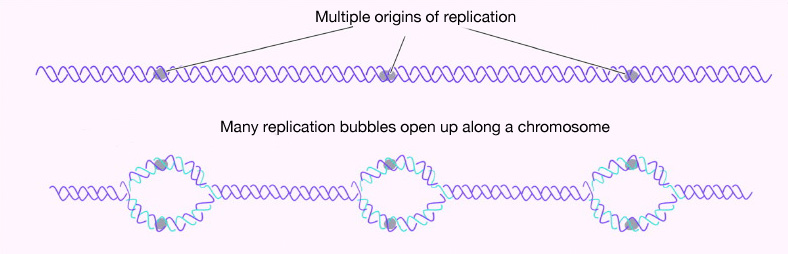
¿Cuántos orígenes de replicación hay en un cromosoma? En el caso de E. coli, existe un único origen de replicación en su cromosoma circular. En las células eucariotas puede haber muchos miles de orígenes de replicación, teniendo cada cromosoma cientos (Figura 7.16). Por lo tanto, la replicación del ADN se inicia en múltiples puntos a lo largo de cada cromosoma en eucariotas. Las micrografías de electrones de ADN replicante de células eucariotas muestran muchas burbujas de replicación en un solo cromosoma. Esto tiene sentido a la luz de la gran cantidad de ADN que hay que copiar en células como la nuestra, donde comenzar en un extremo de cada cromosoma y replicar todo el camino hasta el otro extremo desde un solo origen simplemente llevaría demasiado tiempo. Esto a pesar de que las ADN polimerasas en las células humanas son capaces de construir nuevas cadenas de ADN a una tasa muy respetable de ¡aproximadamente 50 nucleótidos por segundo!
- Se debe desenrollar una molécula parental de doble hélice para exponer cadenas individuales de ADN que puedan servir como moldes para la síntesis de nuevas cadenas de ADN.
Desenrollar
Una vez que se abre una pequeña región del ADN en cada origen de replicación, se debe desenrollar la hélice del ADN para permitir que la replicación continúe. El desenrollamiento de la hélice del ADN requiere la acción de una enzima llamada helicasa.
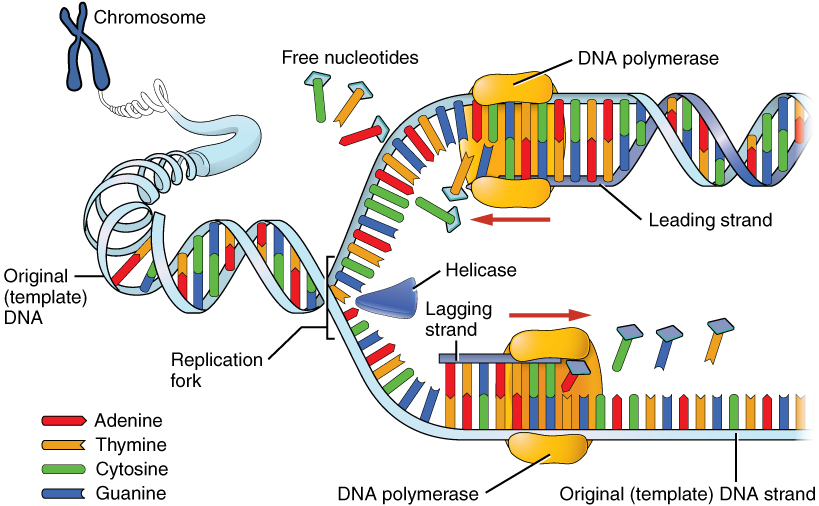
La helicasa utiliza la energía liberada cuando se hidroliza ATP, para romper los enlaces de hidrógeno entre las bases en el ADN y separar las dos cadenas (Figura 7.17). Tenga en cuenta que una burbuja de replicación está compuesta por dos horquillas de replicación que se “mueven” o se abren, en direcciones opuestas. En cada horquilla de replicación, las cadenas de ADN parentales deben desenrollarse para exponer nuevas secciones de molde monocatenario.
- Este desenrollado debe realizarse sin introducir distorsión topológica en la molécula.
¿Cuál es el efecto de desenrollar una región de la doble hélice? El desenrollado local de la doble hélice causa sobrebobinado (aumento del superbobinado positivo) por delante de la región desenrollada.
El ADN delante de la horquilla de replicación tiene que girar, o se retorcerá sobre sí mismo y detendrá la replicación. Este es un problema importante, no sólo para los cromosomas bacterianos circulares, sino también para los cromosomas eucariotas lineales, que, en principio, podrían rotar para aliviar el estrés causado por el aumento del superenrollamiento.
Topoisomerasas
La razón por la que esto es problemático es que no es posible rotar toda la longitud de un cromosoma, con sus millones de pares de bases, ya que el ADN en la horquilla de replicación se desenrolla. ¿Cómo, entonces, se resuelve este problema? Las enzimas llamadas topoisomerasas pueden aliviar el estrés topológico causado por el “desenrollado” local de los vientos extra de la doble hélice. Hacen esto cortando una o ambas hebras del ADN y permitiendo que las hebras giren una alrededor de la otra para liberar la tensión antes de volver a unir los extremos. En E. coli, la topoisomerasa que realiza esta función se llama girasa.
- Se debe evitar que las cadenas individuales separadas de ADN se vuelvan a unir para que las nuevas cadenas sean sintetizadas.
Proteína de unión a ADN monocatenario
Una vez separadas las dos cadenas de la molécula de ADN parental, se debe evitar que vuelvan a estar juntas para formar ADN bicatenario. Para asegurar que las regiones desenrolladas del ADN parental permanezcan monocatenarias y disponibles para copiarse, las cadenas separadas del ADN parental están unidas por muchas moléculas de una proteína llamada proteína de unión al ADN monocatenario (SSB - Figura 7.18).
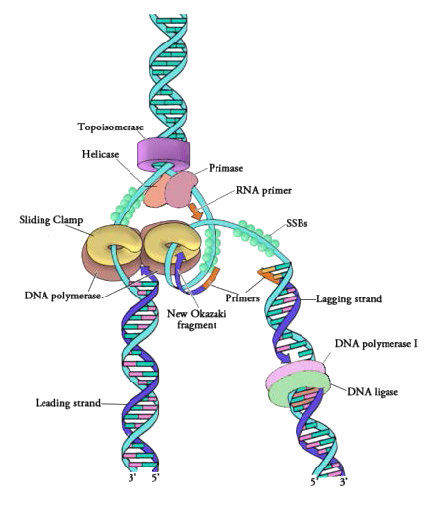
Figura 7.18 - Proteínas en una horquilla de replicación de ADN procariota - Imagen de Martha Baker
- Las ADN polimerasas no pueden comenzar la síntesis de una nueva cadena de ADN de novo y requieren un OH 3' libre al que pueden agregar nucleótidos de ADN.
Aunque el ADN parental monocatenario ya está disponible para copiar, las ADN polimerasas no pueden comenzar la síntesis de una cadena complementaria de novo. Esto simplemente significa que las ADN polimerasas solo pueden agregar nuevos nucleótidos en el extremo 3' de una cadena preexistente, y no pueden iniciar una cadena de nucleótidos por sí mismas. Debido a esta limitación, alguna enzima que no sea una ADN polimerasa debe primero hacer una pequeña región de ácido nucleico, complementaria a la cadena parental, que pueda proporcionar un OH 3' libre al que la ADN polimerasa puede agregar un desoxirribonucleótido. Esta tarea se logra mediante una enzima llamada primasa, que ensambla un tramo corto de ARN emparejado por bases al molde de ADN parental. Esto proporciona una región corta de pares de bases, llamada cebador de ARN, con un grupo 3'OH libre al que la ADN polimerasa puede agregar el primer nucleótido de ADN nuevo (Figura 7.12).
Abrazadera deslizante
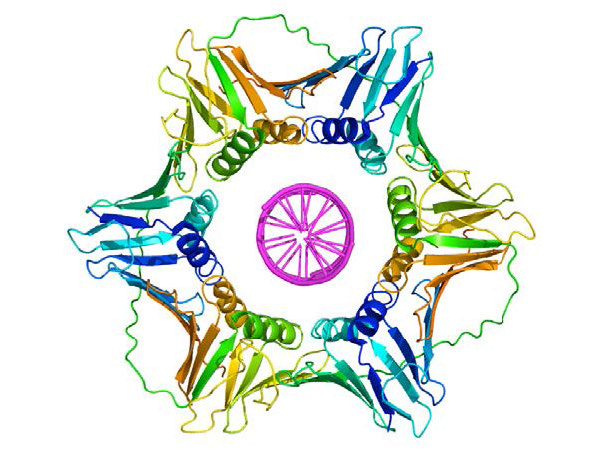
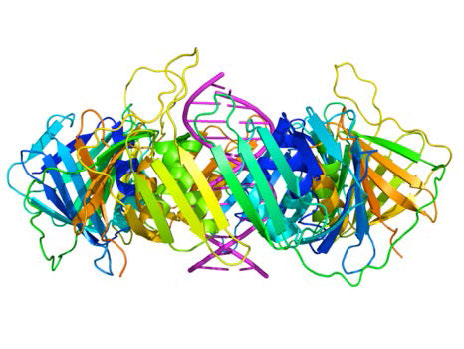
Una vez que un cebador proporciona un 3'OH libre para extensión, otras proteínas entran en el acto. Estas proteínas están involucradas en cargar la ADN polimerasa en el molde cebado y mantenerlo asociado con el ADN. El primero de ellos es el cargador de abrazaderas. Como su nombre indica, la pinza cargadora ayuda a cargar un complejo proteico llamado pinza deslizante sobre el ADN en la horquilla de replicación (Figura 7.19 y 7.20). La pinza deslizante, una proteína en forma de anillo de múltiples subunidades, se une luego por la ADN Polimerasa. La función de la pinza deslizante es mantener la polimerasa asociada con la horquilla de replicación; de hecho, se ha descrito como un cinturón de seguridad para la ADN polimerasa. La pinza deslizante asegura que la ADN polimerasa sea capaz de sintetizar largos tramos de nuevo ADN antes de que se disocie de la plantilla. La propiedad de permanecer asociado con el molde durante mucho tiempo antes de disociarse se conoce como la procesividad de la enzima. En presencia de la pinza deslizante, las ADN polimerasas son mucho más procesativas, lo que hace que la replicación sea más rápida y eficiente.
Extendiendo la imprimación
La ADN polimerasa ahora está preparada para iniciar la síntesis de la nueva cadena de ADN (en E. coli, la polimerasa replicativa primaria se llama ADN polimerasa III). Como ya sabrás, la síntesis de nuevo ADN se logra mediante la adición de nuevos nucleótidos complementarios a los de la cadena parental. La ADN polimerasa cataliza la reacción mediante la cual se agrega un desoxirribonucleótido entrante, complementario al molde, en el extremo 3' del nucleótido anterior, comenzando con el 3'OH en el extremo del cebador de ARN. La importancia del grupo 3'OH radica en la naturaleza de la reacción que construye una cadena de nucleótidos.
La reacción catalizada por la ADN polimerasa se produce a través del ataque nucleófilo del grupo 3'OH al final de una cadena de ácido nucleico sobre el α fosfato del dNTP entrante (Figura 7.21). La hidrólisis inmediata del pirofosfato que se escinde del dNTP entrante impulsa la reacción hacia adelante. La adición secuencial de nuevos nucleótidos en el extremo 3' de la cadena creciente de ADN explica el hecho de que la cadena crece en una dirección 5' a 3'.
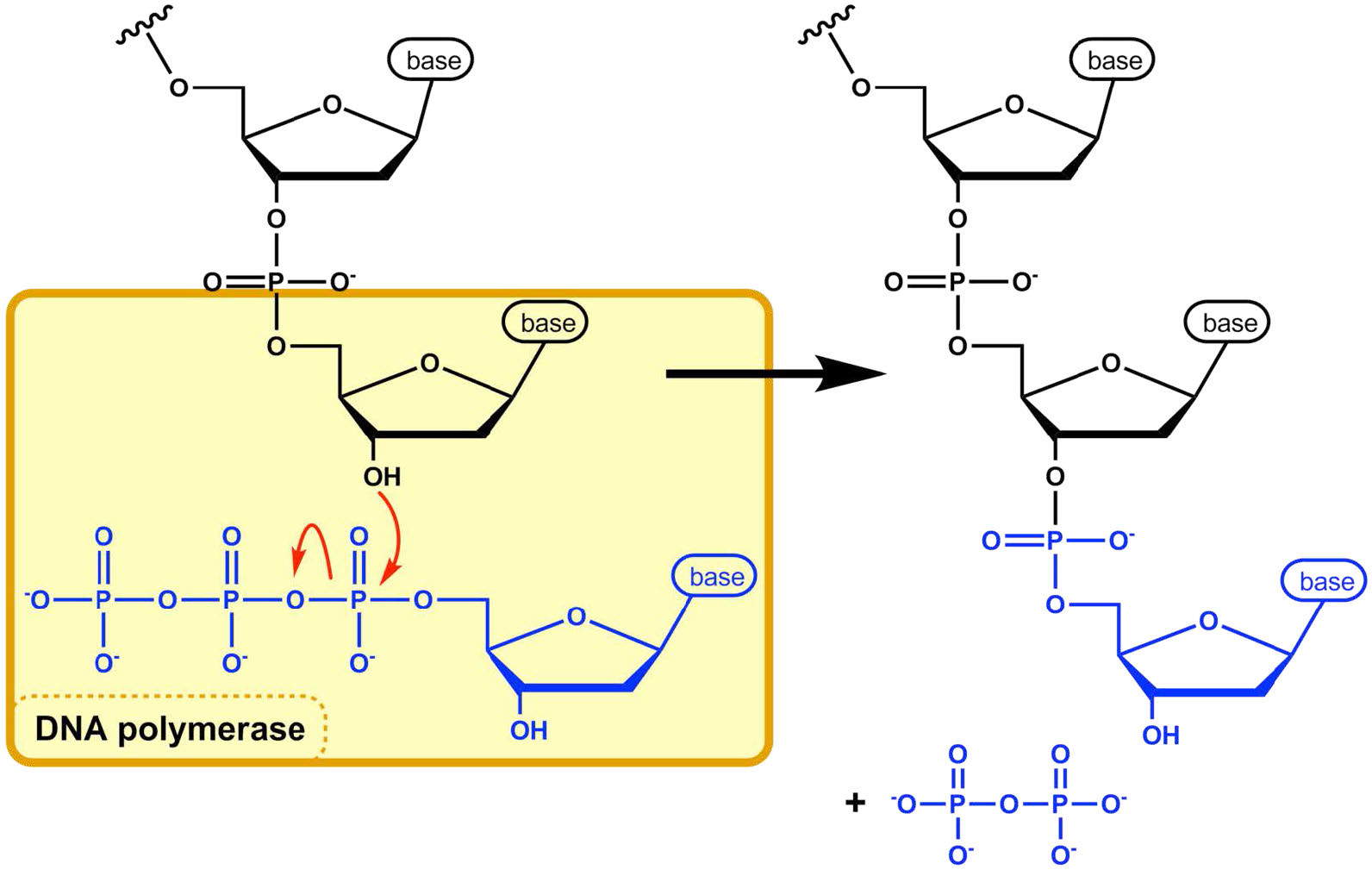
El fosfato 5' en cada nucleótido entrante es unido por la ADN polimerasa al OH 3' en el extremo de la cadena de ácido nucleico en crecimiento, para formar un enlace fosfodiéster. Cada nucleótido agregado proporciona un nuevo 3'OH, permitiendo que la cadena se extienda mientras la ADN polimerasa continúe sintetizando la nueva cadena. Como ya señalamos, las nuevas cadenas de ADN se sintetizan mediante la adición de nucleótidos de ADN al extremo de un cebador de ARN. Por lo tanto, la nueva molécula de ADN tiene una pieza corta de ARN al principio.
- Las ADN polimerasas solo pueden extender una cadena en la dirección 5' a 3'. El crecimiento de 5' a 3' de ambas nuevas hebras significa que una de las hebras está hecha en trozos.
Hetrón principal
Sabemos que las ADN polimerasas solo pueden construir una nueva cadena de ADN en la dirección 5' a 3'. También sabemos que las dos cadenas parentales de ADN son antiparalelas. Esto significa que en cada horquilla de replicación, una nueva hebra, llamada la cadena principal, se puede sintetizar continuamente en la dirección 5' a 3' porque se está haciendo en la misma dirección en la que se está abriendo la horquilla de replicación.
hebra rezagada
La síntesis de la otra nueva hebra, llamada la hebra rezagada, también procede en la dirección 5' a 3'. Pero debido a que las hebras de la plantilla corren en direcciones opuestas, la hebra rezagada se está extendiendo en la dirección opuesta a la abertura de la horquilla de replicación (Figura 7.22). A medida que se abre la bifurcación de replicación, será necesario copiar la región detrás del punto de inicio original para la cadena retrasada. Esto significa que se debe colocar y extender otro cebador de ARN. Este proceso se repite a medida que se abre la bifurcación de replicación, con múltiples cebadores de ARN colocados y extendidos, produciendo muchas piezas cortas que luego se unen. Estas piezas cortas de ácido nucleico, cada una compuesta por un pequeño tramo de cebador de ARN y alrededor de 1000-2000 nucleótidos de ADN, se denominan fragmentos de Okazaki, para Reiji Okazaki, el científico que demostró por primera vez su existencia.
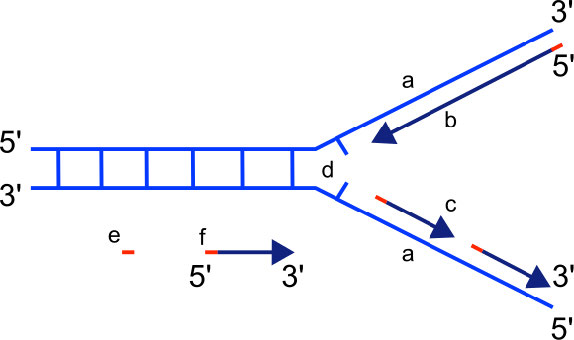
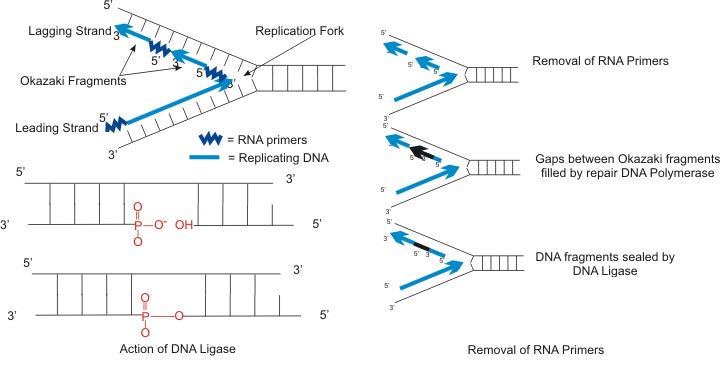
- El uso de cebadores de ARN requiere que los nucleótidos de ARN se eliminen y reemplacen con nucleótidos de ADN.
Eliminación de imprimación
Hemos visto que cada pieza de ADN recién sintetizada comienza con un cebador de ARN, haciendo efectivamente una nueva cadena de ácido nucleico que es parte ARN y parte ADN. No se puede permitir que la cadena de ADN recién hecha tenga fragmentos de ARN unidos. Entonces, se deben eliminar los nucleótidos de ARN y rellenar los huecos con nucleótidos de ADN (Figura 7.23). Esto se realiza mediante ADN polimerasa I en E. coli. Esta enzima comienza a agregar nucleótidos de ADN al final de cada fragmento de Okazaki. Sin embargo, el extremo de un fragmento de Okazaki es adyacente al cebador de ARN al comienzo del siguiente fragmento de Okazaki. La ADN polimerasa I tiene una actividad exonucleasa que actúa en la dirección 5' a 3' que elimina los nucleótidos de ARN por delante de ella, mientras que la actividad polimerasa reemplaza los nucleótidos de ARN con dNTP. Una vez que se han eliminado todos los nucleótidos de ARN, la hebra rezagada se compone de tramos de ADN. Las piezas de ADN son luego unidas entre sí por la enzima ADN ligasa.
Los pasos descritos anteriormente completan esencialmente el proceso de replicación del ADN. Pero aún queda un tema.
- Asegurar precisión en la copia de tanta información
Precisión
¿Qué tan precisa es la copia de la información por la ADN polimerasa? Como ustedes saben, los cambios en la secuencia del ADN (mutaciones) pueden cambiar la secuencia de aminoácidos de las proteínas codificadas y que esto suele ser, aunque no siempre, perjudicial para el funcionamiento del organismo. Cuando se copian miles de millones de bases en el ADN durante la replicación, ¿cómo aseguran las células que el ADN recién sintetizado sea una copia fiel de la información original?
Las ADN polimerasas, como hemos señalado anteriormente funcionan rápido (promediando 50 bases por segundo en células humanas y hasta 200 veces más rápido en E. coli). Sin embargo, tanto las células humanas como las bacterianas parecen replicar su ADN con bastante precisión. Esto se debe a que las ADN polimerasas replicativas tienen una función correctora que permite a la polimerasa detectar cuándo se ha insertado la base incorrecta frente a una cadena molde, retroceder y eliminar la base insertada erróneamente, antes de continuar con la síntesis (Figura 7.24).
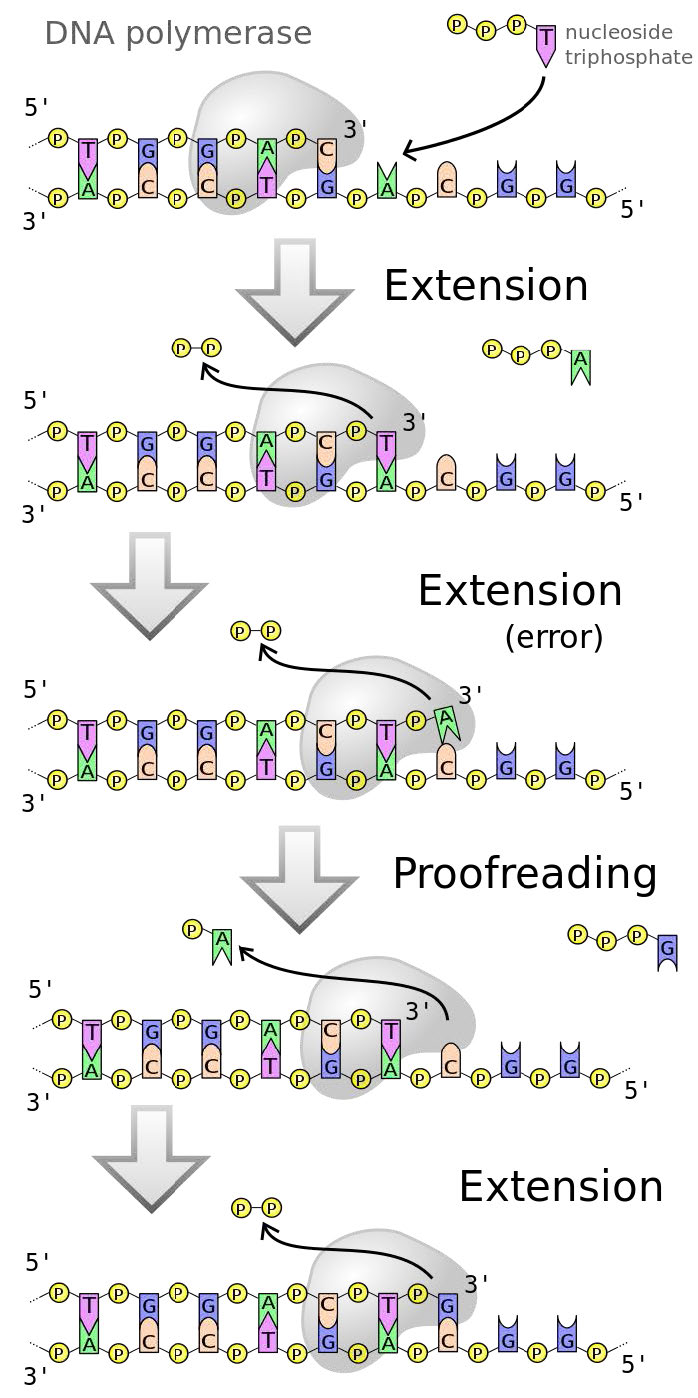
Figura 7.24 - Error corregido por ADN polimerasas
Múltiples actividades
Esto es posible porque la mayoría de las ADN polimerasas son enzimas de doble función. Pueden extender una cadena de ADN en virtud de su actividad polimerasa 5' a 3'. Algunas polimerasas como la ADN polimerasa I también pueden eliminar cebadores de ARN en la dirección 5' a 3', aunque esa no es una actividad común de las polimerasas. Muchas polimerasas, sin embargo, tienen la capacidad de retroceder y eliminar la última base insertada debido a que poseen una actividad exonucleasa de 3' a 5'.
La actividad exonucleasa de una ADN polimerasa le permite extirpar una base insertada erróneamente, después de lo cual la actividad polimerasa inserta la base correcta y procede con la extensión de la cadena.
En otras palabras, la ADN polimerasa está monitoreando su propia precisión (también denominada su fidelidad) a medida que produce nuevo ADN, corrigiendo errores inmediatamente antes de pasar a agregar la siguiente base. Este mecanismo, que opera durante la replicación del ADN, corrige muchos errores a medida que ocurren, reduciendo en aproximadamente 100 veces los errores que se cometen cuando se copia el ADN.
ADN polimerasas
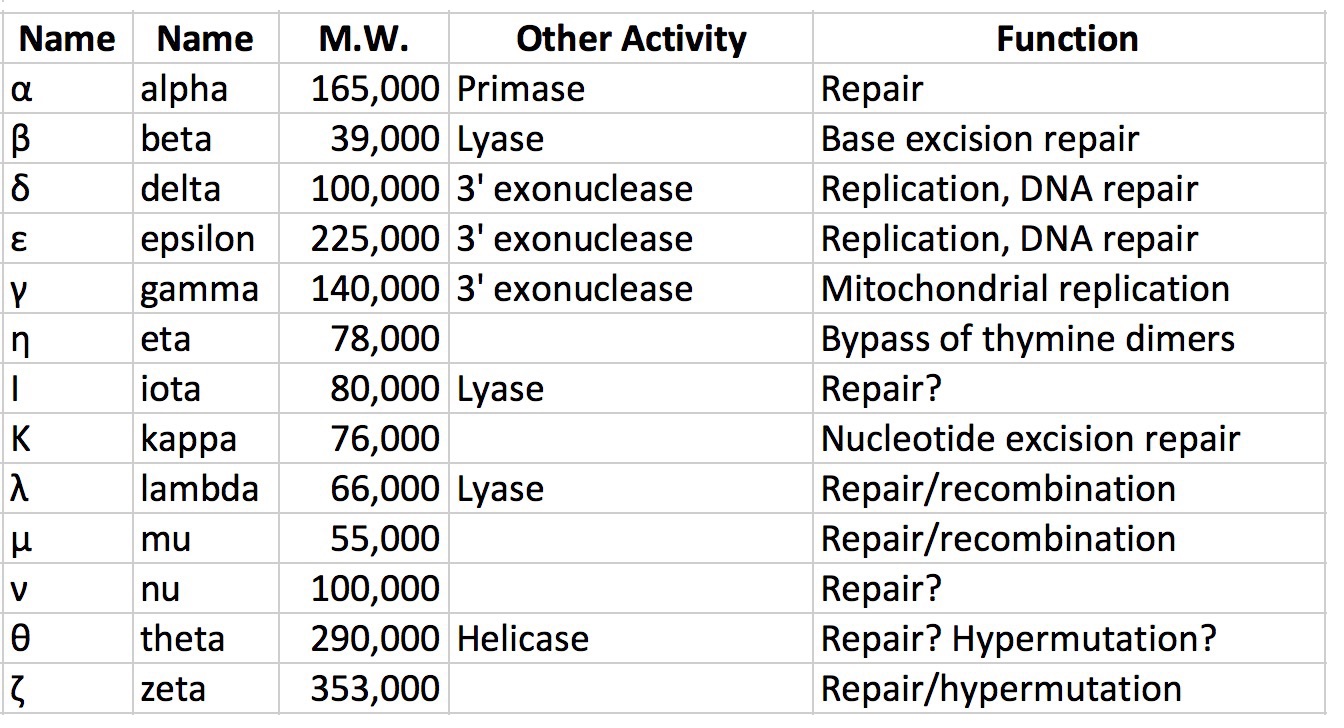
Como se señaló anteriormente, tanto las células procariotas como las eucariotas tienen múltiples ADN polimerasas. En E. coli, por ejemplo, la ADN polimerasa III es la principal polimerasa replicativa (también conocida como replicasa) mientras que la ADN polimerasa I es responsable de la reparación del ADN así como de la eliminación de los cebadores de ARN y su reemplazo con nucleótidos de ADN durante la replicación. La ADN polimerasa II juega un papel en el reinicio de la replicación después de que el daño del ADN detiene la replicación, mientras que las ADN polimerasas IV y V son requeridas en la síntesis de trans-lesión, o bypass, lo que permite la replicación más allá de los sitios de daño del ADN.
Polimerasas eucariotas
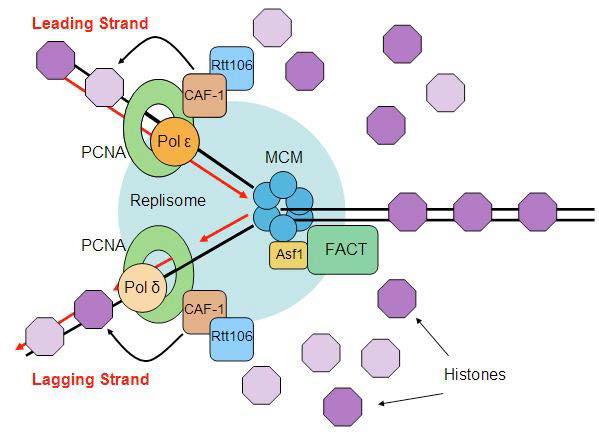
En eucariotas, hay más de quince ADN polimerasas diferentes. Las polimerasas replicativas primarias en el núcleo son y ε. La ADN polimerasa α también es importante para la replicación porque tiene actividades de primasa y reparación. La replicación se inicia en células eucariotas por la ADN polimerasa α, que se une al complejo de iniciación en el origen y establece un cebador de ARN, seguido de aproximadamente 25 nucleótidos de ADN. Luego se sustituye por otra polimerasa, en un paso llamado interruptor pol. La ADN polimerasa o ε luego continúa sintetizando ADN, dependiendo de la hebra. El papel de la polimerasa ε parece ser la síntesis de la cadena principal debido a su alta procesividad y precisión, mientras que la polimerasa extiende los fragmentos de Okazaki en las hebras rezagadas. También están presentes proteínas análogas a la pinza cargadora y a la pinza deslizante. La proteína RFC desempeña el papel de cargador de pinza, mientras que otra proteína, PCNA actúa como la pinza deslizante. Varias otras ADN polimerasas como β, γ y μ funcionan en la reparación de huecos. Sin embargo, otros están involucrados en la síntesis de trans-lesiones después del daño del ADN y están asociados con hipermutación.
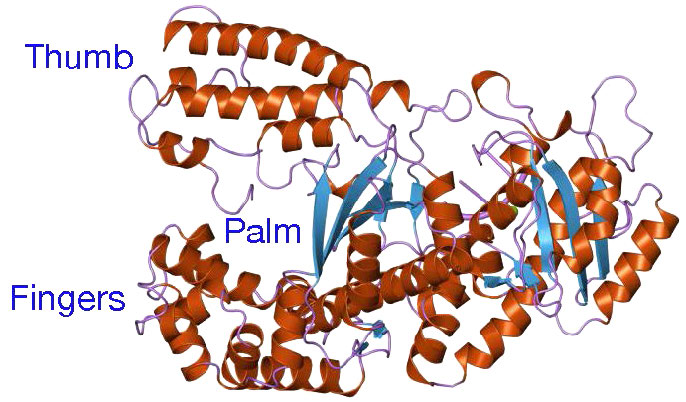
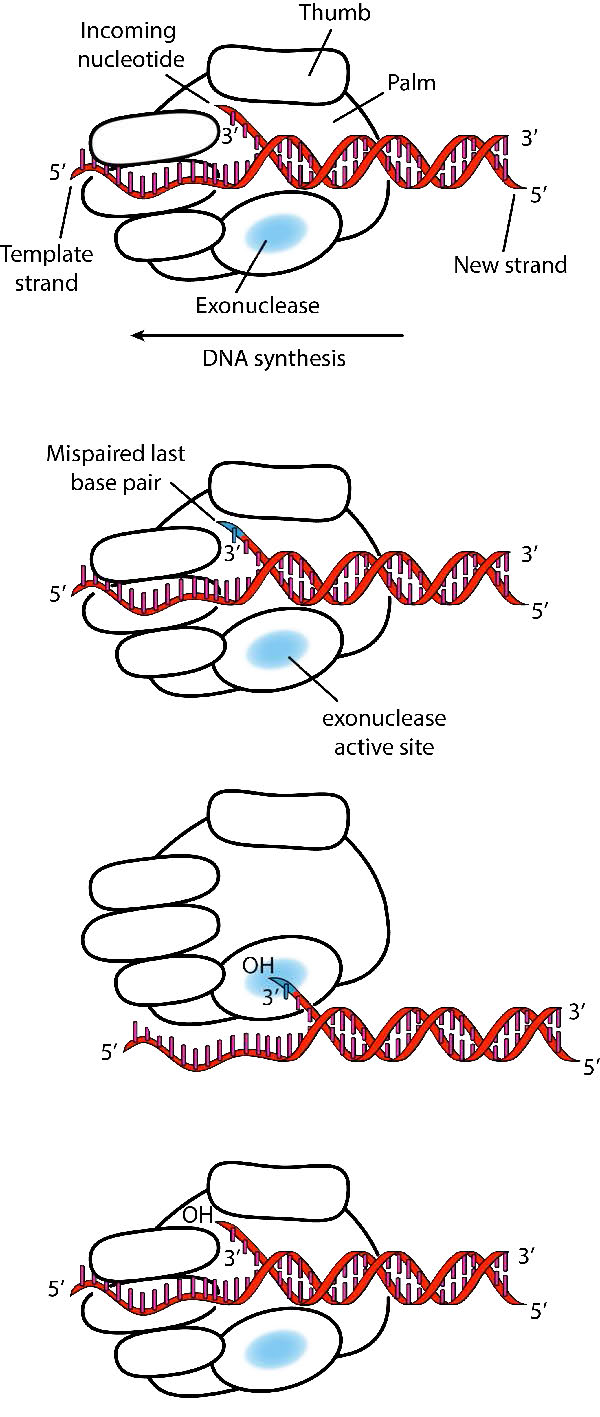
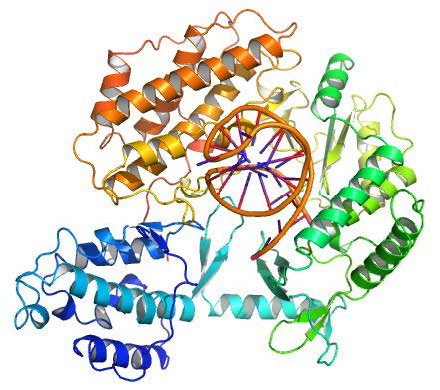
A pesar de su diversidad, las ADN polimerasas comparten algunas características estructurales comunes. Los estudios cristalográficos de rayos X han demostrado que estas enzimas tienen una estructura que ha sido comparada con una mano derecha humana (Figuras 7.25 y 7.26). La “palma” de la mano forma una hendidura en la que se encuentra el ADN. La hendidura es también el lugar donde reside la actividad catalítica de la polimerasa. Aquí es donde se agrega el nucleótido entrante a la cadena en crecimiento. “Los dedos” posicionan el ADN en el sitio activo, mientras que el “pulgar” sostiene el ADN a medida que sale de la polimerasa. Un dominio separado contiene la actividad exonucleasa (corrección) de la enzima.
La enzima alterna entre su actividad polimerizante y su actividad correctora. Cuando un par de bases no emparejado está en el sitio catalítico de la polimerasa, el extremo 3' de la cadena en crecimiento se mueve del sitio de la polimerasa al sitio activo de la exonucleasa (Figura 7.26). El mal apareamiento al final es eliminado por la exonucleasa, seguido de reposicionamiento del extremo 3' en el sitio activo de la polimerasa para continuar la síntesis.
Terminación de la replicación
En los cromosomas bacterianos circulares, existen secuencias específicas conocidas como sitios terminadores o Ter. Estas son múltiples secuencias cortas que sirven como sitios de terminación, permitiendo que las horquillas de replicación que viajan en sentido horario y antihorario a través del cromosoma circular se encuentren en uno de los sitios.
La unión de una proteína, Tus, en un sitio Ter impide un mayor movimiento de la horquilla de replicación y termina la replicación. El ADN parental y circular recién hecho están, en este punto topológicamente entrelazados y deben separarse con la ayuda de la topoisomerasa.
El problema de replicación final
No hay sitio fijo para la terminación en cromosomas eucariotas lineales. A medida que las horquillas de replicación alcanzan los extremos del cromosoma, la cadena principal se puede sintetizar hasta el final de la cadena molde. En la cadena rezagada, la necesidad de un cebador de ARN para iniciar la síntesis crea un desafío. Cuando se elimina el cebador de ARN en el extremo extremo de la cadena retrasada, hay un pequeño tramo de la cadena molde que no se puede copiar. Como resultado, en cada ronda de replicación se perderá una secuencia corta en los extremos del cromosoma. Con el tiempo, con muchos ciclos de replicación, los cromosomas se volverían notablemente más cortos. Este acortamiento de cromosomas se ha observado in vitro, en células somáticas de mamífero cultivadas. También se observa en organismos intactos, al aumentar la edad.
Telómeros
¿Qué efecto tiene en las células la pérdida de secuencia de los extremos de los cromosomas? Sabemos que los extremos de los cromosomas se caracterizan por estructuras llamadas telómeros (Figura 7.28). Los telómeros están formados por muchas copias de secuencias cortas repetidas (en humanos, la repetición es TTAGGG) y proteínas especiales que se unen específicamente a estas secuencias. Esta estructura de los telómeros es útil para distinguir los extremos de los cromosomas de las roturas bicatenarias en el ADN, evitando así que los mecanismos de reparación del ADN en las células se unan a los cromosomas de extremo a extremo.
La otra ventaja de las secuencias repetidas, que no codifican proteínas, es que perder algunas de las repeticiones no conduce a la pérdida de información importante de codificación. Así, las repeticiones actúan como una especie de zona tampón, donde la pérdida de secuencia no condena a la célula. Sin embargo, el acortamiento de los cromosomas no puede continuar indefinidamente. Después de cierto número de ciclos de replicación, se sabe que las células dejan de dividirse y entran en un estado conocido como senescencia replicativa. Esto sugiere que el acortamiento de los telómeros sirve como una especie de reloj, con el grado de contracción de los cromosomas sirviendo como medida del envejecimiento. Eventualmente las células que entran en senescencia morirán.
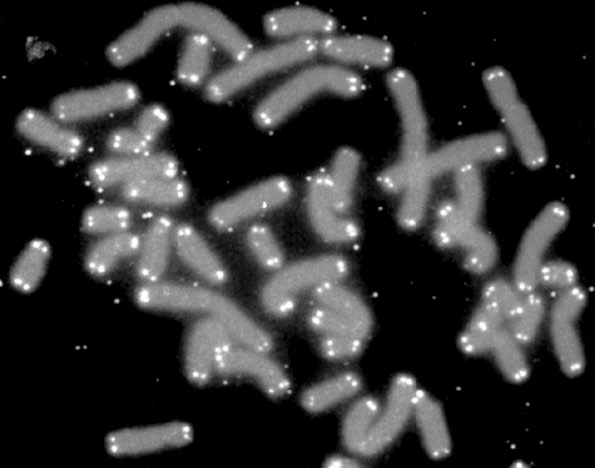
Figura 7.28 - Cromosomas con telómeros marcados en blanco
Problemas con la pérdida de secuencia
Incluso si nuestras células son capaces de funcionar con cromosomas más cortos durante nuestras vidas, esto nos deja con otro problema. Si nuestros cromosomas se acortan con la edad, entonces presumiblemente nuestros hijos, que heredan nuestros cromosomas, nacerán con cromosomas más cortos de los que empezamos. Ellos, a su vez, harían que sus cromosomas se encogieran a medida que crecían, y sus hijos tendrían cromosomas aún más cortos. En el transcurso de múltiples generaciones, esto llevaría al punto en que una mayor contracción cromosómica daría como resultado células que entrarían en senescencia muy temprano en la vida y morirían poco después. Esto obviamente no sucede. Generación tras generación de niños nacen con cromosomas de longitud completa, por lo que existe un mecanismo que debe asegurar que al menos en las células reproductivas, los cromosomas no se acorten.
Para entender este mecanismo, es necesario examinar primero el extremo de una molécula de ADN recién hecha (Figura 7.29). Mientras que la hebra delantera, que crece en la misma dirección que el movimiento de la horquilla de replicación, puede copiar su plantilla hasta el final, la hebra rezagada encuentra un problema. Los cebadores de ARN son, como señalamos, necesarios para iniciar cada uno de los fragmentos de Okazaki de la hebra rezagada. Los cebadores deben ser retirados posteriormente, y los nucleótidos de ARN reemplazados por nucleótidos de ADN. Cuando se elimina el cebador de ARN frente al extremo de la cadena parental, los nucleótidos de ARN no pueden reemplazarse por nucleótidos de ADN porque la ADN polimerasa no tiene cebador para comenzar. Por lo tanto, no se puede copiar una región corta de la plantilla.
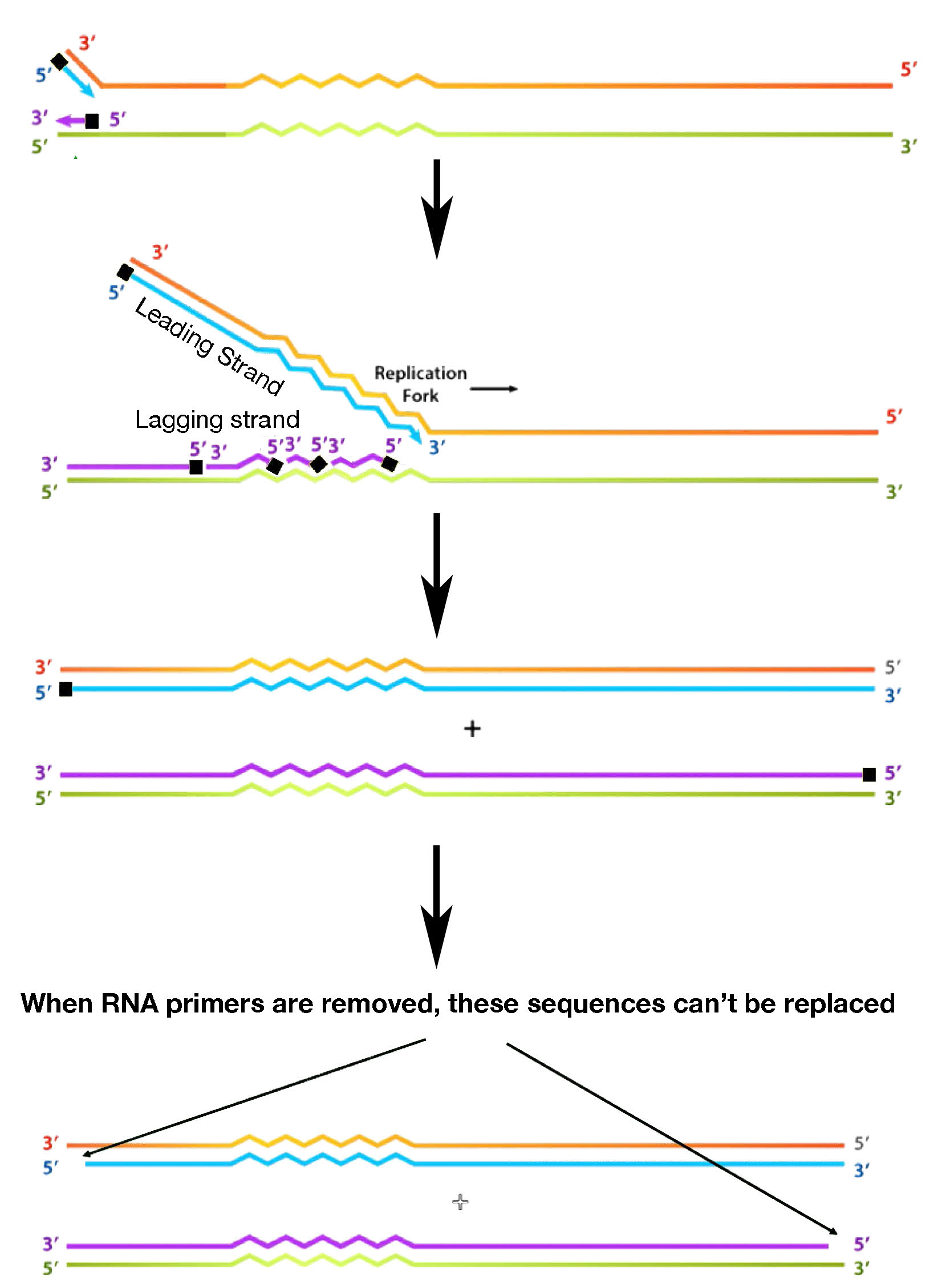
Figura 7.29 - La replicación de un cromosoma lineal da como resultado la pérdida de secuencias en los extremos con cada ronda de replicación
Telomerasa
¿Cómo se puede resolver este problema? Se puede observar a partir de la Figura 7.29 que el extremo de la cadena molde original tiene un saliente 3' corto resultante de la eliminación del cebador de ARN a través de ella. Para rellenar esta región, se necesitaría otro cebador, situado más allá del extremo de la cadena molde. Pero para construir tal imprimación, sería necesario que el voladizo de la plantilla fuera más largo. Si fuera posible alargar la cadena molde, entonces se podría colocar otro cebador frente a su extremo y se podría copiar el extremo de la hebra. Tal extensión de la cadena plantilla es exactamente lo que sucede en nuestras células reproductivas. La cadena molde parental es extendida por la enzima telomerasa, que agrega repeticiones de telómeros y alarga el molde. Veremos en breve cómo logra esa hazaña.
Plantilla de ARN
La telomerasa es una enzima inusual, ya que está compuesta por dos componentes, un ARN y una transcriptasa inversa. Una transcriptasa inversa es una ADN polimerasa dependiente de ARN, una enzima que copia un molde de ARN para producir ADN. El componente de ARN de la telomerasa humana, llamado hTERC, tiene una secuencia que es complementaria a la repetición del telómero, TAGGG. Como se ve en la Figura 7.31, este ARN puede emparejarse por bases con la última repetición del telómero en la cadena de ADN parental, mientras que una porción del ARN permanece desapareada.
Plantilla para extensión
La función de la región no apareada del ARN es servir como molde que se puede utilizar para extender el extremo 3' saliente de la molécula de ADN original. El componente proteico de la telomerasa tiene actividad transcriptasa inversa y puede copiar la secuencia de ARN en ADN. En la telomerasa humana, el componente proteico se conoce como hTERT (transcriptasa inversa de telomerasa). Como se ve en la Figura 7.31 y 7.32, la transcriptasa inversa extiende el saliente 3' original usando el componente de ARN como molde. La telomerasa puede entonces disociarse y repetir el proceso varias veces para agregar muchas repeticiones de la secuencia del telómero.
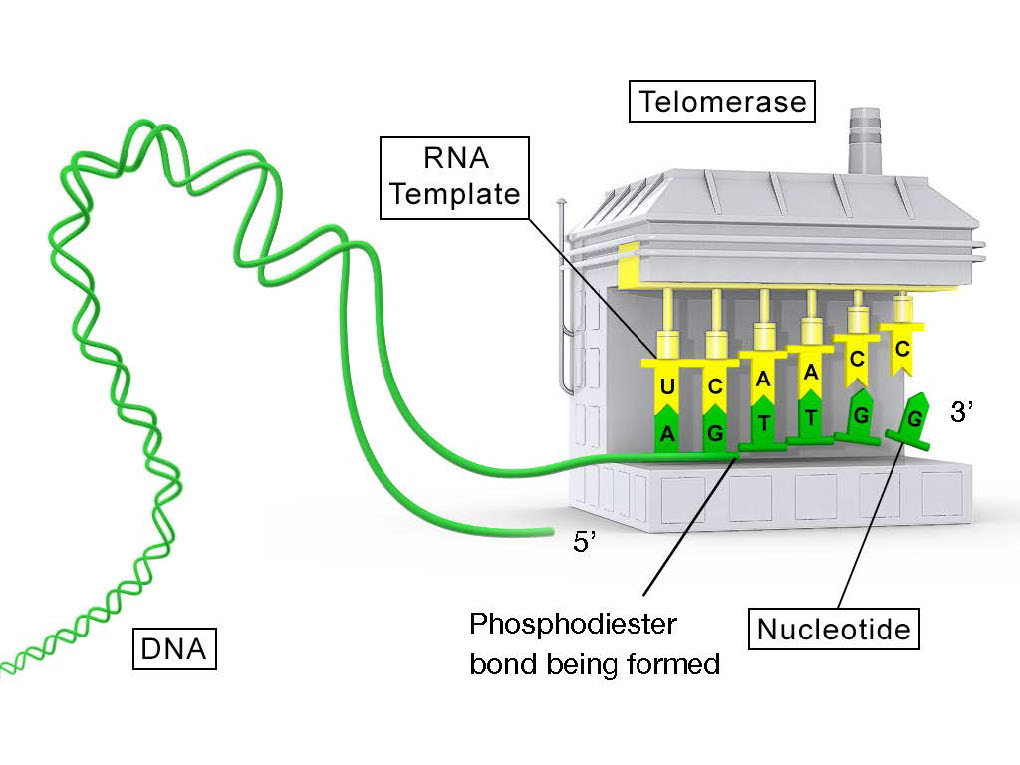
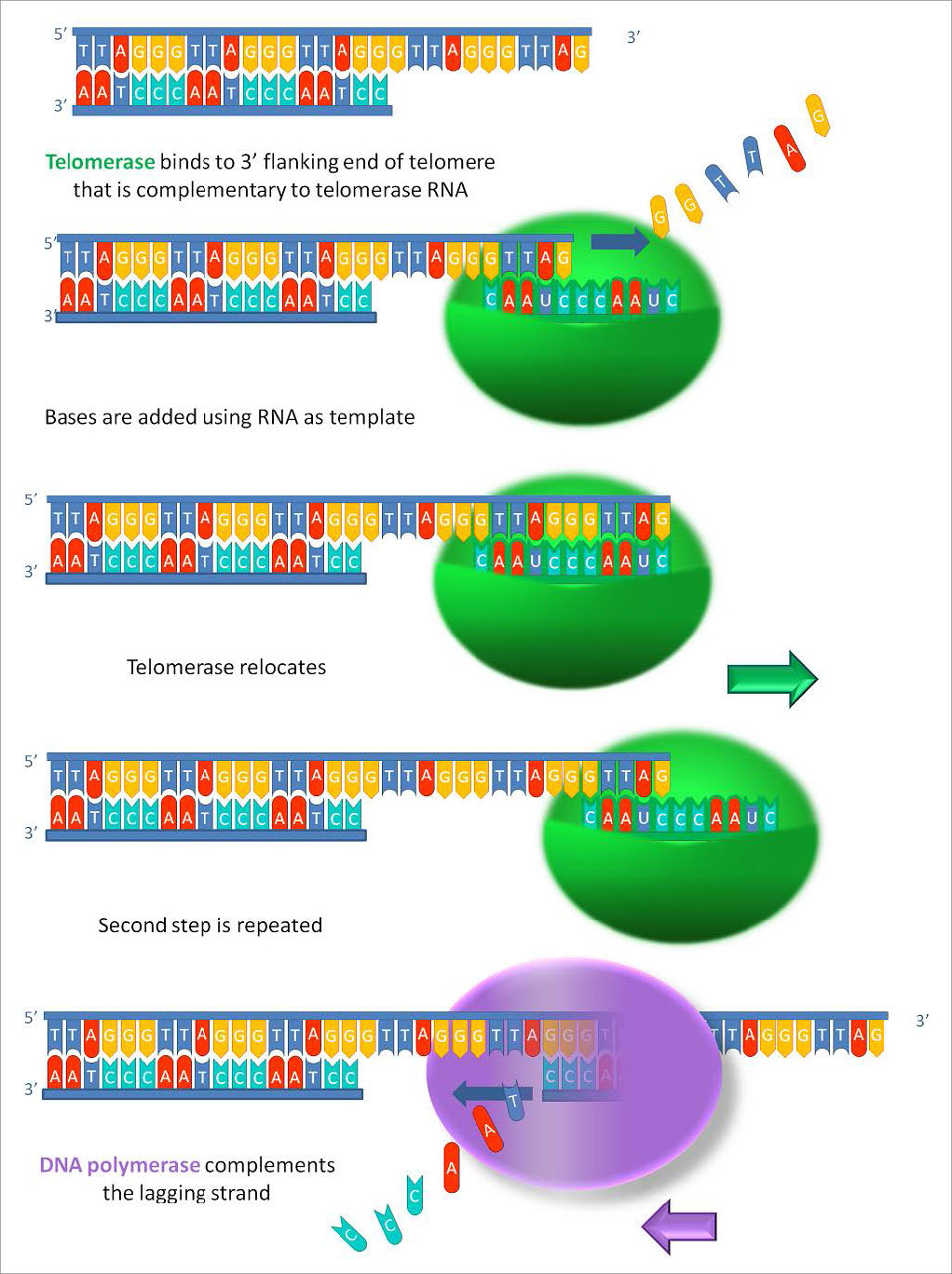
Una vez que el saliente se ha extendido mediante la adición de al menos varias repeticiones de telómeros, ahora hay espacio para la síntesis de un cebador de ARN complementario al saliente recién extendido (apuntando hacia el resto del cromosoma). Este cebador puede entonces extenderse para completar la síntesis de la cadena retrasada hasta el final de la cadena de ADN parental original. Así, la adición de repeticiones de telómeros en las cadenas de ADN parentales evita que las cadenas de ADN recién hechas se vuelvan más cortas con cada ciclo de replicación. El hecho de que esto ocurra en las células germinales (células reproductivas) explica por qué cada generación no tiene cromosomas más cortos que la generación parental.
La función de corrección de ADN polimerasas monitorea la precisión de la replicación del ADN mientras que la enzima telomerasa evita que los cromosomas que se transmitirán a la descendencia se acorten. Entre ellas, estas dos actividades aseguran que la información genética se copie con precisión, y que las generaciones venideras reciban un complemento completo de la información genética
Desmontaje y reensamblaje de nucleosomas
Los eventos de replicación tienen un giro adicional en eucariotas. Recordemos que el ADN se encuentra en las células eucariotas como la cromatina, un complejo del ADN con proteínas. Al menos condensada, la cromatina parece una cadena de perlas, que consiste en el ADN envuelto alrededor de núcleos de histonas para hacer nucleosomas. La estructura del nucleosoma debe alterarse para que el ADN esté disponible para la replicación y restaurarse después de que se complete la replicación (Figura 7.33).
Antes de la horquilla de replicación, la estructura de la cromatina es desensamblada por complejos de remodelación de cromatina dependientes de ATP, permitiendo el acceso al molde de ADN. Una vez sintetizadas las nuevas cadenas de ADN, tanto los nucleosomas originales como los nuevos nucleosomas deben ser reensamblados detrás de la horquilla de replicación. Dado que la replicación da lugar a dos moléculas de ADN donde había una, se necesita el doble de la cantidad de histonas para empaquetar el ADN. La preparación para la replicación del ADN, por lo tanto, implica la síntesis de grandes cantidades de histonas para suplir la necesidad. Curiosamente, parece que el ADN recién sintetizado se empaqueta en nucleosomas utilizando las histonas originales que fueron desplazadas para permitir el paso de la horquilla de replicación, así como histonas recién sintetizadas.
También sabemos que las modificaciones postraduccionales como la acetilación, metilación o fosforilación de las histonas pueden regular el grado en que una región determinada del genoma es accesible para su uso. Una pregunta que sigue siendo objeto de intensa investigación es cómo estas modificaciones se transmiten con precisión a los nuevos nucleosomas.