10.2: Agotamiento del ozono
- Page ID
- 52729
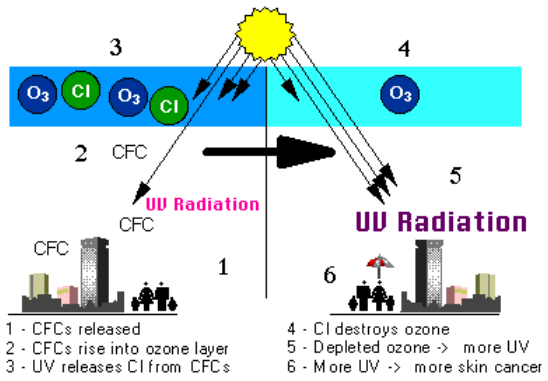
El proceso de agotamiento del ozono comienza cuando se emiten CFC (clorofluorocarbonos) y otras sustancias que agotan el ozono (SAO) a la atmósfera. Las moléculas de CFC son extremadamente estables y no se disuelven en la lluvia. Después de un periodo de varios años, las moléculas de ODS alcanzan la estratosfera, a unos 10 kilómetros por encima de la superficie terrestre. Los CFCs fueron utilizados por la industria como refrigerantes, solventes desengrasantes y propelentes.
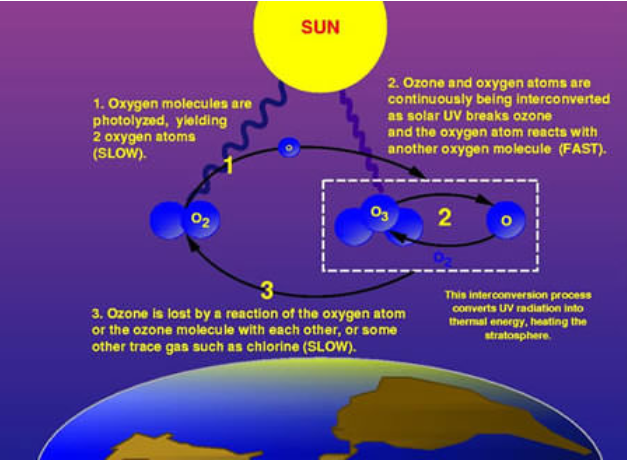
El ozono (O 3) se produce constantemente y se destruye en un ciclo natural, como se muestra en la Figura\(\PageIndex{1}\). Sin embargo, la cantidad total de ozono es esencialmente estable. Este equilibrio se puede considerar como la profundidad de un arroyo en una ubicación particular. Aunque las moléculas de agua individuales se mueven más allá del observador, la profundidad total permanece constante. De igual manera, si bien la producción y destrucción de ozono están equilibradas, los niveles de ozono permanecen estables Esta fue la situación hasta las últimas décadas. Sin embargo, los grandes aumentos en las SAO estratosféricas han alterado ese equilibrio. En efecto, están eliminando el ozono más rápido de lo que las reacciones de creación de ozono natural pueden mantenerse al día. Por lo tanto, los niveles de ozono caen.
Políticas para reducir la destrucción del ozono
Una historia de éxito en la reducción de contaminantes que dañan la atmósfera se refiere a los químicos destructores del ozono En 1973, los científicos calcularon que los CFC podrían llegar a la estratosfera y romperse. Esto liberaría átomos de cloro, que luego destruirían el ozono. Con base únicamente en sus cálculos, Estados Unidos y la mayoría de los países escandinavos prohibieron los CFC en latas de aerosol en 1978. Se necesitaba más confirmación de que los CFC descomponen el ozono antes de que se hiciera más para reducir la producción de productos químicos destructores del ozono. En 1985, miembros del British Antarctic Survey informaron que en los tres manantiales anteriores se había encontrado una reducción del 50% en la capa de ozono sobre la Antártida.
Dos años después del informe British Antarctic Survey, el “Protocolo de Montreal sobre Sustancias que Agotan la Capa de Ozono” fue ratificado por naciones de todo el mundo. El Protocolo de Montreal controla la producción y consumo de 96 químicos que dañan la capa de ozono (Figura\(\PageIndex{3}\)). Los CFC se han eliminado en su mayoría desde 1995, aunque se utilizaron en países en desarrollo hasta 2010. Algunas de las sustancias menos peligrosas no se eliminarán gradualmente hasta 2030. El Protocolo también requiere que las naciones más ricas donen dinero para desarrollar tecnologías que sustituyan a estos químicos.
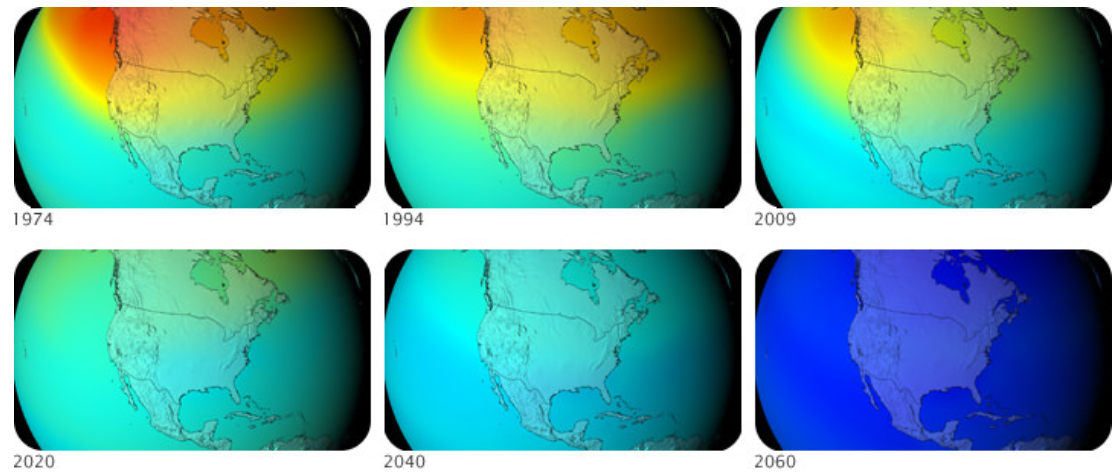
Debido a que los CFC tardan muchos años en llegar a la estratosfera y pueden sobrevivir allí mucho tiempo antes de que se descompongan, el agujero de ozono probablemente seguirá creciendo durante algún tiempo antes de que comience a encogerse. La capa de ozono alcanzará los mismos niveles que tenía antes de 1980 alrededor de los niveles de 2068 y 1950 en uno o dos siglos.
Efectos sobre la salud y el medio ambiente del agotamiento de la capa de ozono
Hay tres tipos de luz UV: UVA, UVB y UVC. Las reducciones en los niveles de ozono estratosférico conducirán a que niveles más altos de UVB lleguen a la superficie de la Tierra. La salida solar de UVB no cambia; más bien, menos ozono significa menos protección, y de ahí que más UVB llegue a la Tierra. Los estudios han demostrado que en la Antártida, la cantidad de UVB medida en la superficie puede duplicarse durante el agujero anual de ozono.
Estudios epidemiológicos y de laboratorio demuestran que la UVB causa cánceres de piel no melanoma y juega un papel importante en el desarrollo del melanoma maligno. Además, la UVB se ha relacionado con cataratas, una opacidad del cristalino del ojo. Toda la luz solar contiene algo de UVB, incluso con niveles normales de ozono estratosférico. Por lo tanto, siempre es importante proteger tu piel y ojos del sol. El agotamiento de la capa de ozono aumenta la cantidad de UVB y el riesgo de efectos sobre la salud.
El UVB es generalmente dañino para las células, y por lo tanto para todos los organismos. El UVB no puede penetrar en un organismo muy lejos y por lo tanto tiende a afectar solo a las células de la piel. Los microbios como las bacterias, sin embargo, están compuestos por una sola célula y por lo tanto pueden ser dañados por UVB,
Colaboradores y Atribuciones
- Esenciales de la Ciencia Ambiental por Kamala Doršner está licenciado bajo CC BY 4.0. Modificado del original por Matthew R. Fisher.


