17.4: Reconocimiento de Patógenos y Fagocitosis
- Page ID
- 54387
Objetivos de aprendizaje
- Explicar cómo los leucocitos migran de la sangre periférica a los tejidos infectados
- Explicar los mecanismos por los cuales los leucocitos reconocen patógenos
- Explicar el proceso de fagocitosis y los mecanismos por los cuales los fagocitos destruyen y degradan patógenos
Varios de los tipos celulares discutidos en la sección anterior pueden describirse como fagocitos, células cuya función principal es buscar, ingerir y matar patógenos. Este proceso, llamado fagocitosis, fue observado por primera vez en estrellas de mar en la década de 1880 por el zoólogo ganador del Premio Nobel Ilya Metchnikoff (1845—1916), quien hizo la conexión con los glóbulos blancos (WBC) en humanos y otros animales. En su momento, Pasteur y otros científicos creían que los glóbulos blancos estaban propagando patógenos en lugar de matarlos (lo cual es cierto para algunas enfermedades, como la tuberculosis). Pero en la mayoría de los casos, los fagocitos proporcionan una defensa fuerte, rápida y efectiva contra una amplia gama de microbios, convirtiéndolos en un componente crítico de la inmunidad innata inespecífica. Esta sección se centrará en los mecanismos por los cuales los fagocitos son capaces de buscar, reconocer y destruir patógenos.
Extravasación (Diapedesis) de Leucocitos
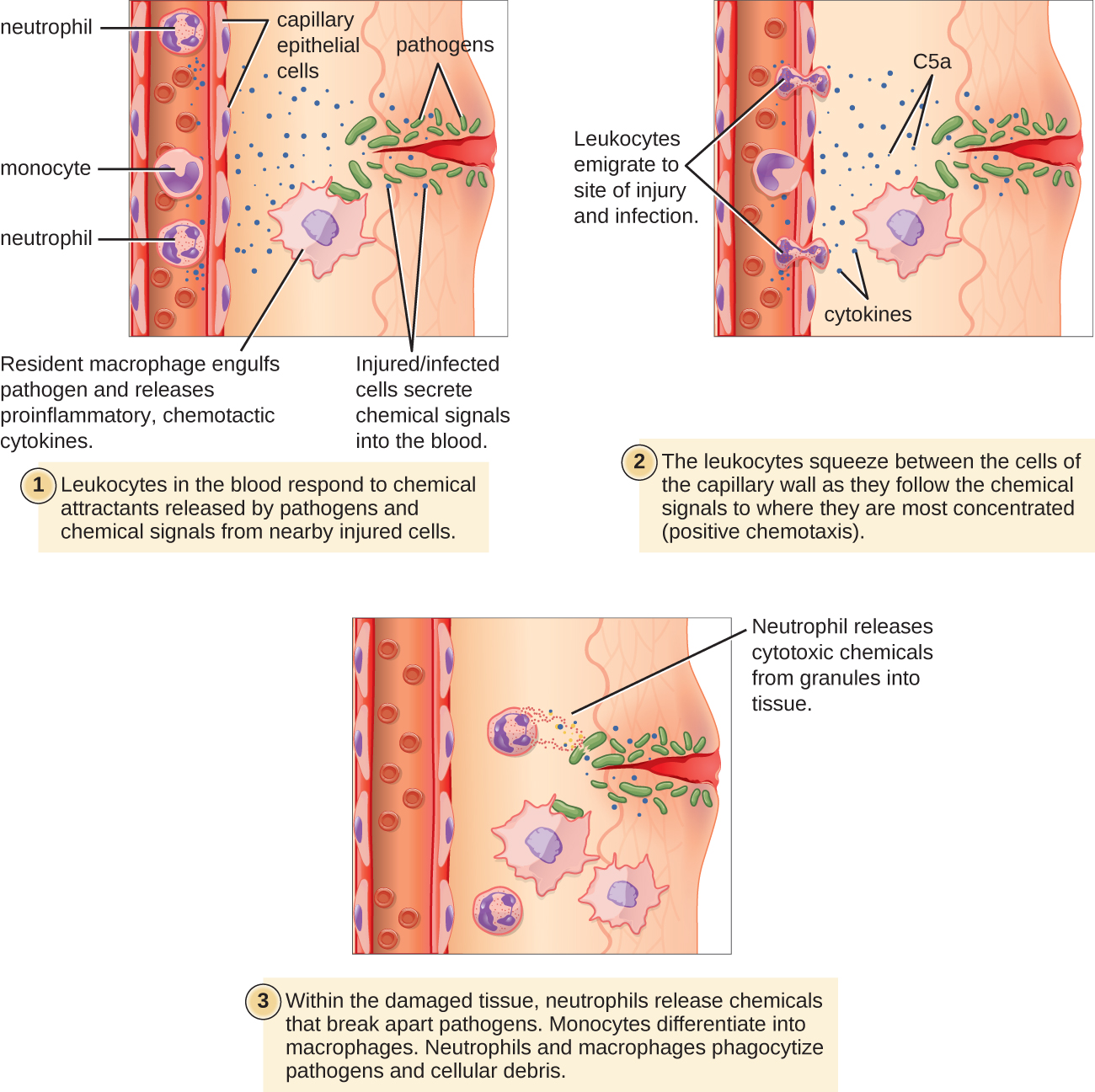
Algunos fagocitos son leucocitos (WBC) que normalmente circulan en el torrente sanguíneo. Para llegar a patógenos localizados en tejido infectado, los leucocitos deben pasar a través de las paredes de pequeños vasos sanguíneos capilares dentro de los tejidos. Este proceso, denominado extravasación, o diapedesis, es iniciado por el factor del complemento C5a, así como las citocinas liberadas en las inmediaciones por macrófagos residentes y células tisulares que responden a la presencia del agente infeccioso (Figura\(\PageIndex{1}\)). Similar a C5a, muchas de estas citocinas son proinflamatorias y quimiotácticas, y se unen a células de pequeños vasos sanguíneos capilares, iniciando una respuesta en las células endoteliales que recubren el interior de las paredes de los vasos sanguíneos. Esta respuesta implica la sobrerregulación y expresión de diversas moléculas de adhesión celular y receptores. Los leucocitos que pasan se adherirán ligeramente a las moléculas de adhesión, disminuyendo la velocidad y rodando a lo largo de las paredes de los vasos sanguíneos cerca del área infectada. Cuando alcanzan una unión celular, se unirán a aún más de estas moléculas de adhesión, aplanándose y apretando a través de la unión celular en un proceso conocido como migración transendotelial. Este mecanismo de “adhesión rodante” permite que los leucocitos salgan del torrente sanguíneo y entren en las zonas infectadas, donde pueden comenzar a fagocitar a los patógenos invasores.
Tenga en cuenta que la extravasación no ocurre en arterias o venas. Estos vasos sanguíneos están rodeados por paredes protectoras multicapa más gruesas, en contraste con las delgadas paredes de una sola capa celular de los capilares. Además, el flujo sanguíneo en las arterias es demasiado turbulento para permitir la adhesión rodante. Además, algunos leucocitos tienden a responder a una infección más rápidamente que otros. Los primeros en llegar típicamente son los neutrófilos, a menudo a las pocas horas de una infección bacteriana. Por contrato, los monocitos pueden tardar varios días en salir del torrente sanguíneo y diferenciarse en macrófagos.
Vea los siguientes videos sobre extravasación de leucocitos y balanceo de leucocitos para obtener más información.
Ejercicio\(\PageIndex{1}\)
Explicar el papel de las moléculas de adhesión en el proceso de extravasación.
Reconocimiento de Patógenos
Como se describe en la sección anterior, la opsonización de patógenos por anticuerpos; los factores del complemento C1q, C3b y C4b; y las lectinas pueden ayudar a las células fagocíticas en el reconocimiento de patógenos y la unión para iniciar la fagocitosis. Sin embargo, no todo el reconocimiento de patógenos es dependiente de opsonina. Los fagocitos también pueden reconocer estructuras moleculares que son comunes a muchos grupos de microbios patógenos. Tales estructuras se denominan patrones moleculares asociados a patógenos (PAMP). Los PAMP comunes incluyen los siguientes:
- peptidoglicano, que se encuentra en las paredes celulares bacterianas;
- flagelina, una proteína que se encuentra en flagelos bacterianos;
- lipopolisacárido (LPS) de la membrana externa de bacterias gramnegativas;
- lipopéptidos, moléculas expresadas por la mayoría de bacterias; y
- ácidos nucleicos tales como ADN viral o ARN.
Al igual que muchos otros PAMP, estas sustancias son parte integral de la estructura de amplias clases de microbios.
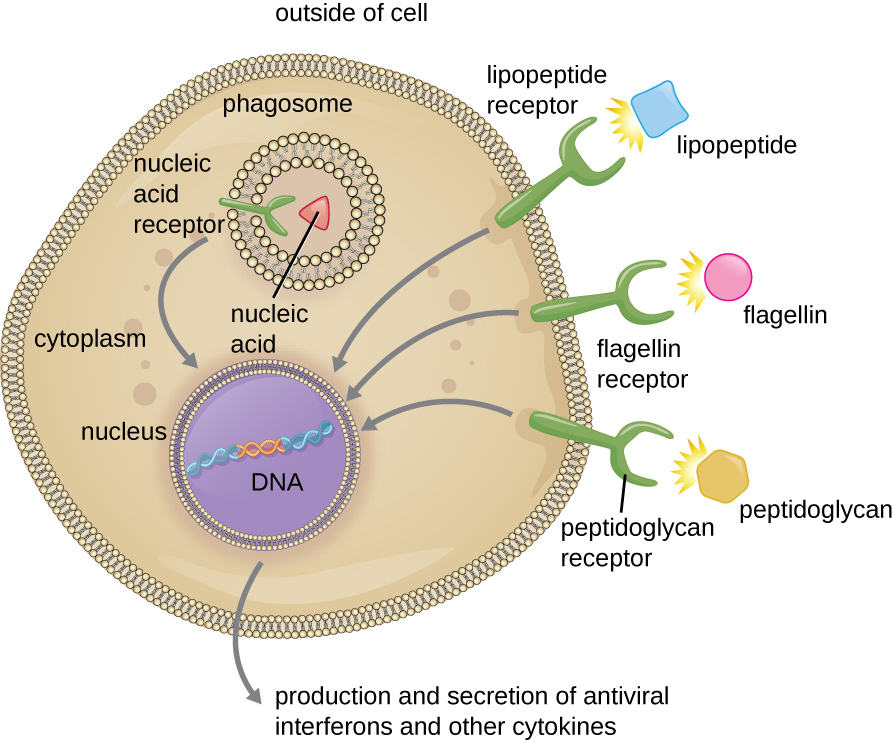
Las estructuras que permiten que las células fagocíticas detecten PAMP se denominan receptores de reconocimiento de patrones (PRR). Un grupo de PRR son los receptores tipo Toll (TLR), que se unen a varios PAMP y se comunican con el núcleo del fagocito para provocar una respuesta. Muchos TLR (y otros PRR) se encuentran en la superficie de un fagocito, pero algunos también se pueden encontrar incrustados en las membranas de los compartimentos interiores y orgánulos (Figura\(\PageIndex{2}\)). Estos PRR interiores pueden ser útiles para la unión y el reconocimiento de patógenos intracelulares que pueden haber obtenido acceso al interior de la célula antes de que pudiera tener lugar la fagocitosis. Los ácidos nucleicos virales, por ejemplo, podrían encontrarse con un PRR interior, desencadenando la producción de la citocina interferón antiviral.
Además de proporcionar el primer paso de reconocimiento de patógenos, la interacción entre PAMP y PRR en macrófagos proporciona una señal intracelular que activa el fagocito, provocando que pase de un estado latente de preparación y proliferación lenta a un estado de hiperactividad, proliferación, producción/secreción de citocinas y aumento de la destrucción intracelular. Los PRR en los macrófagos también responden a las señales de socorro químico de las células dañadas o estresadas. Esto permite a los macrófagos extender sus respuestas más allá de la protección contra enfermedades infecciosas a un papel más amplio en la respuesta inflamatoria iniciada por lesiones u otras enfermedades.
Ejercicio\(\PageIndex{2}\)
- Nombrar cuatro patrones moleculares asociados a patógenos (PAMP).
- Describir el proceso de activación de fagocitos.
Degradación de patógenos
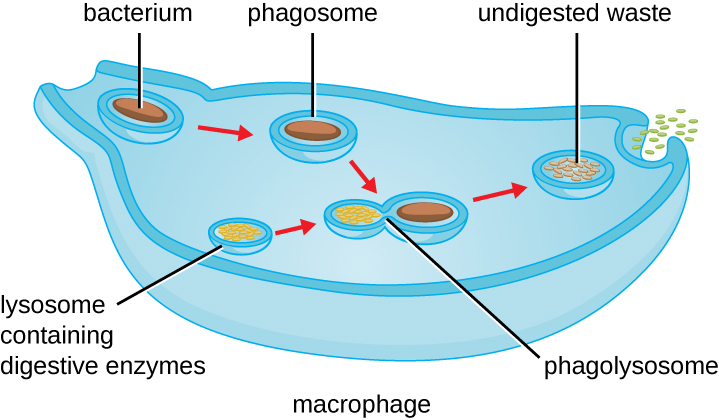
Una vez que se produce el reconocimiento y la unión del patógeno, el patógeno se engulle en una vesícula y se lleva al compartimento interno del fagocito en un proceso llamado fagocitosis (Figura\(\PageIndex{3}\)). Los PRR pueden ayudar en la fagocitosis al unirse primero a la superficie del patógeno, pero los fagocitos también son capaces de engullir elementos cercanos incluso si no están unidos a receptores específicos. Para engullir al patógeno, el fagocito forma un pseudopodo que envuelve al patógeno y luego lo pellizca en una vesícula de membrana llamada fagosoma. La acidificación del fagosoma (el pH disminuye al rango de 4—5) proporciona un importante mecanismo antibacteriano temprano. El fagosoma que contiene el patógeno se fusiona con uno o más lisosomas, formando un fagolisosoma. La formación del fagolisosoma potencia la acidificación, la cual es esencial para la activación de las enzimas lisosómicas digestivas dependientes del pH y la producción de peróxido de hidrógeno y especies tóxicas reactivas de oxígeno. Enzimas lisosómicas como lisozima, fosfolipasa y proteasas digieren el patógeno. Otras enzimas están involucradas con un estallido respiratorio. Durante el estallido respiratorio, los fagocitos aumentarán su captación y consumo de oxígeno, pero no para la producción de energía. El aumento del consumo de oxígeno se centra en la producción de anión superóxido, peróxido de hidrógeno, radicales hidroxilo y otras especies reactivas de oxígeno que son antibacterianas.
Además de las especies reactivas de oxígeno producidas por el estallido respiratorio, también se pueden formar compuestos reactivos de nitrógeno con potencial citotóxico (destructor celular). Por ejemplo, el óxido nítrico puede reaccionar con superóxido para formar peroxinitrito, un compuesto de nitrógeno altamente reactivo con capacidades degradantes similares a las de las especies reactivas de oxígeno. Algunos fagocitos incluso contienen un depósito interno de proteínas defensinas microbicidas (por ejemplo, gránulos de neutrófilos). Estas fuerzas destructivas pueden ser liberadas en el área alrededor de la célula para degradar los microbios externamente. Los neutrófilos, especialmente, pueden ser bastante eficientes en este mecanismo antimicrobiano secundario.
Una vez completada la degradación, los residuos sobrantes se excretan de la célula en una vesícula exocítica. Sin embargo, es importante señalar que no todos los restos del patógeno se excretan como desechos. Los macrófagos y las células dendríticas también son células presentadoras de antígeno involucradas en la respuesta inmune adaptativa específica. Estas células procesan aún más los restos del patógeno degradado y presentan antígenos clave (proteínas patógenas específicas) en su superficie celular. Este es un paso importante para la estimulación de algunas respuestas inmunes adaptativas, como se discutirá con más detalle en el próximo capítulo.
Visita este enlace para ver un fagocito que persigue y envuelve a un patógeno.
Ejercicio\(\PageIndex{3}\)
¿Cuál es la diferencia entre un fagosoma y un lisosoma?
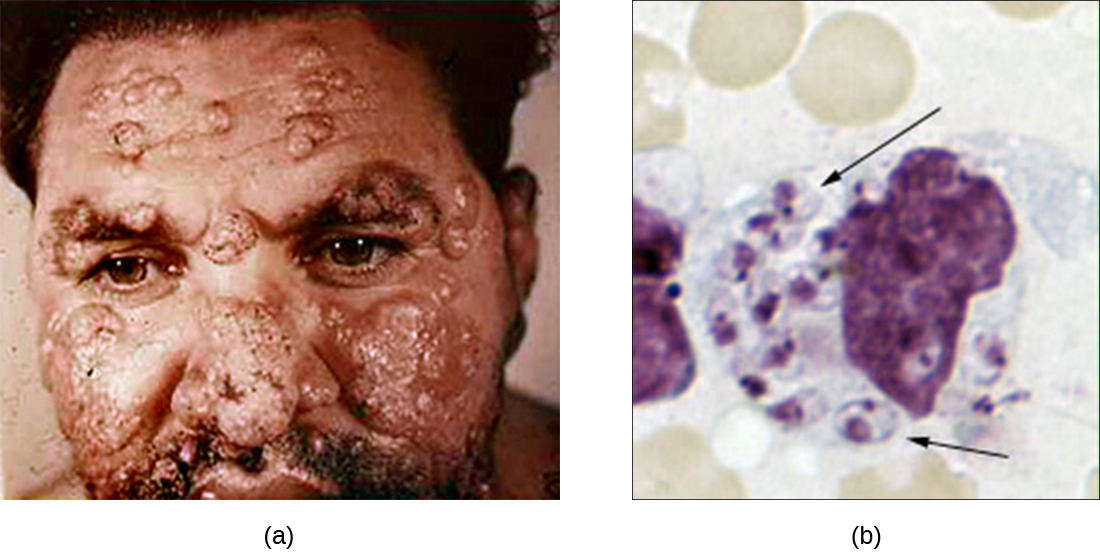
Aunque la fagocitosis destruye con éxito muchos patógenos, algunos son capaces de sobrevivir e incluso explotar este mecanismo de defensa para multiplicarse en el cuerpo y provocar una infección generalizada. Protozoos del género Leishmania son un ejemplo. Estos parásitos intracelulares obligados son flagelados transmitidos a los humanos por la picadura de una mosca de la arena. Las infecciones causan llagas y úlceras graves y a veces desfigurantes en la piel y otros tejidos (Figura\(\PageIndex{4}\)). A nivel mundial, se estima que 1.3 millones de personas se infectan recientemente con leishmaniasis anualmente. 1
Los péptidos salivales de la mosca de la arena activan los macrófagos hospedadores en el sitio de su picadura. La vía clásica o alternativa para la activación del complemento se produce con la opsonización C3b del parásito. Las células de Leishmania se fagocitan, pierden sus flagelos y se multiplican en una forma conocida como amastigoto (cuerpo de Leishman-Donovan) dentro del fagolisosoma. Aunque muchos otros patógenos son destruidos en el fagolisosoma, la supervivencia de los amastigotos de Leishmania se mantiene por la presencia de lipofosfoglicano superficial y fosfatasa ácida. Estas sustancias inhiben el estallido respiratorio macrófago y las enzimas lisosómicas. El parásito luego se multiplica dentro de la célula y lisa el macrófago infectado, liberando los amastigotos para infectar a otros macrófagos dentro del mismo huésped. Si otra mosca de la arena muerde a una persona infectada, podría ingerir amastigotes y luego transmitirlos a otro individuo a través de otra mordedura.
Existen varias formas diferentes de leishmaniasis. La más común es una forma cutánea localizada de la enfermedad causada por L. tropica, que generalmente se resuelve espontáneamente con el tiempo pero con alguna infiltración linfocitaria significativa y cicatrización permanente. Una forma mucocutánea de la enfermedad, causada por L. viannia brasilienfsis, produce lesiones en el tejido de la nariz y la boca y puede ser potencialmente mortal. Una forma visceral de la enfermedad puede ser causada por varias de las diferentes especies de Leishmania. Afecta a diversos sistemas de órganos y provoca agrandamiento anormal del hígado y bazo. Fiebres irregulares, anemia, disfunción hepática y pérdida de peso son signos y síntomas de leishmaniasis visceral. Si no se trata, suele ser fatal.
Conceptos clave y resumen
- Los fagocitos son células que reconocen patógenos y los destruyen a través de la fagocitosis.
- El reconocimiento a menudo se lleva a cabo mediante el uso de receptores de fagocitos que se unen a moléculas que se encuentran comúnmente en patógenos, conocidos como patrones moleculares asociados a patógenos (PAMP).
- Los receptores que se unen a PAMP se denominan receptores de reconocimiento de patrones, o PRR. Los receptores tipo Toll (TLR) son un tipo de PRR que se encuentra en los fagocitos.
- La extravasación de glóbulos blancos del torrente sanguíneo hacia el tejido infectado se produce a través del proceso de migración transendotelial.
- Los fagocitos degradan los patógenos a través de la fagocitosis, lo que implica engullir al patógeno, matarlo y digerirlo dentro de un fagolisosoma, y luego excretar materia no digerida.
Notas al pie
- 1 Organización Mundial de la Salud. “Leishmaniasis”. 2016. http://www.who.int/mediacentre/factsheets/fs375/en/.


