15.11: La desintegración radiactiva como medida de la edad
- Page ID
- 108518
¿Cuándo dejas de contar?
Pretende que el gran cilindro verde es un isótopo padre. Ahora se puede visualizar la decadencia del padre a la hija. Es fácil ver que el segundo cilindro es la mitad del tamaño del primero. El tercero es la mitad del tamaño del segundo. Pero cuando los cilindros se hacen pequeños, las diferencias son mucho más difíciles de ver. En algún momento, queda muy poco del padre. Ese par de isótopos ya no es útil para fechar.
Desintegración radiactiva
La desintegración radiactiva es la descomposición de elementos inestables en elementos estables. Para entender este proceso, recordemos que los átomos de todos los elementos contienen las partículas protones, neutrones y electrones.
Isótopos
Un elemento se define por el número de protones que contiene. Todos los átomos de un elemento dado contienen el mismo número de protones. El número de neutrones en un elemento puede variar. Los átomos de un elemento con diferentes números de neutrones se denominan isótopos.
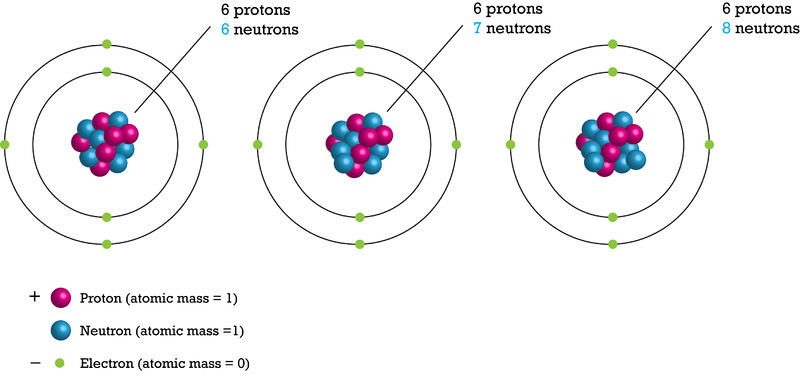
Considera el carbono como ejemplo. A continuación se muestran dos isótopos de carbono (Figura a continuación). Compara sus protones y neutrones. Ambos contienen seis protones. Pero el carbono-12 tiene seis neutrones y el carbono-14 tiene ocho neutrones.
Los isótopos reciben su nombre por su número de protones más neutrones. Si un átomo de carbono tuviera siete neutrones, ¿cómo se llamaría?
Casi todos los átomos de carbono son carbono-12. Este es un isótopo estable de carbono. Sólo un pequeño porcentaje de átomos de carbono son carbono-14. carbono-14 es inestable. Es un isótopo radiactivo de carbono. A continuación se muestra el dióxido de carbono (Figura abajo), que se forma en la atmósfera a partir del carbono-14 y el oxígeno. Los neutrones en los rayos cósmicos golpean átomos de nitrógeno en la atmósfera. El nitrógeno forma carbono-14. El carbono en la atmósfera se combina con el oxígeno para formar dióxido de carbono. Las plantas absorben dióxido de carbono durante la fotosíntesis. De esta manera, el carbono-14 entra en las cadenas alimentarias.
El carbono-14 se forma en la atmósfera. Se combina con oxígeno y forma dióxido de carbono. ¿Cómo termina el carbono-14 en los fósiles?
Desintegración de isótopos inestables
Al igual que otros isótopos inestables, el carbono-14 se descompone o se descompone. Los átomos originales se llaman isótopos progenitores. Para la desintegración del carbono-14, cada átomo de carbono-14 pierde una partícula beta, o un neutrón que se divide en un protón y un electrón. Cambia a un átomo estable de nitrógeno-14. El átomo estable al final es el producto hijo (Figura a continuación).
Los isótopos inestables, como el carbono-14, se descomponen al perder partículas atómicas. Forman elementos diferentes y estables cuando se descomponen.
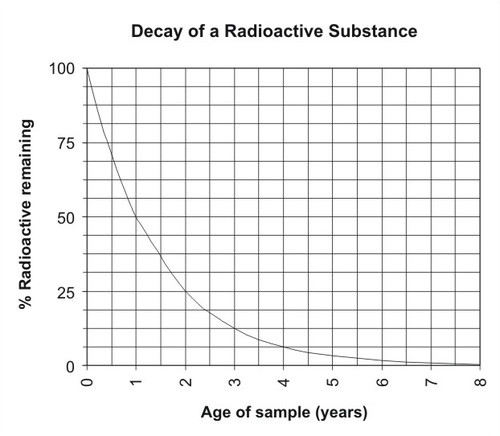
La descomposición de un isótopo inestable a un elemento estable ocurre a una velocidad constante. Esta tasa es diferente para cada par de isótopos padre-hija. La tasa de decaimiento se mide en una unidad llamada semivida. La vida media es el tiempo que tarda la mitad de una cantidad dada de un isótopo en desintegrarse. Por ejemplo, la vida media del carbono-14 es de 5,730 años. Imagina que comienzas con 100 gramos de carbono-14. En 5 mil 730 años, la mitad de ella decae. Esto deja 50 gramos de carbono-14. En los próximos 5 mil 730 años, la mitad de la cantidad restante se desintegrará. Ahora hay 25 gramos de carbono-14. ¿Cuántos gramos habrá en otros 5,730 años? La siguiente figura grafica la tasa de descomposición de una sustancia (Figura a continuación).
La tasa de desintegración de una sustancia radiactiva es constante a lo largo del tiempo.
Resumen
- Una vida media es el tiempo que tarda la mitad de los isótopos progenitores de un elemento en cambiar al producto hijo.
- Con la desintegración alfa, el núcleo pierde dos protones y dos neutrones.
- El carbono-14 tiene una vida media de 5,730 años.
Revisar
- ¿Qué hace que un isótopo sea radioactivo? ¿Todos los isótopos son radiactivos?
- ¿Qué es un isótopo padre y un producto hijo?
- Describir la vida media. Usa un ejemplo.