11.4: Las propiedades coligativas
- Page ID
- 1889
habilidades para desarrollar
- Expresar las concentraciones de los componentes de la solución usando la fracción molar y la molalidad
- Describir el efecto de la concentración de soluto en varias propiedades de la solución (presión de vapor, punto de ebullición, punto de congelación y presión osmótica)
- Realizar cálculos usando las ecuaciones matemáticas que describen estos diversos efectos coligativos.
- Describir el proceso de destilación y sus aplicaciones prácticas.
- Explicar el proceso de ósmosis y describir cómo se aplica industrialmente y en la naturaleza.
Las propiedades de una solución son diferentes de las de soluto(s) puro o solvente. Muchas propiedades de la solución dependen de la identidad química del soluto. En comparación con el agua pura, una solución de cloruro de hidrógeno es más ácida, una solución de amoníaco es más básica, una solución de cloruro de sodio es más densa y una solución de sacarosa es más viscosa. Sin embargo, hay algunas propiedades de solución que dependen solo de la concentración total de especies de solutos, independientemente de sus identidades. Estas propiedades coligativas incluyen la disminución de la presión de vapor, elevación del punto de ebullición, depresión del punto de congelación y presión osmótica. Este pequeño conjunto de propiedades es de importancia central para muchos fenómenos naturales y aplicaciones tecnológicas, como se describirá en este módulo.
La fracción molar y la molalidad
En un capítulo anterior de este texto, se introdujeron varias unidades comúnmente usadas para expresar las concentraciones de los componentes de la solución, cada una de las cuales proporciona ciertos beneficios para su uso en diferentes aplicaciones. Por ejemplo, la molaridad (M) es una unidad conveniente para usar en cálculos estequiométricos, ya que se define en términos de las cantidades molares de especies de solutos:
\[M=\dfrac{\text{mol solute}}{\text{L solution}} \label{11.5.1}\]
Debido a que los volúmenes de la solución varían con la temperatura, las concentraciones molares también variarán. Cuando se expresa como molaridad, la concentración de una solución con un número idéntico de especies de soluto y disolvente será diferente a diferentes temperaturas, debido a la contracción/expansión de la solución. Más apropiados para los cálculos que involucran muchas propiedades coligativas son las unidades de concentración basadas en moles cuyos valores no dependen de la temperatura. Dos de estas unidades son la fracción molar (introducida en el capítulo anterior sobre gases) y la molalidad.
La fracción molar, \(X\), de un componente es la relación entre su cantidad molar y el número total de moles de todos los componentes de la solución:
\[X_\ce{A}=\dfrac{\text{mol A}}{\text{total mol of all components}} \label{11.5.2}\]
La molalidad es una unidad de concentración definida como la relación entre el número de moles de soluto y la masa del solvente en kilogramos:
\[m=\dfrac{\text{mol solute}}{\text{kg solvent}} \label{11.5.3}\]
Dado que estas unidades se calculan usando solo masas y cantidades molares, no varían con la temperatura y, por lo tanto, son más adecuadas para aplicaciones que requieren concentraciones independientes de la temperatura, incluidas varias propiedades coligativas, como se describirá en este módulo del capítulo.
Ejemplo \(\PageIndex{1}\): CÁLCULO DE FRACCIÓN Y MOLALIDAD DEL MOLE
El anticongelante en la mayoría de los radiadores de automóviles es una mezcla de volúmenes iguales del etilenglicol y el agua, con pequeñas cantidades de otros aditivos que evitan la corrosión. ¿Cuáles son la (a) fracción molar y (b) la molalidad del etilenglicol, C2H4(OH)2, en una solución preparada a partir de \(\mathrm{2.22\times10^3\;g}\) del etilenglicol y \(\mathrm{2.00\times10^3\;g}\) del agua (aproximadamente 2 L de glicol y 2 L de agua)?
Solución
(a) La fracción molar del etilenglicol se puede calcular derivando primero las cantidades molares de ambos componentes de la solución y luego sustituyendo estas cantidades en la definición de la unidad.
\(\mathrm{mol\:H_2O=2000\:g×\dfrac{1\:mol\:H_2O}{18.02\:g\:H_2O}=111\:mol\:H_2O}\)
\(X_\mathrm{ethylene\:glycol}=\mathrm{\dfrac{35.8\:mol\:C_2H_4(OH)_2}{(35.8+111)\:mol\: total}=0.245}\)
Observe que la fracción molar es una propiedad adimensional, que es la relación de propiedades con unidades idénticas (moles).
(b) Para encontrar la molalidad, necesitamos saber los moles del soluto y la masa del solvente (en kg).
Primero, use la masa dada del etilenglicol y su masa molar para encontrar los moles de soluto:
Luego, convierta la masa del agua de gramos a kilogramos:
Finalmente, calcule la molaridad según su definición:
\ce{molality}&=\mathrm{\dfrac{mol\: solute}{kg\: solvent}}\\
\ce{molality}&=\mathrm{\dfrac{35.8\:mol\:C_2H_4(OH)_2}{2\:kg\:H_2O}}\\
\ce{molality}&=17.9\:m
\end{align}\)
Ejercicio \(\PageIndex{1}\)
¿Cuáles son la fracción molar y la molalidad de una solución que contiene 0.850 g de amoniaco, NH3, disuelto en 125 g de agua?
- Respuesta
-
7.14 × 10−3; 0.399 m
Ejemplo \(\PageIndex{2}\): CONVERTIR FRACCIÓN DE MOLE Y CONCENTRACIONES MOLALES
Calcule la fracción molar del soluto y disolvente en una solución de cloruro de sodio de 3.0 m.
Solución
La conversión de una unidad de concentración a otra se logra comparando primero las dos definiciones de unidad. En este caso, ambas unidades tienen el mismo numerador (moles de soluto) pero diferentes denominadores. La concentración molal proporcionada se puede escribir como:
\[\mathrm{\dfrac{3.0\;mol\; NaCl}{1.0\; kg\; H_2O}} \label{11.5.X}\]
El numerador para la fracción molar de esta solución es, por lo tanto, 3.0 mol de NaCl. El denominador se puede calcular derivando la cantidad molar del agua correspondiente a 1.0 kg
\(\mathrm{1.0\:kg\:H_2O\left(\dfrac{1000\:g}{1\:kg}\right)\left(\dfrac{mol\:H_2O}{18.02\:g}\right)=55\:mol\:H_2O}\)
y luego sustituyendo estas cantidades molares en la definición de fracción molar.
\[\begin{align*}
X_\mathrm{H_2O}&=\mathrm{\dfrac{mol\:H_2O}{mol\: NaCl + mol\:H_2O}}\\
X_\mathrm{H_2O}&=\mathrm{\dfrac{55\:mol\:H_2O}{3.0\:mol\: NaCl+55\:mol\:H_2O}}\\
X_\mathrm{H_2O}&=0.95\\
X_\mathrm{NaCl}&=\mathrm{\dfrac{mol\: NaCl}{mol\: NaCl+mol\:H_2O}}\\
X_\mathrm{NaCl}&=\mathrm{\dfrac{3.0\:mol\:NaCl}{3.0\:mol\: NaCl+55\:mol\:H_2O}}\\
X_\mathrm{NaCl}&=0.052
\end{align*}\]
Ejercicio \(\PageIndex{2}\)
La fracción molar del yodo, \(\mathrm{I_2}\), disuelta en el diclorometano, \(\mathrm{CH_2Cl_2}\), es 0.115. ¿Cuál es la concentración molal, m, del yodo en esta solución?
- Respuesta
-
1.50 m
Reducción de presión de vapor
Como se describe en el capítulo sobre los líquidos y los sólidos, la presión de vapor de equilibrio de un líquido es la presión ejercida por su fase gaseosa cuando la vaporización y la condensación se producen a velocidades iguales:
\[ \text{liquid} \rightleftharpoons \text{gas} \label{11.5.4}\]
La disolución de una sustancia no volátil en un líquido volátil da como resultado una disminución de la presión de vapor del líquido. Este fenómeno puede racionalizarse considerando el efecto de las moléculas de soluto agregadas en los procesos de vaporización y condensación del líquido. Para vaporizar, las moléculas solventes deben estar presentes en la superficie de la solución. La presencia de soluto disminuye el área de superficie disponible para las moléculas de disolvente y, por lo tanto, reduce la velocidad de vaporización del disolvente. Dado que la velocidad de condensación no se ve afectada por la presencia del soluto, el resultado neto es que el equilibrio de vaporización-condensación se logra con menos moléculas de disolvente en la fase de vapor (es decir, a una presión de vapor más baja) (Figura \(\PageIndex{1}\)). Mientras esta interpretación cinética es útil, no tiene en cuenta varios aspectos importantes de la naturaleza coligativa de la reducción de la presión de vapor. Una explicación más rigurosa involucra la propiedad de la entropía, un tema de discusión en un capítulo de texto posterior sobre la termodinámica. Para comprender la disminución de la presión de vapor de un líquido, es adecuado tener en cuenta que la mayor entropía de una solución en comparación con su disolvente y soluto separados sirve para estabilizar efectivamente las moléculas de disolvente y dificultar su vaporización. Se produce una presión de vapor más baja y un punto de ebullición correspondientemente más alto como se describe en la siguiente sección de este módulo.
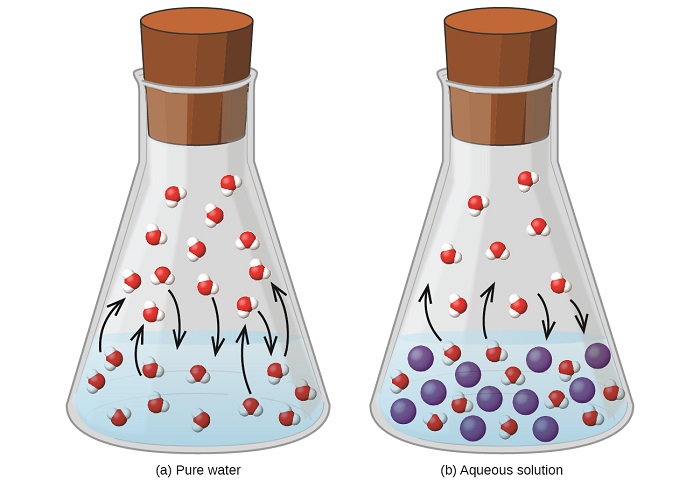
La ley de Raoult describe la relación entre las presiones de vapor de los componentes de la solución y las concentraciones de esos componentes: la presión parcial ejercida por cualquier componente de una solución ideal es igual a la presión de vapor del componente puro multiplicado por su fracción molar en la solución.
\[P_\ce{A}=X_\ce{A}P^\circ_\ce{A} \label{11.5.5}\]
donde PA es la presión parcial ejercida por el componente A en la solución, \(P^\circ_\ce{A}\) es la presión de vapor de A puro, y XA es la fracción molar de A en la solución. (La fracción molar es una unidad de concentración introducida en el capítulo sobre gases).
Recordando que la presión total de una mezcla gaseosa es igual a la suma de presiones parciales para todos sus componentes (ley de Dalton de presiones parciales), la presión de vapor total ejercida por una solución que contiene i componentes es
\[P_\ce{solution}=\sum_{i}P_i=\sum_{i}X_iP^\circ_i \label{11.5.6}\]
Una sustancia no volátil es aquella cuya presión de vapor es insignificante (P° ≈ 0), por lo que la presión de vapor sobre una solución que contiene solo solutos no volátiles se debe solo al disolvente:
\[P_\ce{solution}=X_\ce{solvent}P^\circ_\ce{solvent} \label{11.5.7}\]
Ejemplo \(\PageIndex{3}\): CÁLCULO DE la PRESIÓN DE VAPOR
Calcule la presión de vapor de una solución ideal que contiene 92.1 g de glicerina, C3H5(OH)3 y 184.4 g de etanol, C2H5OH, a 40 °C. La presión de vapor del etanol puro es de 0.178 atm a 40 °C. La glicerina es esencialmente no volátil a esta temperatura.
Solución
Dado que el disolvente es el único componente volátil de esta solución, su presión de vapor puede calcularse según la ley de Raoult como:
\(P_\ce{solution}=X_\ce{solvent}P^\circ_\ce{solvent}\)
Primero, calcule las cantidades molares de cada componente de la solución usando los datos de masa proporcionados.
\(\mathrm{92.1\cancel{g\:C_3H_5(OH)_3}×\dfrac{1\:mol\:C_3H_5(OH)_3}{92.094\cancel{g\:C_3H_5(OH)_3}}=1.00\:mol\:C_3H_5(OH)_3}\)
Luego, calcule la fracción molar del solvente (etanol) y use la ley de Raoult para calcular la presión de vapor de la solución.
\(X_\mathrm{C_2H_5OH}=\mathrm{\dfrac{4.000\:mol}{(1.00\:mol+4.000\:mol)}=0.800}\)
Ejercicio \(\PageIndex{3}\)
Una solución contiene 5.00 g de urea, CO(NH2)2 (un soluto no volátil) y 0.100 kg de agua. Si la presión de vapor del agua pura a 25 °C es 23.7 torr, ¿Cuál es la presión de vapor de la solución?
- Respuesta
-
23.4 torr
Elevación del punto de ebullición de un solvente
Como se describió en el capítulo sobre los líquidos y los sólidos, el punto de ebullición de un líquido es la temperatura a la cual su presión de vapor es igual a la presión atmosférica ambiental. Dado que la presión de vapor de una solución se reduce debido a la presencia de solutos no volátiles, es lógico que el punto de ebullición de la solución se incremente posteriormente. En comparación con el disolvente puro, una solución, por lo tanto, requerirá una temperatura más alta para lograr cualquier presión de vapor dada, incluida una equivalente a la de la atmósfera circundante. El aumento en el punto de ebullición observado cuando el soluto no volátil se disuelve en un solvente, \(ΔT_b\), se llama la elevación del punto de ebullición y es directamente proporcional a la concentración molal de especies de soluto:
\[ΔT_b=K_bm \label{11.5.8}\]
donde
- \(K_\ce{b}\) es el constante de elevación del punto de ebullición, o el constante ebullioscópica y+-
- \(m\) es la concentración molal (molalidad) de todas las especies de solutos.
Los constantes de elevación del punto de ebullición son propiedades características que dependen de la identidad del disolvente. Los valores de Kb para varios solventes se enumeran en la Tabla \(\PageIndex{1}\).
| Solvente | Punto de ebullición (°C a 1 atm) | Kb (Cm−1) | Punto de congelación(°C a 1 atm) | Kf (Cm−1) |
|---|---|---|---|---|
| agua | 100.0 | 0.512 | 0.0 | 1.86 |
| acetato de hidrógeno | 118.1 | 3.07 | 16.6 | 3.9 |
| benceno | 80.1 | 2.53 | 5.5 | 5.12 |
| cloroformo | 61.26 | 3.63 | −63.5 | 4.68 |
| nitrobenceno | 210.9 | 5.24 | 5.67 | 8.1 |
La medida en que se reduce la presión de vapor de un disolvente y se eleva el punto de ebullición depende del número total de partículas de soluto presentes en una cantidad dada de disolvente, no de la masa o el tamaño o las identidades químicas de las partículas. Una solución acuosa de sacarosa de 1 m (342 g/mol) y una solución acuosa de etilenglicol de 1 m (62 g/mol) exhibirán el mismo punto de ebullición porque cada solución tiene un mol de partículas de soluto (moléculas) por kilogramo de disolvente.
Ejemplo \(\PageIndex{4}\): CALCULANDO EL PUNTO DE EBULLICIÓN DE UNA SOLUCIÓN
¿Cuál es el punto de ebullición de una solución de 0.33 m de un soluto no volátil en benceno?
Solución
Use la ecuación que relaciona la elevación del punto de ebullición con la molalidad del soluto para resolver este problema en dos pasos.

- Calcule el cambio en el punto de ebullición.
- Agregue la elevación del punto de ebullición al punto de ebullición del solvente puro.
\(\mathrm{Boiling\: temperature=80.1\:°C+0.83\:°C=80.9\:°C}\)
Ejercicio \(\PageIndex{4}\)
¿Cuál es el punto de ebullición del anticongelante descrito en el Ejemplo \(\PageIndex{4}\)?
- Respuesta
-
109.2 °C
Ejemplo \(\PageIndex{5}\): El punto de ebullición de una solución de yodo
Encuentre el punto de ebullición de una solución de 92.1 g de yodo, I2, en 800.0 g de cloroformo, CHCl3, suponiendo que el yodo no sea volátil y que la solución sea ideal.
Solución
Podemos resolver este problema usando cuatro pasos.
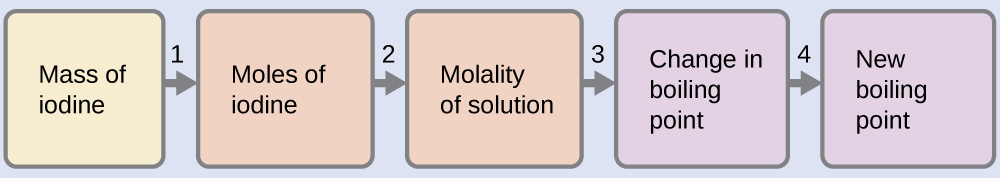
- Convierte de gramos a moles de I2 usando la masa molar de I2 en el factor de conversión de la unidad.
- Determine la molalidad de la solución a partir del número de moles de soluto y la masa de solvente, en kilogramos. Resultado: 0.454 m
- Use la proporcionalidad directa entre el cambio en el punto de ebullición y la concentración molal para determinar cuánto cambia el punto de ebullición. Resultado: 1.65 °C
- Determine el nuevo punto de ebullición a partir del punto de ebullición del disolvente puro y el cambio. Resultado: 62.91 °C Verifique cada resultado como una autoevaluación.
- Verifique cada resultado como una autoevaluación.
Ejercicio \(\PageIndex{5}\)
¿Cuál es el punto de ebullición de una solución de 1.0 g de glicerina, C3H5(OH)3, en 47.8 g de agua? Asume una solución ideal.
- Respuesta
-
100.12 °C
Destilación de las Soluciones
La destilación es una técnica para separar los componentes de las mezclas que se aplica ampliamente tanto en el laboratorio como en entornos industriales. Se utiliza para refinar petróleo, para aislar productos de fermentación y para purificar agua. Esta técnica de separación implica el calentamiento controlado de una mezcla de muestra para vaporizar, condensar y recoger selectivamente uno o más componentes de interés. Un aparato típico para destilaciones a escala de laboratorio se muestra en la Figura \(\PageIndex{2}\).
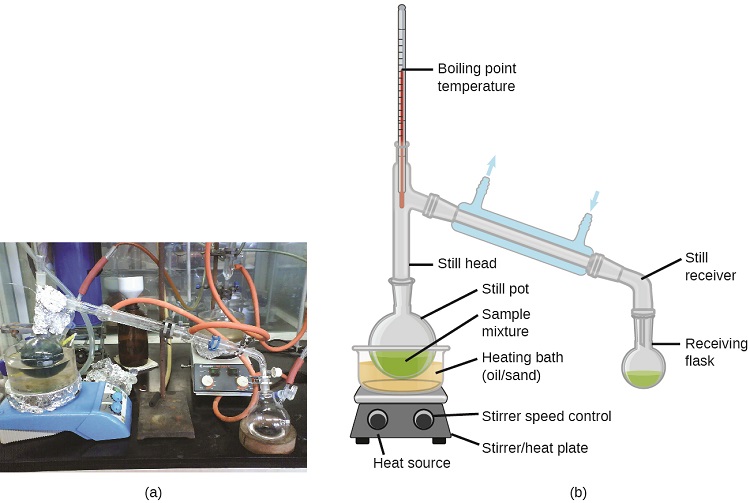
Las refinerías de petróleo usan la destilación fraccionada a gran escala para separar los componentes del petróleo crudo. El petróleo crudo se calienta a altas temperaturas en la base de una columna de fraccionamiento alta, vaporizando muchos de los componentes que se elevan dentro de la columna. A medida que los componentes vaporizados alcanzan zonas adecuadamente frías durante su ascenso, se condensan y se recogen. Los líquidos recolectados son mezclas más simples de hidrocarburos y otros compuestos de petróleo que son de composición apropiada para diversas aplicaciones (por ejemplo, el combustible diesel, la queroseno, la gasolina), como se muestra en la Figura \(\PageIndex{3}\).
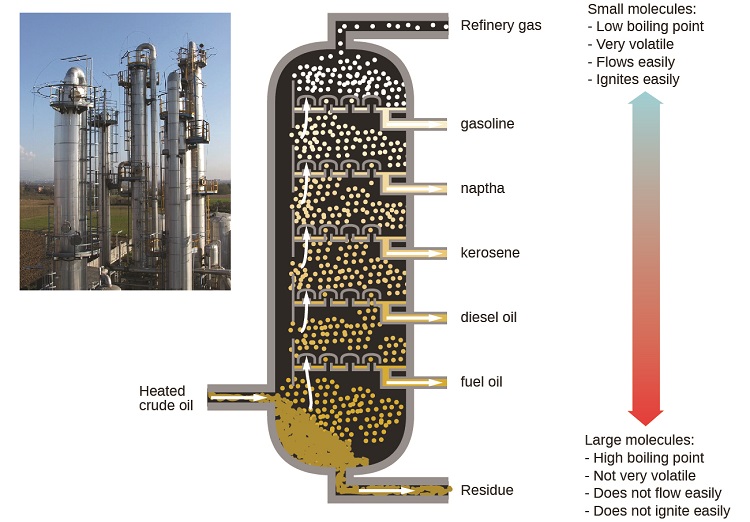
Depresión del punto de congelación de un solvente
Las soluciones se congelan a temperaturas más bajas que los líquidos puros. Este fenómeno se explota en las esquemas de "descongelación" que usan sal (Figura \(\PageIndex{4}\)), cloruro de calcio o urea para derretir el hielo en las carreteras y las aceras, y en el uso del etilenglicol como " el anticongelante "en radiadores de automóviles. El agua del mar se congela a una temperatura más baja que el agua dulce, por lo que los océanos ártico y antártico permanecen sin congelar incluso a temperaturas de bajo de 0 °C (al igual que los fluidos corporales de peces y otros animales marinos de sangre fría que viven en estos océanos).

La disminución del punto de congelación de una solución diluida en comparación con la del disolvente puro, ΔTf, se llama la depresión del punto de congelación y es directamente proporcional a la concentración molal del soluto.
\[ΔT_\ce{f}=K_\ce{f}m \label{11.5.9}\]
donde
- \(m\) es la concentración molal del soluto en el solvente y
- \(K_f\) se llama el constante de depresión del punto de congelación (o el constante crioscópica).
Al igual que para los constantes de elevación del punto de ebullición, estas son propiedades características cuyos valores dependen de la identidad química del disolvente. Los valores de Kf para varios solventes se enumeran en la Tabla \(\PageIndex{1}\).
Ejemplo \(\PageIndex{5}\): CÁLCULO DEL PUNTO DE CONGELACIÓN DE UNA SOLUCIÓN
¿Cuál es el punto de congelación de una solución de 0.33 m de un soluto no volátil no electrolítico en benceno descrito en el Ejemplo \(\PageIndex{4}\)?
Solución
Use la ecuación que relaciona la depresión del punto de congelación con la molalidad del soluto para resolver este problema en dos pasos.

- Calcule el cambio en el punto de congelación. \[ΔT_\ce{f}=K_\ce{f}m=5.12\:°\ce C\:m^{−1}×0.33\:m=1.7\:°\ce C\]
- Reste el cambio del punto de congelación observado del punto de congelación del solvente puro. [\mathrm{Freezing\: Temperature=5.5\:°C−1.7\:°C=3.8\:°C}\]
Ejercicio \(\PageIndex{6}\)
¿Cuál es el punto de congelación de una solución de 1.85 m de un soluto no volátil no electrolítico en nitrobenceno?
- Respuesta
-
−9.3 °C
Propiedades colectivas y eliminación
El cloruro de sodio y sus análogos del grupo 2 como el cloruro de calcio y el magnesio se usan a menudo para descongelar las carreteras y las aceras, debido al hecho de que una solución de cualquiera de estas sales tendrá un punto de congelación de bajo de 0 °C, el punto de congelación de el agua pura. Las sales metálicas del grupo 2 se mezclan con frecuencia con el cloruro de sodio ("sal de roca") más barato y más fácilmente disponible para su uso en las carreteras, ya que tienden a ser algo menos corrosivos que el NaCl, y proporcionan una mayor depresión del punto de congelación , ya que se disocian para producir tres partículas por unidad de fórmula, en lugar de dos partículas como el cloruro de sodio.
Debido a que estos compuestos iónicos tienden a acelerar la corrosión del metal, no sería una buena idea usar los anticongelantes para el radiador de su automóvil o descongelar un avión antes del despegue. Para estas aplicaciones, a menudo se usan compuestos covalentes, como el etileno o el propilenglicol. Los glicoles usados en el fluido del radiador no solo reducen el punto de congelación del líquido, sino que también elevan el punto de ebullición, haciendo que el fluido sea útil tanto en el invierno como en el verano. Los glicoles calentados a menudo se rocían sobre la superficie de los aviones antes del despegue en condiciones climáticas adversas en invierno para eliminar el hielo que ya se ha formado y evitar la formación de más hielo, lo que sería particularmente peligroso si se forma en las superficies de control de la aeronave (Video \(\PageIndex{1}\)).
Video \(\PageIndex{1}\): La depresión del punto de congelación se explota para eliminar el hielo de las superficies de control de los aviones.
Diagrama de fase para una solución acuosa de un no electrolito
Los efectos coligativos sobre la presión de vapor, el punto de ebullición y el punto de congelación descritos en la sección anterior se resumen convenientemente comparando los diagramas de fase para un líquido puro y una solución derivada de ese líquido. Los diagramas de fase para el agua y una solución acuosa se muestran en la Figura \(\PageIndex{5}\).
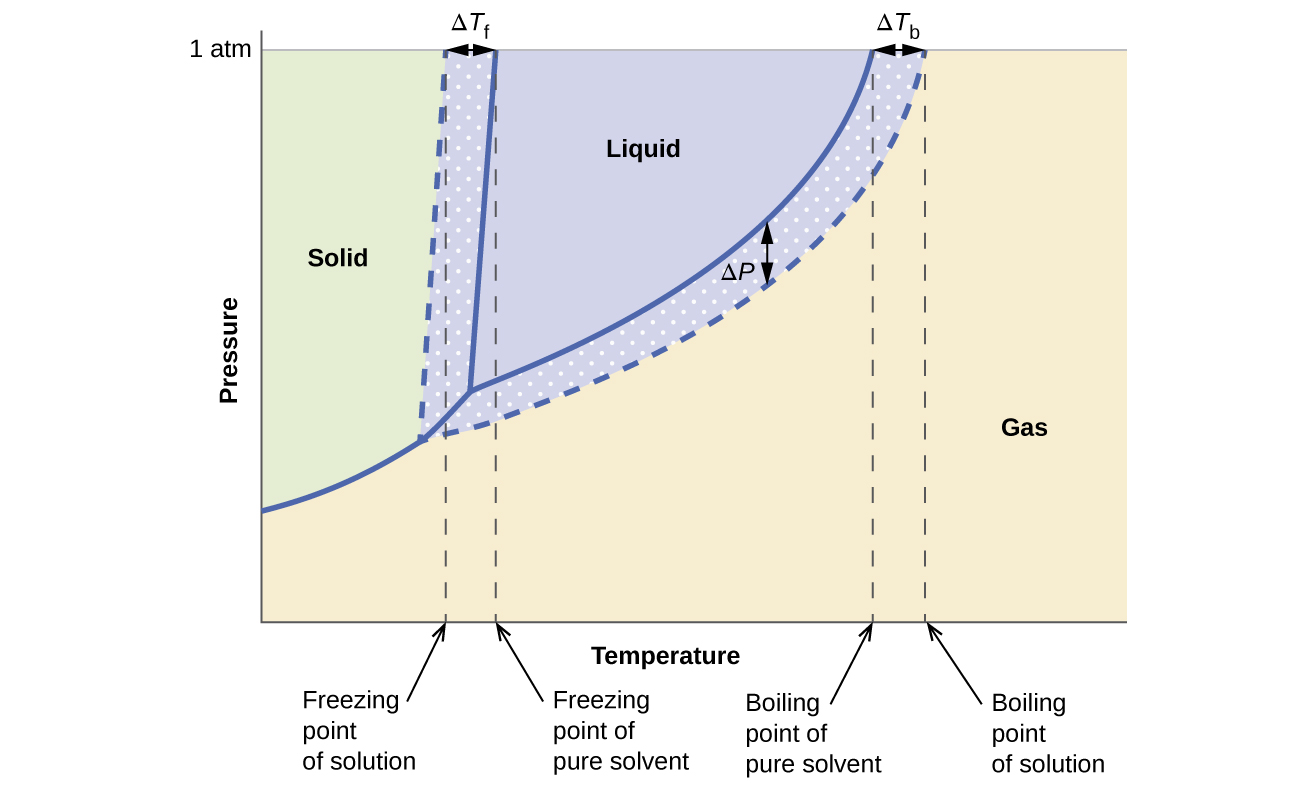
La curva de vapor-líquido para la solución se encuentra debajo de la curva correspondiente para el disolvente, que representa la disminución de la presión de vapor, ΔP, que resulta de la disolución del soluto no volátil. En consecuencia, a cualquier presión dada, el punto de ebullición de la solución se observa a una temperatura más alta que la del solvente puro, lo que refleja la elevación del punto de ebullición, ΔTb, asociada con la presencia del soluto no volátil. La curva de sólido-líquido para la solución se desplaza a la izquierda de la del disolvente puro, lo que representa la depresión del punto de congelación, ΔTf, que acompaña a la formación de la solución. Finalmente, observe que las curvas de gas sólido para el solvente y su solución son idénticas. Este es el caso para muchas soluciones que comprenden de solventes líquidos y de solutos no volátiles. Al igual que para la vaporización, cuando una solución de este tipo se congela, en realidad son solo las moléculas de solvente las que experimentan la transición de líquido a sólido, formando solvente sólido puro que excluye las especies de solutos. Las fases sólida y gaseosa, por lo tanto, están compuestas de solventes solamente, por lo que las transiciones entre estas fases no experimentan efectos coligativos.
La osmosis y la presión osmótica de las soluciones
Varios materiales naturales y sintéticos exhiben permeación selectiva, lo que significa que solo las moléculas o los iones de cierto tamaño, forma, polaridad, carga, etc., pueden atravesar (penetrar) el material. Las membranas celulares biológicas proporcionan ejemplos elegantes de permeación selectiva en la naturaleza, mientras que los tubos de diálisis usados para eliminar los desechos metabólicos de la sangre son un ejemplo tecnológico más simplista. Independientemente de cómo se puedan fabricar, estos materiales generalmente se refieren como membranas semipermeables.
Considere el aparato ilustrado en la Figura \(\PageIndex{6}\), en el que las muestras de solvente puro y una solución están separadas por una membrana que solo las moléculas de solvente pueden penetrar. Las moléculas de los solventes se difundirán a través de la membrana en ambas direcciones. Dado que la concentración de solvente es mayor en el solvente puro que en la solución, estas moléculas se difundirán desde el lado del solvente de la membrana al lado de la solución a una velocidad más rápida que en la dirección inversa. El resultado es una transferencia neta de moléculas de disolvente del disolvente puro a la solución. La transferencia impulsada por la difusión de las moléculas del disolvente a través de una membrana semipermeable es un proceso conocido como la ósmosis.
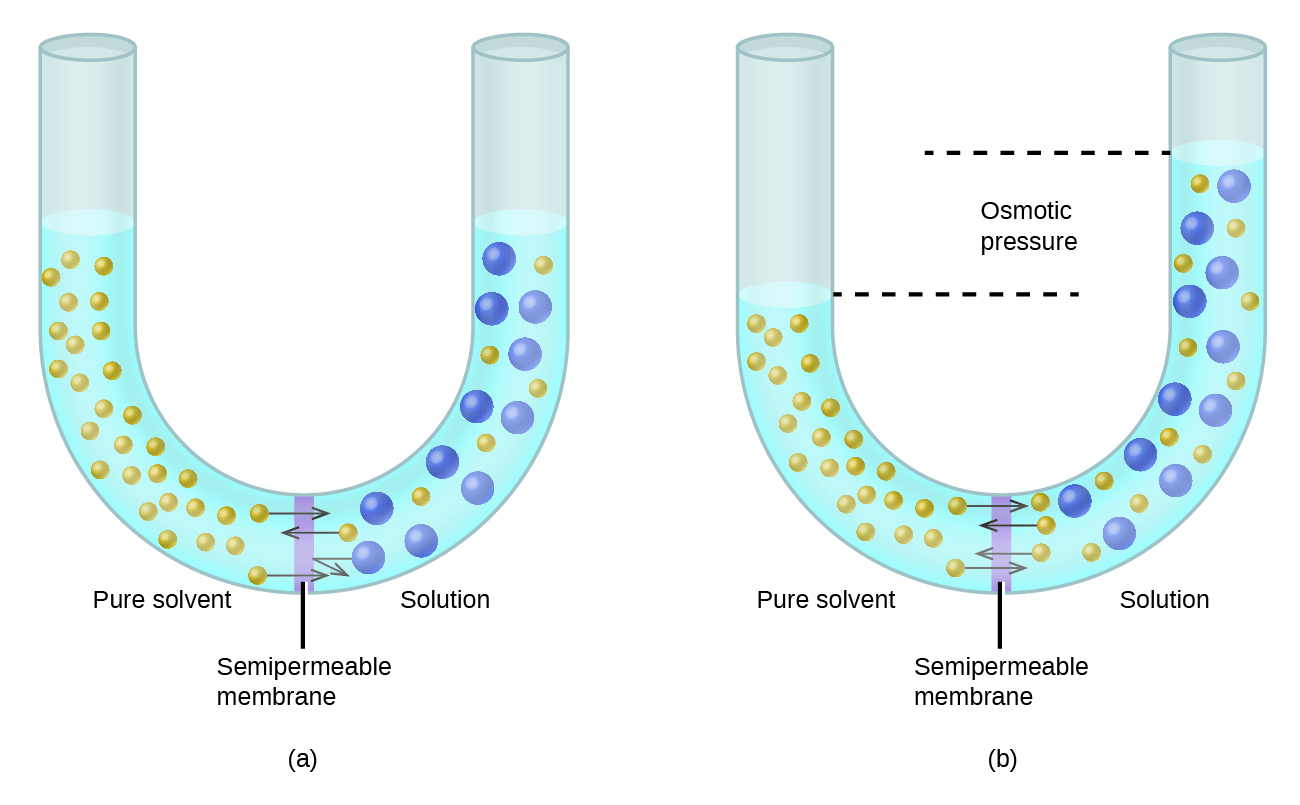
Cuando la ósmosis se lleva a cabo en un aparato como el que se muestra en la Figura \(\PageIndex{6}\), el volumen de la solución aumenta a medida que se diluye por la acumulación de solvente. Esto hace que el nivel de la solución aumente, aumentando su presión hidrostática (debido al peso de la columna de solución en el tubo) y resultando en una transferencia más rápida de moléculas de solvente de regreso al lado del solvente puro. Cuando la presión alcanza un valor que produce una velocidad de transferencia de solvente inversa igual a la velocidad de la ósmosis, la transferencia masiva de solvente para. Esta presión se llama la presión osmótica (\(\Pi\)) de la solución. La presión osmótica de una solución diluida está relacionada con su molaridad de soluto, M, y su temperatura absoluta, T, de acuerdo con la ecuación
donde \(R\) es el constante universal del gas
Ejemplo \(\PageIndex{7}\): Calculation of Osmotic Pressure
¿Cuál es la presión osmótica (atm) de una solución de glucosa 0.30 M en el agua que se usa para infusión intravenosa a temperatura corporal, 37 °C?
Solución
Podemos encontrar la presión osmótica, Π, usando la fórmula Π = MRT, donde T está en la escala Kelvin (310 K) y el valor de R se expresa en unidades apropiadas (0.08206 L atm/mol K).
\(\begin{align}
Π&=MRT\\
&=\mathrm{0.03\:mol/L×0.08206\: L\: atm/mol\: K×310\: K}\\
&=\mathrm{7.6\:atm}
\end{align}\)
Ejercicio \(\PageIndex{7}\)
¿Cuál es la presión osmótica (atm) una solución con un volumen de 0.750 L que contiene 5.0 g de metanol, CH3OH, en agua a 37 °C?
- Respuesta
-
5.3 atm
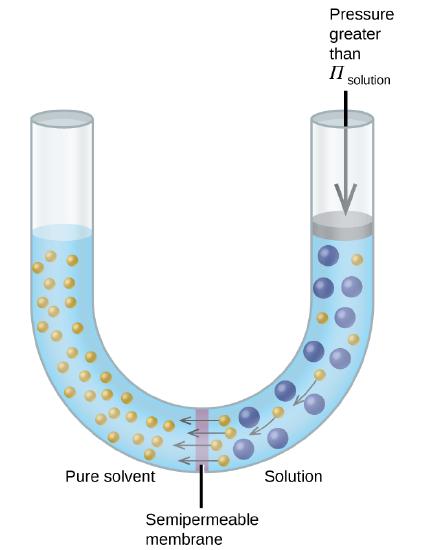
Si se coloca una solución en un aparato como el que se muestra en la Figura \(\PageIndex{7}\), la aplicación de una presión mayor que la presión osmótica de la solución invierte la ósmosis y empuja las moléculas de disolvente de la solución al disolvente puro. Esta técnica de ósmosis inversa se usa para la desalinización a gran escala de agua de mar y en escalas más pequeñas para producir el agua del grifo de alta pureza para beber.
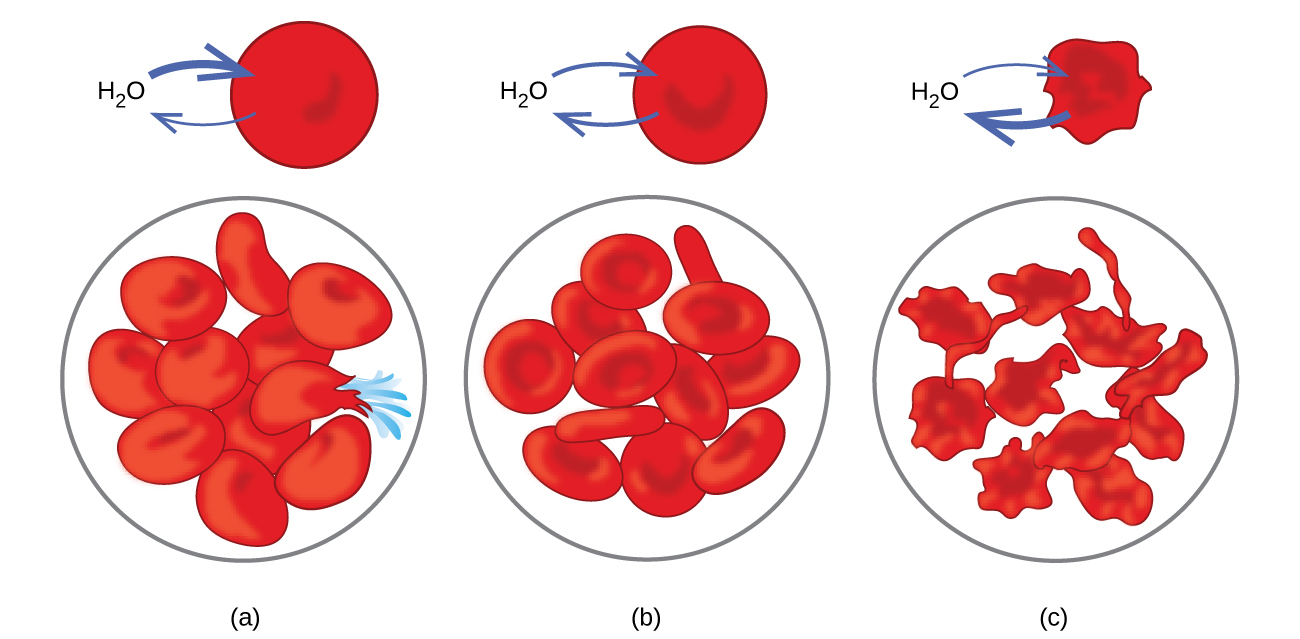
Los ejemplos de la ósmosis son evidentes en muchos sistemas biológicos porque las células están rodeadas de membranas semipermeables. Los vegetales como las zanahorias y el apio que se han vuelto flácidos porque han perdido agua pueden volverse crujientes si vuelve a ponerlos en el agua. El agua se mueve hacia las células de la zanahoria o el apio por la ósmosis. Un pepino colocado en una solución salina concentrada pierde agua por la ósmosis y absorbe un poco de sal para convertirse en un pepinillo. La ósmosis también puede afectar las células de los animales. Las concentraciones de solutos son particularmente importantes cuando se inyectan soluciones en el cuerpo. Los solutos en los fluidos celulares del cuerpo y el suero sanguíneo le dan a estas soluciones una presión osmótica de aproximadamente 7.7 atm. Las soluciones inyectadas en el cuerpo deben tener la misma presión osmótica que el suero sanguíneo; es decir, deben ser isotónicos con suero sanguíneo. Si se inyecta una solución menos concentrada, una solución hipotónica, en cantidad suficiente para diluir el suero sanguíneo, el agua del suero diluido pasa a las células sanguíneas por ósmosis, haciendo que las células se expandan y se rompan. Este proceso se llama hemólisis. Cuando se inyecta una solución más concentrada, una solución hipertónica, las células pierden agua a la solución más concentrada, se marchitan y posiblemente mueren en un proceso llamado la crenation (Figura 11.5.8).
Determinación de las masas molares
La presión osmótica y los cambios en el punto de congelación, el punto de ebullición y la presión de vapor son directamente proporcionales a la concentración de soluto presente. En consecuencia, podemos usar una medición de una de estas propiedades para determinar la masa molar del soluto a partir de las mediciones.
Ejemplo \(\PageIndex{8}\): DETERMINANDO LA MASA MOLAR DE LA DEPRESIÓN DEL PUNTO DE CONGELACIÓN
Se encuentra que una solución de 4.00 g de un no electrolito disuelto en 55.0 g de benceno se congela a 2.32 °C. ¿Cuál es la masa molar de este compuesto?
Solución
Podemos resolver este problema usando los siguientes pasos.
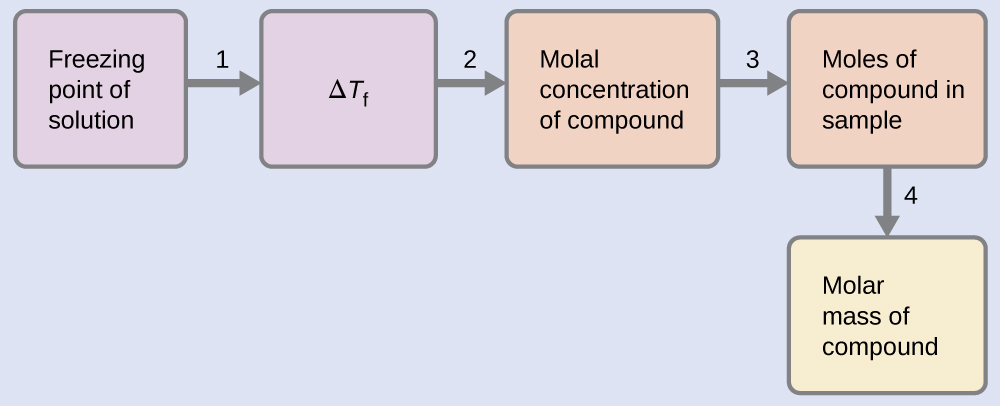
- Determine el cambio en el punto de congelación desde el punto de congelación observado y el punto de congelación del benceno puro (Tabla 11.5.1).
- Determine la concentración molal de Kf, celonstante de depresión del punto de congelación para el benceno (Table 11.5.1), y ΔTf.
\(ΔT_\ce{f}=K_\ce{f}m\)
\(m=\dfrac{ΔT_\ce{f}}{K_\ce{f}}=\dfrac{3.2\:°\ce C}{5.12\:°\ce C m^{−1}}=0.63\:m\) - Determine el número de moles de compuesto en la solución a partir de la concentración molal y la masa de solvente usado para preparar la solución.
\(\mathrm{Moles\: of\: solute=\dfrac{0.62\:mol\: solute}{1.00\cancel{kg\: solvent}}×0.0550\cancel{kg\: solvent}=0.035\:mol}\)
- Determine la masa molar a partir de la masa del soluto y el número de moles en esa masa.
\(\mathrm{Molar\: mass=\dfrac{4.00\:g}{0.034\:mol}=1.2×10^2\:g/mol}\)
Ejercicio \(\PageIndex{8}\)
Una solución de 35.7 g de un no electrolito en 220.0 g de cloroformo tiene un punto de ebullición de 64.5 °C. ¿Cuál es la masa molar de este compuesto?
- Respuesta
-
1.8 × 102 g/mol
Ejemplo\(\PageIndex{9}\): DETERMINACIÓN DE la MASA MOLAR a partir de la PRESIÓN OSMÓTICA
Una muestra de 0.500 L de una solución acuosa que contiene 10.0 g de la hemoglobina tiene una presión osmótica de 5.9 torr a 22 °C. ¿Cuál es la masa molar de la hemoglobina?
Solución
Aquí hay un conjunto de pasos que se pueden usar para resolver este problema:
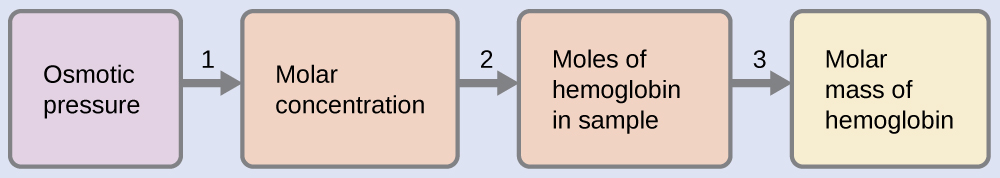
1. Convierta la presión osmótica en atmósferas, luego determine la concentración molar de la presión osmótica.
\[\Pi=\mathrm{\dfrac{5.9\:torr×1\:atm}{760\:torr}=7.8×10^{−3}\:atm}\]
\[\Pi=MRT\]
\(M=\dfrac{Π}{RT}=\mathrm{\dfrac{7.8×10^{−3}\:atm}{(0.08206\:L\: atm/mol\: K)(295\:K)}=3.2×10^{−4}\:M}\)
2. Determine el número de moles de la hemoglobina en la solución a partir de la concentración y el volumen de la solución.
\(\mathrm{moles\: of\: hemoglobin=\dfrac{3.2×10^{−4}\:mol}{1\cancel{L\: solution}}×0.500\cancel{L\: solution}=1.6×10^{−4}\:mol}\)
3. Determine la masa molar a partir de la masa de hemoglobina y el número de moles en esa masa.
\(\mathrm{molar\: mass=\dfrac{10.0\:g}{1.6×10^{−4}\:mol}=6.2×10^4\:g/mol}\)
Ejercicio \(\PageIndex{9}\)
¿Cuál es la masa molar de una proteína si una solución de 0.02 g de la proteína en 25.0 mL de solución tiene una presión osmótica de 0.56 torr a 25 °C?
- Respuesta
-
2.7 × 104 g/mol
Las propiedades coligativas de los electrolitos
Como aprendimos anteriormente en este módulo, las propiedades coligativas de una solución dependen solo del número, no del tipo, de las especies de los solutos disueltos. Por ejemplo, 1 mol de cualquier no electrolito disuelto en 1 kilogramo de disolvente produce la misma disminución del punto de congelación que 1 mol de cualquier otro no electrolito. Sin embargo, 1 mol de cloruro de sodio (un electrolito) forma 2 moles de iones cuando se disuelve en la solución. Cada ion individual produce el mismo efecto en el punto de congelación que una molécula.
Ejemplo \(\PageIndex{10}\):EL PUNTO DE CONGELACIÓN DE UNA SOLUCIÓN DE UN ELECTROLITO
La concentración de los iones en el agua de mar es aproximadamente la misma que en una solución que contiene 4.2 g de NaCl disuelto en 125 g de agua. Suponga que cada uno de los iones en la solución de NaCl tiene el mismo efecto sobre el punto de congelación del agua que una molécula no electrolítica, y determine la temperatura de congelación de la solución (que es aproximadamente igual a la temperatura de congelación del agua de mar).
Solución
Podemos resolver este problema usando la siguiente serie de pasos.
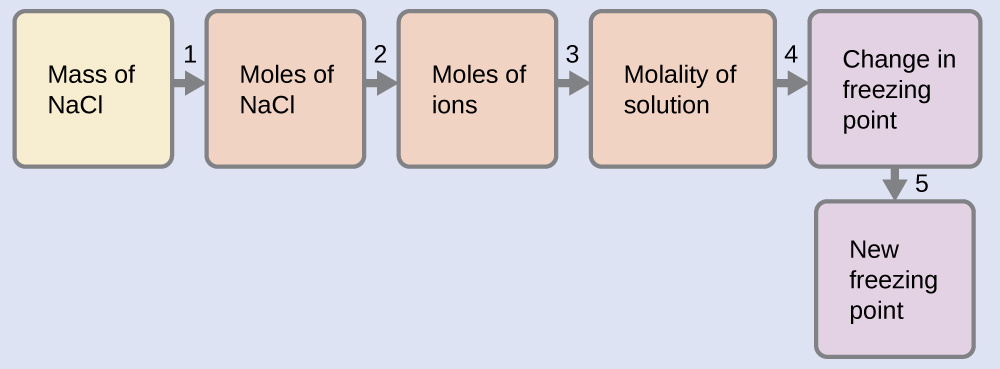
- Convierta de gramos a moles de NaCl usando la masa molar de NaCl en el factor de conversión de unidades. Resultado: 0.072 mol de NaCl
- Determine la cantidad de moles de iones presentes en la solución usando la cantidad de moles de iones en 1 mol de NaCl como el factor de conversión (2 iones mol/1 mol de NaCl). Resultado: 0.14 mol de iones
- Determine la molalidad de los iones en la solución a partir del número de moles de iones y la masa de solvente, en kilogramos. Resultado: 1.1 m
- Use la proporcionalidad directa entre el cambio en el punto de congelación y la concentración molal para determinar el cambio en el punto de congelación. Resultado: 2.0 °C
- Determine el nuevo punto de congelación a partir del punto de congelación del disolvente puro y el cambio. Resultado: −2.0 °C
Verifique cada resultado como una autoevaluación.
Ejercicio \(\PageIndex{10}\)
Suponga que cada uno de los iones en el cloruro de calcio, CaCl2, tiene el mismo efecto en el punto de congelación del agua que una molécula no electrolítica. Calcule el punto de congelación de una solución de 0.724 g de CaCl2 en 175 g de agua.
- Respuesta
-
−0.208 °C
Asumiendo una disociación completa, una solución acuosa de NaCl de 1.0 m contiene 2.0 moles de iones (1.0 mol de Na+ y 1.0 mol de Cl−) por cada kilogramo de agua, y se espera que su depresión del punto de congelación sea
\[ΔT_\ce{f}=\mathrm{2.0\:mol\: ions/kg\: water×1.86\:°C\: kg\: water/mol\: ion=3.7\:°C.} \label{11.5.11}\]
Sin embargo, cuando esta solución se prepara en realidad y se mide su depresión del punto de congelación, se obtiene un valor de 3.4 °C. Se observan discrepancias similares para otros compuestos iónicos, y las diferencias entre los valores medidos y esperados de las propiedades coligativas generalmente se vuelven más significativas cuando aumentan las concentraciones del soluto. Estas observaciones sugieren que los iones de cloruro de sodio (y otros electrolitos fuertes) no están completamente disociados en la solución.
Para considerar esto y evitar los errores que acompañan a la suposición de una disociación total, se usa un parámetro medido experimentalmente en honor del químico alemán ganador del Premio Nobel Jacobus Henricus van’t Hoff. El factor de vant Hoff (i) se define como la relación de partículas de soluto en solución al número de unidades de fórmula disueltas:
\[i=\dfrac{\textrm{moles of particles in solution}}{\textrm{moles of formula units dissolved}} \label{11.5.12}\]
Los valores para los factores de van’t Hoff medidos para varios solutos, junto con los valores pronosticados que suponen una disociación completa, se muestran en la Tabla \(\PageIndex{2}\).
| Electrolito | Partículas en Solución | i (Previsto) | i (Medido) |
|---|---|---|---|
| HCl | H+, Cl− | 2 | 1.9 |
| NaCl | Na+, Cl− | 2 | 1.9 |
| MgSO4 | Mg2+, \(\ce{SO4^2-}\) | 2 | 1.3 |
| MgCl2 | Mg2+, 2Cl− | 3 | 2.7 |
| FeCl3 | Fe3+, 3Cl− | 4 | 3.4 |
| glucosa (un no electrolito) | C12H22O11 | 1 | 1.0 |
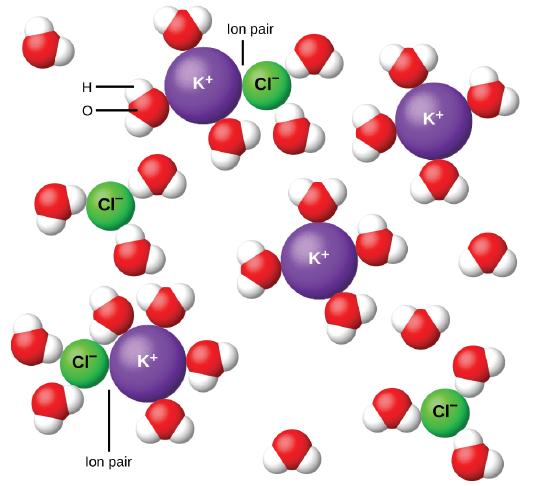
En 1923, los químicos Peter Debye y Erich Hückel propusieron una teoría para explicar la aparente ionización incompleta de los electrolitos fuertes. Sugirieron que, aunque la atracción interiónica en una solución acuosa se reduce en gran medida por la solvatación de los iones y la acción aislante del disolvente polar, no se anula por completo. Las atracciones residuales impiden que los iones se comporten como partículas totalmente independientes (Figura \(\PageIndex{9}\)). En algunos casos, un ion positivo y un ion negativo en realidad pueden tocar, dando una unidad solvatada llamada un par de iones. Por lo tanto, la actividad, o la concentración efectiva, de cualquier tipo particular de ion es menor que la actividad indicada por la concentración real. Los iones se separan cada vez más cuanto más se diluye la solución, y las atracciones interiónicas residuales se disminuyan. Por lo tanto, en soluciones extremadamente diluidas, las concentraciones efectivas de los iones (sus actividades) son esencialmente iguales a las concentraciones reales. Tenga en cuenta que los factores de van’t Hoff para los electrolitos en la Tabla \(\PageIndex{2}\) son para soluciones de 0.05 m, en cual la concentración del valor de i para NaCl es 1.9, en oposición a un valor ideal de 2.
Resumen
Las propiedades de una solución que dependen solo de la concentración de las partículas del soluto se llaman las propiedades coligativas. Incluyen cambios en la presión de vapor, el punto de ebullición y el punto de congelación del solvente en la solución. Las magnitudes de estas propiedades dependen solo de la concentración total de las partículas del soluto en la solución, no del tipo de las partículas. La concentración total de partículas de soluto en una solución también determina su presión osmótica. Esta es la presión que se debe aplicar a la solución para evitar la difusión de las moléculas del disolvente puro a través de una membrana semipermeable hacia la solución. Los compuestos iónicos pueden no disociarse completamente en la solución debido a los efectos de la actividad, en cual caso los efectos coligativos observados pueden ser menores que la predicción.
Ecuaciones Clave
- \(\left(P_\ce{A}=X_\ce{A}P^\circ_\ce{A}\right)\)
- \(P_\ce{solution}=\sum_{i}P_i=\sum_{i}X_iP^\circ_i\)
- \(P_\ce{solution}=X_\ce{solvent}P^\circ_\ce{solvent}\)
- ΔTb = Kbm
- ΔTf = Kfm
- Π = MRT
Notas al Pie de la Página
- Un no electrolito mostrado para comparación
Glosario
- elevación del punto de ebullición
- elevación del punto de ebullición de un líquido mediante la adición de un soluto
- constante de elevación del punto de ebullición
- el constante de proporcionalidad en la ecuación que relaciona la elevación del punto de ebullición con la molalidad del soluto; también conocida como el constante ebullioscópica
- propiedad coligativa
- propiedad de una solución que depende solo de la concentración de una especie de soluto
- crenation
- proceso por el cual las células biológicas se encogen debido a la pérdida de agua por ósmosis
- depresión del punto de congelación
- disminución del punto de congelación de un líquido mediante la adición de un soluto
- punto de congelación depresión constante
- (también, constante crioscópica) constante de proporcionalidad en la ecuación que relaciona la depresión del punto de congelación con la molalidad del soluto
- hemólisis
- ruptura de glóbulos rojos debido a la acumulación de exceso de agua por ósmosis
- hipertónico
- de mayor presión osmótica
- hipotónico
- de presión osmótica baja
- par de iones
- par aniónico / catión solvatado unido por moderada atracción electrostática
- isotónico
- de presión osmótica igual
- molalidad (m)
- una unidad de concentración definida como la relación entre el número de moles de soluto y la masa del solvente en kilogramos
- ósmosis
- difusión de moléculas solventes a través de una membrana semipermeable
- presión osmótica (Π)
- presión opuesta requerida para evitar la transferencia masiva de moléculas de disolvente a través de una membrana semipermeable
- Ley de Raoult
- la presión parcial ejercida por un componente de la solución es igual al producto de la fracción molar del componente en la solución y su presión de vapor de equilibrio en estado puro
- membrana semipermeable
- una membrana que permite selectivamente el paso de ciertos iones o moléculas
- factor de van’t Hoff (i)
- la relación entre el número de moles de partículas en una solución y el número de moles de unidades de fórmula disueltas en la solución
Contribuyentes
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


