13.1: Preludio al equilibrio químico
- Page ID
- 1903
Imagínese una playa poblada de bañistas y nadadores. Los que toman el sol se calientan demasiado por el sol se y quieren refrescar. Se dirigen a las olas para nadar. Cuando los nadadores se cansan, se dirigen a la playa para descansar. Si estas dos tasas de transferencia (bañistas que entran al agua, nadadores que salen del agua) son iguales, el número de bañistas y nadadores sería constante, o en equilibrio, aunque las identidades de las personas cambian constantemente de bañista a nadador y viceversa. Una situación análoga ocurre en las reacciones químicas. Las reacciones pueden ocurrir en ambas direcciones simultáneamente (reactivos a productos y productos a reactivos) y eventualmente alcanzar un estado de equilibrio.
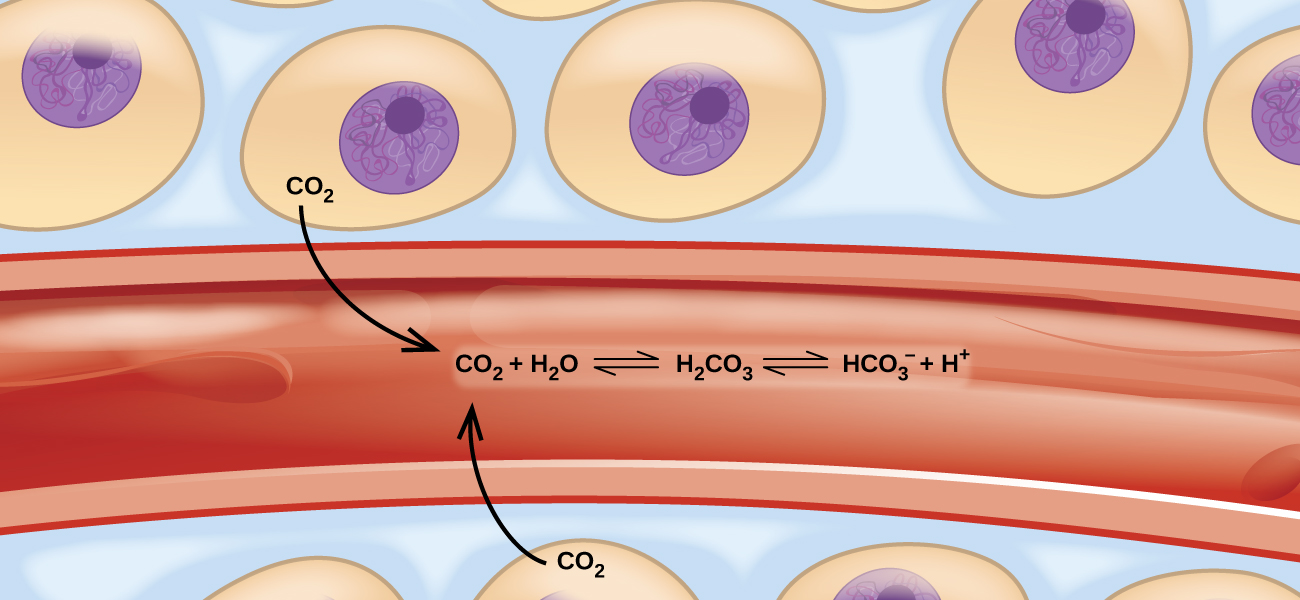
Estas reacciones bidireccionales balanceadas ocurren por todas partes e incluso en nuestros cuerpos. Por ejemplo, ocurren en nuestra sangre, donde la reacción entre el dióxido de carbono y el agua forma el ácido carbónico \(\ce{(HCO3-)}\) (Figura \(\PageIndex{1}\)). La fisiología humana se adapta a la cantidad de productos ionizados producidos por esta reacción (\(\ce{HCO3-}\) y H+). En este capítulo, aprenderá cómo predecir la posición del equilibrio y el rendimiento de un producto de una reacción en condiciones específicas, cómo cambiar las condiciones de una reacción para aumentar o reducir el rendimiento de un producto y cómo evaluar la reacción de un sistema de equilibrio con alteraciones.
Contribuyentes
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


