18.1: La periodicidad
- Page ID
- 1952
Habilidades para desarrollar
- Clasificar los elementos
- Hacer predicciones sobre las propiedades de periodicidad de los elementos representativos
Comenzamos esta sección por examinando el comportamiento de los metales representativos en relación con sus posiciones en la tabla periódica. El enfoque principal de esta sección será la aplicación de la periodicidad a los metales representativos.
Es posible dividir los elementos en grupos según sus configuraciones electrónicas. Los elementos representativos son los elementos donde se llenan los orbitales s y p. Los elementos de transición son elementos donde se llenan los orbitales d (grupos 3–11 en la tabla periódica), y los metales de transición internos son los elementos donde se llenan los orbitales f. Los orbitales d se llenan con los elementos del grupo 11; por lo tanto, los elementos del grupo 12 se califican como elementos representativos porque el último electrón entra en un orbital s. Los metales entre los elementos representativos son los metales representativos. El carácter metálico resulta de la capacidad de un elemento para perder sus electrones de valencia externos y da como resultado una alta conductividad térmica y eléctrica, entre otras propiedades físicas y químicas. Hay 20 metales representativos no radiactivos en los grupos 1, 2, 3, 12, 13, 14 y 15 de la tabla periódica (los elementos de color amarillo en la Figura \(\PageIndex{1}\)). Los elementos radiactivos copernicium, flerovium, polonio y livermorio también son metales, pero no los cubriremos en este capítulo.
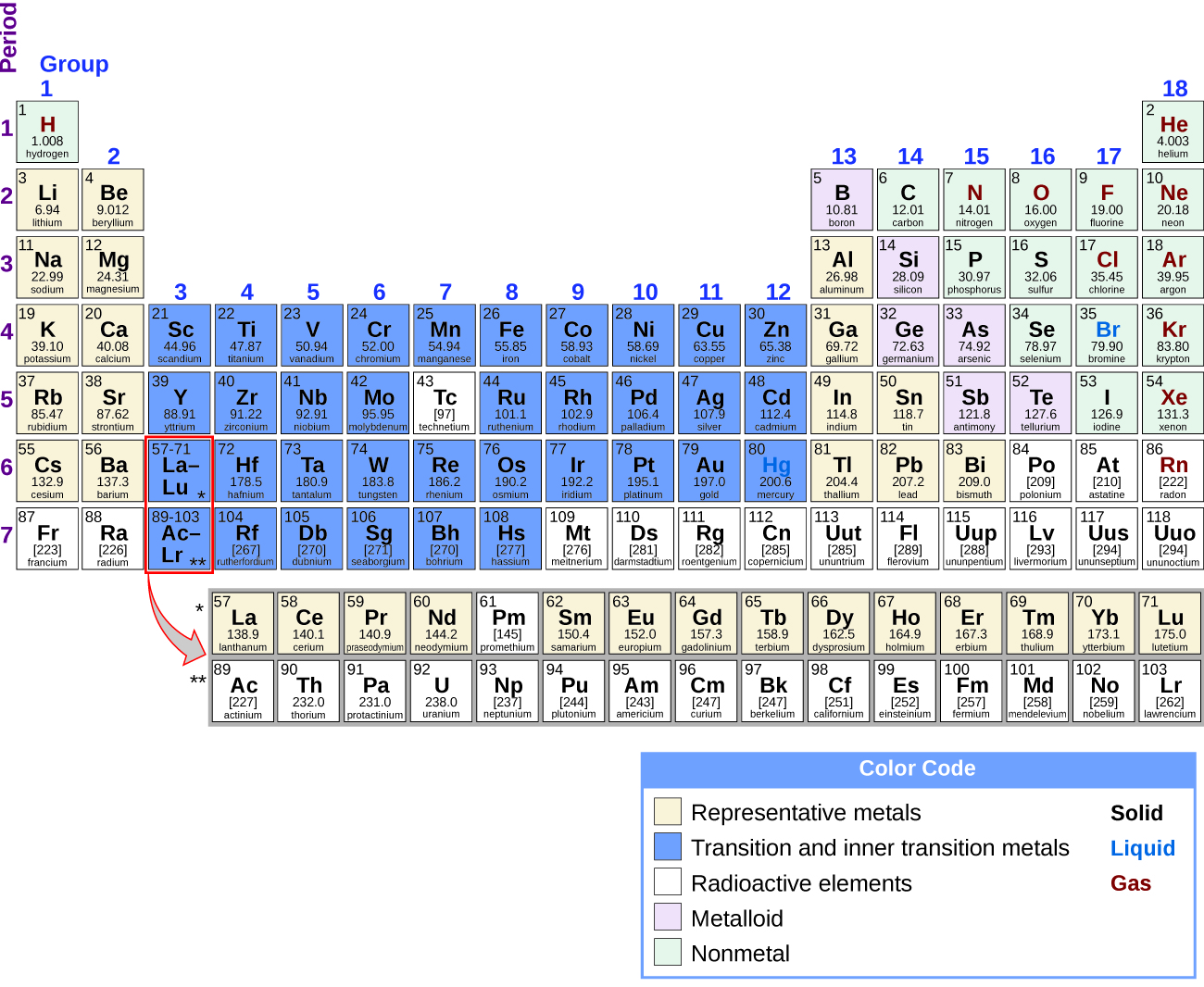
Figura \(\PageIndex{1}\): La ubicación de los metales representativos se muestra en la tabla periódica. Los no metales se muestran en verde, los metaloides en violeta y los metales de transición y los metales de transición internos en azul.
Además de los metales representativos, algunos de los elementos representativos son los metaloides. Un metaloide es un elemento que tiene propiedades que se encuentran entre las de los metales y los no metales; estos elementos son típicamente semiconductores. Los elementos representativos que sobran son no metales. Diferente a los metales, que normalmente forman cationes y compuestos iónicos (que contienen enlaces iónicos), los no metales tienden a formar aniones o compuestos moleculares. En general, la combinación de un metal y un no metal produce una sal. Una sal es un compuesto iónico que consiste en cationes y aniones.
Una sal es un compuesto iónico que consiste en cationes y aniones.
La mayoría de los metales representativos no se encuentran naturalmente en un estado no combinado porque reaccionan fácilmente con el agua y el oxígeno en el aire. Sin embargo, es posible aislar el berilio elemental, magnesio, zinc, cadmio, mercurio, aluminio, estaño y plomo de sus minerales naturales y usarlos porque reaccionan muy lentamente con el aire. Parte de la razón por la cual estos elementos reaccionan lentamente es que estos elementos reaccionan con el aire para formar una capa protectora. La formación de esta capa protectora se llama la pasivación. La capa protectora es una capa no reactiva de óxido o algún otro compuesto. El magnesio, el aluminio, el zinc y el estaño elementales son importantes en la fabricación de muchos artículos familiares, como los alambres, utensilios de cocina, papel de aluminio y muchos objetos domésticos y personales. Aunque el berilio, el cadmio, el mercurio y el plomo están disponibles fácilmente, existen limitaciones en su uso debido a su toxicidad.
Grupo 1: Los metales alcalinos
Los metales alcalinos como el litio, sodio, potasio, rubidio, cesio y francio constituyen el grupo 1 de la tabla periódica. Aunque el hidrógeno está en el grupo 1 (y también en el grupo 17), es un no metal y merece una consideración separada más adelante en este capítulo. El nombre “metal alcalino” se refiere al hecho de que estos metales y sus óxidos reaccionan con el agua para formar soluciones muy básicas (alcalinas).
Las propiedades de los metales alcalinos son similares entre sí como se esperaba para los elementos de la misma familia. Los metales alcalinos tienen los radios atómicos más grandes y la primera energía de ionización más baja en sus períodos. Esta combinación hace que sea muy fácil eliminar el único electrón en la capa más externa (valencia) de cada uno. La pérdida fácil de este electrón de valencia significa que estos metales fácilmente forman cationes estables con una carga de 1+. Su reactividad aumenta con el aumento del número atómico debido a la facilidad de perder el único electrón de valencia (disminución de la energía de ionización). Dado que la oxidación es tan fácil, la reducción inversa es difícil, lo que explica por qué es difícil aislar los elementos. Los metales alcalinos sólidos son muy blandos; el litio, que se muestra en la Figura \(\PageIndex{2}\), tiene la densidad más baja de cualquier metal (0.5 g / cm3).

Figura \(\PageIndex{2}\): El litio flota en el aceite de parafina porque su densidad es menor que la densidad del aceite de parafina.
Todos los metales alcalinos reaccionan vigorosamente con el agua para formar el gas hidrógeno y una solución básica del hidróxido metálico. Esto significa que son más fáciles de oxidar que el hidrógeno. Como ejemplo, la reacción del litio con el agua es:
Los metales alcalinos reaccionan directamente con todos los no metales (excepto los gases nobles) para producir los compuestos iónicos binarios que contienen los iones metálicos 1+. Estos metales son tan reactivos que es necesario evitar el contacto tanto con la humedad como con el oxígeno del aire. Por lo tanto, se almacenan en recipientes sellados bajo aceite mineral, como se muestra en la Figura \(\PageIndex{3}\), para evitar el contacto con el aire y la humedad. Los metales puros nunca existen libres (no combinados) en la naturaleza debido a su alta reactividad. Además, esta alta reactividad hace necesario preparar los metales por la electrólisis de compuestos de metales alcalinos.

Figura\(\PageIndex{3}\): Para evitar el contacto con el aire y el agua, el potasio para uso en el laboratorio viene en forma de barras o perlas almacenadas en la queroseno o el aceite mineral, o en recipientes sellados. (crédito: http://images-of-elements.com/potassium.php)
Diferente a muchos otros metales, la reactividad y la blandura de los metales alcalinos hacen que estos metales no sean adecuados para las aplicaciones estructurales. Sin embargo, existen aplicaciones en las que la reactividad de los metales alcalinos es una ventaja. Por ejemplo, la producción de los metales como el titanio y el circonio depende, en parte, de la capacidad del sodio para reducir los compuestos de estos metales. La fabricación de muchos compuestos orgánicos, como ciertos tintes, medicamentos y perfumes, usa la reducción del litio o el sodio.
Figura\(\PageIndex{4}\): Las llamas de color de estroncio, cesio, sodio y litio (de izquierda a derecha). Imagen cortesía de Claire Murray y Annabelle Baker de Diamond Light Source.
El sodio y sus compuestos causan que la llama sea un color fuerte amarillo como se ve en la Figura \(\PageIndex{4}\). Pasando una descarga eléctrica a través del vapor de sodio también produce este color. En ambos casos, este es un ejemplo de un espectro de emisión como se discutió en el capítulo sobre la estructura electrónica. A veces, las luces de calle usan luces de vapor de sodio porque el vapor de sodio penetra la niebla mejor que la mayoría de otras luces. Esto se debe a que la niebla no dispersat la luz amarilla tanto como la blanca. Los otros metales alcalinos y sus sales también toman parte en el color de la llama. El litio causa un color carmesí brillante, mientras que los otros causan un color violeta pálido.
Video \(\PageIndex{1}\): Este vídeo demuestra las reacciones de los metales alcalinos con el agua.
Grupo 2: Los metales alcalinotérreos
Los metales alcalinotérreos (el berilio, magnesio, calcio, estroncio, bario y radio) constituyen el grupo 2 de la tabla periódica. El nombre “metal alcalino” proviene del hecho de que los óxidos de los miembros más pesados del grupo reaccionan con el agua para formar las soluciones alcalinas. La carga nuclear aumenta al pasar del grupo 1 al grupo 2. Debido a este aumento de carga, los átomos de los metales alcalinotérreos son más pequeños y tienen energías de primera ionización más altas que los metales alcalinos en el mismo período. La mayor energía de ionización hace que los metales alcalinotérreos sean menos reactivos que los metales alcalinos; sin embargo, siguen siendo elementos muy reactivos. Su reactividad aumenta, como se esperaba, al aumentar el tamaño y disminuir la energía de ionización. En las reacciones químicas, estos metales fácilmente pierden ambos electrones de valencia para formar compuestos en los que exhiben un estado de oxidación de 2+. Debido a su alta reactividad, es común producir los metales alcalinotérreos, como los metales alcalinos, por la electrólisis. Aunque las energías de ionización son bajas, los dos metales con las energías de ionización más altas (el berilio y el magnesio) forman compuestos que exhiben algunos caracteres covalentes. Como los metales alcalinos, los metales alcalinotérreos más pesados imparten color a la llama. Como en el caso de los metales alcalinos, éste forma parte del espectro de emisión de estos elementos. El calcio y el estroncio producen tonos de rojo, mientras que el bario produce un color verde.
El magnesio es un metal de color blanco plateado que es maleable y dúctil a altas temperaturas. La pasivación disminuye la reactividad del magnesio metálico. Tras la exposición al aire, se forma una capa fuertemente adherida de oxicarbonato de magnesio en la superficie del metal e inhibe que la reacción siga. (El carbonato proviene de la reacción del dióxido de carbono en la atmósfera). El magnesio es el más liviano de los metales estructurales más usados, por eso la mayor parte de la producción de magnesio es para aleaciones livianas.
El magnesio (Figura \(\PageIndex{5}\)), el calcio, el estroncio y el bario reaccionan con el agua y el aire. A temperatura ambiente, el bario demuestra la reacción más vigorosa. Los productos de la reacción con el agua son el hidrógeno y el hidróxido metálico. La formación de gas hidrógeno indica que los metales alcalinotérreos más pesados son mejores agentes reductores (se oxidan más fácilmente) que el hidrógeno. Como se esperaba, estos metales reaccionan tanto con los ácidos como con los no metales para formar los compuestos iónicos. Diferente a la mayoría de las sales de los metales alcalinos, muchas de las sales comunes de los metales alcalinotérreos son insolubles en el agua debido a las altas energías reticulares de estos compuestos, que contienen un ión metálico divalente.

Figura \(\PageIndex{5}\): De izquierda a derecha: Mg(s), el agua tibia a pH 7 y la solución resultante con un pH superior a 7, como lo indica el color rosa del indicador de fenolftaleína. (crédito: modificación del trabajo de Sahar Atwa)
El potente poder reductor del magnesio caliente es útil para preparar algunos metales a partir de sus óxidos. De hecho, la afinidad del magnesio por el oxígeno es tan grande que, al quemar el magnesio, reacciona con el dióxido de carbono, produciendo el carbono elemental:
\[\ce{2Mg}(s)+\ce{CO2}(g)⟶\ce{2MgO}(s)+\ce{C}(s)\]
Por esta razón, un extintor de CO2 no extinguirá un incendio de magnesio. Además, la luz blanca brillante emitida por la quema del magnesio lo hace útil en los cohetes de señales y los fuegos artificiales.
Grupo 12: Metales
Los elementos del grupo 12 son elementos de transición; sin embargo, el último electrón agregado no es un electrón d, sino un electrón s. Dado que el último electrón agregado es un electrón s, estos elementos califican como metales representativos o metales postransición. Los elementos del grupo 12 se comportan más como los metales alcalinotérreos que como los metales de transición. El grupo 12 contiene los cuatro elementos zinc, cadmio, mercurio y copernicio. Cada uno de estos elementos tiene dos electrones en su capa de valencia (ns2). Cuando los átomos de estos metales forman cationes con una carga de 2+, donde se pierden los dos electrones externos, tienen configuraciones de electrones de gas pseudo-noble. El mercurio es a veces una excepción porque también exhibe un estado de oxidación de 1+ en compuestos que contienen un ion diatómico \(\ce{Hg2^2+}\). En sus formas elementales y en compuestos, el cadmio y el mercurio son tóxicos.
El zinc es el más reactivo del grupo 12 y el mercurio es el menos reactivo. (Esto es lo contrario de la tendencia de reactividad de los metales de los grupos 1 y 2, en la que la reactividad aumenta hacia abajo de un grupo. El aumento de la reactividad con el número atómico más grande solo ocurre para los metales de los grupos 1 y 2.) La reactividad decreciente es debido a la formación de iones con una configuración de gas pseudo-noble y a otros factores que no discutiremos en esta sección. Los comportamientos químicos del zinc y el cadmio son bastante similares entre sí, pero difieren de los del mercurio.
El zinc y el cadmio tienen potenciales de reducción más bajos que el hidrógeno y, al igual que los metales alcalinos y los metales alcalinotérreos, producirán gas hidrógeno cuando reaccionen con los ácidos. La reacción del zinc con el ácido clorhídrico, que se muestra en la Figura \(\PageIndex{6}\), es:

Figura \(\PageIndex{6}\): El zinc es un metal activo. Se disuelve en el clorhídrico y forma una solución de iones Zn2+ incoloros, iones Cl– e hidrógeno gaseoso.
El zinc es un metal plateado que rápidamente se deslustra a una apariencia gris azulada. Este cambio de color se debe a un recubrimiento adherente de un carbonato básico, Zn2(OH)2CO3, que pasiva el metal para inhibir la corrosión adicional. Las pilas secas y alcalinas contienen un ánodo de zinc. El latón (Cu y Zn) y un poco de bronce (Cu, Sn y, a veces, Zn) son importantes aleaciones del zinc. Aproximadamente la mitad de la producción de zinc sirve para proteger el hierro y otros metales de la corrosión. Esta protección puede tomar la forma de un ánodo de sacrificio (también se llama un ánodo galvánico, que provee protección catódica para varios metales) o como una capa delgada sobre el metal protegido. El acero galvanizado es acero con una capa protectora de zinc.
Los ánodos de sacrificio
Un ánodo de sacrificio, o ánodo galvánico, es un modo de proveer protección catódica a varios metales. La protección catódica se refiere a la prevención de la corrosión mediante la conversión del metal corroído en un cátodo. Como cátodo, el metal resiste la corrosión, que es un proceso de oxidación. La corrosión ocurre en el ánodo de sacrificio en lugar de en el cátodo.
La construcción de dicho sistema comienza con la unión de un metal más activo (potencial de reducción más negativo) al metal que necesita protección. La fijación puede ser directa o por cable. Se necesita un puente salino para completar el circuito. Este puente salino suele ser agua de mar o agua subterránea. Ya que se complete el circuito, la oxidación (corrosión) ocurre en el ánodo en vez del cátodo.
Los ánodos de sacrificio comúnmente usados son el magnesio, aluminio y zinc. El magnesio tiene el potencial de reducción más negativo de los tres y sirve mejor cuando el puente salino es menos eficiente debido a una baja concentración de electrolitos, como en el agua dulce. El zinc y el aluminio funcionan mejor en el agua salada que el magnesio. El aluminio es más ligero que el zinc y tiene una mayor capacidad; sin embargo, un revestimiento de óxido puede pasivar el aluminio. En casos especiales, otros materiales son útiles. Por ejemplo, el hierro puede proteger al cobre.
El mercurio es muy diferente al zinc o el cadmio. El mercurio es el único metal que es un líquido a 25 °C. Muchos metales se disuelven en el mercurio y forman soluciones llamadas amalgamas (vea la característica sobre amalgamas), que son aleaciones de mercurio con uno o más metales. El mercurio, que se muestra en la Figura \(\PageIndex{7}\), es un elemento no reactivo que es más difícil de oxidar que el hidrógeno. En consecuencia, no desplaza el hidrógeno de los ácidos; sin embargo, reaccionará con los ácidos oxidantes fuertes, como el ácido nítrico:
\[\ce{Hg}(l)+\ce{HCl}(aq)⟶\textrm{no reaction}\]
\[\ce{3Hg}(l)+\ce{8HNO3}(aq)⟶\ce{3Hg(NO3)2}(aq)+\ce{4H2O}(l)+\ce{2NO}(g)\]
El NO que se formó inicialmente se oxida rápidamente y se vuelve color marrón rojizo NO2.

Figura \(\PageIndex{7}\): De izquierda a derecha: Hg(l), Hg + HCl concentrado, Hg + HNO3 concentrado. (crédito: Sahar Atwa)
La mayoría de los compuestos de mercurio se descomponen cuando se calientan. La mayoría de los compuestos de mercurio contienen mercurio con un estado de oxidación 2+. Cuando hay un gran exceso de mercurio, es posible formar compuestos que contiene el ión \(\ce{Hg2^2+}\). Todos los compuestos de mercurio son tóxicos y es necesario tener mucho cuidado en su síntesis.
Amalgamas
Una amalgama es una aleación de mercurio con uno o más metales. Esto es similar a considerar que el acero es una aleación de hierro con otros metales. La mayoría de los metales formarán una amalgama con el mercurio y las principales excepciones son el hierro, el platino, el tungsteno y el tantalio. Debido que el mercurio es toxico, ha habido una disminución significativa en el uso de las amalgamas. Históricamente, las amalgamas fueron importantes en las celdas electrolíticas y en la extracción del oro. Las amalgamas de metales alcalinos todavía se usan porque son agentes reductores fuertes y más fáciles de manipular que los metales alcalinos puros. Los prospectores tuvieron un problema cuando encontraron oro finamente dividido. Aprendieron que, al agregar mercurio a sus sartenes, el oro se acumulaba en el mercurio para formar una amalgama y facilitar la recolección. Desafortunadamente, las pérdidas de pequeñas cantidades de mercurio a lo largo de los años dejaron muchos arroyos en California contaminados con el mercurio. Los dentistas usan amalgamas que contienen plata y otros metales para rellenar las caries. Hay varias razones para usar una amalgama, son baratas y la fáciles de manipular y tienen más longevidad en comparación con materiales alternativos. Las amalgamas dentales contienen aproximadamente un 50% de mercurio en peso, lo que, en los últimos años, se ha convertido en una preocupación debido a la toxicidad del mercurio.
Después de revisar los mejores datos disponibles, la Administración de Alimentos y Medicamentos (FDA) considera que los empastes de amalgama son seguros para adultos y niños mayores de seis años. Incluso con múltiples empastes, los niveles de mercurio en los pacientes permanecen muy por debajo de los niveles más bajos asociados con el daño. Los estudios clínicos no han encontrado ninguna correlación entre las amalgamas dentales y los problemas de la salud. Los problemas de la salud pueden diferentes entre los casos de niños menores de seis años o mujeres embarazadas. Las conclusiones de la FDA están en línea con las opiniones de la Agencia de Protección Ambiental (EPA) y los Centros para el Control de Enfermedades (CDC). La única consideración de salud observada es que algunas personas son alérgicas a la amalgama o uno de sus componentes.
Grupo 13
El grupo 13 contiene el metaloide boro y los metales aluminio, galio, indio y talio. El elemento más ligero, el boro, es un semiconductor y sus compuestos binarios tienden a ser covalentes y no iónicos. Los elementos que sobran del grupo son metales, pero sus óxidos e hidróxidos cambian de carácter. Los óxidos e hidróxidos de aluminio y galio exhiben comportamientos tanto ácidos como básicos. Una sustancia, como estas dos, que reaccionará tanto con ácidos como con bases es anfótera. Esta característica ilustra la combinación de comportamientos metálicos y no metálicos de estos dos elementos. Los óxidos e hidróxidos de indio y talio presentan únicamente un comportamiento básico, de acuerdo con el carácter claramente metálico de estos dos elementos. El punto de fusión del galio es inusualmente bajo (alrededor de 30 ° C) y se puede derretir en su mano.
El aluminio es anfótero porque reacciona tanto con los ácidos como con los bases. Una reacción típica con un ácido es:
\[\ce{2Al}(s)+\ce{6HCl}(aq)⟶\ce{2AlCl3}(aq)+\ce{3H2}(g)\]
Los productos de la reacción del aluminio con una base dependen de las condiciones de la reacción, con la siguiente siendo una posibilidad:
\[\ce{2Al}(s)+\ce{2NaOH}(aq)+\ce{6H2O}(l)⟶\ce{2Na[Al(OH)4]}(aq)+\ce{3H2}(g)\]
Las reacciones entre ambos ácidos y bases generan el gas hidrógeno.
Los elementos del grupo 13 tienen una configuración electrónica de valencia de ns2np1. El aluminio normalmente usa todos sus electrones de valencia cuando reacciona, causando que tenga un estado de oxidación de 3+ en los compuestos. Aunque muchos de estos compuestos son covalentes, otros, como AlF3 y Al2(SO4)3, son iónicos. Las soluciones acuosas de sales de aluminio contienen el catión \(\ce{[Al(H2O)6]^3+}\), abreviado como Al3+(aq). El galio, el indio y el talio también forman compuestos iónicos que contienen los iones M3+. Estos tres elementos exhiben no solo el estado de oxidación esperado de 3+ de los tres electrones de valencia, sino también un estado de oxidación (en este caso, 1+) que es dos por debajo del valor esperado. Este fenómeno, el efecto de par inerte, se refiere a la formación de un ion estable con un estado de oxidación dos veces menor al esperado para el grupo. El par de electrones es el orbital de valencia de esos elementos. En general, el efecto de par inerte es importante para los elementos del bloque p más bajos. En una solución acuosa, el ion Tl+ (aq) es más estable que el Tl3+ (aq). En general, estos metales reaccionarán con el aire y el agua para formar 3+ iones; sin embargo, el talio reacciona para dar derivados de talio (I). Todos los metales del grupo 13 reaccionan directamente con no metales como el azufre, el fósforo y los halógenos, formando compuestos binarios.The metals of group 13 (Al, Ga, In, and Tl) are all reactive. However, passivation occurs as a tough, hard, thin film of the metal oxide forms upon exposure to air. Disruption of this film may counter the passivation, allowing the metal to react. One way to disrupt the film is to expose the passivated metal to mercury. Some of the metal dissolves in the mercury to form an amalgam, which sheds the protective oxide layer to expose the metal to further reaction. The formation of an amalgam allows the metal to react with air and water.
Vídeo \(\PageIndex{2}\): Aunque se oxida fácilmente, la pasivación del aluminio lo hace muy útil como un material de construcción porque es ligero y resistente. Debido a la formación de una amalgama, el mercurio es corrosivo para los materiales estructurales hechos de aluminio. Este vídeo demuestra cómo se puede destruir la integridad de una viga de aluminio mediante la adición de una pequeña cantidad de mercurio elemental.
Los usos más importantes del aluminio se encuentran en las industrias de la construcción y el transporte, y en la fabricación de latas de aluminio y papel de aluminio. Estos usos dependen de la ligereza, tenacidad y resistencia del metal, y también su resistencia a la corrosión. Debido a que el aluminio es un excelente conductor de calor y resiste a la corrosión, es útil en la fabricación de los utensilios de la cocina.
El aluminio es un muy buen agente reductor y puede reemplazar a otros agentes reductores en el aislamiento de ciertos metales de sus óxidos. Aunque es más caro que la reducción por el carbono, el aluminio es importante para el aislamiento de Mo, W y Cr de sus óxidos.
Grupo 14
Los miembros metálicos del grupo 14 son el estaño, plomo y flerovium. El carbono es un no metal típico. Los elementos que faltan son el silicio y el germanio y son ejemplos de semimetales o metaloides. El estaño y el plomo forman los cationes divalentes estables, Sn2+ y Pb2+, con estados de oxidación dos por debajo del estado de oxidación del grupo 4+. La estabilidad de este estado de oxidación esta causado por el efecto de par inerte. El estaño y el plomo también forman compuestos covalentes con un estado de oxidación 4+ formal. Por ejemplo, SnCl4 y PbCl4 son líquidos covalentes de bajo punto de ebullición.

Figura \(\PageIndex{8}\): (a) El cloruro de estaño (II) es un sólido iónico; (b) el cloruro de estaño (IV) es un líquido covalente.
El estaño reacciona fácilmente con los no metales y los ácidos para formar los compuestos de estaño (II) (lo que indica que se oxida más fácilmente que el hidrógeno) y con los no metales para formar los compuestos de estaño (II) o de estaño (IV) (Figura \(\PageIndex{8}\)), dependiendo de la estequiometría y las condiciones de la reacción. El plomo es menos reactivo. Es solo un poco más fácil de oxidar que el hidrógeno, y la oxidación normalmente requiere un ácido muy concentrado que esta caliente.
Muchos de estos elementos existen como alótropos. Los alótropos son dos o más formas del mismo elemento en el mismo estado físico con diferentes propiedades químicas y físicas. Hay dos alótropos comunes de estaño. Estos alótropos son el estaño gris (quebradizo) y el estaño blanco. Similarmente a otros alótropos, la diferencia entre estas formas de estaño es la disposición de los átomos. El estaño blanco es estable a temperaturas más altas que 13.2 °C y es maleable como otros metales. A bajas temperaturas, el estaño gris es la forma más estable. El estaño gris es frágil y se tiende a descomponer en polvo. En consecuencia, los artículos hechos de estaño se desintegrarán en climas fríos, especialmente si la ola de frío es prolongada. El cambio progresa lentamente desde el lugar de origen, y el estaño gris que se forma primero cataliza cambios adicionales. En cierto modo, este efecto es similar a la propagación de una infección en el cuerpo de una planta o animal, causando que las personas llaman este proceso la enfermedad del estaño o la plaga del estaño.
El uso principal del estaño es en el revestimiento del acero para formar las planchas de estaño, que constituyen el estaño en las latas. Las aleaciones de estaño importantes son el bronce (Cu y Sn) y el solder (Sn y Pb). El plomo es importante en las baterías de almacenamiento de plomo de los automóviles.
Grupo 15
El bismuto, es el elemento más pesado del grupo 15 y es un metal menos reactivo que los otros metales representativos. Puede fácilmente ceder tres de sus cinco electrones de valencia a no metales activos para formar el ion tri-positivo, Bi3+. Forma compuestos con el estado de oxidación de grupo de 5+ solo cuando se trata con agentes oxidantes fuertes. La estabilidad del estado de oxidación 3+ es otro ejemplo del efecto de par inerte.
Resumen
Esta sección se enfoca en la periodicidad de los elementos representativos. Estos son los elementos que tienen electrones que entran en los orbitales s y p. Los elementos representativos se encuentran en los grupos 1, 2 y 12-18. Estos elementos son metales, metaloides y no metales representativos. Los metales alcalinos (grupo 1) son muy reactivos y fácilmente forman iones con una carga de 1+ para formar compuestos iónicos que normalmente son solubles en el agua y reaccionan vigorosamente con el agua para formar el gas hidrógeno y una solución básica del hidróxido metálico. Los electrones más externos de los metales alcalinotérreos (grupo 2) son más difíciles de ceder que los electrones externos de los metales alcalinos, lo que hace que los metales del grupo 2 sean menos reactivos que los del grupo 1. Estos elementos fácilmente forman compuestos en los que los metales exhiben un estado de oxidación de 2+. El zinc, el cadmio y el mercurio (grupo 12) normalmente exhiben el estado de oxidación de grupo de 2+ (aunque el mercurio también exhibe un estado de oxidación de 1+ en compuestos que contienen \(\ce{Hg2^2+}\)). El aluminio, el galio, el indio y el talio (grupo 13) son más fáciles de oxidar que el hidrógeno. El aluminio, el galio y el indio se presentan con un estado de oxidación 3+ (sin embargo, el talio también se presenta comúnmente como el ion Tl+). El estaño y el plomo forman cationes divalentes estables y compuestos covalentes en los que los metales exhiben el estado de oxidación 4+.
Glosario
- metal alcalinotérreo
- cualquiera de los metales (berilio, magnesio, calcio, estroncio, bario y radio) que están en el grupo 2 de la tabla periódica; son metales reactivos, divalentes que forman óxidos básicos
- alótropos
- dos o más formas del mismo elemento, en el mismo estado físico, con diferentes estructuras químicas
- bismuto
- el elemento más pesado del grupo 15; un metal menos reactivo que otros metales representativos
- metal (representativo)
- átomos de los elementos metálicos de los grupos 1, 2, 12, 13, 14, 15 y 16, que forman compuestos iónicos al perder electrones de sus orbitales externos s o p
- metaloide
- elemento que tiene propiedades que se encuentran entre las de los metales y los no metales; estos elementos normalmente son semiconductores
- pasivación
- metales con una capa protectora no reactiva de óxido u otro compuesto que inhibe las reacciones químicas; la eliminación física o química de la capa pasiva permite que los metales demuestren su reactividad química esperada.
- elemento representativo
- elemento donde se llenan los orbitales s y p
- metal representativo
- el metal entre los elementos representativos
Contribuyentes y atribuciones
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


