18.5: La ocurrencia, preparación y los compuestos de hidrógeno
- Page ID
- 1956
Habilidades para desarrollar
- Describir las propiedades, la preparación y los compuestos del hidrógeno.
El hidrógeno es el elemento más abundante del universo. El sol y otras estrellas están hechas principalmente del hidrógeno. Los astrónomos estiman que el 90% de los átomos del universo son átomos de hidrógeno. El hidrógeno es un componente de más compuestos que cualquier otro elemento. El agua es el compuesto de hidrógeno más abundante que se encuentra en la tierra. El hidrógeno es una parte importante del petróleo, muchos minerales, celulosa y almidón, azúcar, grasas, aceites, alcoholes, ácidos y miles de otras sustancias.
A temperaturas ordinarias, el hidrógeno es un gas incoloro, inodoro, insípido y no venenoso que consiste en la molécula diatómica de H2. El hidrógeno está hecho de tres isótopos y diferentemente a otros elementos, estos isótopos tienen diferentes nombres y símbolos químicos: protio, 1H, deuterio, 2H (o "D") y tritio 3H (o "T"). En una muestra natural de hidrógeno, hay un átomo de deuterio por cada 7000 átomos de H y un átomo de tritio radiactivo por cada 1018 átomos de H. Las propiedades químicas de los diferentes isótopos son muy similares porque tienen estructuras electrónicas idénticas, pero difieren en algunas propiedades físicas debido a sus diferentes masas atómicas. El deuterio y el tritio elementales tienen una presión de vapor más baja que el hidrógeno ordinario. En consecuencia, cuando el hidrógeno líquido se evapora, los isótopos más pesados se concentran en las últimas porciones para evaporarse. La electrólisis del agua pesada, D2O, produce el deuterio. La mayor parte del tritio esta hecho por reacciones nucleares.
La preparación del hidrógeno
El hidrógeno elemental se debe preparar a partir de compuestos rompiendo los enlaces químicos. Después se describirán los métodos más comunes para la preparación del hidrógeno.
De vapor y carbono o hidrocarburos
El agua es la fuente de hidrógeno más barata y abundante. Pasando el vapor sobre el coque (una forma impura del carbono elemental) a 1000 °C produce una mezcla de monóxido de carbono e hidrógeno conocida como el gas de agua:
\[\ce{C}(s)+\ce{H2O}(g)\:\mathrm{\xrightarrow{1000\:°C}}\:\underset{\Large\mathrm{water\: gas}}{\ce{CO}(g)+\ce{H2}(g)}\]
El gas de agua es un combustible industrial. Es posible producir hidrógeno adicional mediante la mezcla del gas de agua con el vapor en presencia de un catalizador para convertir el CO en CO2. Esta reacción es la reacción de desplazamiento de agua-gas.
También es posible preparar una mezcla de hidrógeno y monóxido de carbono pasando los hidrocarburos de gas natural o petróleo y vapor sobre un catalizador con una base níquel. El propano es un ejemplo de un hidrocarbonado reactivo:
La electrólisis
El hidrógeno se forma cuando la electricidad de la corriente continua pasa a través del agua (electrólisis) que contiene un electrólito como el H2SO4 (Figura (\PageIndex{1}\)) Se forman burbujas de hidrógeno en el cátodo y el oxígeno se forma en el ánodo. La reacción neta es:
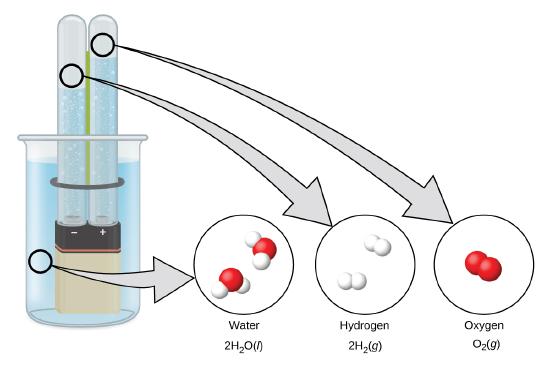
Figura\(\PageIndex{1}\): La electrólisis del agua produce el hidrógeno y el oxígeno. Debido a que hay dos veces más átomos de hidrógeno que átomos de oxígeno y ambos elementos son diatómicos, hay dos veces el volumen de hidrógeno producido en el cátodo que el oxígeno producido en el ánodo.
La reacción de los metales con los ácidos
Este es el método de laboratorio más conveniente para producir el hidrógeno. Los metales con potenciales de reducción más bajos reducen el ion hidrógeno en ácidos diluidos para producir el gas hidrógeno y las sales metálicas. Por ejemplo, como se muestra en la Figura \(\PageIndex{2}\), el hierro en ácido clorhídrico diluido produce el gas hidrógeno y el cloruro de hierro (II):
\[\ce{Fe}(s)+\ce{2H3O+}(aq)+\ce{2Cl-}(aq)⟶\ce{Fe^2+}(aq)+\ce{2Cl-}(aq)+\ce{H2}(g)+\ce{2H2O}(l)\]

Figura\(\PageIndex{2}\): La reacción del hierro con un ácido produce el hidrógeno. Aquí, el hierro reacciona con el ácido clorhídrico (crédito: Mark Ott).
La reacción de los hidruros metálicos iónicos con el agua
Es posible producir hidrógeno a partir de la reacción de hidruros de los metales activos, que contienen el muy basico anión H−, con el agua:
\[\ce{CaH2}(s)+\ce{2H2O}(l)⟶\ce{Ca^2+}(aq)+\ce{2OH-}(aq)+\ce{2H2}(g)\]
Los hidruros metálicos son fuentes de hidrógeno caras pero convenientes, especialmente donde el espacio y el peso son factores importantes. Son importantes en el inflado de chalecos salvavidas, balsas salvavidas y globos militares.
Las reacciones
En condiciones normales, el hidrógeno es relativamente inactivo químicamente, pero cuando se calienta, toma parte en muchas reacciones químicas.
Dos tercios de la producción mundial del hidrógeno se dedica a la fabricación del amoniaco, que es un fertilizante y se usa en la fabricación del ácido nítrico. También, grandes cantidades de hidrógeno son importantes en el proceso de la hidrogenación, que se analiza en el capítulo sobre la química orgánica.
Es posible usar el hidrógeno como un combustible no contaminante. La reacción del hidrógeno con el oxígeno es una reacción muy exotérmica, liberando 286 kJ de energía por mol de agua formado. El hidrógeno se quema sin explotar en condiciones controladas. El soplete de oxígeno-hidrógeno puede alcanzar temperaturas de hasta 2800 °C debido al alto calor de combustión del hidrógeno. La llama caliente de este soplete es útil para cortar láminas gruesas de muchos metales. El hidrógeno líquido también es un combustible importante para los cohetes (Figura \(\PageIndex{3}\)).
<
Figura \(\PageIndex{3}\): Antes del retiro de la flota en 2011, se utilizaba el hidrógeno líquido y el oxígeno líquido en los tres motores principales de un transbordador espacial. Dos compartimentos en el gran tanque contenían estos líquidos hasta que se lanzó el transbordador espacial. (crédito: “reynermedia”/Flickr)
Un átomo de hidrógeno no combinado consiste en un núcleo y un electrón de valencia en el orbital 1s. La capa de valencia n = 1 puede tener dos electrones al tiempo y el hidrógeno puede legítimamente ocupar dos ubicaciones en la tabla periódica. Es posible considerar al hidrógeno como un elemento del grupo 1 porque el hidrógeno puede perder un electrón para formar el catión, H+. También es posible considerar que el hidrógeno es un elemento del grupo 17 porque solo necesita un electrón para llenar su orbital de valencia para formar un ion hidruro, H-, o puede compartir un electrón para formar un solo enlace covalente. En realidad, el hidrógeno es un elemento único que casi merece su propia ubicación en la tabla periódica.
Reacciones con elementos
Cuando se calienta, el hidrógeno reacciona con los metales del grupo 1 y con Ca, Sr y Ba (los metales más activos del grupo 2). Los compuestos formados son los hidruros iónicos cristalinos que contienen el anión hidruro, H-, un agente reductor fuerte y una base fuerte, que reacciona vigorosamente con el agua y otros ácidos para formar el gas hidrógeno.
Las reacciones del hidrógeno con los no metales generalmente producen compuestos de hidrógeno ácido con hidrógeno en el estado de oxidación 1+. Las reacciones llegan a ser más exotérmicas y vigorosas cuando aumenta la electronegatividad del no metal. El hidrógeno reacciona con el nitrógeno y el azufre solo cuando se calienta, pero reacciona explosivamente con el flúor (formando HF) y, en algunas condiciones, con el cloro (formando HCl). Una mezcla de hidrógeno y oxígeno explota si se enciende. Debido a la naturaleza explosiva de la reacción, es necesario tener cuidado al manipular el hidrógeno (o cualquier otro gas combustible) para evitar la formación de una mezcla explosiva en un espacio confinado. Aunque la mayoría de los hidruros de los no metales son ácidos, el amoníaco y la fosfina (PH3) son ácidos muy, muy débiles y generalmente funcionan como bases. Hay un resumen de estas reacciones del hidrógeno con los elementos en la Tabla \(\PageIndex{1}\).
| Ecuación General | Comentarios |
|---|---|
| \(\ce{MH\: or\: MH2⟶MOH\: or\: M(OH)2 + H2}\) | los hidruros iónicos del grupo 1 y Ca, Sr y Ba |
| \(\ce{H2 + C⟶ (no\: reaction)}\) | |
| \(\ce{3H2 + N2 ⟶ 2NH3}\) | requiere alta presión y temperatura; bajo rendimiento |
| \(\ce{2H2 + O2 ⟶ 2H2O}\) | exotérmico y potencialmente explosivo |
| Exotérmico y potencialmente explosivo | requiere calentamiento; bajo rendimiento |
| \(\ce{H2 + X2 ⟶ 2HX}\) | X = F, Cl, Br, y I; explosivo con F2; bajo rendimiento con I2 |
Las reacciones con los compuestos
El hidrógeno reduce los óxidos calentados de muchos metales, con la formación del metal y el vapor del agua. Por ejemplo, pasando el hidrógeno sobre el CuO calentado forma el cobre y el agua. El hidrógeno también puede reducir los iones metálicos en algunos óxidos metálicos a estados de oxidación más bajos:
Los compuestos de hidrógeno
Aparte de los gases nobles, cada uno de los no metales forma compuestos con el hidrógeno. Para la simplificación aquí discutiremos solo algunos compuestos de hidrógeno de los no metales.
Compuestos de hidrógeno y nitrógeno
El amoníaco, NH3, se forma naturalmente cuando cualquier material orgánico que contiene nitrógeno se descompone en ausencia del aire. La preparación del amoníaco en el laboratorio es mediante la reacción de una sal de amonio con una base fuerte como el hidróxido de sodio. La reacción ácido-base con el ion de amonio que es un ácido débil produce el amoníaco, como se muestra en la Figura \(\PageIndex{4}\). El amoníaco también se forma cuando los nitruros iónicos reaccionan con el agua. El ion nitruro es una base mucho más fuerte que el ion hidróxido:
\[\ce{Mg3N2}(s)+\ce{6H2O}(l)⟶\ce{3Mg(OH)2}(s)+\ce{2NH3}(g)\]
La producción comercial del amoníaco ocurre mediante la combinación directa de los elementos del proceso Haber:
\[\ce{N2}(g)+\ce{3H2}(g)\xrightleftharpoons{\ce{catalyst}}\ce{2NH3}(g) \hspace{20px} ΔH°=\mathrm{−92\: kJ}\]
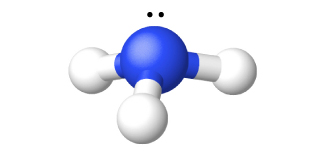
Figura \(\PageIndex{4}\): La estructura del amoníaco se muestra con un átomo de nitrógeno central y tres átomos de hidrógeno.
El amoníaco es un gas incoloro con un olor fuerte y penetrante. Las sales aromáticas usan este olor fuerte. El amoníaco gaseoso se licua fácilmente para producir un líquido incoloro que hierve a -33 °C. Debido al enlace de hidrógeno intermolecular, la entalpía de vaporización del amoníaco líquido es mayor que la de cualquier otro líquido excepto el agua, por esta razón el amoníaco es útil como un refrigerante. El amoníaco es bastante soluble en agua (658 L en STP se disuelven en 1 L H2O).
Las propiedades químicas del amoniaco son las siguientes:
- El amoníaco puede tener un comportamiento acídico, aunque es un ácido mucho más débil que el agua. Como otros ácidos, el amoniaco reacciona con los metales, pero es tan débil que altas temperaturas son necesarias. Se forma el hidrógeno y (dependiendo de la estequiometría) amidas (sales de \(\ce{NH2-}\)), imidas (sales de NH2-) o nitruros (sales de N3-).
- El átomo de nitrógeno en el amoníaco tiene el estado de oxidación más bajo posible (3−) y por eso no es susceptible a la reducción. Sin embargo, se puede oxidar. El amoníaco explota en el aire, produciendo el NO y el agua. El amoníaco caliente y el ion amonio son agentes reductores activos. De particular interés son las oxidaciones del ion amonio por el ion nitrito, \(\ce{NO2-}\), para producir el nitrógeno puro por ion nitrato para producir el óxido nitroso, N2O.
- Hay varios compuestos que podemos considerar derivados del amoníaco mediante el reemplazo de uno o más átomos de hidrógeno por otro átomo o grupo de átomos. Las derivaciones inorgánicas incluyen la cloramina, NH2Cl y la hidracina, N2H4:
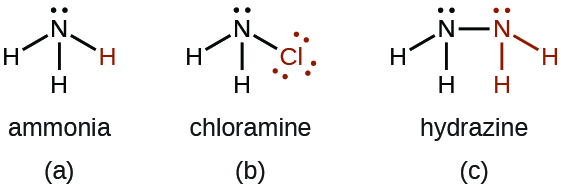
La cloramina, NH2Cl, resulta de la reacción del hipoclorito de sodio, NaOCl, con el amoniaco en una solución básica. En la presencia de un gran exceso de amoníaco a una temperatura baja, la cloramina reacciona más para producir la hidrazina, N2H4:
\[\ce{NH3}(aq)+\ce{OCl-}(aq)⟶\ce{NH2Cl}(aq)+\ce{OH-}(aq)\]
\[\ce{NH2Cl}(aq)+\ce{NH3}(aq)+\ce{OH-}(aq)⟶\ce{N2H4}(aq)+\ce{Cl-}(aq)+\ce{H2O}(l)\]
La hidracina anhidra es relativamente estable a pesar de su energía libre de formación positiva:
\[\ce{N2}(g)+\ce{2H2}(g)⟶\ce{N2H4}(l) \hspace{20px} ΔG^\circ_\ce{f}=\mathrm{149.2\:kJ\:mol^{−1}}\]
La hidracina es un líquido incoloro y humeante que tiene algunas propiedades físicas notablemente similares a las del H2O (se funde a 2 °C, hierve a 113.5 °C y tiene una densidad a 25 °C de 1.00 g/mL). Se quema rápida y completamente en el aire con una evolución sustancial de calor:
\[\ce{N2H4}(l)+\ce{O2}(g)⟶\ce{N2}(g)+\ce{2H2O}(l) \hspace{20px} ΔH°=\mathrm{−621.5\:kJ\:mol^{−1}}\]
Como el amoníaco, la hidracina es una base de Brønsted y una base de Lewis, aunque es más débil que el amoníaco. Reacciona con los ácidos fuertes y forma dos series de sales que contienen los iones \(\ce{N2H5+}\) y \(\ce{N2H6^2+}\), respectivamente. Algunos cohetes usan la hidracina como combustible.
Los compuestos de hidrógeno de fósforo
El hidruro de fósforo más importante es la fosfina, PH3, un gas similar al amoníaco en términos de fórmula y estructura. Diferentemente al amoníaco, no es posible formar la fosfina por la unión directa de los elementos. Hay dos métodos para la preparación de la fosfina. Un método es mediante la acción de un ácido sobre un fosfuro iónico. El otro método es la desproporción del fósforo blanco con una base concentrada caliente para producir la fosfina y el ion fosfito de hidrógeno:
\[\ce{AlP}(s)+\ce{3H3O+}(aq)⟶\ce{PH3}(g)+\ce{Al^3+}(aq)+\ce{3H2O}(l)\]
\[\ce{P4}(s)+\ce{4OH-}(aq)+\ce{2H2O}(l)⟶\ce{2HPO3^2-}(aq)+\ce{2PH3}(g)\]
La fosfina es un gas incoloro, muy venenoso, que tiene un olor parecido al del pescado pudrido. El calor descompone la fosfina fácilmente \((\ce{4PH3} ⟶ \ce{P4}+\ce{6H2})\) y el compuesto se quema en el aire. Los principales usos de la fosfina son como fumigante para los granos y en el procesamiento de los semiconductores. Similarmente al amoníaco, la fosfina gaseosa se une con los haluros de hidrógeno gaseosos, formando compuestos de fosfonio como PH4Cl y PH4I. La fosfina es una base mucho más débil que el amoníaco; por eso estos compuestos se descomponen en el agua y el PH3 insoluble se escapa de la solución.
Los compuestos de hidrógeno de azufre
El sulfuro de hidrógeno, H2S, es un gas incoloro que es responsable por el olor desagradable de los huevos podridos y de muchas fuentes termales. El sulfuro de hidrógeno es tan tóxico como el cianuro de hidrógeno; por eso se debe tener mucho cuidado al manipularlo. El sulfuro de hidrógeno es particularmente engañoso porque paraliza los nervios olfatorios; después de una breve exposición, no se puede oler.
La producción del sulfuro de hidrógeno mediante la reacción directa de los elementos (H2 + S) es insatisfactoria porque el rendimiento es bajo. Un método de preparación más efectivo es la reacción de un sulfuro metálico con un ácido diluido. Por ejemplo:
\[\ce{FeS}(s)+\ce{2H3O+}(aq)⟶\ce{Fe^2+}(aq)+\ce{H2S}(g)+\ce{2H2O}(l)\]
Es fácil oxidar el azufre en los sulfuros metálicos y en el sulfuro de hidrógeno, esto causa que los sulfuros metálicos y el H2S sean buenos agentes reductores. En soluciones ácidas, el sulfuro de hidrógeno reduce Fe3+ a Fe2+, \(\ce{MnO4-}\) a Mn2+, \(\ce{Cr2O7^2-}\) a Cr3+ y HNO3 a NO2. El azufre en H2S generalmente se oxida al azufre elemental, a menos que esté presente un gran exceso del agente oxidante. En cual caso, el sulfuro se puede oxidar a \(\ce{SO3^ 2 -}\) o \(\ce{SO4^2-}\) (o a SO2 o SO3 en la ausencia del agua):
\[\ce{2H2S}(g)+\ce{O2}(g)⟶\ce{2S}(s)+\ce{2H2O}(l)\]
Este proceso de oxidación causa la eliminación del sulfuro de hidrógeno que se encuentra en muchas fuentes de gas natural. Los depósitos de azufre en las regiones volcánicas pueden ser el resultado de la oxidación del H2S presente en los gases volcánicos.
El sulfuro de hidrógeno es un ácido diprótico débil que se disuelve en el agua para formar el ácido hidrosulfúrico. El ácido se ioniza en dos etapas y produce los iones de sulfuro de hidrógeno, HS−, en la primera etapa e los iones de sulfuro, S2−, en la segunda. Ya que el sulfuro de hidrógeno es un ácido débil, las soluciones acuosas de sulfuros solubles y sulfuros de hidrógeno son básicas:
\[\ce{S^2-}(aq)+\ce{H2O}(l)⇌\ce{HS-}(aq)+\ce{OH-}(aq)\]
\[\ce{HS-}(aq)+\ce{H2O}(l)⇌\ce{H2S}(g)+\ce{OH-}(aq)\]
Los compuestos de los haluros de hidrógeno
Los compuestos binarios que solo contienen el hidrógeno y un halógeno se llaman los haluros de hidrógeno. A temperatura ambiente, los haluros de hidrógeno puro: HF, HCl, HBr y HI son gases.
En general, es posible preparar los haluros usando las técnicas generales usadas para preparar otros ácidos. El flúor, el cloro y el bromo reaccionan directamente con el hidrógeno para formar el haluro de hidrógeno respectivo. Esta es una reacción comercialmente importante para preparar el cloruro de hidrógeno y el bromuro de hidrógeno.
La reacción ácido-base entre un ácido fuerte no volátil y un haluro metálico produce un haluro de hidrógeno. El escape del haluro de hidrógeno gaseoso hace que la reacción este completa. Por ejemplo, el método habitual para preparar el fluoruro de hidrógeno es calentando una mezcla de fluoruro de calcio, CaF2 y el ácido sulfúrico concentrado:
\[\ce{CaF2}(s)+\ce{H2SO4}(aq)⟶\ce{CaSO4}(s)+\ce{2HF}(g)\]
El fluoruro de hidrógeno gaseoso también es un subproducto en la preparación de los fertilizantes fosfatados por la reacción de fluoroapatita, Ca5(PO4)3F, con el ácido sulfúrico. La reacción de ácido sulfúrico concentrado con una sal de cloruro produce el cloruro de hidrógeno tanto comercialmente como en el laboratorio.
En la mayoría de los casos, el cloruro de sodio es el cloruro seleccionado porque es el cloruro más barato. El bromuro de hidrógeno y el yoduro de hidrógeno no se pueden preparar usando el ácido sulfúrico porque este ácido es un agente oxidante que puede oxidar tanto el bromuro como el yoduro. Sin embargo, es posible preparar tanto el bromuro de hidrógeno como el yoduro de hidrógeno usando un ácido como el ácido fosfórico porque es un agente oxidante más débil. Por ejemplo:
\[\ce{H3PO4}(l)+\ce{Br-}(aq)⟶\ce{HBr}(g)+\ce{H2PO4-}(aq)\]
Todos los haluros de hidrógeno son muy solubles en el agua y forman los ácidos hidrohalicos. Con la excepción del fluoruro de hidrógeno, que tiene un fuerte enlace de hidrógeno-fluoruro, son ácidos fuertes. Las reacciones de los ácidos hidrácidos con los metales, hidróxidos, óxidos o carbonatos metálicos producen las sales de los haluros. La mayoría de las sales de cloruro son solubles en el agua. AgCl, PbCl2 y Hg2Cl2 son las excepciones más comunes.
Los iones de haluro les dan a las sustancias las propiedades asociadas con X- (aq). Los iones de haluro mas pesados (Cl-, Br-, y I-) pueden actuar como agentes reductores, y los iones de haluro más ligeros o otros agentes oxidantes los oxidaran:
\ce{Br2}(aq)+\ce{2e-}⟶\ce{2Br-}(aq) \hspace{20px} E°=\mathrm{1.09\:V}\\
\ce{I2}(aq)+\ce{2e-}⟶\ce{2I-}(aq) \hspace{20px} E°=\mathrm{0.54\:V}\]
Por ejemplo, el bromo oxida el yodo:
\[\ce{Br2}(aq)+\ce{2HI}(aq)⟶\ce{2HBr}(aq)+\ce{I2}(aq) \hspace{20px} E°=\mathrm{0.55\:V}\]
El ácido fluorhídrico es único en sus reacciones con la arena (el dióxido de silicio) y con el vidrio, que es una mezcla de silicatos:
\[\ce{SiO2}(s)+\ce{4HF}(aq)⟶\ce{SiF4}(g)+\ce{2H2O}(l)\]
\[\ce{CaSiO3}(s)+\ce{6HF}(aq)⟶\ce{CaF2}(s)+\ce{SiF4}(g)+\ce{3H2O}(l)\]
El tetrafluoruro de silicio volátil escapa de estas reacciones. Esto ocurre porque el fluoruro de hidrógeno ataca el vidrio, puede congelar o grabar el vidrio y se usa para grabar marcas en termómetros, buretas y otras cosas hechas de vidrio.
El uso más grande del fluoruro de hidrógeno es la producción de hidroclorofluorocarbonos para los refrigerantes, plásticos y propulsores. El segundo uso más importante está en la fabricación de la criolita, Na3AlF6, que es importante en la producción del aluminio. El ácido también es importante en la producción de otros fluoruros inorgánicos (como BF3), que sirven como catalizadores en la síntesis industrial de ciertos compuestos orgánicos.
El ácido clorhídrico es relativamente barato. Es un ácido importante y versátil en la industria y es importante para la fabricación de los cloruros metálicos, tintes, pegamento, glucosa y varios otros productos químicos. Una cantidad considerable también es importante para la activación de los pozos de petróleo y como licor de encurtido, un ácido que se usa para eliminar el revestimiento de óxido de hierro o acero que se va a galvanizar, estañar o esmaltar. Las cantidades de ácido bromhídrico y ácido yodhídrico usadas comercialmente son insignificantes en comparación.
Resumen
El hidrógeno es el elemento más abundante del universo y su química es verdaderamente única. Aunque tiene alguna reactividad química similar a la de los metales alcalinos, el hidrógeno tiene muchas de las mismas propiedades químicas de un no metal con una electronegatividad relativamente baja. Forma hidruros iónicos con metales activos, compuestos covalentes en los que tiene un estado de oxidación de 1− con menos elementos electronegativos y compuestos covalentes en los que tiene un estado de oxidación de 1+ con no metales más electronegativos. Reacciona explosivamente con el oxígeno, flúor y cloro pero menos fácilmente con el bromo y mucho menos con el yodo, azufre y nitrógeno. El hidrógeno reduce los óxidos de metales con menores potenciales de reducción que el cromo para formar el metal y el agua. Todos los haluros de hidrógeno son ácidos cuando se disuelven en el agua.
Glosario
- Proceso Haber
- proceso industrial usado para producir amoníaco a partir del nitrógeno e hidrógeno; involucra el uso de un catalizador de hierro y temperaturas y presiones elevadas
- haluro de hidrogeno
- compuesto binario formado entre el hidrógeno y los halógenos: HF, HCl, HBr y HI
- la hidrogenación
- la adición del hidrógeno (H2) para reducir un compuesto
Contribuyentes y atribuciones
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


