18.10: La ocurrencia, preparación y propiedades del azufre
- Page ID
- 1961
Habilidades para desarrollar
- Describir las propiedades, la preparación y los usos del azufre.
El azufre existe en la naturaleza como depósitos elementales y también como sulfuros de hierro, zinc, plomo y cobre, y sulfatos de sodio, calcio, bario y magnesio. A veces, el sulfuro de hidrógeno es un componente del gas natural y se encuentra en muchos gases volcánicos, como los que se muestran en la Figura \(\PageIndex{1}\). El azufre es un componente de muchas proteínas y es esencial para la vida.

Figura \(\PageIndex{1}\): Los gases volcánicos contienen el sulfuro de hidrógeno. (crédito: Daniel Julie / Wikimedia Commons)
El proceso Frasch, que se muestra en la Figura \(\PageIndex{2}\), es importante en la extracción del azufre libre de enormes depósitos subterráneos en Texas y Louisiana. El agua sobrecalentada (170 °C y 10 atm de presión) se empuja hacia abajo por la más externa de tres tuberías concéntricas hasta el depósito subterráneo. El agua caliente derrite el azufre. La tubería más interna conduce el aire comprimido hacia el azufre líquido. El aire fuerza al azufre líquido, mezclado con aire, a fluir hacia arriba a través del tubo de salida. Transferir la mezcla a tinas de sedimentación grandes permite que el azufre sólido se separe al enfriarse. Este azufre tiene una pureza del 99.5% al 99.9% y no requiere purificación para casi todos sus usos.
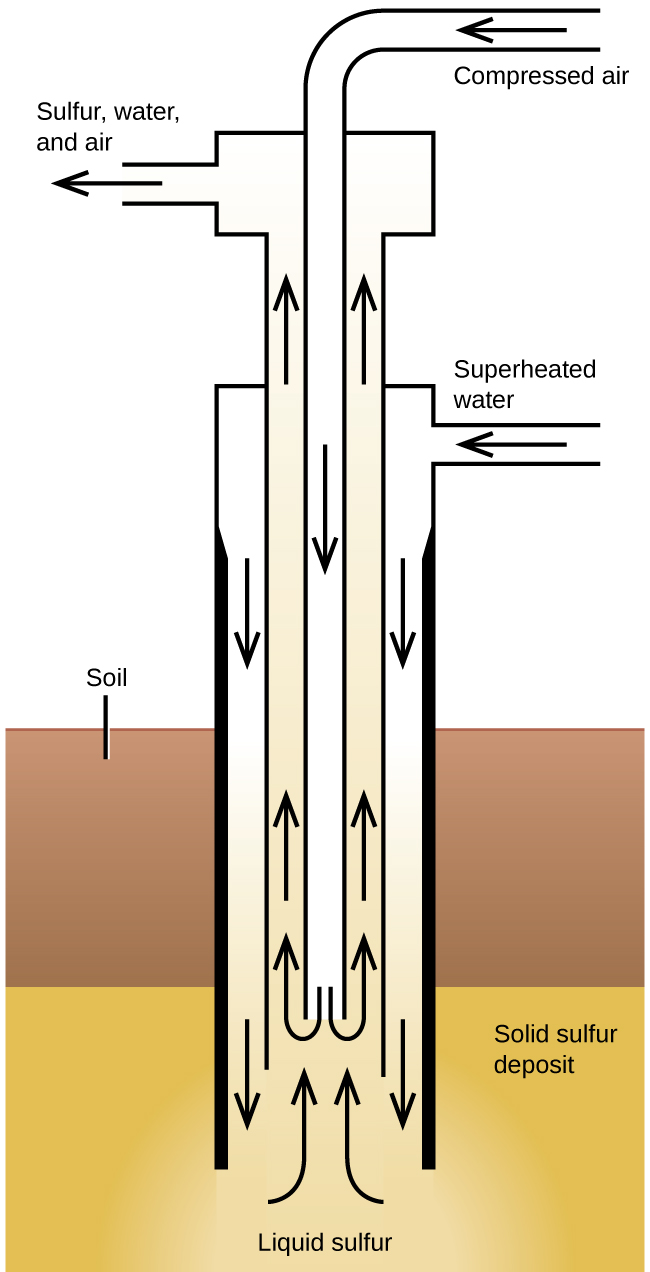
Figura \(\PageIndex{2}\): El proceso Frasch se usa para extraer el azufre de depósitos subterráneos.
Grandes cantidades de azufre también provienen del sulfuro de hidrógeno recuperado durante la purificación del gas natural.
El azufre existe en varias formas alotrópicas. La forma estable a temperatura ambiente contiene anillos de ocho miembros, por eso su fórmula verdadera es S8. Sin embargo, los químicos comúnmente usan S para simplificar los coeficientes en ecuaciones químicas, seguiremos esta práctica en este libro.
Al igual que el oxígeno, que también es miembro del grupo 16, el azufre exhibe un comportamiento no metálico. Oxida los metales, produciendo una variedad de sulfuros binarios en los que el azufre exhibe un estado de oxidación negativo (2−). El azufre elemental oxida menos no metales electronegativos, y los no metales más electronegativos, como el oxígeno y los halógenos, oxidarán al azufre elemental. Otros agentes oxidantes fuertes también oxidan el azufre. Por ejemplo, el ácido nítrico concentrado oxida el azufre al ion sulfato, con la formación simultánea del óxido de nitrógeno (IV):
\[\ce{S}(s)+\ce{6HNO3}(aq)⟶\ce{2H3O+}(aq)+\ce{SO4^2-}(aq)+\ce{6NO2}(g)\]
La química del azufre con un estado de oxidación de 2− es similar a la del oxígeno. Sin embargo, diferentemente al oxígeno, el azufre forma muchos compuestos en los que tiene estados de oxidación positivos.
Resumen
El azufre (grupo 16) reacciona con casi todos los metales y fácilmente forma el ion sulfuro, S2−, en el que tiene un estado de oxidación de 2−. El azufre reacciona con casi todos los no metales.
Glosario
- El proceso Frasch
- este proceso es importante en la extracción del azufre libre de enormes depósitos subterráneos
Contribuyentes y Atribuciones
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


