21.1: La estructura y estabilidad nuclear
- Page ID
- 1978
Habilidades para desarrollar
- Describir la estructura nuclear en términos de protones, neutrones y electrones
- Calcular el defecto de masa y la energía de enlace para los núcleos
- Explicar las tendencias en la estabilidad relativa de los núcleos
La química nuclear es el estudio de las reacciones que involucran cambios en la estructura nuclear. El capítulo sobre los átomos, moléculas e iones introdujo la idea básica de la estructura nuclear, que el núcleo de un átomo está hecho de protones y, con la excepción de \(\ce{^1_1H}\), neutrones. Recuerde que la cantidad de protones en el núcleo se llama el número atómico (\(Z\)) del elemento, y la suma de la cantidad de protones y la cantidad de neutrones es el número másico (\(A\)). Los átomos con el mismo número atómico pero diferentes números de masa son isótopos del mismo elemento. A veces, cuando nos referimos a un solo tipo de núcleo usamos el término nucleido y lo identificamos por la notación:
\[\ce{^{A}_{Z}X} \label{Eq1}\]
donde
- \(X\) es el símbolo del elemento,
- \(A\) es el número másico y
- \(Z\) es el número atómico.
A veces, se refiere un nucleido por el nombre del elemento seguido por un guión y el número de masa. Por ejemplo, \(\ce{^{14}_6C}\) se llama "carbono-14".
Los protones y neutrones, llamados colectivamente nucleones, están empaquetados en un núcleo. Con un radio de unos 10-15 metros, un núcleo es bastante pequeño en comparación con el radio de todo el átomo, que es de unos 10-10 metros. Los núcleos son extremadamente densos en comparación con la materia a granel, con un promedio de \(1.8\veces10^{14}\) gramos por centímetro cúbico. Por ejemplo, el agua tiene una densidad de 1 gramo por centímetro cúbico y el iridio, uno de los elementos más densos que se conocen, tiene una densidad de 22.6 g/cm3. Si la densidad de la Tierra fuera igual a la densidad nuclear promedio, el radio de la Tierra sería de sólo unos 200 metros (el radio real de la Tierra es aproximadamente \(6.4\veces 10^6\) metros, 30.000 veces más grande). El ejemplo \(\PageIndex{1}\) demuestra que grandes pueden ser las densidades nucleares en el mundo natural.
Ejemplo \(\PageIndex{1}\): Los neutrones de las estrellas
La densidad de una estrella de neutrones se forma cuando el núcleo de una estrella muy masiva pasa por un colapso gravitacional, lo que hace que las capas exteriores de la estrella exploten en una supernova. Las estrellas más densas que existen en el universo están hechas casi en su totalidad por neutrones, con densidades comparables a la densidad media de un núcleo atómico. Una estrella de neutrones en una galaxia lejana tiene una masa igual a 2.4 masas solares (1 masa solar = \(M_☉\) = masa del sol = \(\mathrm{1.99\times 10^{30}\; kg}\)) y un diámetro de 26 km.
-
¿Cuál es la densidad \(\rho\) de esta estrella de neutrones?
-
¿Cómo se compara la densidad de esta estrella de neutrones con la densidad de un núcleo de uranio, que tiene un diámetro de aproximadamente 15 fm (1 fm = 10-15 m)?
Solución
Podemos tratar tanto a la estrella de neutrones como al núcleo U-235 como esferas. Entonces la densidad para ambos viene dada por:
\[\rho = \dfrac{m}{V}\]
con
\[V = \dfrac{4}{3} \pi r^3\]
(a) El radio de la estrella de neutrones es \(\mathrm{\dfrac{1}{2}\times 26\; km = \dfrac{1}{2}\times 2.6 \times10^4\; m = 1.3 \times10^4\;m}\) por eso la densidad de la estrella de neutrones es:
\[\rho=\dfrac{m}{V}=\dfrac{m}{\frac{4}{3}\pi r^3} =\mathrm{\dfrac{2.4(1.99 \times 10^{30}\;kg)}{\frac{4}{3} \pi (1.3 \times 10^4m)^3}=5.2 \times 10^{17}\;kg/m^3}\]
\[\rho=\dfrac{m}{V}=\dfrac{m}{\frac{4}{3}\pi r^3} =\mathrm{\dfrac{235\;amu\left(\frac{1.66 \times 10^{-27}\;kg}{1\;amu}\right)}{\frac{4}{3} \pi (7.5 \times 10^{-15}m)^3}=2.2 \times 10^{17}\;kg/m^3}\]
Estos valores son bastante similares (mismo orden de magnitud), pero el núcleo es más del doble de denso que la estrella de neutrones.
Ejercicio \(\PageIndex{1}\)
Encuentre la densidad de una estrella de neutrones con una masa de 1.97 masas solares y un diámetro de 13 km, y compárela con la densidad de un núcleo de hidrógeno, que tiene un diámetro de 1.75 fm (\(\mathrm{1\;fm=1\por10^{-15}\;m}\)).
Respuesta
La densidad de la estrella de neutrones es \(\mathrm{3.4\times10^{18}\;kg/m^3}\). La densidad de un núcleo de hidrógeno es \(\mathrm{6.0\ times10^{17}\;kg/m^3}\). La estrella de neutrones es 5.7 veces más densa que el núcleo de hidrógeno.
Mantener juntos los protones cargados positivamente en el volumen muy pequeño de un núcleo requiere interacciones de atracción muy fuertes porque los protones cargados positivamente se repelen entre sí con la fuerza a distancias tan cortas. La fuerza de atracción que mantiene unido el núcleo es la fuerza nuclear fuerte. (Esta fuerza es una de las cuatro fuerzas fundamentales que se sabe que existen. Las otras son la fuerza electromagnética, la fuerza gravitacional y la fuerza nuclear débil). Esta fuerza actúa entre los protones, neutrones y entre protones y neutrones. Es muy diferente de la fuerza electrostática que mantiene los electrones cargados negativamente alrededor de un núcleo cargado positivamente (la atracción entre las cargas opuestas). En distancias menos que 10-15 metros y dentro del núcleo, la fuerza nuclear fuerte es mucho más fuerte que las repulsiones electrostáticas entre los protones; en distancias más grandes y fuera del núcleo, es esencialmente inexistente.
La energía de unión nuclear
Como un ejemplo simple de la energía asociada con la fuerza nuclear fuerte, considere el átomo de helio hecho por dos protones, dos neutrones y dos electrones. La masa total de estas seis partículas subatómicas se puede calcular como:
\[ \underset{\Large\text{protons}}{(2 \times 1.0073\; \text{amu})} + \underset{\Large\text{neutrons}}{(2 \times 1.0087\; \text{amu})} + \underset{\Large\text{electrons}}{(2 \times 0.00055\; \text{amu})}= 4.0331\; \text{amu }\label{Eq2}\]
Sin embargo, las mediciones espectrométricas de las masas revelan que la masa de un átomo de \(\ce{_2^4He}\) es 4.0026 amu, menos que las masas combinadas de sus seis partículas subatómicas constituyentes. Esta diferencia entre las masas calculadas y medidas experimentalmente se conoce como el defecto de masa del átomo. En el caso del helio, el defecto de masa indica una "pérdida" de masa de 4.0331 amu - 4.0026 amu = 0.0305 amu. La pérdida de masa que acompaña a la formación de un átomo a partir de protones, neutrones y electrones se debe a la conversión de esa masa en energía que se produce cuando se forma el átomo. La energía de enlace nuclear es la energía producida cuando los nucleones de los átomos se unen; esta es también la energía necesaria para romper un núcleo en sus protones y neutrones constituyentes. En comparación con las energías de enlace químico, las energías de enlace nuclear son mucho más grades, como aprenderemos en esta sección. En consecuencia, los cambios de energía asociados con las reacciones nucleares son mucho mayores que los de las reacciones químicas.
La conversión entre la masa y energía está representada por la ecuación de equivalencia de masa-energía que fue establecida por Albert Einstein:
\[E=mc^2 \label{Eq3}\]
donde E es la energía, m es la masa de la materia que se está convirtiendo y c es la velocidad de la luz en el vacío. Esta ecuación se puede usar para encontrar la cantidad de energía que resulta cuando la materia se convierte en energía. Usando esta ecuación de equivalencia masa-energía, la energía de enlace nuclear de un núcleo se puede calcular a partir de su defecto de masa, como se demuestra en el Ejemplo \(\PageIndex{2}\). Una variedad de unidades se usan comúnmente para las energías de enlace nuclear, incluidos los electronvoltios (eV), con 1 eV igual a la cantidad de energía necesaria para mover la carga de un electrón a través de una diferencia de potencial eléctrico de 1 voltio, haciendo \(\mathrm{1\;eV=1.602\times10^{-19}\;J}\).
Ejemplo \(\PageIndex{2}\): Calculando la energía de enlace nuclear
Determine la energía de enlace del nucleido \(\ce{^4_2 He}\) en:
-
julios por mol de núcleos
-
julios por núcleo
-
MeV por núcleo
Solución
El defecto de masa para un núcleo \(\ce{^4_2He}\) es 0.0305 amu, como se mostró anteriormente. Determine la energía de enlace en julios por núclido usando la ecuación de equivalencia masa-energía. Para acomodar las unidades de energía requeridas, el defecto de masa se debe expresar en kilogramos (recuerde que 1 J = 1 kg m2/s2).
(a) Primero, exprese el defecto de masa en g/mol. Esto se hace fácilmente considerando la equivalencia numérica de la masa atómica (amu) y masa molar (g/mol) que resulta de las definiciones de amu y unidades molares (se necesita, consulte la discusión anterior en el capítulo sobre los átomos, moléculas e iones). Por lo tanto, el defecto de masa es de 0.0305 g/mol. Para acomodar las unidades de los otros términos en la ecuación masa-energía, la masa se debe expresar en kg, ya que 1 J = 1 kg m2/s2. Convertir los gramos a kilogramos produce un defecto de masa de \(\mathrm{3.05\times10^{-5}\;kg/mol}\). Sustituyendo esta cantidad en la ecuación de equivalencia de masa-energía nos da:
\[E=mc^2=\mathrm{\dfrac{3.05 \times 10^{-5}\;kg}{mol} \times \left(\dfrac{2.998 \times 10^8\;m}{s}\right)^2=2.74×10^{12}\:kg\:m^2s^{-2}mol^{-1}}\]
\[\mathrm{=2.74 \times 10^{12}\;J/mol=2.74\: TJ /mol}\]
(b) La energía de enlace para un solo núcleo se calcula usando la energía de enlace molar utilizando el número de Avogadro:
(c) Recall that \(\mathrm{1\; eV = 1.602 \times 10^{-19}\; J}\). Usando la energía de enlace calculado en parte (b):
\[E=\mathrm{4.55×10^{-12}\:J×\dfrac{1\: eV}{1.602×10^{-19}\:J}=2.84×10^7\:eV=28.4\: MeV}\]
Ejercicio \(\PageIndex{2}\)
¿Cuál es la energía de enlace para el núclido \(\ce{^{19} _9F}\) (masa atómica: 18.9984 amu) en MeV por núcleo?
- Respuesta
-
148.4 MeV
Debido a que los cambios de energía para romper y formar los enlaces son tan pequeños en comparación con los cambios de energía para romper o formar los núcleos, los cambios de masa durante todas las reacciones químicas ordinarias son casi indetectables. Como se discutió en el capítulo sobre la termoquímica, las reacciones químicas más energéticas exhiben entalpías del orden de miles de kJ/mol, lo que equivale a diferencias de masa en el rango de nanogramos (10–9 g). Por otro lado, las energías de enlace nuclear son típicamente del orden de miles de millones de kJ/mol, lo que corresponde a las diferencias de masa en el rango de miligramos (10–3 g).
La estabilidad nuclear
Un núcleo es estable si no se puede transformar en otra configuración sin agregar energía del exterior. De los miles de nucleidos que existen, unos 250 son estables. Una gráfica del número de neutrones versus el número de protones para los núcleos estables revela que los isótopos estables caen en una banda angosta. Esta región se conoce como la banda de estabilidad (también llamada el cinturón, zona o valle de estabilidad). La línea recta en la Figura \(\PageIndex{1}\) representa los núcleos que tienen una proporción de protones a neutrones de 1: 1 (proporción n: p). Tenga en cuenta que en general los núcleos estables más ligeros tienen el mismo número de protones y neutrones. Por ejemplo, el nitrógeno 14 tiene siete protones y siete neutrones. Los núcleos estables más pesados, sin embargo, tienen cada vez más neutrones que protones. Por ejemplo: el hierro-56 tiene 30 neutrones y 26 protones, una relación n: p de 1.15, mientras que el núclido estable plomo-207 tiene 125 neutrones y 82 protones, una relación n: p igual a 1.52. Esto se debe a que los núcleos más grandes tienen más repulsiones protón-protón y requieren más neutrones para proporcionar las fuerzas compensatorias fuertes para superar estas repulsiones electrostáticas y mantener unido el núcleo.
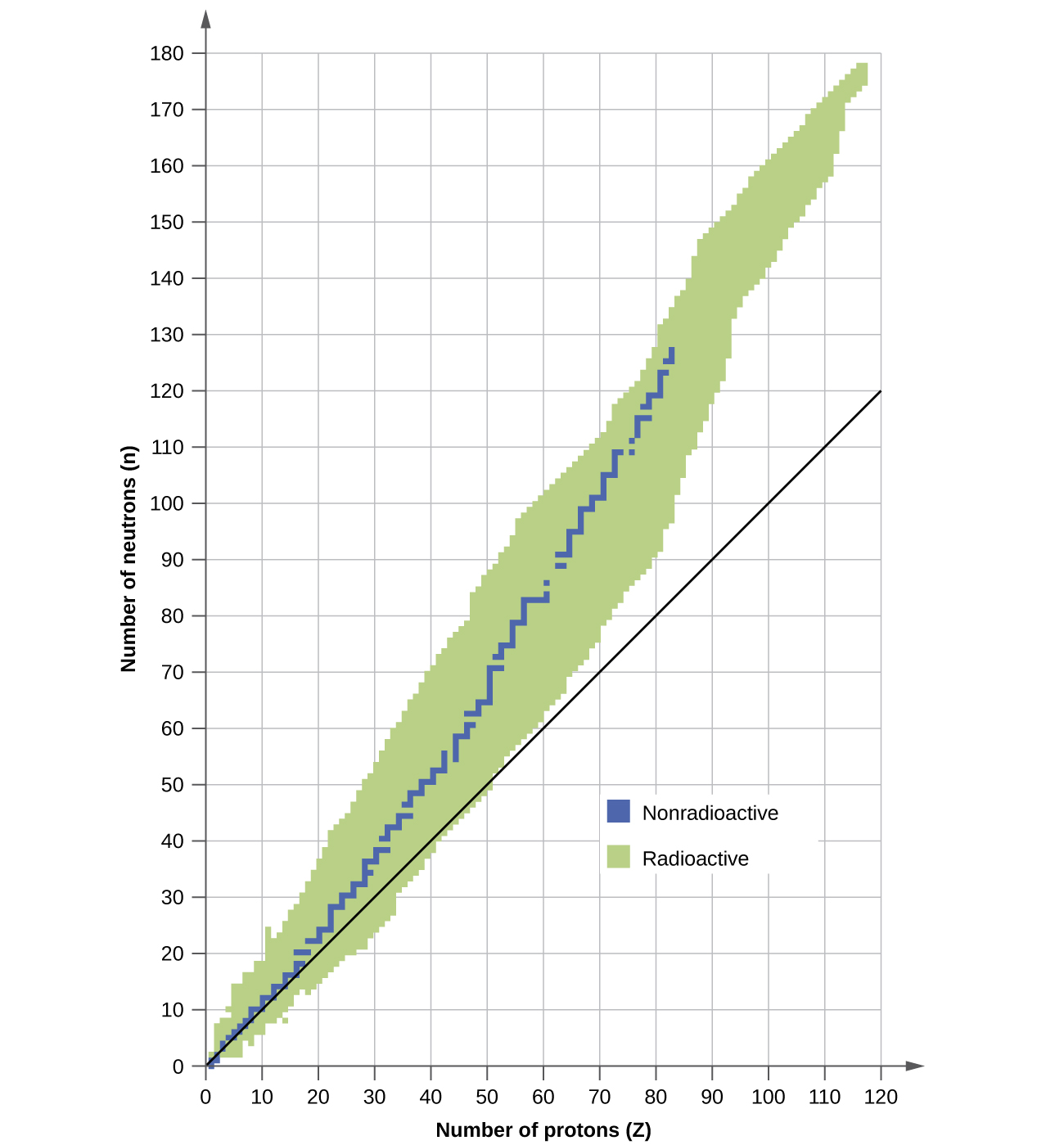
Figura \(\PageIndex{1}\): Esta gráfica muestra los nucleidos que se sabe que existen y los que son estables. Los nucleidos estables se indican en azul y los nucleidos inestables se indican en verde. Tenga en cuenta que todos los isótopos de elementos con números atómicos mayores que 83 son inestables. La línea continua es la línea donde n = Z.
Los núcleos que se encuentran a la izquierda o a la derecha de la banda de estabilidad son inestables y exhiben radiactividad. Cambian espontáneamente (decaen) en otros núcleos que están dentro o más cerca de la banda de estabilidad. Estas reacciones de desintegración nuclear convierten un isótopo inestable (o radioisótopo) en otro isótopo más estable. Discutiremos la naturaleza y los productos de esta desintegración radiactiva en las siguientes secciones de este capítulo.
Se pueden hacer varias observaciones sobre la relación entre la estabilidad de un núcleo y su estructura. Es más probable que los núcleos con números pares de protones, neutrones o ambos sean estables (Tabla \(\PageIndex{1}\)). Los núcleos con cierto número de nucleones, conocidos como números mágicos, son estables contra la desintegración nuclear. Estos números de protones o neutrones (2, 8, 20, 28, 50, 82 y 126) forman capas completas en el núcleo. Estos son similares en concepto a las capas de electrones estables observadas para los gases nobles. Núcleos que tienen números mágicos de protones y neutrones, como \(\ce{^4_2He}\), \(\ce{^{16}_8O}\), \(\ce{^{40}_{20}Ca}\) y \(\ce{^{208} _{82}Pb}\) y son particularmente estables. Estas tendencias en la estabilidad nuclear se pueden racionalizar considerando un modelo mecánico cuántico de estados de energía nuclear similar al que se usa para describir los estados electrónicos anteriormente en este libro de texto. Los detalles de este modelo están más allá del alcance de este capítulo.
| Número de isótopos estables | Número de protones | Número de neutrones |
|---|---|---|
| 5 | impar | impar |
| 50 | impar | par |
| 53 | par | impar |
| 157 | par | par |
La estabilidad relativa de un núcleo se correlaciona con su energía de enlace por nucleón, la energía de enlace total para el núcleo se divida por el número de nucleones en el núcleo. Por ejemplo, la energía de enlace para un núcleo \(\ce{^4_2He}\) es por lo tanto:
\[\mathrm{\dfrac{28.4\; MeV}{4\; nucleons}=7.10\; MeV/nucleon} \label{Eq3a}\]
La energía de enlace por nucleón de un nucleido en la curva que se muestra en la Figura \(\PageIndex{2}\)6
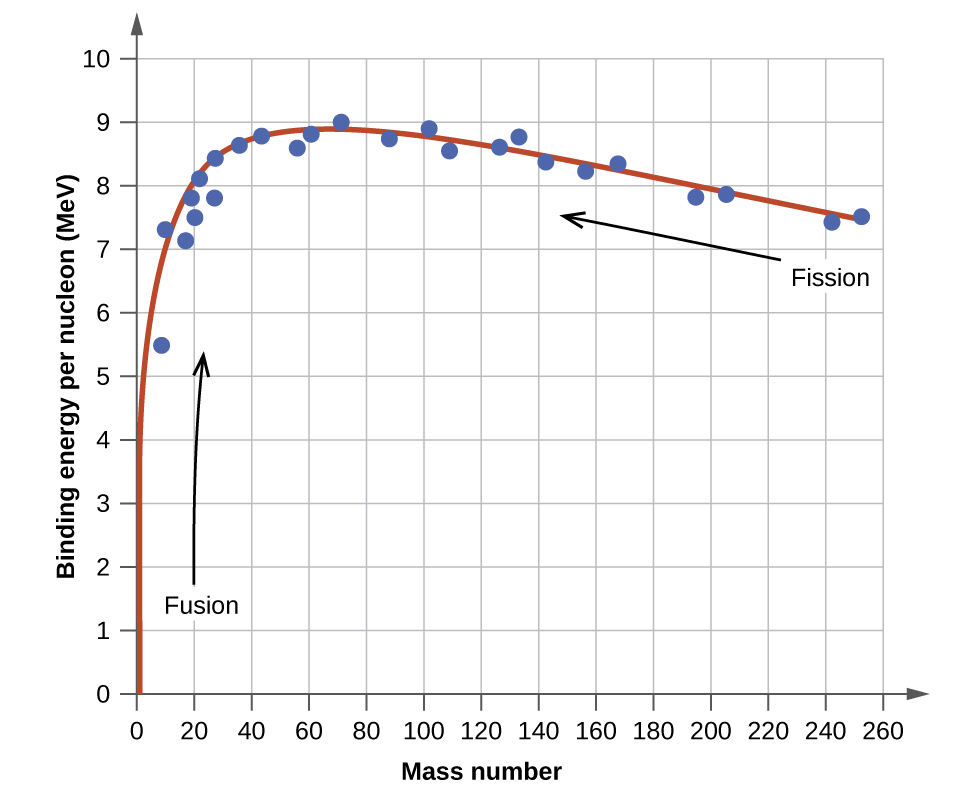
Figura \(\PageIndex{2}\): La energía de enlace por nucleón es más grande para los nucleidos con un número de masa de aproximadamente 56.
Ejemplo \(\PageIndex{3}\): Calculando la energía enlace por nucleón
El nucleido de hierro \(\ce{^{56}_{26}Fe}\) se encuentra cerca de la parte superior de la curva de energía de enlace (Figura \(\PageIndex{2}\)) y es uno de los nucleidos más estables. ¿Cuál es la energía de enlace por nucleón (en MeV) para el núclido \(\ce{^{56}_{26}Fe}\) (masa atómica de 55.9349 uma)?
Solución
Como en el ejemplo, primero determinamos el defecto de masa del nucleido, que es la diferencia entre la masa de 26 protones, 30 neutrones y 26 electrones, y la masa observada de un \(\ce{^{56}_{26}Fe}\) átomo:
\[\begin{align*}
\mathrm{Mass\: defect}&=\mathrm{[(26×1.0073\: amu)+(30×1.0087\: amu)+(26×0.00055\: amu)]−55.9349\: amu}\\
&=\mathrm{56.4651\: amu−55.9349\: amu}\\
&=\mathrm{0.5302\: amu}
\end{align*}\]
A continuación, calculamos la energía de enlace para un núcleo usando del defecto de masa utilizando la ecuación de equivalencia de masa-energía:
\[\begin{align*}
E&=mc^2=\mathrm{0.5302\: amu×\dfrac{1.6605×10^{-27}\:kg}{1\: amu}×(2.998×10^8\:m/s)^2}\\
&=\mathrm{7.913×10^{−11}\:\textrm{kg⋅m}/s^2}\\
&=\mathrm{7.913×10^{−11}\:J}
\end{align*}\]
Luego convertimos la energía de enlace en julios por núcleo en unidades de MeV por nucleido:
\[\mathrm{7.913×10^{−11}\:J×\dfrac{1\: MeV}{1.602×10^{−13}\:J}=493.9\: MeV}\]
Finalmente, determinamos la energía de enlace por nucleón dividiendo la energía de enlace nuclear total por el número de nucleones en el átomo:
\[\textrm{Binding energy per nucleon}=\mathrm{\dfrac{493.9\: MeV}{56}=8.820\: MeV/nucleon}\]
Tenga en cuenta que esto es casi 25% más grande que la energía de enlace por nucleón para \(\ce{^4_2He}\). (Tenga en cuenta también que este es el mismo proceso que en el Ejemplo, pero con un paso adicional de dividir el enlace nuclear total energía por el número de nucleones.)
Ejercicio \(\PageIndex{3}\)
¿Cuál es la energía de enlace por nucleón en \(\ce{^{19} _9F}\) (masa atómica, 18.9984 uma)?
- Respuesta
-
7.810 MeV/nucleón
Resumen
Un núcleo atómico consiste en protones y neutrones, llamados colectivamente nucleones. Aunque los protones se repelen entre sí, el núcleo se mantiene firmemente unido por una fuerza de corto alcance, llamada la interacción nuclear fuerte. Un núcleo tiene menos masa que la masa total de sus nucleones constituyentes. Esta masa "faltante" es el defecto de masa, que se ha convertido en la energía de enlace que mantiene unido el núcleo de acuerdo con la ecuación de equivalencia masa-energía de Einstein, E = mc2. De los muchos nucleidos que existen, solo un poco son estable. Es especialmente probable que los nucleidos con un número par de protones o neutrones, o aquellos con un número mágico de nucleones, sean estables. Estos nucleidos estables ocupan una banda estrecha de estabilidad en un gráfico de número de protones versus número de neutrones. La energía de enlace por nucleón es más grande para los elementos con números de masa cerca de 56; estos son los núcleos más estables.
Ecuaciones clave
- E = mc2
Glosario
- banda de estabilidad
- (también, cinturón de estabilidad, zona de estabilidad o valle de estabilidad) región del gráfico del número de protones versus el número de neutrones que contienen nucleidos estables (no radiactivos)
- energía de enlace por nucleón
- energía de enlace total para el núcleo dividida por el número de nucleones en el núcleo
- electronvoltio (eV)
- unidad de medida de las energías de enlace nuclear, con 1 eV igual a la cantidad de energía causada por el movimiento de un electrón a través de una diferencia de potencial eléctrico de 1 voltio
- número mágico
- núcleos con números específicos de nucleones que están dentro de la banda de estabilidad
- defecto masivo
- diferencia entre la masa de un átomo y la masa sumada de sus partículas subatómicas constituyentes (o la masa "perdida" cuando los nucleones se juntan para formar un núcleo)
- ecuación de equivalencia masa-energía
- relación de Albert Einstein que muestra que la masa y la energía son equivalentes
- energía de enlace nuclear
- energía perdida cuando los nucleones de un átomo están unidos (o la energía necesaria para romper un núcleo en sus protones y neutrones constituyentes)
- química nuclear
- el estudio de la estructura de los núcleos atómicos y procesos que cambian la estructura nuclear.
- nucleón
- término colectivo para los protones y neutrones en un núcleo
- nucleido
- núcleo de un isótopo particular
- radioactividad
- fenómeno causado por un nucleón inestable que espontáneamente se transforma en un nucleón que es más estable; se dice que un nucleón inestable es radiactivo
- radioisótopo
- isótopo que es inestable y se convierte en un isótopo diferente, más estable
- interacción nuclear fuerte
- interacción de atracción entre los nucleones que mantiene a un núcleo unido
Contribuyentes y atribuciones
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


