6.5: Reglas de Wade
- Page ID
- 69426
Ken Wade (Figura\(\PageIndex{1}\)) desarrolló un método para la predicción de formas de racimos de boranos; sin embargo, puede ser utilizado para una amplia gama de boranos sustituidos (como los carboranos) así como otras clases de compuestos de conglomerados.

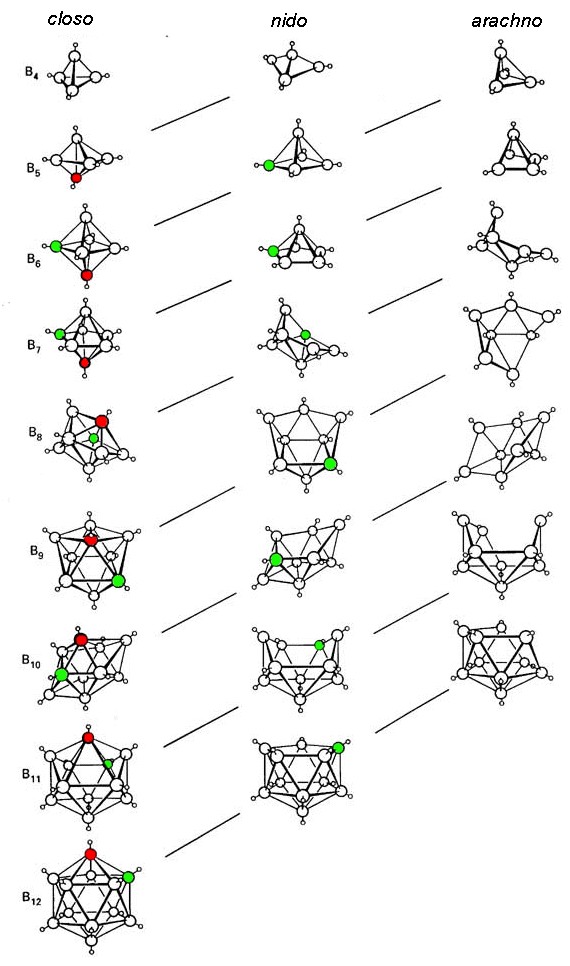
Las reglas de Wade se utilizan para racionalizar la forma de los cúmulos de boranos calculando el número total de pares de electrones esqueléticos (SEP) disponibles para la unión de conglomerados. Al usar las reglas de Wade es clave entender la relación estructural de varios boranos (Figura\(\PageIndex{2}\)).
La metodología general a seguir al aplicar las reglas de Wade es la siguiente:
- Determinar el número total de electrones de valencia a partir de la fórmula química, es decir, 3 electrones por B y 1 electrón por H.
- Restar 2 electrones por cada unidad B-H (o C-H en un carborano).
- Divide el número de electrones restantes por 2 para obtener el número de pares de electrones esqueléticos (SEP).
- Un grupo con n vértices (es decir, n átomos de boro) y n +1 SEP para la unión tiene una estructura closo.
- Un cúmulo con n-1 vértices (es decir, n -1 átomos de boro) y n +1 SEP para la unión tiene una estructura nido.
- Un grupo con n -2 vértices (es decir, n -2 átomos de boro) y n +1 SEP para la unión tiene una estructura aracno.
- Un grupo con n -3 vértices (es decir, n -3 átomos de boro) y n +1 SEP para la unión tiene una estructura hifo.
- Si el número de átomos de boro (es decir, n) es mayor que n +1 SEP entonces el boro extra ocupa una posición de terminación en una fase triangular.
¿Cuál es la estructura de B 5 H 11?
- Número total de electrones de valencia = (5 x B) + (11 x H) = (5 x 3) + (11 x 1) = 26
- Número de electrones por cada unidad B-H = (5 x 2) = 10
- Número de electrones esqueléticos = 26 — 10 = 16
- Número SEP = 16/2 = 8
- Si n +1 = 8 y n -2 = 5 átomos de boro, entonces n = 7
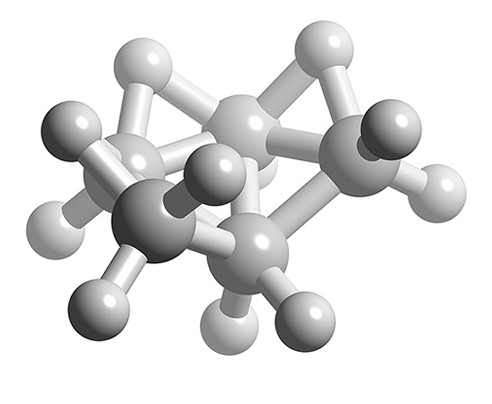
- La estructura de n = 7 es bipirámide pentagonal (Figura\(\PageIndex{2}\)), por lo tanto B 5 H 11 es un aracno basado en una bipirámide pentagonal con dos vértices faltantes (Figura\(\PageIndex{3}\)).
¿Cuál es la estructura de B 5 H 9?
- Número total de electrones de valencia = (5 x B) + (9 x H) = (5 x 3) + (9 x 1) = 24
- Número de electrones por cada unidad B-H = (5 x 2) = 10
- Número de electrones esqueléticos = 24 — 10 = 14
- Número SEP = 14/2 = 7
- Si n +1 = 7 y n -1 = 5 átomos de boro, entonces n = 6
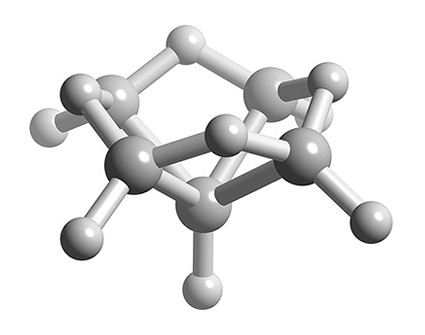
- La estructura de n = 6 es octaédrica (Figura\(\PageIndex{2}\)), por lo tanto, B 5 H 9 es una estructura nido basada en una estructura octaédrica con un ápice faltante (Figura\(\PageIndex{4}\)).
Ejemplo\(\PageIndex{1}\)
¿Cuál es la estructura de B 6 H 6 2-?
Solución
- Número total de electrones de valencia = (6 x B) + (3 x H) = (6 x 3) + (6 x 1) + 2 = 26
- Número de electrones por cada unidad B-H = (6 x 2) = 12
- Número de electrones esqueléticos = 26 — 12 = 14
- Número SEP = 14/2 = 7
- Si n +1 = 7 y n átomos de boro, entonces n = 6
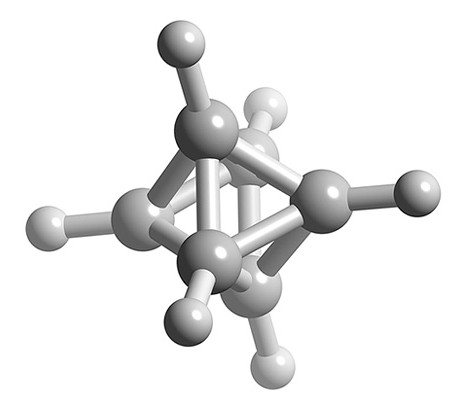
- La estructura de n = 6 es octaédrica (Figura\(\PageIndex{2}\)), por lo tanto B 6 H 6 2- es una estructura closo basada en una estructura octaédrica (Figura\(\PageIndex{5}\)).
\(\PageIndex{1}\)La tabla proporciona un resumen del cúmulo de boranos con la fórmula general B n H n x- y sus estructuras definidas por las reglas de Wade.
| Tipo | Fórmula básica | Ejemplo | # de verticies | # de vacantes | # de e- en B + cargo | # de MoS de unión |
|---|---|---|---|---|---|---|
| Closo | B n H n 2- | B 6 H 6 2- | n | 0 | 3n + 2 | n + 1 |
| Nido | B n H n 4- | B 5 H 9 | n + 1 | 1 | 3n + 4 | n + 2 |
| Aracno | B n H n 6- | B 4 H 10 | n + 2 | 2 | 3n + 6 | n + 3 |
| Hypho | B n H n 8- | B 5 H 11 2- | n + 3 | 3 | 3n + 8 | n + 4 |
Bibliografía
- R. W. Rudolph, Acc. Chem. Res., 1976, 9, 446.
- K. Wade, Adv. Inorg. Chem. Radioquímica. , 1976, 18, 1.


