6: Alcoholes e introducción a tioles, aminas, éteres y sulfuros
- Page ID
- 76978
En este capítulo, vamos a echar un vistazo más de cerca a las familias de compuestos que tienen carbono unido a través de un único enlace covalente a una\(\mathrm{O}\),\(\mathrm{N}\), o\(\mathrm{S}\). Estos se conocen como alcoholes (\(\mathrm{R-OH}\)), aminas (\(\mathrm{R-NH}_{2}\),\(\mathrm{RR}^{\prime}\mathrm{-NH}\),\(\mathrm{RR}^{\prime}\mathrm{R}^{\prime \prime}\mathrm{-N}\)), tioles (\(\mathrm{R-SH}\)), éteres (\(\mathrm{R-OR}^{\prime}\)) y sulfuros (\(\mathrm{R-SR}^{\prime}\)). Agrupamos estos compuestos en base a las similitudes y diferencias predecibles en sus propiedades químicas y físicas, específicamente el hecho de que cada uno de estos grupos funcionales tiene un elemento relativamente electronegativo (\(\mathrm{O}\),\(\mathrm{N}\) o\(\mathrm{S}\)) unido por un enlace sencillo al carbono y cada uno tiene disponibles pares de electrones solitarios que pueden ser donados a H + u otros electrófilos. El resultado es que los alcoholes, tioles y aminas (primarias y secundarias) tienen hidrógenos relativamente ácidos, lo que influye en sus reactividades químicas y todas muestran propiedades nucleofílicas.
Tabla\(6.0.1\) Ejemplos de grupos funcionales, sus nombres y\(\mathrm{pK}_{\mathrm{a}}\) aproximados
| Grupo Funcional | Ejemplo | Nombre | \(\mathrm{pK}_{\mathrm{a}}\) |
| Alcohol | 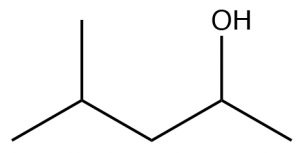 |
Retire -ane, agregue -ol.
4-metilpentan-2-ol |
(aproximado)
\(\sim 15-16\) |
| Alcohol | 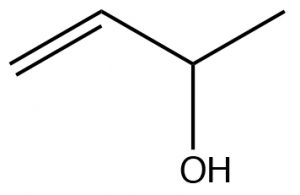 |
Los alcoholes tienen prioridad sobre
alquenos, Pero-3-en-2-ol |
|
| Tiol | 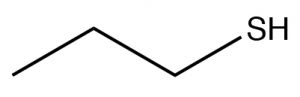 |
Cadena más larga, añadir -tiol
Propano-1-tiol |
\(\sim 10\) |
| Amina primaria | 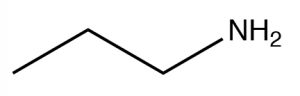 |
Cadena más larga, eliminar e, agregar
-amina Propanamina o propil amina |
\(\sim 33\) |
| Amina secundaria | 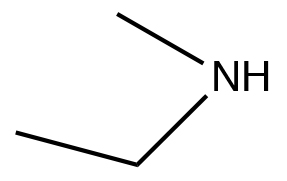 |
N-metiletanamina | \(\sim 33\) |
| Amina terciaria |  |
N-etil-N-metilpropanamina | N/A |
| Éter | 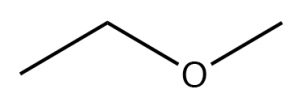 |
Metoxietano
Éter etílico metílico |
N/A |
| Sulfuro | 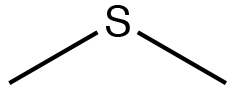 |
Dimetilsulfano
Sulfuro de dimetilo |
N/A |
Concentraremos nuestra discusión en los compuestos oxigenados, pero notaremos reactividades a través de los diversos grupos para ilustrar sus similitudes (y diferencias).


