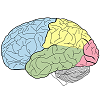
1.7: El Sistema Endocrino
- Page ID
- 121837
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Introducción

Después de estudiar este capítulo, podrás:
- Identificar las contribuciones del sistema endocrino a la homeostasis
- Discutir la composición química de las hormonas y los mecanismos de acción hormonal
- Resumir el sitio de producción, regulación y efectos de las hormonas de las glándulas pituitaria, tiroides, paratiroides, suprarrenales y pineales
- Discutir la regulación hormonal del sistema reproductivo
- Explicar el papel de las células endocrinas pancreáticas en la regulación de la glucosa en sangre
- Identificar las hormonas liberadas por el corazón, los riñones y otros órganos con funciones endocrinas secundarias
- Discutir varias enfermedades comunes asociadas a la disfunción del sistema endocrino
- Discutir el desarrollo embrionario y los efectos del envejecimiento en el sistema endocrino
Puede que nunca lo hayas pensado de esta manera, pero cuando envías un mensaje de texto a dos amigos para que te encuentren en el comedor a las seis, estás enviando señales digitales que (esperas) afectarán su comportamiento, aunque estén a cierta distancia. De igual manera, ciertas células envían señales químicas a otras células del cuerpo que influyen en su comportamiento. Esta comunicación intercelular de larga distancia, coordinación y control es fundamental para la homeostasis, y es la función fundamental del sistema endocrino.
Una visión general del sistema endocrino
Al final de esta sección, podrás:
- Distinguir los tipos de comunicación intercelular, su importancia, mecanismos y efectos
- Identificar los principales órganos y tejidos del sistema endocrino y su ubicación en el cuerpo
La comunicación es un proceso en el que un emisor transmite señales a uno o más receptores para controlar y coordinar acciones. En el cuerpo humano, dos principales sistemas de órganos participan en una comunicación relativamente “larga distancia”: el sistema nervioso y el sistema endocrino. Juntos, estos dos sistemas son los principales responsables de mantener la homeostasis en el cuerpo.
Señalización neural y endocrina
El sistema nervioso utiliza dos tipos de comunicación intercelular—señalización eléctrica y química— ya sea por la acción directa de un potencial eléctrico, o en este último caso, a través de la acción de neurotransmisores químicos como la serotonina o la norepinefrina. Los neurotransmisores actúan local y rápidamente. Cuando una señal eléctrica en forma de potencial de acción llega al terminal sináptico, se difunden a través de la hendidura sináptica (la brecha entre una neurona emisora y una neurona receptora o célula muscular). Una vez que los neurotransmisores interactúan (se unen) con los receptores en la célula receptora (possináptica), la estimulación del receptor se transduce en una respuesta como señalización eléctrica continua o modificación de la respuesta celular. La célula diana responde dentro de los milisegundos de recibir el “mensaje” químico; esta respuesta cesa muy rápidamente una vez que termina la señalización neuronal. De esta manera, la comunicación neuronal permite funciones corporales que implican acciones rápidas y breves, como el movimiento, la sensación y la cognición.En contraste, el sistema endocrino utiliza solo un método de comunicación: la señalización química. Estas señales son enviadas por los órganos endocrinos, que secretan sustancias químicas —la hormona — al líquido extracelular. Las hormonas se transportan principalmente a través del torrente sanguíneo por todo el cuerpo, donde se unen a los receptores en las células diana, induciendo una respuesta característica. Como resultado, la señalización endocrina requiere más tiempo que la señalización neuronal para provocar una respuesta en las células diana, aunque la cantidad precisa de tiempo varía con las diferentes hormonas. Por ejemplo, las hormonas liberadas cuando te enfrentas a una situación peligrosa o aterradora, llamada respuesta de lucha o huida, ocurren por la liberación de hormonas suprarrenales —epinefrina y norepinefrina— en cuestión de segundos. Por el contrario, las células diana pueden tardar hasta 48 horas en responder a ciertas hormonas reproductivas.
Además, la señalización endocrina es típicamente menos específica que la señalización neural. La misma hormona puede desempeñar un papel en una variedad de procesos fisiológicos diferentes dependiendo de las células diana involucradas. Por ejemplo, la hormona oxitocina promueve las contracciones uterinas en mujeres en trabajo de parto. También es importante en la lactancia materna, y puede estar involucrada en la respuesta sexual y en sentimientos de apego emocional tanto en hombres como en mujeres.
En general, el sistema nervioso implica respuestas rápidas a cambios rápidos en el ambiente externo, y el sistema endocrino suele actuar más lentamente, cuidando el ambiente interno del cuerpo, manteniendo la homeostasis y controlando la reproducción (Tabla (Sistemas Endocrinos y Nerviosos)). Entonces, ¿cómo ocurre tan rápidamente la respuesta de lucha o huida que se mencionó anteriormente si las hormonas suelen actuar más lentamente? Es porque los dos sistemas están conectados. Es la acción rápida del sistema nervioso en respuesta al peligro en el ambiente lo que estimula a las glándulas suprarrenales a secretar sus hormonas. Como resultado, el sistema nervioso puede provocar respuestas endocrinas rápidas para mantenerse al día con cambios repentinos tanto en el ambiente externo como en el interno cuando sea necesario.
| Endocrino y Nervioso | ||
|---|---|---|
| Sistema endocrino | Sistema Nervioso | |
| Mecanismo (es) de señalización | Químico | Químico/eléctrico |
| Señal química primaria | Hormonas | Neurotransmisores |
| Distancia recorrida | Largo o corto | Siempre corto |
| Tiempo de respuesta | Rápido o lento | Siempre rápido |
| Medio ambiente dirigido | Interno | Interno y externo |
Estructuras del Sistema Endocrino
El sistema endocrino consiste en células, tejidos y órganos que secretan hormonas como función primaria o secundaria. La glándula endocrina es el actor principal en este sistema. La función principal de estas glándulas sin conductos es secretar sus hormonas directamente en el líquido circundante. El líquido intersticial y los vasos sanguíneos transportan entonces las hormonas por todo el cuerpo. El sistema endocrino incluye las glándulas pituitaria, tiroides, paratiroides, suprarrenales y pineales (Figura 1. Sistema Endocrino). Algunas de estas glándulas tienen funciones tanto endocrinas como no endocrinas. Por ejemplo, el páncreas contiene células que funcionan en la digestión así como células que secretan las hormonas insulina y glucagón, que regulan los niveles de glucosa en sangre. El hipotálamo, timo, corazón, riñones, estómago, intestino delgado, hígado, piel, ovarios femeninos y testículos masculinos son otros órganos que contienen células con función endocrina. Además, desde hace mucho tiempo se sabe que el tejido adiposo produce hormonas, y investigaciones recientes han revelado que incluso el tejido óseo tiene funciones endocrinas.

Las glándulas endocrinas sin conductos no deben confundirse con el sistema exocrino del cuerpo, cuyas glándulas liberan sus secreciones a través de conductos. Ejemplos de glándulas exocrinas incluyen las glándulas sebáceas y sudoríparas de la piel. Como se acaba de señalar, el páncreas también tiene una función exocrina: la mayoría de sus células secretan jugo pancreático a través de los conductos pancreáticos y accesorios hasta la luz del intestino delgado.
Otros tipos de señalización química
En la señalización endocrina, las hormonas secretadas en el líquido extracelular se difunden en la sangre o la linfa, y luego pueden viajar grandes distancias por todo el cuerpo. En contraste, la señalización autocrina se lleva a cabo dentro de la misma célula. Un autocrino (auto- = “self”) es una sustancia química que provoca una respuesta en la misma célula que la secretó. La interleucina-1, o IL-1, es una molécula de señalización que juega un papel importante en la respuesta inflamatoria. Las células que secretan IL-1 tienen receptores en su superficie celular que se unen a estas moléculas, dando como resultado una señalización autocrina.
La comunicación intercelular local es la provincia de lo paracrino, también llamado factor paracrino, que es una sustancia química que induce una respuesta en las células vecinas. Aunque los paracrinos pueden ingresar al torrente sanguíneo, su concentración es generalmente demasiado baja para provocar una respuesta de tejidos distantes. Un ejemplo familiar para las personas con asma es la histamina, una paracrina que es liberada por las células inmunes en el árbol bronquial. La histamina hace que las células musculares lisas de los bronquios se contraigan, estrechando las vías respiratorias. Otro ejemplo son los neurotransmisores del sistema nervioso, que actúan solo localmente dentro de la hendidura sináptica.
Endocrinólogo
Endocrinología es una especialidad en el campo de la medicina que se enfoca en el tratamiento de trastornos del sistema endocrino. Los endocrinólogos, médicos especializados en este campo, son expertos en el tratamiento de enfermedades asociadas con los sistemas hormonales, que van desde la enfermedad tiroidea hasta la diabetes mellitus. Los cirujanos endocrinos tratan la enfermedad endocrina mediante la extirpación, o resección, de la glándula endocrina afectada.
Los pacientes que son derivados a endocrinólogos pueden tener signos y síntomas o resultados de análisis de sangre que sugieren un funcionamiento excesivo o alterado de una glándula endocrina o células endocrinas. El endocrinólogo puede ordenar análisis de sangre adicionales para determinar si los niveles hormonales del paciente son anormales, o pueden estimular o suprimir la función de la glándula endocrina sospechosa y luego tomar sangre para su análisis. El tratamiento varía según el diagnóstico. Algunos trastornos endocrinos, como la diabetes tipo 2, pueden responder a cambios en el estilo de vida, como la pérdida de peso modesta, la adopción de una dieta saludable y la actividad física regular. Otros trastornos pueden requerir medicación, como reemplazo hormonal, y monitoreo de rutina por parte del endocrinólogo. Estos incluyen trastornos de la glándula pituitaria que pueden afectar el crecimiento y trastornos de la glándula tiroides que pueden resultar en una variedad de problemas metabólicos.
Algunos pacientes experimentan problemas de salud como consecuencia de la disminución normal de las hormonas que pueden acompañar al envejecimiento. Estos pacientes pueden consultar con un endocrinólogo para sopesar los riesgos y beneficios de la terapia de reemplazo hormonal destinada a aumentar sus niveles naturales de hormonas reproductivas.
Además de tratar a los pacientes, los endocrinólogos pueden estar involucrados en investigaciones para mejorar la comprensión de los trastornos del sistema endocrino y desarrollar nuevos tratamientos para estas enfermedades.
Revisión del Capítulo
El sistema endocrino consiste en células, tejidos y órganos que secretan hormonas críticas para la homeostasis. El cuerpo coordina sus funciones a través de dos grandes tipos de comunicación: neuronal y endocrina. La comunicación neuronal incluye señalización eléctrica y química entre neuronas y células diana. La comunicación endocrina implica la señalización química a través de la liberación de hormonas en el líquido extracelular. A partir de ahí, las hormonas se difunden en el torrente sanguíneo y pueden viajar a regiones distantes del cuerpo, donde provocan una respuesta en las células diana. Las glándulas endocrinas son glándulas sin conductos que secretan hormonas. Muchos órganos del cuerpo con otras funciones primarias, como el corazón, el estómago y los riñones, también tienen células secretoras de hormonas.
Hormonas
Al final de esta sección, podrás:
- Identificar las tres clases principales de hormonas sobre la base de la estructura química
- Comparar y contrastar receptores hormonales intracelulares y de membrana celular
- Describir las vías de señalización que involucran AMPc e IP3
- Identificar varios factores que influyen en la respuesta de una célula diana
- Discutir el papel de los bucles de retroalimentación y los estímulos humorales, hormonales y neuronales en el control hormonal
Si bien una hormona dada puede viajar por todo el cuerpo en el torrente sanguíneo, afectará la actividad solo de sus células diana; es decir, células con receptores para esa hormona en particular. Una vez que la hormona se une al receptor, se inicia una cadena de eventos que conduce a la respuesta de la célula diana. Las hormonas juegan un papel crítico en la regulación de los procesos fisiológicos debido a las respuestas de las células diana que regulan. Estas respuestas contribuyen a la reproducción humana, el crecimiento y desarrollo de los tejidos corporales, el metabolismo, el equilibrio de líquidos y electrolitos, el sueño y muchas otras funciones corporales. Las principales hormonas del cuerpo humano y sus efectos se identifican en la Tabla (Glándulas Endocrinas y sus Hormonas Mayores).
| Glándulas endocrinas y sus principales hormonas | |||
|---|---|---|---|
| Glándula endocrina | Hormonas asociadas | Clase química | Efecto |
| Hipófisis (anterior) | Hormona del crecimiento (GH) | Proteína | Promueve el crecimiento de los tejidos corporales |
| Hipófisis (anterior) | Prolactina (PRL) | Péptido | Promueve la producción de leche |
| Hipófisis (anterior) | Hormona estimulante de la tiroides (TSH) | Glicoproteína | Estimula la liberación de hormona tiroides |
| Hipófisis (anterior) | Hormona adrenocorticotrópica (ACTH) | Péptido | Estimula la liberación hormonal por corteza suprarrenal |
| Hipófisis (anterior) | Hormona foliculoestimulante (FSH) | Glicoproteína | Estimula la producción de gametos |
| Hipófisis (anterior) | Hormona luteinizante (LH) | Glicoproteína | Estimula la producción de andrógenos por gónadas |
| Hipófisis (posterior) | Hormona antidiurética (ADH) | Péptido | Estimula la reabsorción de agua por los riñones |
| Hipófisis (posterior) | Oxitocina | Péptido | Estimula las contracciones uterinas durante el parto |
| Tiroides | Tiroxina (T 4), triyodotironina (T 3) | Amina | Estimula la tasa metabólica basal |
| Tiroides | Calcitonina | Péptido | Reduce los niveles de Ca 2+ en sangre |
| Paratiroides | Hormona paratiroidea (PTH) | Péptido | Aumenta los niveles de Ca 2+ en sangre |
| Corteza suprarrenal | Aldosterona | Esteroide | Aumenta los niveles de Na + en sangre |
| Corteza suprarrenal | Cortisol, corticosterona, cortisona | Esteroide | Aumentar los niveles de glucosa en sangre |
| Suprarrenal (médula) | Epinefrina, norepinefrina | Amina | Estimular la respuesta de la huida o |
| Pineal | Melatonina | Amina | Regula los ciclos de sueño |
| Páncreas | Insulina | Proteína | Reduce los niveles de glucosa en sangre |
| Páncreas | Glucagón | Proteína | Aumenta los niveles de glucosa en sangre |
| Testículos | Testosterona | Esteroide | Estimula el desarrollo de características sexuales secundarias masculinas y la producción de esperma |
| Ovarios | Estrógenos y progesterona | Esteroide | Estimular el desarrollo de las características del sexo secundario femenino y preparar el cuerpo para el parto |
Tipos de Hormonas
Las hormonas del cuerpo humano se pueden dividir en dos grupos principales sobre la base de su estructura química. Las hormonas derivadas de aminoácidos incluyen aminas, péptidos y proteínas. Los derivados de lípidos incluyen esteroides (Figura 1. Estructura de Amina, Péptido, Proteína y Hormona Esteroide). Estos grupos químicos afectan la distribución de una hormona, el tipo de receptores a los que se une y otros aspectos de su función.

Hormonas de amina
Las hormonas derivadas de la modificación de aminoácidos se denominan hormonas amínicas. Típicamente, la estructura original del aminoácido se modifica de tal manera que se elimina un grupo -COOH, o carboxilo, mientras que el grupo -NH 3 +, o amina, permanece.
Las hormonas amínicas se sintetizan a partir de los aminoácidos triptófano o tirosina. Un ejemplo de una hormona derivada del triptófano es la melatonina, que es secretada por la glándula pineal y ayuda a regular el ritmo circadiano. Los derivados de tirosina incluyen las hormonas tiroideas reguladoras del metabolismo, así como las catecolaminas, como la epinefrina, la norepinefrina y la dopamina. La epinefrina y la norepinefrina son secretadas por la médula suprarrenal y juegan un papel en la respuesta de lucha o huida, mientras que la dopamina es secretada por el hipotálamo e inhibe la liberación de ciertas hormonas hipofisarias anteriores.
Hormonas de péptidos y proteínas
Mientras que las hormonas amínicas se derivan de un solo aminoácido, las hormonas peptídicas y proteicas consisten en múltiples aminoácidos que se unen para formar una cadena de aminoácidos. Las hormonas peptídicas consisten en cadenas cortas de aminoácidos, mientras que las hormonas proteicas son polipéptidos más largos. Ambos tipos se sintetizan como otras proteínas del cuerpo: el ADN se transcribe en ARNm, que se traduce en una cadena de aminoácidos.
Ejemplos de hormonas peptídicas incluyen la hormona antidiurética (ADH), una hormona pituitaria importante en el equilibrio de líquidos, y el péptido atrio-natriurético, que es producido por el corazón y ayuda a disminuir la presión arterial. Algunos ejemplos de hormonas proteicas incluyen la hormona del crecimiento, que es producida por la glándula pituitaria, y la hormona folículo estimulante (FSH), que tiene un grupo de carbohidratos unido y por lo tanto se clasifica como una glicoproteína. La FSH ayuda a estimular la maduración de los óvulos en los ovarios y los espermatozoides en los testículos.
Hormonas esteroides
Las hormonas primarias derivadas de los lípidos son los esteroides. Las hormonas esteroides se derivan del colesterol lipídico. Por ejemplo, las hormonas reproductivas testosterona y los estrógenos, que son producidos por las gónadas (testículos y ovarios), son hormonas esteroides. Las glándulas suprarrenales producen la hormona esteroide aldosterona, que interviene en la osmorregulación, y el cortisol, que juega un papel en el metabolismo.
Al igual que el colesterol, las hormonas esteroides no son solubles en agua (son hidrofóbicas). Debido a que la sangre es a base de agua, las hormonas derivadas de lípidos deben viajar a su célula diana unida a una proteína de transporte. Esta estructura más compleja extiende la vida media de las hormonas esteroides mucho más tiempo que la de las hormonas derivadas de aminoácidos. La vida media de una hormona es el tiempo requerido para que se degrada la mitad de la concentración de la hormona. Por ejemplo, la hormona cortisol derivada de lípidos tiene una vida media de aproximadamente 60 a 90 minutos. Por el contrario, la hormona epinefrina derivada de aminoácidos tiene una vida media de aproximadamente un minuto.
Vías de acción hormonal
El mensaje que envía una hormona es recibido por un receptor hormonal, una proteína ubicada ya sea dentro de la célula o dentro de la membrana celular. El receptor procesará el mensaje iniciando otros eventos de señalización o mecanismos celulares que dan como resultado la respuesta de la célula diana. Los receptores hormonales reconocen moléculas con formas y grupos laterales específicos, y responden únicamente a aquellas hormonas que son reconocidas. El mismo tipo de receptor puede estar localizado en células en diferentes tejidos corporales, y desencadenar respuestas algo diferentes. Así, la respuesta desencadenada por una hormona depende no sólo de la hormona, sino también de la célula diana.
Una vez que la célula diana recibe la señal hormonal, puede responder de diversas maneras. La respuesta puede incluir la estimulación de la síntesis de proteínas, activación o desactivación de enzimas, alteración en la permeabilidad de la membrana celular, tasas alteradas de mitosis y crecimiento celular, y estimulación de la secreción de productos. Además, una sola hormona puede ser capaz de inducir diferentes respuestas en una célula dada.
Vías que involucran receptores hormonales intracelulares
Los receptores hormonales intracelulares se localizan dentro de la célula. Las hormonas que se unen a este tipo de receptores deben poder atravesar la membrana celular. Las hormonas esteroides se derivan del colesterol y por lo tanto pueden difundirse fácilmente a través de la bicapa lipídica de la membrana celular para alcanzar el receptor intracelular (Figura 2. Fijación de Hormonas Lipido-Solubles) Las hormonas tiroideas, que contienen anillos de benceno tachonados de yodo, también son solubles en lípidos y pueden ingresar a la célula.
La ubicación de la unión a la hormona esteroide y tiroidea difiere ligeramente: una hormona esteroide puede unirse a su receptor dentro del citosol o dentro del núcleo. En cualquier caso, esta unión genera un complejo hormona-receptor que se mueve hacia la cromatina en el núcleo celular y se une a un segmento particular del ADN de la célula. En contraste, las hormonas tiroideas se unen a receptores ya unidos al ADN. Tanto para las hormonas esteroides como tiroideas, la unión del complejo hormona-receptor con ADN desencadena la transcripción de un gen diana al ARNm, que se mueve al citosol y dirige la síntesis de proteínas por los ribosomas.

Vías que involucran receptores hormonales de membrana celular
Las hormonas hidrofílicas o solubles en agua son incapaces de difundirse a través de la bicapa lipídica de la membrana celular y, por lo tanto, deben transmitir su mensaje a un receptor ubicado en la superficie de la célula. Excepto las hormonas tiroideas, que son solubles en lípidos, todas las hormonas derivadas de aminoácidos se unen a receptores de membrana celular que se encuentran, al menos en parte, en la superficie extracelular de la membrana celular. Por lo tanto, no afectan directamente la transcripción de genes diana, sino que inician una cascada de señalización que es llevada a cabo por una molécula llamada segundo mensajero. En este caso, la hormona se llama primer mensajero.
El segundo mensajero utilizado por la mayoría de las hormonas es el monofosfato de adenosina cíclico (AMPc). En el sistema de segundo mensajero AMPc, una hormona soluble en agua se une a su receptor en la membrana celular (Paso 1 en la Figura 3. (Fijación de Hormonas Hidrosolubles)). Este receptor está asociado con un componente intracelular llamado proteína G, y la unión de la hormona activa el componente de proteína G (Paso 2). La proteína G activada a su vez activa una enzima llamada adenilil ciclasa, también conocida como adenilato ciclasa (Paso 3), que convierte el trifosfato de adenosina (ATP) en AMPc (Paso 4). Como segundo mensajero, el AMPc activa un tipo de enzima llamada proteína quinasa que está presente en el citosol (Paso 5). Las proteínas quinasas activadas inician una cascada de fosforilación, en la que múltiples proteínas quinasas fosforilan (agregan un grupo fosfato a) numerosas y diversas proteínas celulares, incluyendo otras enzimas (Paso 6).

La fosforilación de proteínas celulares puede desencadenar una amplia variedad de efectos, desde el metabolismo de los nutrientes hasta la síntesis de diferentes hormonas y otros productos. Los efectos varían según el tipo de célula diana, las proteínas G y quinasas involucradas, y la fosforilación de proteínas. Ejemplos de hormonas que usan AMPc como segundo mensajero incluyen la calcitonina, que es importante para la construcción ósea y la regulación de los niveles de calcio en sangre; el glucagón, que juega un papel en los niveles de glucosa en sangre; y la hormona estimulante de la tiroides, que provoca la liberación de T 3 y T 4 de la glándula tiroides.
En general, la cascada de fosforilación aumenta significativamente la eficiencia, velocidad y especificidad de la respuesta hormonal, ya que miles de eventos de señalización pueden iniciarse simultáneamente en respuesta a una concentración muy baja de hormona en el torrente sanguíneo. Sin embargo, la duración de la señal hormonal es corta, ya que el AMPc es rápidamente desactivado por la enzima fosfodiesterasa (PDE), que se localiza en el citosol. La acción de la PDE ayuda a asegurar que la respuesta de una célula diana cesa rápidamente a menos que lleguen nuevas hormonas a la membrana celular.
Es importante destacar que también hay proteínas G que disminuyen los niveles de AMPc en la célula en respuesta a la unión hormonal. Por ejemplo, cuando la hormona inhibidora de la hormona del crecimiento (GHIH), también conocida como somatostatina, se une a sus receptores en la glándula pituitaria, el nivel de AMPc disminuye, inhibiendo así la secreción de la hormona del crecimiento humana.
No todas las hormonas solubles en agua inician el sistema de segundo mensajero AMPc. Un sistema alternativo común utiliza iones de calcio como segundo mensajero. En este sistema, las proteínas G activan la enzima fosfolipasa C (PLC), la cual funciona de manera similar a la adenilil ciclasa. Una vez activado, el PLC escinde un fosfolípido unido a la membrana en dos moléculas: diacilglicerol (DAG) e inositol trifosfato (IP 3). Al igual que el AMPc, DAG activa proteínas quinasas que inician una cascada de fosforilación. Al mismo tiempo, IP 3 provoca la liberación de iones de calcio de los sitios de almacenamiento dentro del citosol, como desde el interior del retículo endoplásmico liso. Los iones calcio actúan entonces como segundos mensajeros de dos maneras: pueden influir directamente en las actividades enzimáticas y otras actividades celulares, o pueden unirse a proteínas de unión al calcio, la más común de las cuales es la calmodulina. Al unirse al calcio, la calmodulina es capaz de modular la proteína quinasa dentro de la célula. Ejemplos de hormonas que utilizan iones de calcio como sistema de segundo mensajero incluyen la angiotensina II, que ayuda a regular la presión arterial a través de la vasoconstricción, y la hormona liberadora de hormona de crecimiento (GHRH), que hace que la glándula pituitaria libere hormonas de crecimiento.
Factores que afectan la respuesta de las células diana
Recordarás que las células diana deben tener receptores específicos de una hormona dada si esa hormona va a desencadenar una respuesta. Pero varios otros factores influyen en la respuesta de las células diana. Por ejemplo, la presencia de un nivel significativo de una hormona que circula en el torrente sanguíneo puede hacer que sus células diana disminuyan su número de receptores para esa hormona. Este proceso se llama regulación a la baja, y permite que las células se vuelvan menos reactivas a los niveles excesivos de hormonas. Cuando el nivel de una hormona se reduce crónicamente, las células diana participan en la regulación positiva para aumentar su número de receptores. Este proceso permite que las células sean más sensibles a la hormona que está presente. Las células también pueden alterar la sensibilidad de los propios receptores a diversas hormonas.
Dos o más hormonas pueden interactuar para afectar la respuesta de las células de diversas maneras. Los tres tipos más comunes de interacción son los siguientes:
- El efecto permisivo, en el que la presencia de una hormona permite que otra hormona actúe. Por ejemplo, las hormonas tiroideas tienen complejas relaciones permisivas con ciertas hormonas reproductivas. Por lo tanto, una deficiencia dietética de yodo, un componente de las hormonas tiroideas, puede afectar el desarrollo y funcionamiento del sistema reproductivo.
- El efecto sinérgico, en el que dos hormonas con efectos similares producen una respuesta amplificada. En algunos casos, se requieren dos hormonas para una respuesta adecuada. Por ejemplo, se requieren dos hormonas reproductivas diferentes —FSH de la glándula pituitaria y estrógenos de los ovarios— para la maduración de los óvulos femeninos (óvulos).
- El efecto antagónico, en el que dos hormonas tienen efectos opuestos. Un ejemplo familiar es el efecto de dos hormonas pancreáticas, la insulina y el glucagón. La insulina aumenta el almacenamiento de glucosa en el hígado como glucógeno, disminuyendo la glucosa en sangre, mientras que el glucagón estimula la descomposición de las reservas de glucógeno, aumentando la glucosa en sangre.
Regulación de la secreción hormonal
Para prevenir niveles hormonales anormales y un estado potencial de enfermedad, los niveles hormonales deben controlarse estrechamente. El cuerpo mantiene este control equilibrando la producción hormonal y la degradación. Los bucles de retroalimentación gobiernan el inicio y mantenimiento de la mayor parte de la secreción hormonal en respuesta a diversos estímulos.
Papel de los bucles de retroalimentación
La contribución de los bucles de retroalimentación a la homeostasis solo se revisará brevemente aquí. Los bucles de retroalimentación positiva se caracterizan por la liberación de hormona adicional en respuesta a una liberación hormonal original. La liberación de oxitocina durante el parto es un ciclo de retroalimentación positiva. La liberación inicial de oxitocina comienza a indicar que los músculos uterinos se contraigan, lo que empuja al feto hacia el cuello uterino, haciendo que se estire. Esto, a su vez, indica a la glándula pituitaria que libere más oxitocina, provocando que las contracciones del parto se intensifiquen. La liberación de oxitocina disminuye después del nacimiento del niño.
El método más común de regulación hormonal es el bucle de retroalimentación negativa. La retroalimentación negativa se caracteriza por la inhibición de la secreción posterior de una hormona en respuesta a niveles adecuados de esa hormona. Esto permite que los niveles sanguíneos de la hormona se regulen dentro de un rango estrecho. Un ejemplo de un bucle de retroalimentación negativa es la liberación de hormonas glucocorticoides de las glándulas suprarrenales, según lo dirigido por el hipotálamo y la glándula pituitaria. A medida que aumentan las concentraciones de glucocorticoides en la sangre, el hipotálamo y la glándula pituitaria reducen su señalización a las glándulas suprarrenales para evitar la secreción adicional de glucocorticoides (Figura 4. Bucle de retroalimentación negativa).

Papel de los estímulos de las glándulas endocrinas
Los reflejos desencadenados por estímulos químicos y neuronales controlan la actividad endocrina. Estos reflejos pueden ser simples, involucrando solo una respuesta hormonal, o pueden ser más complejos e involucrar a muchas hormonas, como es el caso del control hipotalámico de varias hormonas controladas por la hipófisis anterior.
Los estímulos humorales son cambios en los niveles sanguíneos de sustancias químicas no hormonales, como nutrientes o iones, que provocan la liberación o inhibición de una hormona para, a su vez, mantener la homeostasis. Por ejemplo, los osmorreceptores en el hipotálamo detectan cambios en la osmolaridad sanguínea (la concentración de solutos en el plasma sanguíneo). Si la osmolaridad de la sangre es demasiado alta, lo que significa que la sangre no está suficientemente diluida, los osmorreceptores señalan al hipotálamo que libere ADH. La hormona hace que los riñones reabsorban más agua y reduzcan el volumen de orina producida. Esta reabsorción provoca una reducción de la osmolaridad de la sangre, diluyendo la sangre al nivel apropiado. La regulación de la glucosa en sangre es otro ejemplo. Los niveles altos de glucosa en sangre provocan la liberación de insulina del páncreas, lo que aumenta la captación de glucosa por las células y el almacenamiento hepático de glucosa como glucógeno.
Una glándula endocrina también puede secretar una hormona en respuesta a la presencia de otra hormona producida por una glándula endocrina diferente. Dichos estímulos hormonales suelen involucrar al hipotálamo, que produce hormonas liberadoras e inhibidoras que controlan la secreción de una variedad de hormonas pituitarias.
Además de estas señales químicas, también se pueden liberar hormonas en respuesta a estímulos neuronales. Un ejemplo común de estímulos neuronales es la activación de la respuesta de lucha o huida por parte del sistema nervioso simpático. Cuando un individuo percibe peligro, las neuronas simpáticas señalan a las glándulas suprarrenales que secretan norepinefrina y epinefrina. Las dos hormonas dilatan los vasos sanguíneos, aumentan la frecuencia cardíaca y respiratoria, y suprimen los sistemas digestivo e inmunológico. Estas respuestas potencian el transporte de oxígeno del cuerpo hacia el cerebro y los músculos, mejorando así la capacidad del cuerpo para luchar o huir.
Bisfenol A y alteración endocrina
Es posible que hayas escuchado reportajes noticiosos sobre los efectos de un químico llamado bisfenol A (BPA) en diversos tipos de envases de alimentos. El BPA se utiliza en la fabricación de plásticos duros y resinas epoxi. Los artículos comunes relacionados con los alimentos que pueden contener BPA incluyen el revestimiento de latas de aluminio, recipientes de plástico para almacenar alimentos, vasos para beber, así como biberones y vasos para “sorber”. Otros usos del BPA incluyen equipos médicos, empastes dentales y revestimiento de tuberías de agua.
La investigación sugiere que el BPA es un disruptor endocrino, lo que significa que interfiere negativamente con el sistema endocrino, particularmente durante el período de desarrollo prenatal y postnatal. En particular, el BPA imita los efectos hormonales de los estrógenos y tiene el efecto contrario: el de los andrógenos. La Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) señala en su declaración sobre la seguridad del BPA que aunque los estudios tradicionales de toxicología han apoyado la seguridad de niveles bajos de exposición al BPA, estudios recientes que utilizan enfoques novedosos para probar efectos sutiles han llevado a cierta preocupación sobre los efectos potenciales de BPA en el cerebro, el comportamiento y la glándula prostática en fetos, lactantes y niños pequeños. Actualmente, la FDA está facilitando la disminución del uso de BPA en materiales relacionados con los alimentos. Muchas empresas estadounidenses han retirado voluntariamente el BPA de los biberones, las tazas “sippy” y los forros de las latas de fórmula infantil, y la mayoría de las botellas de agua reutilizables de plástico que se venden hoy en día cuentan con que están “libres de BPA”. En contraste, tanto Canadá como la Unión Europea han prohibido por completo el uso del BPA en productos para bebés.
Los posibles efectos nocivos del BPA se han estudiado tanto en modelos animales como en humanos e incluyen una gran variedad de efectos sobre la salud, como retraso en el desarrollo y enfermedad. Por ejemplo, la exposición prenatal al BPA durante el primer trimestre del embarazo humano puede estar asociada con sibilancias y comportamiento agresivo durante la infancia. Los adultos expuestos a altos niveles de BPA pueden experimentar alteración de la señalización tiroidea y disfunción sexual masculina. Se ha observado que la exposición al BPA durante el período prenatal o posnatal de desarrollo en modelos animales causa retrasos neurológicos, cambios en la estructura y función cerebral, disfunción sexual, asma y aumento del riesgo de múltiples cánceres. Estudios in vitro también han demostrado que la exposición al BPA causa cambios moleculares que inician el desarrollo de cánceres de mama, próstata y cerebro. Aunque estos estudios han implicado al BPA en numerosos efectos nocivos para la salud, algunos expertos advierten que algunos de estos estudios pueden ser defectuosos y que es necesario realizar más investigaciones. Mientras tanto, la FDA recomienda que los consumidores tomen precauciones para limitar su exposición al BPA. Además de comprar alimentos en envases libres de BPA, los consumidores deben evitar llevar o almacenar alimentos o líquidos en botellas con el código de reciclaje 3 o 7. Los alimentos y líquidos no deben calentarse en el microondas en ninguna forma de plástico: use papel, vidrio o cerámica en su lugar.
Revisión del Capítulo
Las hormonas se derivan de aminoácidos o lípidos. Las hormonas amínicas se originan a partir de los aminoácidos triptófano o tirosina. Las hormonas de aminoácidos más grandes incluyen péptidos y hormonas proteicas. Las hormonas esteroides se derivan del colesterol.
Las hormonas esteroides y la hormona tiroidea son solubles en lípidos. Todas las demás hormonas derivadas de aminoácidos son solubles en agua. Las hormonas hidrófobas son capaces de difundirse a través de la membrana e interactuar con un receptor intracelular. En contraste, las hormonas hidrofílicas deben interactuar con los receptores de la membrana celular. Estos suelen estar asociados con una proteína G, que se activa cuando la hormona se une al receptor. Esto inicia una cascada de señalización que involucra a un segundo mensajero, como el monofosfato de adenosina cíclico (AMPc). Los sistemas de segundo mensajero amplifican enormemente la señal hormonal, creando una respuesta más amplia, más eficiente y más rápida.
Las hormonas se liberan tras la estimulación que es de origen químico o neural. La regulación de la liberación de hormonas se logra principalmente a través de retroalimentación negativa. Diversos estímulos pueden provocar la liberación de hormonas, pero hay tres tipos principales. Los estímulos humorales son cambios en los niveles de iones o nutrientes en la sangre. Los estímulos hormonales son cambios en los niveles hormonales que inician o inhiben la secreción de otra hormona. Finalmente, un estímulo neural ocurre cuando un impulso nervioso provoca la secreción o inhibición de una hormona.
La glándula pituitaria y el hipotálamo
Al final de esta sección, podrás:
- Explicar las interrelaciones de la anatomía y funciones del hipotálamo y los lóbulos posterior y anterior de la glándula pituitaria
- Identificar las dos hormonas liberadas de la hipófisis posterior, sus células diana y sus acciones principales
- Identificar las seis hormonas producidas por el lóbulo anterior de la glándula pituitaria, sus células diana, sus acciones principales y su regulación por el hipotálamo
El complejo hipotálamo-hipófisis puede considerarse como el “centro de mando” del sistema endocrino. Este complejo secreta varias hormonas que producen directamente respuestas en los tejidos diana, así como hormonas que regulan la síntesis y secreción de hormonas de otras glándulas. Además, el complejo hipotálamo-hipófisis coordina los mensajes de los sistemas endocrino y nervioso. En muchos casos, un estímulo recibido por el sistema nervioso debe pasar por el complejo hipotálamo-hipofisario para traducirse en hormonas que puedan iniciar una respuesta.
El hipotálamo es una estructura del diencéfalo del cerebro localizado anterior e inferior al tálamo (Figura 1. Complejo Hipotalámico-Hipofisario). Tiene funciones tanto neuronales como endocrinas, produciendo y secretando muchas hormonas. Además, el hipotálamo está anatómica y funcionalmente relacionado con la glándula pituitaria (o hipófisis), órgano del tamaño de un frijol suspendido de ella por un tallo llamado infundíbulo (o tallo hipofisario). La glándula pituitaria está acunada dentro de la sellaturcica del hueso esfenoidal del cráneo. Consta de dos lóbulos que surgen de distintas partes del tejido embrionario: la hipófisis posterior (neurohipófisis) es tejido neural, mientras que la pituitaria anterior (también conocida como adenohipófisis) es tejido glandular que se desarrolla a partir del tracto digestivo primitivo. Las hormonas secretadas por la hipófisis posterior y anterior, y la zona intermedia entre los lóbulos se resumen en la Tabla (Hormonas Pituitarias).

| Hormonas hipofisarias | |||
|---|---|---|---|
| Lóbulo hipofisario | Hormonas asociadas | Clase química | Efecto |
| Anterior | Hormona del crecimiento (GH) | Proteína | Promueve el crecimiento de los tejidos corporales |
| Anterior | Prolactina (PRL) | Péptido | Promueve la producción de leche de las glándulas mamarias |
| Anterior | Hormona estimulante de la tiroides (TSH) | Glicoproteína | Estimula la liberación de hormona tiroidea del tiroides |
| Anterior | Hormona adrenocorticotrópica (ACTH) | Péptido | Estimula la liberación hormonal por corteza suprarrenal |
| Anterior | Hormona foliculoestimulante (FSH) | Glicoproteína | Estimula la producción de gametos en gónadas |
| Anterior | Hormona luteinizante (LH) | Glicoproteína | Estimula la producción de andrógenos por gónadas |
| Posterior | Hormona antidiurética (ADH) | Péptido | Estimula la reabsorción de agua por los riñones |
| Posterior | Oxitocina | Péptido | Estimula las contracciones uterinas durante el parto |
| Zona intermedia | Hormona estimulante de melanocitos | Péptido | Estimula la formación de melanina en melanocitos |
Hipófisis Posterior
La hipófisis posterior es en realidad una extensión de las neuronas de los núcleos paraventricular y supraóptico del hipotálamo. Los cuerpos celulares de estas regiones descansan en el hipotálamo, pero sus axones descienden como el tracto hipotálamo-hipófisario dentro del infundíbulo, y terminan en terminales axónicas que comprenden la hipófisis posterior (Figura 2. Pituitaria Posterior).

La glándula pituitaria posterior no produce hormonas, sino que almacena y secreta hormonas producidas por el hipotálamo. Los núcleos paraventriculares producen la hormona oxitocina, mientras que los núcleos supraópticos producen ADH. Estas hormonas viajan a lo largo de los axones hacia sitios de almacenamiento en las terminales axónicas de la hipófisis posterior. En respuesta a las señales de las mismas neuronas hipotalámicas, las hormonas se liberan desde los terminales axónicos hacia el torrente sanguíneo.
Oxitocina
Cuando se completa el desarrollo fetal, la hormona derivada del péptido oxitocina (tocia- = “parto”) estimula las contracciones uterinas y la dilatación del cuello uterino. Durante la mayor parte del embarazo, los receptores de la hormona oxitocina no se expresan en niveles altos en el útero. Hacia el final del embarazo, aumenta la síntesis de receptores de oxitocina en el útero, y las células del músculo liso del útero se vuelven más sensibles a sus efectos. La oxitocina se libera continuamente durante el parto a través de un mecanismo de retroalimentación positiva. Como se señaló anteriormente, la oxitocina provoca contracciones uterinas que empujan la cabeza fetal hacia el cuello uterino. En respuesta, el estiramiento cervical estimula la oxitocina adicional para ser sintetizada por el hipotálamo y liberada de la hipófisis. Esto aumenta la intensidad y efectividad de las contracciones uterinas y provoca dilatación adicional del cuello uterino. El ciclo de retroalimentación continúa hasta el nacimiento.
Aunque los niveles altos de oxitocina en la sangre de la madre comienzan a disminuir inmediatamente después del nacimiento, la oxitocina continúa desempeñando un papel en la salud materna y neonatal. Primero, la oxitocina es necesaria para el reflejo de eyección de leche (comúnmente conocido como “decepción”) en mujeres que amamantan. A medida que el recién nacido comienza a mamar, los receptores sensoriales en los pezones transmiten señales al hipotálamo. En respuesta, la oxitocina es secretada y liberada al torrente sanguíneo. En cuestión de segundos, las células en los conductos de la leche materna se contraen, expulsando leche a la boca del lactante. En segundo lugar, tanto en machos como en hembras, se cree que la oxitocina contribuye al vínculo padre-recién nacido, conocido como apego. También se piensa que la oxitocina está involucrada en los sentimientos de amor y cercanía, así como en la respuesta sexual.
Hormona antidiurética (ADH)
La concentración de soluto en la sangre, u osmolaridad sanguínea, puede cambiar en respuesta al consumo de ciertos alimentos y líquidos, así como en respuesta a enfermedades, lesiones, medicamentos u otros factores. La osmolaridad sanguínea es monitoreada constantemente por osmorreceptores, células especializadas dentro del hipotálamo que son particularmente sensibles a la concentración de iones de sodio y otros solutos.
En respuesta a la alta osmolaridad sanguínea, que puede ocurrir durante la deshidratación o después de una comida muy salada, los osmorreceptores señalan a la hipófisis posterior que libere la hormona antidiurética (ADH). Las células diana de la ADH se localizan en las células tubulares de los riñones. Su efecto es aumentar la permeabilidad epitelial al agua, permitiendo una mayor reabsorción de agua. Cuanta más agua reabsorbida del filtrado, mayor es la cantidad de agua que se devuelve a la sangre y menor es la que se excreta en la orina. Una mayor concentración de agua resulta en una concentración reducida de solutos. La ADH también se conoce como vasopresina porque, en concentraciones muy altas, provoca constricción de los vasos sanguíneos, lo que aumenta la presión arterial al aumentar la resistencia periférica. La liberación de ADH es controlada por un bucle de retroalimentación negativa. A medida que disminuye la osmolaridad sanguínea, los osmorreceptores hipotalámicos perciben el cambio y provocan una disminución correspondiente en la secreción de ADH. Como resultado, se reabsorbe menos agua del filtrado de orina.
Curiosamente, las drogas pueden afectar la secreción de ADH. Por ejemplo, el consumo de alcohol inhibe la liberación de ADH, resultando en una mayor producción de orina que eventualmente puede conducir a deshidratación y resaca. Una enfermedad llamada diabetes insípida se caracteriza por una subproducción crónica de ADH que causa deshidratación crónica. Debido a que se produce y secreta poca ADH, no se reabsorbe suficiente agua por los riñones. Aunque los pacientes sienten sed y aumentan su consumo de líquidos, esto no disminuye efectivamente la concentración de soluto en su sangre porque los niveles de ADH no son lo suficientemente altos como para desencadenar la reabsorción de agua en los riñones. Los desequilibrios electrolíticos pueden ocurrir en casos severos de diabetes insípida.
Hipófisis Anterior
La hipófisis anterior se origina en el tracto digestivo en el embrión y migra hacia el cerebro durante el desarrollo fetal. Hay tres regiones: la pars distalis es la más anterior, la pars intermedia es adyacente a la pituitaria posterior y la pars tuberalis es un “tubo” delgado que envuelve el infundíbulo.
Recordemos que la hipófisis posterior no sintetiza hormonas, sino que simplemente las almacena. En contraste, la hipófisis anterior sí fabrica hormonas. Sin embargo, la secreción de hormonas de la hipófisis anterior está regulada por dos clases de hormonas. Estas hormonas, secretadas por el hipotálamo, son las hormonas liberadoras que estimulan la secreción de hormonas de la hipófisis anterior y las hormonas inhibidoras que inhiben la secreción.
Las hormonas hipotalámicas son secretadas por las neuronas, pero ingresan a la hipófisis anterior a través de los vasos sanguíneos (Figura 3. Hipófisis Anterior). Dentro del infundíbulo se encuentra un puente de capilares que conecta el hipotálamo con la hipófisis anterior. Esta red, llamada sistema portal hipofisario, permite que las hormonas hipotalámicas sean transportadas a la hipófisis anterior sin ingresar primero a la circulación sistémica. El sistema se origina en la arteria hipofisaria superior, que se ramifica de las arterias carótidas y transporta sangre al hipotálamo. Las ramas de la arteria hipofisaria superior forman el sistema portal hipofisario (ver Figura 3. Hipófisis Anterior). Las hormonas hipotalámicas liberadoras e inhibidoras viajan a través de un plexo capilar primario hasta las venas porta, las cuales las transportan a la hipófisis anterior. Las hormonas producidas por la hipófisis anterior (en respuesta a la liberación de hormonas) ingresan a un plexo capilar secundario, y de ahí drenan a la circulación.

La hipófisis anterior produce siete hormonas. Estas son la hormona del crecimiento (GH), la hormona estimulante de la tiroides (TSH), la hormona adrenocorticotrópica (ACTH), la hormona folículo estimulante (FSH), la hormona luteinizante (LH), la beta endorfina y la prolactina. De las hormonas de la hipófisis anterior, TSH, ACTH, FSH y LH se denominan colectivamente hormonas trópicas (tropo- = “giro”) porque encienden o apagan la función de otras glándulas endocrinas.
Hormona del crecimiento
El sistema endocrino regula el crecimiento del cuerpo humano, la síntesis de proteínas y la replicación celular. Una hormona importante involucrada en este proceso es la hormona del crecimiento (GH), también llamada somatotropina, una hormona proteica producida y secretada por la glándula pituitaria anterior. Su función principal es anabólica; promueve la síntesis de proteínas y la construcción de tejidos a través de mecanismos directos e indirectos (Figura 4. Regulación Hormonal del Crecimiento). Los niveles de GH están controlados por la liberación de GHRH y GHIH (también conocida como somatostatina) del hipotálamo.

Un efecto ahorrador de glucosa ocurre cuando la GH estimula la lipólisis, o la descomposición del tejido adiposo, liberando ácidos grasos en la sangre. Como resultado, muchos tejidos cambian de la glucosa a los ácidos grasos como su principal fuente de energía, lo que significa que se absorbe menos glucosa del torrente sanguíneo.
La GH también inicia el efecto diabetogénico en el que la GH estimula al hígado para descomponer el glucógeno en glucosa, que luego se deposita en la sangre. El nombre “diabetogénico” se deriva de la similitud en los niveles elevados de glucosa en sangre observada entre individuos con diabetes mellitus no tratada y individuos que experimentan exceso de GH. Los niveles de glucosa en sangre aumentan como resultado de una combinación de efectos ahorradores de glucosa y diabetogénicos.
La GH media indirectamente el crecimiento y la síntesis de proteínas al desencadenar el hígado y otros tejidos para producir un grupo de proteínas llamadas factores de crecimiento similares a la insulina (IGF). Estas proteínas potencian la proliferación celular e inhiben la apoptosis, o la muerte celular programada. Los IGF estimulan a las células para aumentar su captación de aminoácidos de la sangre para la síntesis de proteínas. Las células del músculo esquelético y del cartílago son particularmente sensibles a la estimulación de los IGF.
La disfunción del control del crecimiento del sistema endocrino puede dar lugar a varios trastornos. Por ejemplo, el gigantismo es un trastorno en niños que es causado por la secreción de cantidades anormalmente grandes de GH, resultando en un crecimiento excesivo. Una condición similar en adultos es la acromegalia, un trastorno que da como resultado el crecimiento de huesos en la cara, manos y pies en respuesta a niveles excesivos de GH en individuos que han dejado de crecer. Los niveles anormalmente bajos de GH en los niños pueden causar deterioro del crecimiento, un trastorno llamado enanismo hipofisario (también conocido como deficiencia de la hormona del crecimiento).
Hormona estimulante de la tiroides
La actividad de la glándula tiroides está regulada por la hormona estimulante de la tiroides (TSH), también llamada tirotropina. La TSH se libera de la hipófisis anterior en respuesta a la hormona liberadora de tirotropina (TRH) del hipotálamo. Como se discutió en breve, desencadena la secreción de hormonas tiroideas por parte de la glándula tiroides. En un ciclo clásico de retroalimentación negativa, los niveles elevados de hormonas tiroideas en el torrente sanguíneo desencadenan una caída en la producción de TRH y posteriormente TSH.
Hormona adrenocorticotrópica
La hormona adrenocorticotrópica (ACTH), también llamada corticotropina, estimula la corteza suprarrenal (la “corteza” más superficial de las glándulas suprarrenales) para secretar hormonas corticosteroides como el cortisol. La ACTH proviene de una molécula precursora conocida como pro-opiomelanotropina (POMC) que produce varias moléculas biológicamente activas cuando se escinde, incluyendo ACTH, hormona estimulante de melanocitos y péptidos opioides cerebrales conocidos como endorfinas.
La liberación de ACTH está regulada por la hormona liberadora de corticotropina (CRH) del hipotálamo en respuesta a ritmos fisiológicos normales. Una variedad de factores estresantes también pueden influir en su liberación, y el papel de la ACTH en la respuesta al estrés se discute más adelante en este capítulo.
Hormona foliculoestimulante y hormona luteinizante
Las glándulas endocrinas secretan una variedad de hormonas que controlan el desarrollo y la regulación del sistema reproductivo (estas glándulas incluyen la pituitaria anterior, la corteza suprarrenal y las gónadas, los testículos en los machos y los ovarios en las mujeres). Gran parte del desarrollo del sistema reproductivo ocurre durante la pubertad y está marcado por el desarrollo de características específicas del sexo tanto en adolescentes varones como en mujeres. La pubertad es iniciada por la hormona liberadora de gonadotropina (GnRH), una hormona producida y secretada por el hipotálamo. La GnRH estimula la hipófisis anterior para secretar gonadotropinas, hormonas que regulan la función de las gónadas. Los niveles de GnRH se regulan a través de un bucle de retroalimentación negativa; altos niveles de hormonas reproductivas inhiben la liberación de GnRH. A lo largo de la vida, las gonadotropinas regulan la función reproductiva y, en el caso de las mujeres, el inicio y cese de la capacidad reproductiva.
Las gonadotropinas incluyen dos hormonas glicoproteínicas: la hormona folículo estimulante (FSH) estimula la producción y maduración de las células sexuales, o gametos, incluyendo óvulos en mujeres y espermatozoides en hombres. La FSH también promueve el crecimiento folicular; estos folículos liberan estrógenos en los ovarios femeninos. La hormona luteinizante (LH) desencadena la ovulación en las mujeres, así como la producción de estrógenos y progesterona por los ovarios. La LH estimula la producción de testosterona por los testículos masculinos.
Prolactina
Como su nombre lo indica, la prolactina (PRL) promueve la lactancia (producción de leche) en las mujeres. Durante el embarazo, contribuye al desarrollo de las glándulas mamarias, y después del nacimiento, estimula las glándulas mamarias para producir leche materna. Sin embargo, los efectos de la prolactina dependen en gran medida de los efectos permisivos de los estrógenos, la progesterona y otras hormonas. Y como se señaló anteriormente, la disminución de la leche ocurre en respuesta a la estimulación de la oxitocina.
En una mujer no embarazada, la secreción de prolactina es inhibida por la hormona inhibidora de prolactina (PIH), que en realidad es el neurotransmisor dopamina, y se libera de las neuronas en el hipotálamo. Solo durante el embarazo aumentan los niveles de prolactina en respuesta a la hormona liberadora de prolactina (PRH) del hipotálamo.
Pituitaria Intermedia: Hormona Estimulante de Melan
Las células en la zona entre los lóbulos pituitarios secretan una hormona conocida como hormona estimulante de melanocitos (MSH) que se forma por escisión de la proteína precursora pro-opiomelanocortina (POMC). La producción local de MSH en la piel es responsable de la producción de melanina en respuesta a la exposición a la luz UV. El papel de la MSH que hace la hipófisis es más complicado. Por ejemplo, las personas con piel más clara generalmente tienen la misma cantidad de MSH que las personas con piel más oscura. Sin embargo, esta hormona es capaz de oscurecer la piel al inducir la producción de melanina en los melanocitos de la piel. Las mujeres también muestran una mayor producción de MSH durante el embarazo; en combinación con los estrógenos, puede conducir a una pigmentación de la piel más oscura, especialmente la piel de las areolas y labios menores. Figura 5. (Hormonas Pituitarias Mayores) es un resumen de las hormonas pituitarias y sus principales efectos.

Revisión del Capítulo
El complejo hipotálamo-hipófisis se localiza en el diencéfalo del cerebro. El hipotálamo y la glándula pituitaria están conectados por una estructura llamada infundíbulo, que contiene vasculatura y axones nerviosos. La glándula pituitaria se divide en dos estructuras distintas con diferentes orígenes embrionarios. El lóbulo posterior alberga los terminales axónicos de las neuronas hipotalámicas. Almacena y libera en el torrente sanguíneo dos hormonas hipotalámicas: la oxitocina y la hormona antidiurética (ADH). El lóbulo anterior está conectado al hipotálamo por vasculatura en el infundíbulo y produce y secreta seis hormonas. Su secreción se regula, sin embargo, liberando e inhibiendo hormonas del hipotálamo. Las seis hormonas hipofisarias anteriores son: hormona del crecimiento (GH), hormona estimulante de la tiroides (TSH), hormona adrenocorticotrópica (ACTH), hormona foliculoestimulante (FSH), hormona luteinizante (LH) y prolactina (PRL).
La glándula tiroides
Al final de esta sección, podrás:
- Describir la ubicación y anatomía de la glándula tiroides
- Discutir la síntesis de triyodotironina y tiroxina
- Explicar el papel de las hormonas tiroideas en la regulación del metabolismo basal
- Identificar la hormona producida por las células parafolliculares de la tiroides
Un órgano en forma de mariposa, la glándula tiroides se localiza anterior a la tráquea, justo inferior a la laringe (Figura 1. Glándula tiroides). La región medial, llamada istmo, está flanqueada por lóbulos izquierdo y derecho en forma de ala. Cada uno de los lóbulos tiroideos está incrustado con glándulas paratiroides, principalmente en sus superficies posteriores. El tejido de la glándula tiroides está compuesto principalmente por folículos tiroideos. Los folículos están formados por una cavidad central llena de un líquido pegajoso llamado coloide. Rodeado por una pared de células epiteliales del folículo, el coloide es el centro de producción de la hormona tiroidea, y esa producción depende del componente esencial y único de las hormonas: el yodo.

Síntesis y Liberación de Hormonas Tiroideas
Las hormonas se producen en el coloide cuando los átomos del yodo mineral se unen a una glicoproteína, llamada tiroglobulina, que es secretada al coloide por las células del folículo. Los siguientes pasos describen el ensamblaje de las hormonas:
- La unión de TSH a sus receptores en las células del folículo de la glándula tiroides hace que las células transporten activamente iones yoduro (I —) a través de su membrana celular, desde el torrente sanguíneo hasta el citosol. Como resultado, la concentración de iones yoduro “atrapados” en las células foliculares es muchas veces mayor que la concentración en el torrente sanguíneo.
- Los iones yoduro luego se mueven a la luz de las células del folículo que bordean el coloide. Allí, los iones sufren oxidación (se eliminan sus electrones cargados negativamente). La oxidación de dos iones yoduro (2 I —) da como resultado yodo (I 2), que pasa a través de la membrana celular del folículo hacia el coloide.
- En el coloide, las enzimas peroxidasas vinculan el yodo a los aminoácidos tirosina en la tiroglobulina para producir dos intermediarios: una tirosina unida a un yodo y una tirosina unida a dos yodinas. Cuando uno de cada uno de estos intermediarios está unido por enlaces covalentes, el compuesto resultante es la triyodotironina (T 3), una hormona tiroidea con tres yodinas. Mucho más comúnmente, dos copias del segundo enlace intermediario, formando tetraiodotironina, también conocida como tiroxina (T 4), una hormona tiroidea con cuatro yodinas.
Estas hormonas permanecen en el centro coloide de los folículos tiroideos hasta que la TSH estimula la endocitosis del coloide de regreso a las células del folículo. Allí, las enzimas lisosómicas rompen el coloide tiroglobulina, liberando T 3 y T 4 libres, que se difunden a través de la membrana celular del folículo y entran en el torrente sanguíneo.
En el torrente sanguíneo, menos del uno por ciento de los T 3 y T 4 circulantes permanecen sin consolidar. Esta T 3 y T 4 libres pueden cruzar la bicapa lipídica de las membranas celulares y ser captadas por las células. El 99 por ciento restante de T 3 y T 4 circulantes está unido a proteínas de transporte especializadas llamadas globulinas de unión a tiroxina (TBG), a albúmina, u otras proteínas plasmáticas. Este “empaque” evita su libre difusión hacia las células del cuerpo. Cuando los niveles sanguíneos de T 3 y T 4 comienzan a disminuir, T 3 y T 4 unidos se liberan de estas proteínas plasmáticas y atraviesan fácilmente la membrana de las células diana. T 3 es más potente que T 4, y muchas células convierten T 4 en T 3 a través de la eliminación de un átomo de yodo.
Regulación de la Síntesis TH
La liberación de T 3 y T 4 de la glándula tiroides está regulada por la hormona estimulante de la tiroides (TSH). Como se muestra en la Figura 2. (Classic Negative Feedback Loop), los bajos niveles sanguíneos de T 3 y T 4 estimulan la liberación de la hormona liberadora de tirotropina (TRH) del hipotálamo, lo que desencadena la secreción de TSH de la hipófisis anterior. A su vez, la TSH estimula a la glándula tiroides para que secrete T 3 y T 4. Los niveles de TRH, TSH, T 3 y T 4 están regulados por un sistema de retroalimentación negativa en el que los niveles crecientes de T 3 y T 4 disminuyen la producción y secreción de TSH.

Funciones de las hormonas tiroideas
Las hormonas tiroideas, T 3 y T 4, a menudo se denominan hormonas metabólicas porque sus niveles influyen en la tasa metabólica basal del cuerpo, la cantidad de energía utilizada por el cuerpo en reposo. Cuando T 3 y T 4 se unen a receptores intracelulares localizados en las mitocondrias, provocan un aumento en la descomposición de nutrientes y el uso de oxígeno para producir ATP. Además, T 3 y T 4 inician la transcripción de genes involucrados en la oxidación de la glucosa. Aunque estos mecanismos impulsan a las células a producir más ATP, el proceso es ineficiente y se libera un nivel de calor anormalmente aumentado como subproducto de estas reacciones. Este llamado efecto calorigénico (calor- = “calor”) eleva la temperatura corporal.
También se requieren niveles adecuados de hormonas tiroideas para la síntesis de proteínas y para el desarrollo y crecimiento de tejidos fetales e infantiles. Son especialmente críticos para el desarrollo normal del sistema nervioso tanto en el útero como en la primera infancia, y continúan apoyando la función neurológica en adultos. Como se señaló anteriormente, estas hormonas tiroideas tienen una compleja interrelación con las hormonas reproductivas, y las deficiencias pueden influir en la libido, la fertilidad y otros aspectos de la función reproductiva. Finalmente, las hormonas tiroideas aumentan la sensibilidad del organismo a las catecolaminas (epinefrina y norepinefrina) de la médula suprarrenal mediante la regulación positiva de los receptores en los vasos sanguíneos. Cuando los niveles de las hormonas T 3 y T 4 son excesivos, este efecto acelera la frecuencia cardíaca, fortalece los latidos del corazón y aumenta la presión arterial. Debido a que las hormonas tiroideas regulan el metabolismo, la producción de calor, la síntesis de proteínas y muchas otras funciones del cuerpo, los trastornos tiroideos pueden tener consecuencias graves y
Sistema endocrino: Deficiencia de yodo, hipotiroidismo e hipertiroidismo
Como se discutió anteriormente, se requiere yodo dietético para la síntesis de T 3 y T 4. Pero para gran parte de la población mundial, los alimentos no proporcionan niveles adecuados de este mineral, debido a que la cantidad varía según el nivel en el suelo en el que se cultivó el alimento, así como el riego y fertilizantes utilizados. Los peces y camarones marinos tienden a tener altos niveles porque concentran yodo del agua de mar, pero muchas personas en las regiones sin litoral carecen de acceso a los mariscos. Así, la principal fuente de yodo dietético en muchos países es la sal yodada. La fortificación de la sal con yodo comenzó en Estados Unidos en 1924, y los esfuerzos internacionales para yodar la sal en las naciones más pobres del mundo continúan hoy en día.
La deficiencia de yodo en la dieta puede resultar en la capacidad alterada para sintetizar T 3 y T 4, lo que lleva a una variedad de trastornos graves. Cuando no se pueden producir T 3 y T 4, la TSH se secreta en cantidades crecientes. Como resultado de esta hiperestimulación, la tiroglobulina se acumula en los folículos de la glándula tiroides, incrementando sus depósitos de coloide. La acumulación de coloide aumenta el tamaño general de la glándula tiroides, condición llamada bocio (Figura 3. Bocio). Un bocio es sólo una indicación visible de la deficiencia. Otros trastornos por deficiencia de yodo incluyen problemas de crecimiento y desarrollo, disminución de la fertilidad y muerte prenatal e infantil. Además, la deficiencia de yodo es la principal causa de retraso mental prevenible en todo el mundo. El hipotiroidismo neonatal (cretinismo) se caracteriza por déficits cognitivos, baja estatura, y a veces sordera y mudez en niños y adultos nacidos de madres con deficiencia de yodo durante el embarazo.

En zonas del mundo con acceso a sal yodada, la deficiencia dietética es poco frecuente. En cambio, la inflamación de la glándula tiroides es la causa más común de niveles bajos de hormonas tiroideas en la sangre. Llamado hipotiroidismo, la afección se caracteriza por una baja tasa metabólica, aumento de peso, extremidades frías, estreñimiento, disminución de la libido, irregularidades menstruales y disminución de la actividad mental. Por el contrario, el hipertiroidismo —un nivel sanguíneo anormalmente elevado de hormonas tiroideas— suele ser causado por un tumor hipofisario o tiroideo. En la enfermedad de Graves, el estado hipertiroideo es el resultado de una reacción autoinmune en la que los anticuerpos sobreestimulan las células del folículo de la glándula tiroides. El hipertiroidismo puede provocar un aumento de la tasa metabólica, exceso de calor corporal y sudoración, diarrea, pérdida de peso, temblores y aumento de la frecuencia cardíaca. Los ojos de la persona pueden abultarse (llamados exoftalmos) ya que los anticuerpos producen inflamación en los tejidos blandos de las órbitas. La persona también puede desarrollar bocio.
Calcitonina
La glándula tiroides también secreta una hormona llamada calcitonina que es producida por las células parafolliculares (también llamadas células C) que semental el tejido entre distintos folículos. La calcitonina se libera en respuesta a un aumento en los niveles de calcio en la sangre. Parece tener una función en la disminución de las concentraciones de calcio en la sangre al:
- Inhibir la actividad de los osteoclastos, células óseas que liberan calcio en la circulación al degradar la matriz ósea
- Aumento de la actividad osteoblástica
- Disminuir la absorción de calcio en los intestinos
- Aumento de la pérdida de calcio en la orina
Sin embargo, estas funciones no suelen ser significativas en el mantenimiento de la homeostasis del calcio, por lo que no se entiende del todo la importancia de la calcitonina. A veces se prescriben preparaciones farmacéuticas de calcitonina para reducir la actividad de los osteoclastos en personas con osteoporosis y para reducir la degradación del cartílago en personas con osteoartritis. Las hormonas secretadas por la tiroides se resumen en la Tabla (Hormonas Tiroideas).
| Hormonas tiroideas | ||
|---|---|---|
| Hormonas asociadas | Clase química | Efecto |
| Tiroxina (T 4), triyodotironina (T 3) | Amina | Estimula la tasa metabólica basal |
| Calcitonina | Péptido | Reduce los niveles de Ca 2+ en sangre |
Por supuesto, el calcio es crítico para muchos otros procesos biológicos. Es un segundo mensajero en muchas vías de señalización, y es esencial para la contracción muscular, la transmisión de impulsos nerviosos y la coagulación de la sangre. Dados estos roles, no es sorprendente que los niveles de calcio en la sangre estén estrechamente regulados por el sistema endocrino. Los órganos involucrados en la regulación son las glándulas paratiroides.
Revisión del Capítulo
La glándula tiroides es un órgano en forma de mariposa localizado en el cuello anterior a la tráquea. Sus hormonas regulan el metabolismo basal, el uso de oxígeno, el metabolismo de los nutrientes, la producción de ATP y la homeostasis del calcio. También contribuyen a la síntesis de proteínas y al crecimiento y desarrollo normal de los tejidos corporales, incluida la maduración del sistema nervioso, y aumentan la sensibilidad del cuerpo a las catecolaminas. Las hormonas tiroideas triyodotironina (T 3) y tiroxina (T 4) son producidas y secretadas por la glándula tiroides en respuesta a la hormona estimulante de la tiroides (TSH) de la hipófisis anterior. La síntesis de las hormonas T 3 y T 4 derivadas de aminoácidos requiere yodo. Las cantidades insuficientes de yodo en la dieta pueden provocar bocio, cretinismo y muchos otros trastornos.
Las glándulas paratiroides
Al final de esta sección, podrás:
- Describir la ubicación y estructura de las glándulas paratiroides
- Describir el control hormonal de los niveles de calcio en sangre
- Discutir la respuesta fisiológica de la disfunción paratiroidea
Las glándulas paratiroides son estructuras diminutas y redondas que generalmente se encuentran incrustadas en la superficie posterior de la glándula tiroides (Figura 1. Glándulas Paratiroides). Una gruesa cápsula de tejido conectivo separa las glándulas del tejido tiroideo. La mayoría de las personas tienen cuatro glándulas paratiroides, pero ocasionalmente hay más en los tejidos del cuello o el pecho. La función de un tipo de células paratiroides, las células oxífilas, no está clara. Las células funcionales primarias de las glándulas paratiroides son las células principales. Estas células epiteliales producen y secretan la hormona paratiroidea (PTH), la principal hormona involucrada en la regulación de los niveles de calcio en la sangre.

Las glándulas paratiroides producen y secretan PTH, una hormona peptídica, en respuesta a niveles bajos de calcio en la sangre (Figura 2. Hormona Paratiroidea en el Mantenimiento de la Homeostasis del Calcio Sanguíneo). La secreción de PTH provoca la liberación de calcio de los huesos al estimular los osteoclastos, que secretan enzimas que degradan el hueso y liberan calcio en el líquido intersticial. La PTH también inhibe los osteoblastos, las células involucradas en la deposición ósea, ahorrando así el calcio en la sangre. La PTH provoca una mayor reabsorción de calcio (y magnesio) en los túbulos renales del filtrado de orina. Además, la PTH inicia la producción de la hormona esteroide calcitriol (también conocida como 1,25-dihidroxivitamina D), que es la forma activa de la vitamina D 3, en los riñones. El calcitriol estimula entonces una mayor absorción de calcio dietético por los intestinos. Un bucle de retroalimentación negativa regula los niveles de PTH, con el aumento de los niveles de calcio en la sangre inhibiendo la liberación adicional de PTH.

La actividad anormalmente alta de la glándula paratiroides puede causar hiperparatiroidismo, un trastorno causado por una sobreproducción de PTH que resulta en una reabsorción excesiva de calcio del hueso. El hiperparatiroidismo puede disminuir significativamente la densidad ósea, dando lugar a fracturas espontáneas o deformidades. A medida que aumentan los niveles de calcio en la sangre, disminuye la permeabilidad de la membrana celular al sodio y se reduce la capacidad de respuesta del sistema nervioso. Al mismo tiempo, los depósitos de calcio pueden acumularse en los tejidos y órganos del cuerpo, perjudicando su funcionamiento.
Por el contrario, los niveles anormalmente bajos de calcio en la sangre pueden ser causados por una deficiencia de hormona paratiroidea, llamada hipoparatiroidismo, que puede desarrollarse después de una lesión o cirugía que involucra la glándula tiroides. El nivel bajo de calcio en la sangre aumenta la permeabilidad de la membrana al sodio, lo que resulta en contracciones musculares, calambres, espasmos o convulsiones. Los déficits severos pueden paralizar los músculos, incluidos los involucrados en la respiración, y pueden ser fatales.
Cuando los niveles de calcio en sangre son altos, la calcitonina es producida y secretada por las células parafolliculares de la glándula tiroides. Como se discutió anteriormente, la calcitonina inhibe la actividad de los osteoclastos, reduce la absorción de calcio dietético en el intestino, y señala a los riñones que reabsorban menos calcio, resultando en mayores cantidades de calcio excretado en la orina.
Revisión del Capítulo
El calcio es requerido para una variedad de procesos fisiológicos importantes, incluido el funcionamiento neuromuscular; por lo tanto, los niveles de calcio en la sangre están estrechamente regulados. Las glándulas paratiroides son pequeñas estructuras localizadas en la glándula tiroides posterior que producen hormona paratiroidea (PTH), que regula los niveles de calcio en la sangre. Los niveles bajos de calcio en la sangre provocan la producción y secreción de PTH. En contraste, los niveles elevados de calcio en la sangre inhiben la secreción de PTH y desencadenan la secreción de la hormona tiroidea calcitonina. La subproducción de PTH puede resultar en hipoparatiroidismo. En contraste, la sobreproducción de PTH puede resultar en hiperparatiroidismo.
Las glándulas suprarrenales
Al final de esta sección, podrás:
- Describir la ubicación y estructura de las glándulas suprarrenales
- Identificar las hormonas producidas por la corteza suprarrenal y la médula suprarrenal, y resumir sus células diana y efectos
Las glándulas suprarrenales son cuñas de tejido glandular y neuroendocrino que se adhieren a la parte superior de los riñones mediante una cápsula fibrosa (Figura 1. Glándulas suprarrenales). Las glándulas suprarrenales tienen un rico suministro de sangre y experimentan una de las tasas más altas de flujo sanguíneo en el cuerpo. Son atendidas por varias arterias que se ramifican fuera de la aorta, incluyendo las arterias suprarrenal y renal. La sangre fluye a cada glándula suprarrenal en la corteza suprarrenal y luego drena hacia la médula suprarrenal. Las hormonas suprarrenales se liberan en la circulación a través de las venas suprarrenales izquierda y derecha.

La glándula suprarrenal consiste en una corteza externa de tejido glandular y una médula interna de tejido nervioso. La corteza misma se divide en tres zonas: la zona glomerulosa, la zona fasciculata y la zona reticularis. Cada región secreta su propio conjunto de hormonas.
La corteza suprarrenal, como componente del eje hipotálamo-pituitario-suprarrenal (HPA), secreta hormonas esteroides importantes para la regulación de la respuesta al estrés a largo plazo, la presión arterial y el volumen sanguíneo, la captación y almacenamiento de nutrientes, el equilibrio de líquidos y electrolitos, y la inflamación. El eje HPA implica la estimulación de la liberación hormonal de la hormona adrenocorticotrópica (ACTH) de la hipófisis por el hipotálamo. La ACTH estimula entonces la corteza suprarrenal para producir la hormona cortisol. Esta vía se discutirá con más detalle a continuación.
La médula suprarrenal es tejido neuroendocrino compuesto por neuronas del sistema nervioso simpático postgangliónico (SNS). Realmente es una extensión del sistema nervioso autónomo, que regula la homeostasis en el cuerpo. La vía simpatomedular (SAM) implica la estimulación de la médula por impulsos del hipotálamo a través de neuronas de la médula espinal torácica. La médula es estimulada para secretar las hormonas amina epinefrina y norepinefrina.
Una de las principales funciones de la glándula suprarrenal es responder al estrés. El estrés puede ser físico o psicológico o ambos. Las tensiones físicas incluyen exponer el cuerpo a lesiones, caminar afuera en condiciones frías y húmedas sin abrigo puesto, o desnutrición. Los estreses psicológicos incluyen la percepción de una amenaza física, una pelea con un ser querido, o simplemente un mal día en la escuela.
El cuerpo responde de diferentes maneras al estrés a corto plazo y al estrés a largo plazo siguiendo un patrón conocido como síndrome de adaptación general (GAS). La primera etapa de GAS se llama reacción de alarma. Este es el estrés a corto plazo, la respuesta de lucha o huida, mediada por las hormonas epinefrina y norepinefrina de la médula suprarrenal a través de la vía SAM. Su función es preparar el cuerpo para el esfuerzo físico extremo. Una vez que se alivia este estrés, el cuerpo vuelve rápidamente a la normalidad. La sección sobre la médula suprarrenal cubre esta respuesta con más detalle.
Si el estrés no se alivia pronto, el cuerpo se adapta al estrés en la segunda etapa llamada etapa de resistencia. Si una persona se muere de hambre por ejemplo, el cuerpo puede enviar señales al tracto gastrointestinal para maximizar la absorción de nutrientes de los alimentos.
Sin embargo, si el estrés continúa por un plazo más largo, el cuerpo responde con síntomas bastante diferentes a la respuesta de lucha o huida. Durante la etapa de agotamiento, los individuos pueden comenzar a sufrir depresión, la supresión de su respuesta inmune, fatiga severa, o incluso un ataque cardíaco fatal. Estos síntomas están mediados por las hormonas de la corteza suprarrenal, especialmente el cortisol, liberadas como resultado de las señales del eje HPA.
Las hormonas suprarrenales también tienen varias funciones no relacionadas con el estrés, incluido el aumento de los niveles de sodio y glucosa en sangre, que se describirán en detalle a continuación.
Corteza suprarrenal
La corteza suprarrenal consiste en múltiples capas de células que almacenan lípidos que ocurren en tres regiones estructuralmente distintas. Cada una de estas regiones produce diferentes hormonas.
Hormonas de la Zona Glomerulosa
La región más superficial de la corteza suprarrenal es la zona glomerulosa, la cual produce un grupo de hormonas denominadas colectivamente mineralocorticoides por su efecto sobre los minerales corporales, especialmente el sodio y el potasio. Estas hormonas son esenciales para el equilibrio de líquidos y electrolitos.
La aldosterona es el principal mineralocorticoide. Es importante en la regulación de la concentración de iones de sodio y potasio en orina, sudor y saliva. Por ejemplo, se libera en respuesta a K + en sangre elevada, Na + en sangre baja, presión arterial baja o bajo volumen sanguíneo. En respuesta, la aldosterona aumenta la excreción de K + y la retención de Na +, lo que a su vez aumenta el volumen sanguíneo y la presión arterial. Su secreción es provocada cuando la CRH del hipotálamo desencadena la liberación de ACTH desde la hipófisis anterior.
La aldosterona también es un componente clave del sistema renina-angiotensina-aldosterona (RAAS) en el que células especializadas de los riñones secretan la enzima renina en respuesta a un bajo volumen sanguíneo o presión arterial baja. La renina cataliza entonces la conversión de la proteína sanguínea angiotensinógeno, producida por el hígado, en la hormona angiotensina I. La angiotensina I es convertida en los pulmones en angiotensina II por la enzima convertidora de angiotensina (ACE). La angiotensina II tiene tres funciones principales:
- Iniciando la vasoconstricción de las arteriolas, disminuyendo el flujo sanguíneo
- Estimulando los túbulos renales para reabsorber NaCl y agua, aumentando el volumen sanguíneo
- Señalar a la corteza suprarrenal para secretar aldosterona, cuyos efectos contribuyen aún más a la retención de líquidos, restaurando la presión arterial y el volumen sanguíneo
Para los individuos con hipertensión, o presión arterial alta, se dispone de medicamentos que bloquean la producción de angiotensina II. Estos fármacos, conocidos como inhibidores de la ECA, bloquean que la enzima ACE convierta la angiotensina I en angiotensina II, mitigando así la capacidad de esta última para aumentar la presión arterial.
Hormonas de la Zona Fasciculata
La región intermedia de la corteza suprarrenal es la zona fasciculata, llamada así porque las células forman pequeños fascículos (haces) separados por pequeños vasos sanguíneos. Las células de la zona fasciculata producen hormonas llamadas glucocorticoides por su papel en el metabolismo de la glucosa. El más importante de estos es el cortisol, algunos de los cuales el hígado convierte en cortisona. Un glucocorticoide producido en cantidades mucho menores es la corticosterona. En respuesta a factores estresantes a largo plazo, el hipotálamo secreta CRH, que a su vez desencadena la liberación de ACTH por la hipófisis anterior. La ACTH desencadena la liberación de los glucocorticoides. Su efecto general es inhibir la formación de tejidos mientras se estimula la descomposición de los nutrientes almacenados para mantener los suministros adecuados de combustible. En condiciones de estrés a largo plazo, por ejemplo, el cortisol promueve el catabolismo del glucógeno a glucosa, el catabolismo de los triglicéridos almacenados en ácidos grasos y glicerol, y el catabolismo de las proteínas musculares en aminoácidos. Estas materias primas pueden ser utilizadas para sintetizar glucosa y cetonas adicionales para su uso como combustibles corporales. El hipocampo, que forma parte del lóbulo temporal de las cortezas cerebrales e importante en la formación de la memoria, es altamente sensible a los niveles de estrés debido a sus numerosos receptores de glucocorticoides.
Probablemente esté familiarizado con los medicamentos recetados y de venta libre que contienen glucocorticoides, como inyecciones de cortisona en las articulaciones inflamadas, tabletas de prednisona e inhaladores a base de esteroides utilizados para controlar el asma grave, y cremas de hidrocortisona aplicadas para aliviar las erupciones cutáneas que pican. Estos fármacos reflejan otro papel del cortisol: la regulación negativa del sistema inmune, que inhibe la respuesta inflamatoria.
Hormonas de la Zona Reticularis
La región más profunda de la corteza suprarrenal es la zona reticularis, que produce pequeñas cantidades de una clase de hormonas sexuales esteroideas llamadas andrógenos. Durante la pubertad y la mayor parte de la edad adulta, los andrógenos se producen en las gónadas. Los andrógenos producidos en la zona reticularis complementan los andrógenos gonadales. Se producen en respuesta a ACTH de la hipófisis anterior y se convierten en los tejidos en testosterona o estrógenos. En las mujeres adultas, pueden contribuir al deseo sexual, pero su función en los hombres adultos no se entiende bien. En mujeres posmenopáusicas, a medida que disminuyen las funciones de los ovarios, la principal fuente de estrógenos se convierte en los andrógenos producidos por la zona reticularis.
Médula suprarrenal
Como se señaló anteriormente, la corteza suprarrenal libera glucocorticoides en respuesta al estrés a largo plazo, como una enfermedad grave. En contraste, la médula suprarrenal libera sus hormonas en respuesta al estrés agudo a corto plazo mediado por el sistema nervioso simpático (SNS).
El tejido medular está compuesto por neuronas únicas del SNS postganglionares llamadas células cromafines, que son grandes y de forma irregular, y producen los neurotransmisores epinefrina (también llamada adrenalina) y norepinefrina (o noradrenalina). La epinefrina se produce en mayores cantidades —aproximadamente una proporción de 4 a 1 con la norepinefrina— y es la hormona más poderosa. Debido a que las células cromafines liberan epinefrina y norepinefrina a la circulación sistémica, donde viajan ampliamente y ejercen efectos sobre células distantes, se consideran hormonas. Derivados del aminoácido tirosina, se clasifican químicamente como catecolaminas.
La secreción de epinefrina medular y norepinefrina está controlada por una vía neural que se origina en el hipotálamo en respuesta al peligro o estrés (la vía SAM). Tanto la epinefrina como la norepinefrina señalan al hígado y a las células del músculo esquelético que conviertan el glucógeno en glucosa, lo que resulta en un aumento de los niveles de glucosa Estas hormonas aumentan la frecuencia cardíaca, el pulso y la presión arterial para preparar al cuerpo para combatir la amenaza percibida o huir de ella. Además, la vía dilata las vías respiratorias, elevando los niveles de oxígeno en la sangre. También provoca la vasodilatación, aumentando aún más la oxigenación de órganos importantes como los pulmones, el cerebro, el corazón y el músculo esquelético. Al mismo tiempo, desencadena la vasoconstricción en los vasos sanguíneos que sirven a órganos menos esenciales como el tracto gastrointestinal, los riñones y la piel, y regula a la baja algunos componentes del sistema inmunológico. Otros efectos incluyen sequedad de boca, pérdida de apetito, dilatación de la pupila y pérdida de visión periférica. Las principales hormonas de las glándulas suprarrenales se resumen en la Tabla (Hormonas de las Glándulas Adrenales).
| Hormonas de las glándulas suprarrenales | |||
|---|---|---|---|
| Glándula suprarrenal | Hormonas asociadas | Clase química | Efecto |
| Corteza suprarrenal | Aldosterona | Esteroide | Aumenta los niveles de Na + en sangre |
| Corteza suprarrenal | Cortisol, corticosterona, cortisona | Esteroide | Aumentar los niveles de glucosa en sangre |
| Médula suprarrenal | Epinefrina, norepinefrina | Amina | Estimular la respuesta de la huida o |
Trastornos que involucran a las glándulas suprarrenales
Varios trastornos son causados por la desregulación de las hormonas producidas por las glándulas suprarrenales. Por ejemplo, la enfermedad de Cushing es un trastorno caracterizado por altos niveles de glucosa en sangre y la acumulación de depósitos lipídicos en la cara y el cuello. Es causada por hipersecreción de cortisol. La fuente más común de la enfermedad de Cushing es un tumor hipofisario que secreta cortisol o ACTH en cantidades anormalmente altas. Otros signos comunes de la enfermedad de Cushing incluyen el desarrollo de una cara en forma de Luna, una joroba de búfalo en la parte posterior del cuello, aumento rápido de peso y pérdida de cabello. Los niveles de glucosa crónicamente elevados también se asocian con un riesgo elevado de desarrollar diabetes tipo 2. Además de la hiperglucemia, los glucocorticoides crónicamente elevados comprometen la inmunidad, la resistencia a la infección y la memoria, y pueden resultar en un rápido aumento de peso y pérdida de cabello.
Por el contrario, la hiposecreción de corticosteroides puede resultar en la enfermedad de Addison, un trastorno poco frecuente que causa bajos niveles de glucosa en sangre y bajos niveles de sodio en la sangre. Los signos y síntomas de la enfermedad de Addison son vagos y también son típicos de otros trastornos, lo que dificulta el diagnóstico. Pueden incluir debilidad general, dolor abdominal, pérdida de peso, náuseas, vómitos, sudoración y antojos de comida salada.
Revisión del Capítulo
Las glándulas suprarrenales, localizadas superiores a cada riñón, constan de dos regiones: la corteza suprarrenal y la médula suprarrenal. La corteza suprarrenal, la capa externa de la glándula, produce mineralocorticoides, glucocorticoides y andrógenos. La médula suprarrenal en el núcleo de la glándula produce epinefrina y norepinefrina.
Las glándulas suprarrenales median una respuesta de estrés a corto plazo y una respuesta de estrés a largo plazo. Una amenaza percibida resulta en la secreción de epinefrina y norepinefrina de la médula suprarrenal, que median la respuesta de luchar o huir. La respuesta al estrés a largo plazo está mediada por la secreción de CRH del hipotálamo, lo que desencadena ACTH, que a su vez estimula la secreción de corticosteroides de la corteza suprarrenal. Los mineralocorticoides, principalmente la aldosterona, causan retención de sodio y líquidos, lo que aumenta el volumen sanguíneo y la presión arterial.
La glándula pineal
Al final de esta sección, podrás:
- Describir la ubicación y estructura de la glándula pineal
- Discutir la función de la melatonina
Recordemos que el hipotálamo, parte del diencéfalo del cerebro, se asienta inferior y algo anterior al tálamo. Inferior pero algo posterior al tálamo es la glándula pineal, una pequeña glándula endocrina cuyas funciones no son del todo claras. Se sabe que las células pinealocíticas que componen la glándula pineal producen y secretan la hormona amina melatonina, la cual se deriva de la serotonina.
La secreción de melatonina varía según el nivel de luz recibida del ambiente. Cuando los fotones de luz estimulan las retinas de los ojos, se envía un impulso nervioso a una región del hipotálamo llamada núcleo supraquiasmático (SCN), que es importante para regular los ritmos biológicos. Desde el SCN, la señal nerviosa se lleva a la médula espinal y eventualmente a la glándula pineal, donde se inhibe la producción de melatonina. Como resultado, los niveles sanguíneos de melatonina bajan, promoviendo la vigilia. Por el contrario, a medida que disminuyen los niveles de luz, como durante la noche, la producción de melatonina aumenta, aumentando los niveles sanguíneos y causando somnolencia.
La secreción de melatonina puede influir en los ritmos circadianos del cuerpo, las fluctuaciones de luz oscura que afectan no solo la somnolencia y la vigilia, sino también el apetito y la temperatura corporal. Curiosamente, los niños tienen niveles de melatonina más altos que los adultos, lo que puede impedir la liberación de gonadotropinas de la hipófisis anterior, inhibiendo así el inicio de la pubertad. Finalmente, un papel antioxidante de la melatonina es el tema de investigación actual.
El desfase horario ocurre cuando una persona viaja a través de varias zonas horarias y se siente somnolienta durante el día o despierta por la noche. Viajar a través de múltiples zonas horarias perturba significativamente el ciclo de luz-oscuridad regulado por la melatonina. La síntesis de melatonina puede tardar hasta varios días en ajustarse a los patrones de luz-oscuridad en el nuevo entorno, lo que resulta en jet lag. Algunos viajeros aéreos toman suplementos de melatonina para inducir el sueño.
Revisión del Capítulo
La glándula pineal es una estructura endocrina del diencéfalo del cerebro, y se localiza inferior y posterior al tálamo. Se compone de pinealocitos. Estas células producen y secretan la hormona melatonina en respuesta a los bajos niveles de luz. Los niveles altos de melatonina en la sangre inducen somnolencia. El desfase horario, causado por viajar a través de varias zonas horarias, ocurre porque la síntesis de melatonina tarda varios días en reajustar a los patrones de luz-oscuridad en el nuevo entorno.
Hormonas gonadales y placentarias
Al final de esta sección, podrás:
- Identificar las hormonas más importantes producidas por los testículos y ovarios
- Nombrar las hormonas producidas por la placenta y establecer sus funciones
En esta sección se analiza brevemente el papel hormonal de las gónadas, los testículos masculinos y los ovarios femeninos, que producen las células sexuales (espermatozoides y óvulos) y secretan las hormonas gonadales. Los papeles de las gonadotropinas liberadas de la hipófisis anterior (FSH y LH) se discutieron anteriormente.
La hormona primaria producida por los testículos masculinos es la testosterona, una hormona esteroide importante en el desarrollo del sistema reproductivo masculino, la maduración de los espermatozoides y el desarrollo de características sexuales secundarias masculinas como una voz más profunda, vello corporal y aumento de la masa muscular. Curiosamente, la testosterona también se produce en los ovarios femeninos, pero a un nivel muy reducido. Además, los testículos producen la hormona peptídica inhibina, que inhibe la secreción de FSH de la glándula pituitaria anterior. La FSH estimula la espermatogénesis.
Las hormonas primarias producidas por los ovarios son los estrógenos, que incluyen estradiol, estriol y estrona. Los estrógenos juegan un papel importante en un mayor número de procesos fisiológicos, incluyendo el desarrollo del sistema reproductivo femenino, la regulación del ciclo menstrual, el desarrollo de características del sexo secundario femenino como el aumento de tejido adiposo y el desarrollo de tejido mamario, y el mantenimiento del embarazo. Otra hormona ovárica importante es la progesterona, que contribuye a la regulación del ciclo menstrual y es importante en la preparación del cuerpo para el embarazo así como en el mantenimiento del embarazo. Además, las células granulosas de los folículos ováricos producen inhibina, la cual, como en los varones, inhibe la secreción de FSH.Durante las etapas iniciales del embarazo, un órgano llamado placenta se desarrolla dentro del útero. La placenta suministra oxígeno y nutrientes al feto, excreta productos de desecho y produce y secreta estrógenos y progesterona. La placenta también produce gonadotropina coriónica humana (hCG). La hormona hCG promueve la síntesis de progesterona y reduce la función inmune de la madre para proteger al feto del rechazo inmune. También secreta lactogeno placentario humano (hPL), que juega un papel en la preparación de los senos para la lactancia, y relaxina, que se cree que ayuda a suavizar y ensanchar la sínfisis púbica en preparación para el parto. Las hormonas que controlan la reproducción se resumen en la Tabla (Hormonas Reproductivas).
| Hormonas Reproductivas | |||
|---|---|---|---|
| Gónada | Hormonas asociadas | Clase química | Efecto |
| Testículos | Testosterona | Esteroide | Estimula el desarrollo de características sexuales secundarias masculinas y la producción de esperma |
| Testículos | Inhibina | Proteína | Inhibe la liberación de FSH de la pitu |
| Ovarios | Estrógenos y progesterona | Esteroide | Estimular el desarrollo de las características del sexo secundario femenino y preparar el cuerpo para el parto |
| Placenta | Gonadotropina coriónica humana | Proteína | Promueve la síntesis de progesterona durante el embarazo e inhibe la respuesta inmune contra el feto |
Esteroides Anabólicos
El sistema endocrino puede ser explotado con fines ilegales o poco éticos. Un ejemplo destacado de esto es el uso de medicamentos esteroides por parte de atletas profesionales.
Comúnmente utilizados para mejorar el rendimiento, los esteroides anabólicos son versiones sintéticas de la hormona sexual masculina, la testosterona. Al aumentar los niveles naturales de esta hormona, los atletas experimentan un aumento de la masa muscular. Las versiones sintéticas de la hormona de crecimiento humana también se utilizan para construir masa muscular.
El uso de drogas para mejorar el rendimiento está prohibido por todas las principales organizaciones deportivas universitarias y profesionales de Estados Unidos porque imparten una ventaja injusta a los atletas que los toman. Además, los medicamentos pueden causar efectos secundarios significativos y peligrosos. Por ejemplo, el uso de esteroides anabólicos puede aumentar los niveles de colesterol, elevar la presión arterial y dañar el hígado. Los niveles alterados de testosterona (demasiado bajos o demasiado altos) han sido implicados en causar daño estructural al corazón y aumentar el riesgo de arritmias cardíacas, ataques cardíacos, insuficiencia cardíaca congestiva y muerte súbita. Paradójicamente, los esteroides pueden tener un efecto feminizante en los hombres, incluyendo testículos arrugados y tejido mamario agrandado. En las hembras, su uso puede ocasionar efectos masculinizantes como agrandamiento del clítoris y crecimiento del vello facial. En ambos sexos, su uso puede promover un aumento de la agresión (comúnmente conocida como “roid-rage”), depresión, alteraciones del sueño, acné severo e infertilidad.
Revisión del Capítulo
El sistema reproductor masculino y femenino está regulado por la hormona folículo estimulante (FSH) y la hormona luteinizante (LH) producidas por el lóbulo anterior de la glándula pituitaria en respuesta a la hormona liberadora de gonadotropina (GnRH) del hipotálamo. En los machos, la FSH estimula la maduración espermática, la cual es inhibida por la hormona inhibina. La hormona esteroide testosterona, un tipo de andrógeno, se libera en respuesta a la LH y es responsable de la maduración y mantenimiento del sistema reproductivo masculino, así como del desarrollo de características sexuales secundarias masculinas. En las hembras, la FSH promueve la maduración del óvulo y la LH señala la secreción de las hormonas sexuales femeninas, los estrógenos y la progesterona. Ambas hormonas son importantes en el desarrollo y mantenimiento del sistema reproductivo femenino, así como en el mantenimiento del embarazo. La placenta se desarrolla durante el embarazo temprano, y secreta varias hormonas importantes para mantener el embarazo.
El páncreas endocrino
Al final de esta sección, podrás:
- Describir la ubicación y estructura del páncreas, así como la morfología y función de los islotes pancreáticos
- Comparar y contrastar las funciones de insulina y glucagón
El páncreas es un órgano largo y delgado, la mayor parte del cual se localiza posterior a la mitad inferior del estómago (Figura 1. Páncreas). Aunque es principalmente una glándula exocrina, secretando una variedad de enzimas digestivas, el páncreas tiene una función endocrina. Sus islotes pancreáticos —grupos de células anteriormente conocidos como islotes de Langerhans— secretan las hormonas glucagón, insulina, somatostatina y polipéptido pancreático (PP).

Células y secreciones de los islotes pancreáticos
Los islotes pancreáticos contienen cada uno cuatro variedades de células:
- La célula alfa produce la hormona glucagón y constituye aproximadamente el 20 por ciento de cada islote. El glucagón juega un papel importante en la regulación de la glucosa en sangre; los niveles bajos de glucosa en sangre estimulan su liberación
- La célula beta produce la hormona insulina y constituye aproximadamente el 75 por ciento de cada islote. Los niveles elevados de glucosa en sangre estimulan la liberación de insulina.
- La célula delta representa el cuatro por ciento de las células de los islotes y secreta la hormona peptídica somatostatina. Recordemos que la somatostatina también es liberada por el hipotálamo (como GHIH), y el estómago y los intestinos también la secretan. Una hormona inhibitoria, la somatostatina pancreática inhibe la liberación tanto de glucagón como de insulina.
- La célula PP representa aproximadamente el uno por ciento de las células de los islotes y secreta la hormona polipeptídica pancreática. Se cree que juega un papel en el apetito, así como en la regulación de las secreciones pancreáticas exocrinas y endocrinas. El polipéptido pancreático liberado después de una comida puede reducir el consumo de alimentos; sin embargo, también se libera en respuesta al ayuno.
Regulación de los niveles de glucosa en sangre por insulina y glucagón
La glucosa es necesaria para la respiración celular y es el combustible preferido para todas las células del cuerpo. El cuerpo deriva la glucosa de la descomposición de los alimentos y bebidas que contienen carbohidratos que consumimos. La glucosa no absorbida inmediatamente por las células como combustible puede ser almacenada por el hígado y los músculos como glucógeno, o convertida en triglicéridos y almacenada en el tejido adiposo. Las hormonas regulan tanto el almacenamiento como la utilización de la glucosa según sea necesario. Los receptores localizados en el páncreas detectan los niveles de glucosa en sangre, y posteriormente las células pancreáticas secretan glucagón o insulina para mantener los niveles normales.
Glucagón
Los receptores en el páncreas pueden sentir la disminución de los niveles de glucosa en sangre, como durante periodos de ayuno o durante el parto prolongado o el ejercicio (Figura 2. Regulación Homeostática de los Niveles de Glucosa en Sangre). En respuesta, las células alfa del páncreas secretan la hormona glucagón, que tiene varios efectos:
- Estimula al hígado para que vuelva a convertir sus reservas de glucógeno en glucosa. Esta respuesta se conoce como glucogenólisis. Luego, la glucosa se libera a la circulación para su uso por las células del cuerpo.
- Estimula al hígado a tomar aminoácidos de la sangre y convertirlos en glucosa. Esta respuesta se conoce como gluconeogénesis.
- Estimula la lipólisis, la descomposición de los triglicéridos almacenados en ácidos grasos libres y glicerol. Parte del glicerol libre liberado en el torrente sanguíneo viaja al hígado, lo que lo convierte en glucosa. Esta es también una forma de gluconeogénesis.
Tomadas en conjunto, estas acciones aumentan los niveles de glucosa en sangre. La actividad del glucagón se regula a través de un mecanismo de retroalimentación negativa; el aumento de los niveles de glucosa en sangre inhibe la producción y secreción de glucagón adicional.

Insulina
La función principal de la insulina es facilitar la captación de glucosa en las células del cuerpo. Los glóbulos rojos, así como las células del cerebro, hígado, riñones y el revestimiento del intestino delgado, no tienen receptores de insulina en sus membranas celulares y no requieren insulina para la captación de glucosa. Aunque todas las demás células del cuerpo sí requieren insulina si van a tomar glucosa del torrente sanguíneo, las células del músculo esquelético y las células adiposas son las principales dianas de la insulina.
La presencia de alimentos en el intestino desencadena la liberación de hormonas del tracto gastrointestinal como el péptido insulinotrópico dependiente de glucosa (anteriormente conocido como péptido inhibidor gástrico). Esto es a su vez el desencadenante inicial para la producción y secreción de insulina por las células beta del páncreas. Una vez que ocurre la absorción de nutrientes, el aumento resultante en los niveles de glucosa en sangre estimula aún más la secreción
Precisamente cómo la insulina facilita la captación de glucosa no está del todo claro. Sin embargo, la insulina parece activar un receptor de tirosina quinasa, desencadenando la fosforilación de muchos sustratos dentro de la célula. Estas múltiples reacciones bioquímicas convergen para apoyar el movimiento de vesículas intracelulares que contienen transportadores de glucosa facilitadores hacia la membrana celular. En ausencia de insulina, estas proteínas de transporte normalmente se reciclan lentamente entre la membrana celular y el interior celular. La insulina desencadena el rápido movimiento de un charco de vesículas transportadoras de glucosa hacia la membrana celular, donde se fusionan y exponen los transportadores de glucosa al líquido extracelular. Luego, los transportadores mueven la glucosa al facilitar la difusión hacia el interior de la célula.
La insulina también reduce los niveles de glucosa en sangre al estimular la glucólisis, el metabolismo de la glucosa para la generación de ATP. Además, estimula al hígado para convertir el exceso de glucosa en glucógeno para su almacenamiento, e inhibe las enzimas involucradas en la glucogenólisis y la gluconeogénesis. Finalmente, la insulina promueve la síntesis de triglicéridos y proteínas. La secreción de insulina se regula a través de un mecanismo de retroalimentación negativa. A medida que disminuyen los niveles de glucosa en sangre, se inhibe la liberación adicional de insulina Las hormonas pancreáticas se resumen en la Tabla (Hormonas del Páncreas).
| Hormonas del Páncreas | ||
|---|---|---|
| Hormonas asociadas | Clase química | Efecto |
| Insulina (células beta) | Proteína | Reduce los niveles de glucosa en sangre |
| Glucagón (células alfa) | Proteína | Aumenta los niveles de glucosa en sangre |
| Somatostatina (células delta) | Proteína | Inhibe la liberación de insulina y glucagón |
| Polipéptido pancreático (células PP) | Proteína | Papel en el apetito |
Sistema endocrino: Diabetes Mellitus
La disfunción de la producción y secreción de insulina, así como la capacidad de respuesta de las células diana a la insulina, pueden conducir a una afección llamada diabetes mellitus. Una enfermedad cada vez más común, la diabetes mellitus ha sido diagnosticada en más de 18 millones de adultos en Estados Unidos, y más de 200 mil niños. Se estima que hasta 7 millones de adultos más tienen el padecimiento pero no han sido diagnosticados. Además, se estima que aproximadamente 79 millones de personas en EU tienen prediabetes, afección en la que los niveles de glucosa en sangre son anormalmente altos, pero aún no lo suficientemente altos como para ser clasificados como diabetes.
Hay dos formas principales de diabetes mellitus. La diabetes tipo 1 es una enfermedad autoinmune que afecta a las células beta del páncreas. Se reconoce que ciertos genes aumentan la susceptibilidad. Las células beta de las personas con diabetes tipo 1 no producen insulina; por lo tanto, la insulina sintética debe administrarse por inyección o infusión. Esta forma de diabetes representa menos del cinco por ciento de todos los casos de diabetes.
La diabetes tipo 2 representa aproximadamente el 95 por ciento de todos los casos. Se adquiere, y factores de estilo de vida como la mala alimentación, la inactividad y la presencia de prediabetes aumentan en gran medida el riesgo de una persona. Alrededor del 80 al 90 por ciento de las personas con diabetes tipo 2 tienen sobrepeso u obesidad. En la diabetes tipo 2, las células se vuelven resistentes a los efectos de la insulina. En respuesta, el páncreas aumenta su secreción de insulina, pero con el tiempo, las células beta se agotan. En muchos casos, la diabetes tipo 2 puede revertirse mediante una pérdida moderada de peso, actividad física regular y el consumo de una dieta saludable; sin embargo, si no se pueden controlar los niveles de glucosa en sangre, el diabético eventualmente requerirá insulina.
Dos de las primeras manifestaciones de la diabetes son la micción excesiva y la sed excesiva. Demuestran cómo los niveles fuera de control de glucosa en la sangre afectan la función renal. Los riñones son los encargados de filtrar la glucosa de la sangre. El exceso de glucosa en sangre atrae agua a la orina, y como resultado la persona elimina una cantidad anormalmente grande de orina dulce. El uso de agua corporal para diluir la orina deja el cuerpo deshidratado, por lo que la persona tiene sed inusualmente y continuamente. La persona también puede experimentar hambre persistente debido a que las células del cuerpo no pueden acceder a la glucosa en el torrente sanguíneo.
Con el tiempo, persistentemente altos niveles de glucosa en la sangre lesionan los tejidos de todo el cuerpo, especialmente los de los vasos sanguíneos y los nervios. La inflamación y lesión del revestimiento de las arterias conducen a aterosclerosis y un mayor riesgo de ataque cardíaco y accidente cerebrovascular. El daño a los vasos sanguíneos microscópicos del riñón perjudica la función renal y puede provocar insuficiencia renal. El daño a los vasos sanguíneos que sirven a los ojos puede llevar a la ceguera. El daño a los vasos sanguíneos también reduce la circulación a las extremidades, mientras que el daño a los nervios conduce a una pérdida de sensibilidad, llamada neuropatía, particularmente en las manos y los pies. En conjunto, estos cambios aumentan el riesgo de lesiones, infección y muerte tisular (necrosis), contribuyendo a una alta tasa de amputaciones de dedos, pies y piernas en personas con diabetes. La diabetes incontrolada también puede conducir a una forma peligrosa de acidosis metabólica llamada cetoacidosis. Privadas de glucosa, las células dependen cada vez más de las reservas de grasa como combustible. Sin embargo, en un estado deficiente de glucosa, el hígado se ve obligado a utilizar una vía alternativa de metabolismo lipídico que da como resultado el aumento de la producción de cuerpos cetónicos (o cetonas), que son ácidos. La acumulación de cetonas en la sangre causa cetoacidosis, la cual, si no se trata, puede llevar a un “coma diabético” potencialmente mortal. En conjunto, estas complicaciones hacen de la diabetes la séptima causa principal de muerte en Estados Unidos.
La diabetes se diagnostica cuando las pruebas de laboratorio revelan que los niveles de glucosa en sangre son más altos de lo normal, una condición llamada hiperglucemia. El tratamiento de la diabetes depende del tipo, la gravedad de la afección y la capacidad del paciente para realizar cambios en el estilo de vida. Como se señaló anteriormente, la pérdida moderada de peso, la actividad física regular y el consumo de una dieta saludable pueden reducir los niveles de glucosa en sangre. Algunos pacientes con diabetes tipo 2 pueden ser incapaces de controlar su enfermedad con estos cambios en el estilo de vida, y requerirán medicación. Históricamente, el tratamiento de primera línea de la diabetes tipo 2 fue la insulina. Los avances de la investigación han dado como resultado opciones alternativas, incluyendo medicamentos que mejoran la función pancreática.
Revisión del Capítulo
El páncreas tiene funciones tanto exocrinas como endocrinas. Los tipos de células de los islotes pancreáticos incluyen células alfa, que producen glucagón; células beta, que producen insulina; células delta, que producen somatostatina; y células PP, que producen polipéptido pancreático. La insulina y el glucagón están involucrados en la regulación del metabolismo de la glucosa. La insulina es producida por las células beta en respuesta a altos niveles de glucosa en sangre. Mejora la captación y utilización de glucosa por las células diana, así como el almacenamiento del exceso de glucosa para su uso posterior. La disfunción de la producción de insulina o la resistencia de las células diana a los efectos de la insulina provoca diabetes mellitus, trastorno caracterizado por altos niveles de glucosa en sangre. La hormona glucagón es producida y secretada por las células alfa del páncreas en respuesta a bajos niveles de glucosa en sangre. El glucagón estimula mecanismos que incrementan los niveles de glucosa en sangre, como el catabolismo del glucógeno en glucosa.
Órganos con funciones endocrinas secundarias
Al final de esta sección, podrás:
- Identificar los órganos con una función endocrina secundaria, la hormona que producen y sus efectos
En tu estudio de anatomía y fisiología, ya te has encontrado con algunos de los muchos órganos del cuerpo que tienen funciones endocrinas secundarias. Aquí aprenderá sobre las actividades productoras de hormonas del corazón, el tracto gastrointestinal, los riñones, el esqueleto, el tejido adiposo, la piel y el timo.
Corazón
Cuando el cuerpo experimenta un aumento en el volumen sanguíneo o la presión, las células de la pared auricular del corazón se estiran. En respuesta, las células especializadas en la pared de las aurículas producen y secretan la hormona peptídica péptido natriurético auricular (ANP). ANP señala a los riñones que reduzcan la reabsorción de sodio, disminuyendo así la cantidad de agua reabsorbida del filtrado de orina y reduciendo el volumen sanguíneo. Otras acciones del ANP incluyen la inhibición de la secreción de renina y el inicio del sistema renina-angiotensina-aldosterona (RAAS) y la vasodilatación. Por lo tanto, el ANP ayuda a disminuir la presión arterial, el volumen sanguíneo y los niveles de sodio en la sangre.
Tracto Gastrointestinal
Las células endocrinas del tracto GI se localizan en la mucosa del estómago y del intestino delgado. Algunas de estas hormonas se secretan en respuesta a comer una comida y ayudan en la digestión. Un ejemplo de una hormona secretada por las células del estómago es la gastrina, una hormona peptídica secretada en respuesta a la distensión estomacal que estimula la liberación de ácido clorhídrico. La secretina es una hormona peptídica secretada por el intestino delgado a medida que el quimo ácido (alimento y líquido parcialmente digerido) se mueve desde el estómago. Estimula la liberación de bicarbonato del páncreas, que amortigua el quimo ácido, e inhibe la posterior secreción de ácido clorhídrico por el estómago. La colecistoquinina (CCK) es otra hormona peptídica liberada del intestino delgado. Promueve la secreción de enzimas pancreáticas y la liberación de bilis de la vesícula biliar, ambas de las cuales facilitan la digestión. Otras hormonas producidas por las células intestinales ayudan en el metabolismo de la glucosa, como estimulando las células beta pancreáticas para que secreten insulina, reduciendo la secreción de glucagón de las células alfa o potenciando la sensibilidad celular a la insulina.
Riñones
Los riñones participan en varias vías endocrinas complejas y producen ciertas hormonas. Una disminución en el flujo sanguíneo a los riñones los estimula a liberar la enzima renina, desencadenando el sistema renina-angiotensina-aldosterona (RAAS), y estimulando la reabsorción de sodio y agua. La reabsorción aumenta el flujo sanguíneo y la presión arterial. Los riñones también juegan un papel en la regulación de los niveles de calcio en la sangre a través de la producción de calcitriol a partir de la vitamina D 3, que se libera en respuesta a la secreción de hormona paratiroidea (PTH). Además, los riñones producen la hormona eritropoyetina (EPO) en respuesta a bajos niveles de oxígeno. La EPO estimula la producción de glóbulos rojos (eritrocitos) en la médula ósea, aumentando así el suministro de oxígeno a los tejidos. Es posible que haya oído hablar de la EPO como una droga que mejora el rendimiento (en forma sintética).
Esqueleto
Aunque el hueso ha sido reconocido desde hace mucho tiempo como un objetivo para las hormonas, solo recientemente los investigadores han reconocido que el propio esqueleto produce al menos dos hormonas. El factor de crecimiento de fibroblastos 23 (FGF23) es producido por las células óseas en respuesta al aumento de los niveles sanguíneos de vitamina D 3 o fosfato. Desencadena que los riñones inhiban la formación de calcitriol a partir de la vitamina D 3 y aumenten la excreción de fósforo. La osteocalcina, producida por los osteoblastos, estimula las células beta pancreáticas para aumentar la producción de insulina. También actúa sobre los tejidos periféricos para aumentar su sensibilidad a la insulina y su utilización de glucosa.
Tejido adiposo
El tejido adiposo produce y secreta varias hormonas involucradas en el metabolismo y almacenamiento de los lípidos. Un ejemplo importante es la leptina, una proteína fabricada por células adiposas que circula en cantidades directamente proporcionales a los niveles de grasa corporal. La leptina se libera en respuesta al consumo de alimentos y actúa uniéndose a las neuronas cerebrales involucradas en la ingesta y gasto de energía. La unión de la leptina produce una sensación de saciedad después de una comida, reduciendo así el apetito. También parece que la unión de la leptina a los receptores cerebrales desencadena el sistema nervioso simpático para regular el metabolismo óseo, aumentando la deposición de hueso cortical. La adiponectina, otra hormona sintetizada por las células adiposas, parece reducir la resistencia celular a la insulina y proteger los vasos sanguíneos de la inflamación y la aterosclerosis. Sus niveles son menores en las personas obesas, y suben tras la pérdida de peso.
Piel
La piel funciona como órgano endocrino en la producción de la forma inactiva de vitamina D 3, colecalciferol. Cuando el colesterol presente en la epidermis se expone a la radiación ultravioleta, se convierte en colecalciferol, que luego ingresa a la sangre. En el hígado, el colecalciferol se convierte en un intermedio que viaja a los riñones y se convierte posteriormente en calcitriol, la forma activa de la vitamina D 3. La vitamina D es importante en una variedad de procesos fisiológicos, incluyendo la absorción intestinal de calcio y la función del sistema inmune. En algunos estudios, los niveles bajos de vitamina D se han asociado con mayores riesgos de cáncer, asma severa y esclerosis múltiple. La deficiencia de vitamina D en niños causa raquitismo, y en adultos, osteomalacia, ambas caracterizadas por deterioro óseo.
Thymus
El timo es un órgano del sistema inmune que es más grande y más activo durante la infancia y la primera infancia, y comienza a atrofiarse a medida que envejecemos. Su función endocrina es la producción de un grupo de hormonas llamadas timosinas que contribuyen al desarrollo y diferenciación de los linfocitos T, que son células inmunes. Aunque aún no se entiende bien el papel de las timosinas, es claro que contribuyen a la respuesta inmune. Las timosinas se han encontrado en tejidos distintos al timo y tienen una amplia variedad de funciones, por lo que las timosinas no pueden clasificarse estrictamente como hormonas tímicas.
Hígado
El hígado es responsable de secretar al menos cuatro hormonas importantes o precursores hormonales: factor de crecimiento similar a la insulina (somatomedina), angiotensinógeno, trombopoetina y hepcidina. El factor de crecimiento-1 similar a la insulina es el estímulo inmediato para el crecimiento en el cuerpo, especialmente de los huesos. El angiotensinógeno es el precursor de la angiotensina, mencionada anteriormente, que aumenta la presión arterial. La trombopoetina estimula la producción de las plaquetas de la sangre. Las hepcidinas bloquean la liberación de hierro de las células del cuerpo, ayudando a regular la homeostasis del hierro en nuestros fluidos corporales. Las principales hormonas de estos otros órganos se resumen en la Tabla (Órganos con Funciones Endocrinas Secundarias y Sus Hormonas Mayores).
| Órganos con funciones endocrinas secundarias y sus hormonas principales | ||
|---|---|---|
| Órgano | Hormonas principales | Efectos |
| Corazón | Péptido natriurético auricular (ANP) | Reduce el volumen sanguíneo, la presión arterial y la concentración de Na + |
| Tracto gastrointestinal | Gastrin, secretina y colecistoquinina | Ayuda a la digestión de los alimentos y la amortiguación de los ácidos del estómago |
| Tracto gastrointestinal | Péptido insulinotrópico dependiente de glucosa (GIP) y péptido similar al glucagón 1 (GLP-1) | Estimular las células beta del páncreas para liberar insulina |
| Riñones | Renin | Estimula la liberación de aldosterona |
| Riñones | Calcitriol | Ayudas en la absorción de Ca 2+ |
| Riñones | Eritropoyetina | Desencadena la formación de glóbulos rojos en la médula ósea |
| Esqueleto | FGF23 | Inhibe la producción de calcitriol y aumenta la excreción de fosfato |
| Esqueleto | Osteocalcina | Aumenta la producción de insulina |
| Tejido adiposo | Leptina | Promueve las señales de saciedad en el cerebro |
| Tejido adiposo | Adiponectina | Reduce la resistencia a la insulina |
| Piel | Colecalciferol | Modificado para formar vitamina D |
| Tío (y otros órganos) | TIMOSINAS | Entre otras cosas, ayudas en el desarrollo de los linfocitos T del sistema inmune |
| Hígado | Factor de crecimiento similar a la insulina-1 | Estimula el crecimiento corporal |
| Hígado | Angiotensinógeno | Eleva la presión arterial |
| Hígado | Trombopoetina | Provoca aumento de plaquetas |
| Hígado | Hepcidina | Bloquea la liberación de hierro en los fluidos corporales |
Revisión del Capítulo
Algunos órganos tienen una función endocrina secundaria. Por ejemplo, las paredes de las aurículas del corazón producen la hormona péptido natriurético auricular (ANP), el tracto gastrointestinal produce las hormonas gastrina, secretina y colecistoquinina, que ayudan en la digestión, y los riñones producen eritropoyetina (EPO), que estimula la formación de glóbulos rojos. Incluso el hueso, el tejido adiposo y la piel tienen funciones endocrinas secundarias.
Desarrollo y Envejecimiento del Sistema Endocrino
Al final de esta sección, podrás:
- Describir los orígenes embrionarios del sistema endocrino
- Discutir los efectos del envejecimiento en el sistema endocrino
El sistema endocrino surge de las tres capas germinales embrionarias. Las glándulas endocrinas que producen las hormonas esteroides, como las gónadas y la corteza suprarrenal, surgen del mesodermo. En contraste, las glándulas endocrinas que surgen del endodermo y ectodermo producen las hormonas amina, péptido y proteína. La glándula pituitaria surge de dos áreas distintas del ectodermo: la glándula pituitaria anterior surge del ectodermo oral, mientras que la glándula pituitaria posterior surge del ectodermo neural en la base del hipotálamo. La glándula pineal también surge del ectodermo. Las dos estructuras de las glándulas suprarrenales surgen de dos capas germinales diferentes: la corteza suprarrenal del mesodermo y la médula suprarrenal de las células neuronales del ectodermo. El endodermo da lugar a las glándulas tiroides y paratiroides, así como el páncreas y el timo.
A medida que el cuerpo envejece, ocurren cambios que afectan el sistema endocrino, a veces alterando la producción, secreción y catabolismo de hormonas. Por ejemplo, la estructura de la glándula pituitaria anterior cambia a medida que disminuye la vascularización y el contenido de tejido conectivo aumenta con el aumento de la edad. Esta reestructuración afecta la producción de hormonas de la glándula. Por ejemplo, la cantidad de hormona de crecimiento humana que se produce disminuye con la edad, lo que resulta en la reducción de la masa muscular comúnmente observada en los ancianos.
Las glándulas suprarrenales también sufren cambios a medida que el cuerpo envejece; a medida que aumenta el tejido fibroso, disminuye la producción de cortisol y aldosterona. Curiosamente, la producción y secreción de epinefrina y norepinefrina permanecen normales durante todo el proceso de envejecimiento.
Un ejemplo bien conocido del proceso de envejecimiento que afecta a una glándula endocrina es la menopausia y la disminución de la función ovárica. Al aumentar la edad, los ovarios disminuyen tanto en tamaño como en peso y se vuelven progresivamente menos sensibles a las gonadotropinas. Esto provoca paulatinamente una disminución en los niveles de estrógeno y progesterona, lo que lleva a la menopausia y a la incapacidad de reproducirse. Los niveles bajos de estrógenos y progesterona también están asociados con algunos estados de enfermedad, como osteoporosis, aterosclerosis e hiperlipidemia, o niveles anormales de lípidos en sangre.
Los niveles de testosterona también disminuyen con la edad, una condición llamada andropausia (o viropausia); sin embargo, esta disminución es mucho menos dramática que la disminución de estrógenos en las mujeres, y mucho más gradual, raramente afectando la producción de esperma hasta la vejez. Aunque esto significa que los machos mantienen su capacidad de engendrar hijos durante décadas más que las hembras, la cantidad, calidad y motilidad de sus espermatozoides a menudo se reduce.
A medida que el cuerpo envejece, la glándula tiroides produce menos hormonas tiroideas, provocando una disminución gradual de la tasa metabólica basal. La menor tasa metabólica reduce la producción de calor corporal y aumenta los niveles de grasa corporal. Las hormonas paratiroides, por otro lado, aumentan con la edad. Esto puede deberse a la reducción de los niveles de calcio en la dieta, provocando un aumento compensatorio de la hormona paratiroidea. Sin embargo, el aumento de los niveles de hormona paratiroidea combinado con la disminución de los niveles de calcitonina (y estrógenos en las mujeres) puede conducir a osteoporosis ya que la PTH estimula la desmineralización de los huesos para aumentar los niveles de calcio en la sangre. Observe que la osteoporosis es común tanto en hombres como en mujeres de edad avanzada.
El aumento de la edad también afecta el metabolismo de la glucosa, ya que los niveles de glucosa en sangre aumentan más rápidamente y tardan más en volver a la normalidad en los ancianos Además, el aumento de la intolerancia a la glucosa puede ocurrir debido a una disminución gradual de la sensibilidad celular a la insulina. Casi el 27 por ciento de los estadounidenses de 65 años o más tienen diabetes.
Revisión del Capítulo
El sistema endocrino se origina en las tres capas germinales del embrión, incluyendo el endodermo, ectodermo y mesodermo. En general, diferentes clases de hormonas surgen de distintas capas germinales. El envejecimiento afecta las glándulas endocrinas, afectando potencialmente la producción y secreción de hormonas, y puede causar enfermedades. La producción de hormonas, como la hormona del crecimiento humano, cortisol, aldosterona, hormonas sexuales y las hormonas tiroideas, disminuye con la edad.
Licencia
Esta obra es producida por OpenStaX-CNX y licenciada bajo la Creative Commons Attribution License 3.0. http://cnx.org/content/m46535/1.3/