7.2: La cadena de transporte de electrones (ETC)
- Page ID
- 54259
Todas las células utilizan una cadena de transporte de electrones (ETC) para oxidar sustratos en reacciones exergónicas. El flujo de electrones desde sustratos reducidos a través de un ETC es como el movimiento de electrones entre los polos de una batería. En el caso de la batería, el flujo de electrones libera energía libre para alimentar un motor, luz, celular, etc. En el ETC mitocondrial, los electrones fluyen cuando el electrón reducido (NADH, FADH2) se oxida. En plantas y otros organismos fotosintéticos, una ETC sirve para oxidar el NADPH (una versión fosforilada del portador de electrones NADH). En ambos casos, la energía libre liberada cuando las reacciones redox de una ETC se acoplan al transporte activo de protones (iones H+) a través de una membrana. El resultado es un gradiente químico de iones H+ así como un gradiente de pH. Dado que los protones están cargados, el gradiente de protones también es un gradiente eléctrico. En una especie de taquigrafía, decimos que la energía libre una vez en sustratos reducidos se encuentra ahora en un gradiente electroquímico. Esa energía libre de gradiente es capturada en reacciones de síntesis de ATP acopladas al flujo (difusión) de protones a través de la membrana en el proceso llamado fosforilación oxidativa. En la respiración aeróbica, los electrones se transfieren finalmente de los componentes al final de la ETC a un aceptor de electrones final de oxígeno molecular, O2, haciendo agua. En la fotosíntesis, la transferencia de electrones reduce el CO2 a azúcares.
El Mecanismo Quimosmótico explicó cómo la creación de un gradiente electroquímico y cómo la energía libre de gradiente termina en ATP. Para esta perspicacia, Peter Mitchell ganó el Premio Nobel de Química en 1978. Puedes leer la propuesta original de Mitchell del modelo de quimioósmosis de síntesis mitocondrial de ATP en Mitchell P (1961) Acoplamiento de fosforilación a transferencia de electrones e hidrógeno por un tipo de mecanismo quimiosmótico. Naturaleza 191:144-148. Aquí nos enfocamos en los detalles de la respiración tal como ocurre en las mitocondrias de células eucariotas. Los productos finales del transporte de electrones son NAD+, FAD, agua y protones. Los protones terminan fuera de la matriz mitocondrial porque son bombeados a través de la membrana cristalina utilizando la energía libre del transporte de electrones.
El transporte de electrones y la fosforilación oxidativa se resumen en la siguiente ilustración.
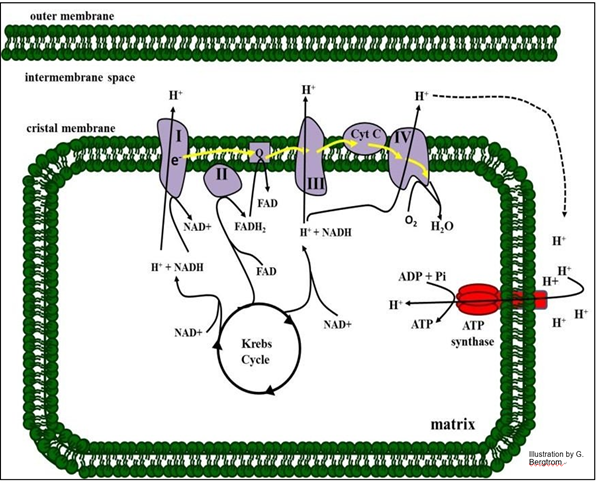
161 El transporte de electrones oxida portadores de electrones reducidos
162 Encontrar la energía libre del transporte de electrones
163 Separación del transporte de electrones de la fosforilación oxidativa
Los complejos proteicos numerados romanos junto con la Coenzima Q (solo “Q” en el dibujo) y el citocromo C (Cyt c) constituyen la ETC), la secuencia de reacciones que oxidan NADH o FADH2 a NAD+ y FAD (respectivamente). Los electrones de estos portadores de electrones reducidos se transfieren de un complejo ETC al siguiente. Al final de la cadena, electrones, protones y oxígeno se unen en el complejo IV para hacer agua. Como cabría esperar, en condiciones estándar en un sistema cerrado, el transporte de electrones es cuesta abajo, con una liberación general de energía libre (dGo negativo) en equilibrio.
En la ilustración anterior, podemos ver tres sitios en el ETC respiratorio que funcionan como bombas H+. En estos sitios, el cambio negativo en la energía libre de transferencia de electrones es grande y se acopla a la acción de una bomba. El resultado es que los protones se acumulan fuera de la matriz de la mitocondria. Debido a que la membrana mitocondrial externa es libremente permeable a los protones, el gradiente electroquímico está vigente entre el citoplasma y la matriz mitocondrial. El flujo de protones hacia la matriz mitocondrial a través de complejos de ATP sintasa en forma de piruleta libera la energía libre de gradiente que se aprovecha como energía química.
164 Bombas de protones almacenan energía libre del ETC en Gradientes de protones


