9.2: Regulación Transcripcional Eucariota
- Page ID
- 52932
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Al igual que con casi todas las comparaciones con los sistemas procariotas, la regulación de la transcripción eucariota es mucho más compleja que el control de genes procariotas, aunque aún se basa en mecanismos similares de activadores y represores. Sin embargo, no hay equivalente eucariótico cercano a los operones: los genes eucariotas siempre se transcriben uno por ARNm. En el capítulo anterior se describió la formación de un complejo de preiniciación de factores de transcripción para la ARN polimerasa II. Estos factores de transcripción (por ejemplo, TFIID, TFIIH, etc.) se conocen como factores de transcripción generales, y son necesarios para la transcripción de cualquier gen a cualquier nivel. Sin embargo, también existen factores de transcripción específicos, generalmente denominados simplemente factores de transcripción (TF), que modulan la frecuencia de transcripción de genes particulares. Algunos elementos aguas arriba y sus TFs asociados son bastante comunes, mientras que otros son específicos de genes o familias génicas. Un ejemplo del primero es el elemento aguas arriba AACCAAT y su factor de transcripción asociado, CP1. Otro factor de transcripción, Sp1, es igualmente común, y se une a una secuencia consenso de ACGCCC. Ambos se utilizan en el control del gen de la beta-globina, junto con factores de transcripción más específicos, como GATA-1, que se une a un AAGTATCACT consenso y se produce principalmente en las células sanguíneas. Esto ilustra otra opción encontrada en el control eucariota que no se encuentra en procariotas: la expresión génica específica de tejido. Los genes, al estar en el ADN, están técnicamente disponibles para todas y cada una de las células, pero obviamente las necesidades de una célula sanguínea difieren mucho de las necesidades de una célula hepática, o una neurona. Por lo tanto, cada célula puede producir factores de transcripción que son específicos de su tipo de célula o tejido. Estos factores de transcripción pueden entonces permitir o reprimir la expresión de múltiples genes que ayudan a este tipo celular en particular, asumiendo que todos tienen las secuencias de reconocimiento para los TF. Estas secuencias de reconocimiento también se conocen como elementos de respuesta (RE).
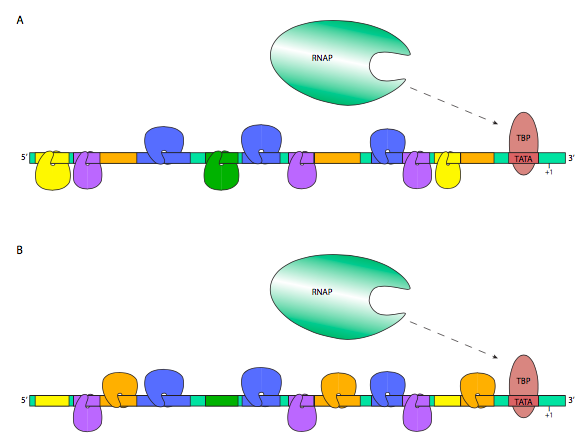
Muy a menudo, una combinación de muchos factores de transcripción, tanto potenciadores como silenciadores, es responsable de la tasa de expresión final de un gen eucariota dado. Esto se puede hacer de manera graduada, en la que la expresión se vuelve más fuerte o más débil a medida que se unen más potenciadores o silenciadores, respectivamente, o puede ser un modo binario de control, en el que se requiere un grupo bien definido de TF para activar la transcripción, y faltar solo uno puede apagarse efectivamente transcripción en su totalidad. En el primer caso, los TFs activadores generalmente se unen a los GTFs o ARN Polimerasa II directamente para ayudarlos a reconocer el promotor de manera más eficiente o estable, mientras que los TFs reprimidos pueden unirse a los TFs activadores, o a los GTFs o RNAP II, en la prevención del reconocimiento del promotor, o desestabilizando el RNAP II complejo de preiniciación. En el segundo caso, la activación depende de la construcción de un potenciosoma, en el que factores de transcripción y elementos de andamiaje proteico y coactivadores se unen para posicionar y estabilizar el complejo de preiniciación y RNAP II sobre el promotor. El coactivador más prominente y casi ubicuo se llama Mediator, y se une al CTD de la subunidad β' de la ARN polimerasa II y también a una variedad de factores de transcripción.
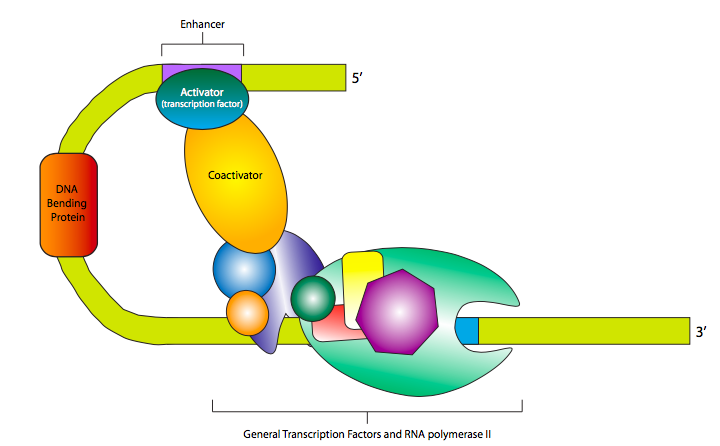
Los factores de transcripción eucariotas, aunque variados, suelen contener al menos uno de los siguientes motivos de factores de transcripción: dedos de zinc, cremalleras de leucina, dominios básicos de hélice-bucle-hélice, dominios de región de homología Rel, o una variación de los mismos.
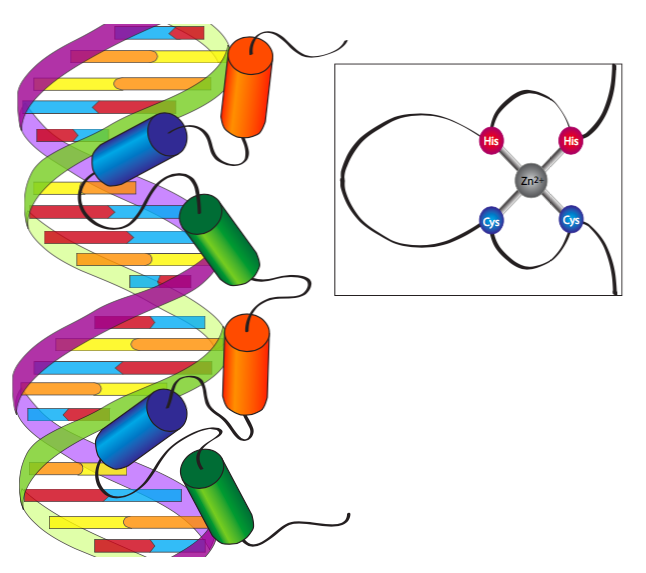
El motivo de dedo de zinc fue el primer dominio de unión al ADN que se descubrió, y se encontró en un factor de transcripción general asociado a la ARN polimerasa III. La estructura inicial encontrada fue un motivo repetitivo de ~30 aminoácidos con dos restos Cys invariantes y dos His invariantes que juntos se unen a un ion Zn 2+ y así juntan un lazo apretado o “dedo” de residuos básicos potencialmente de unión al ADN. El dedo básico se une al surco mayor del ADN, con las características exactas de coincidencia de secuencia determinadas por la topología de los residuos particulares que componen el dedo. Aunque la mayoría de los motivos de unión al ADN insertan un dominio α-helicoidal cargado positivamente en el surco mayor del ADN, las proteínas de dedos de zinc son las únicas que combinan varios de estos motivos para interactuar con el ADN en varios sitios secuenciales.
Además del primer tipo de sitio de unión a Zn 2+ descrito con dos Cys y dos His (Cys 2-His 2), hay dos variaciones principales a tener en cuenta. El primero es el tipo Cys 2-Cys 2, el cual es característico de los factores de transcripción del receptor de esteroides como el receptor de glucocorticoides o el receptor de estrógenos. Los consideraremos con más detalle más adelante con la discusión de la transducción de señales intracelulares, pero por ahora, la idea general es que los receptores de hormonas esteroideas inactivados se encuentren en el citoplasma, donde entran en contacto y se unen a su molécula hormonal afín. Luego se translocan al núcleo, donde dimerizan y son capaces de actuar como factores de transcripción. La segunda variación importante del dedo de zinc es el binuclear Cys 6, que lleva seis residuos de Cys para crear una “cesta” ligeramente más grande en la que se mantienen dos iones Zn 2+, en lugar de solo uno. El ejemplo mejor estudiado de este tipo de proteína con dedos de zinc es GAL4, un factor de transcripción metabólica de levaduras.
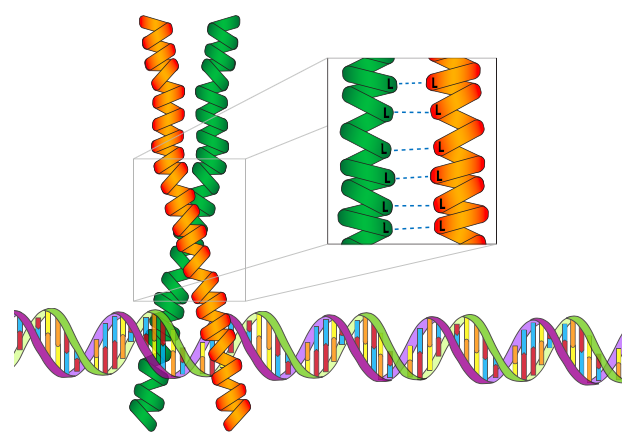
El siguiente motivo es la cremallera de leucina. Aunque este es un motivo común para los factores de transcripción, es importante señalar que a diferencia del dedo de zinc, la cremallera de leucina en sí no es un motivo de unión al ADN. Más bien, es un motivo de dimerización de proteínas, y determina la forma en que interactúan dos subunidades proteicas. Sin embargo, la cremallera de leucina es un motivo estructural común en los factores de transcripción. Funciona a través de dominios opuestos de aminoácidos hidrófobos regularmente espaciados, particularmente leucinas, que son muy efectivos para mantener juntas las dos subunidades en el ambiente acuoso de la célula. Las leucinas se encuentran en cada posición de residuo 7 de un dominio α-helicoidal, lo que lleva a una superestructura de bobina enrollada cuando dos subunidades interactúan. Los dominios de unión al ADN (+) cargados de estas proteínas suelen ser N-terminales a las cremalleras de leucina, como en el caso de la categoría BZip de proteínas de cremallera de leucina (el nombre significa cremallera de leucina de región básica).
Los dominios bHLH o hélice-bucle-hélice básicos parecen ser elaboraciones sobre el tema de la cremallera de leucina. En este caso, la región N-terminal es altamente básica, lo que la hace ideal para interactuar con el ADN, y este dominio básico, que también es helicoidal, conduce a la primera hélice (H1) del motivo, que luego se conecta por un bucle no helicoidal de aminoácidos, conduciendo a una segunda región helicoidal (H2). Más allá del bHLH, estos factores de transcripción pueden fusionarse en un motivo de cremallera de leucina u otro dominio de interacción proteica para la dimerización. Aunque el dominio de unión primario es N-terminal a H1, los dominios H1 también parecen desempeñar un papel en la unión del surco principal del ADN. [Ejemplo myc]
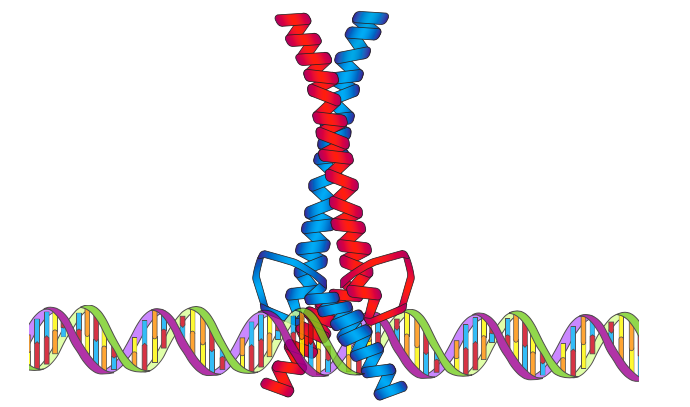
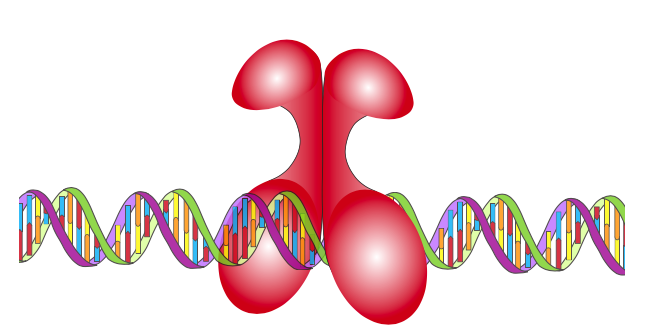
NF-kB (factor nuclear kB) es un factor de transcripción ubicuo descubierto (y más notable) en el sistema inmune. Cuando está activo, es un heterodímero, con ambas subunidades que contienen una región de homología Rel (RHR). Rel es un oncogén, y los RHR se nombran por su similitud con el rel previamente secuenciado. Los dominios RHR se unen al ADN con extraordinaria afinidad, debido en parte a tener bucles ve para el contacto con el ADN por subunidad. Al igual que con los otros tipos de factores de transcripción, algunas proteínas que contienen RHR son represoras, mientras que otras son activadoras.
La regulación del NF-kB es bastante interesante: una vez que está en el núcleo, generalmente es activa. No obstante, es, como casi todas las proteínas celulares, elaboradas en el citoplasma. Los inhibidores de NF-kB (IkB) también residen en el citoplasma, y actúan uniéndose al NF-kB y cubriendo la señal de localización nuclear que permite su importación al núcleo. Así secuestrado, el NF-kB debe permanecer inactivo en el citoplasma hasta que algún estímulo active la IkB quinasa, que fosforila la IkB y conduce a ubiquitinación y degradación, liberando finalmente el NF-kB de sus enlaces.
Debido a que puede movilizarse rápidamente (en comparación con sintetizar nueva proteína), el NF-kB se considera un factor de transcripción de respuesta rápida que a menudo se usa para comenzar la expresión de un gen necesario poco después de que haya sido “ordenado” por una señal, ya sea extracelular o intracelular. No es sorprendente que para un factor descubierto en el sistema inmunitario, se active en respuesta a antígenos bacterianos y virales, así como a otros tipos de estrés o insulto celular.
Además de la regulación relativamente a corto plazo de la expresión génica controlada por factores de transcripción de unión a elementos reguladores, también hay métodos más fuertes para bloquear un gen para evitar su expresión. En el capítulo 7 se discutió la acetilación y desacetilación de histonas como método para disminuir y aumentar su afinidad por el ADN. Esto se puede controlar (Figura\(\PageIndex{11}\) B) mediante el reclutamiento de histona desacetilasa (HDAC) a genes particulares a través de complejos represor/co-represor. La desacetilasa fuerza un fuerte enrollamiento del ADN dirigido a las histonas, impidiendo el acceso por ARN polimerasas o factores de transcripción generales.
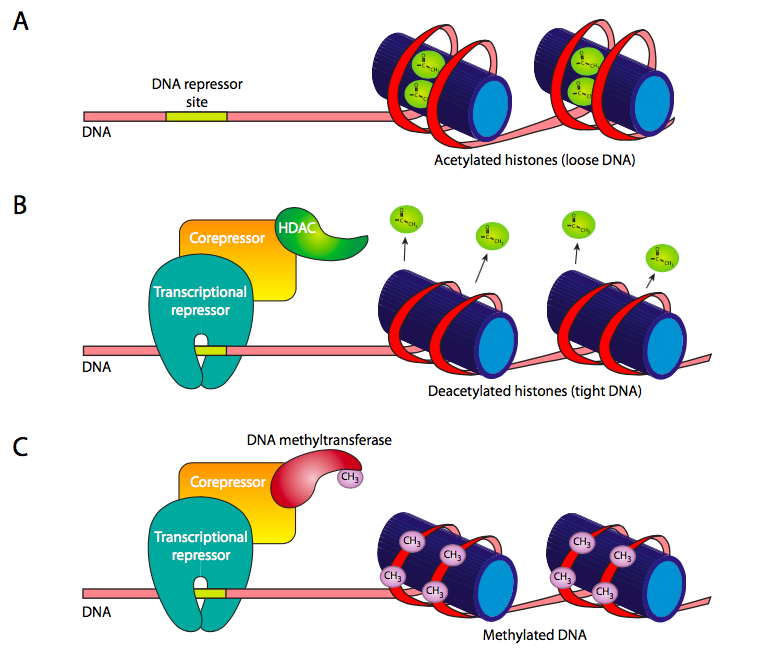
Otro reclutador de HDAC son las proteínas MBD, que se unen al ADN metilado. La metilación del ADN en mamíferos suele ocurrir en secuencias de dinucleótidos CpG. Esta metilación parece tener el efecto de bloquear el acceso de factores de transcripción y enzimas al ADN. Puede hacerlo directamente, o reclutando proteínas MBD (dominio de unión a metil-CpG). En cualquier caso, la metilación es un método a largo plazo para bloquear genes, y es el mecanismo para desactivar genes que nunca se usarían en un tipo celular en particular (por ejemplo, hemoglobina en neuronas).


