8.3: Respiración celular
- Page ID
- 54682
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Objetivos de aprendizaje
- Comparar y contrastar la ubicación y función del sistema de transporte de electrones en una célula procariota y una célula eucariota
- Comparar y contrastar las diferencias entre el nivel de sustrato y la fosforilación oxidativa
- Explicar la relación entre la quimiósmosis y la fuerza motriz de protones
- Describir la función y ubicación de ATP sintasa en una célula procariota versus eucariota
- Comparar y contrastar la respiración aeróbica y anaeróbica
Acabamos de discutir dos vías en el catabolismo de la glucosa, la glucólisis y el ciclo de Krebs, que generan ATP por fosforilación a nivel de sustrato. Sin embargo, la mayor parte del ATP se genera durante un proceso separado llamado fosforilación oxidativa, que ocurre durante la respiración celular. La respiración celular comienza cuando los electrones se transfieren desde NADH y FADH 2 —hechos en la glucólisis, la reacción de transición, y el ciclo de Krebs— a través de una serie de reacciones químicas a un aceptor de electrones inorgánico final (ya sea oxígeno en la respiración aeróbica o moléculas inorgánicas no oxigenadas en respiración anaeróbica). Estas transferencias de electrones tienen lugar en la parte interna de la membrana celular de células procariotas o en complejos proteicos especializados en la membrana interna de las mitocondrias de células eucariotas. La energía de los electrones se recolecta para generar un gradiente electroquímico a través de la membrana, que se utiliza para producir ATP por fosforilación oxidativa.
Sistema de transporte de electrones
El sistema de transporte de electrones (ETS) es el último componente involucrado en el proceso de respiración celular; comprende una serie de complejos proteicos asociados a la membrana y portadores de electrones accesorios móviles asociados. El transporte de electrones es una serie de reacciones químicas que se asemejan a una brigada de baldes en que los electrones de NADH y FADH 2 pasan rápidamente de un portador de electrones ETS al siguiente. Estos portadores pueden pasar electrones en el ETS debido a su potencial redox. Para que una proteína o sustancia química acepte electrones, debe tener un potencial redox más positivo que el donador de electrones. Por lo tanto, los electrones se mueven de portadores de electrones con más potencial redox negativo a aquellos con más potencial redox positivo. Las cuatro clases principales de portadores de electrones involucrados en los sistemas de transporte de electrones eucariotas y procariotas son los citocromos, flavoproteínas, proteínas de hierro-azufre y las quinonas.
En la respiración aeróbica, el aceptor de electrones final (es decir, el que tiene el potencial redox más positivo) al final del ETS es una molécula de oxígeno (O 2) que se reduce a agua (H 2 O) por el portador de ETS final. Este portador de electrones, la citocromo oxidasa, difiere entre tipos bacterianos y puede ser utilizado para diferenciar bacterias estrechamente relacionadas para diagnósticos. Por ejemplo, el oportunista gramnegativo Pseudomonas aeruginosa y el gramnegativo Vibrio cholerae causante de cólera utilizan citocromo c oxidasa, la cual puede ser detectada por la prueba de oxidasa, mientras que otras Enterobacteriaceae gramnegativas, como E. coli, son negativas para esto prueba porque producen diferentes tipos de citocromo oxidasa.
Hay muchas circunstancias en las que la respiración aeróbica no es posible, incluyendo una o más de las siguientes:
- La célula carece de genes que codifican una citocromo oxidasa apropiada para transferir electrones al oxígeno al final del sistema de transporte de electrones.
- La célula carece de genes que codifican enzimas para minimizar los efectos severamente dañinos de los peligrosos radicales de oxígeno producidos durante la respiración aeróbica, como el peróxido de hidrógeno (H 2 O 2) o el superóxido\((\ce{O2-})\).
- La célula carece de una cantidad suficiente de oxígeno para llevar a cabo la respiración aeróbica.
Una posible alternativa a la respiración aeróbica es la respiración anaeróbica, utilizando una molécula inorgánica distinta al oxígeno como aceptor final de electrones. Existen muchos tipos de respiración anaeróbica que se encuentran en bacterias y arqueas. Los desnitrificadores son bacterias importantes del suelo que utilizan nitrato\((\ce{NO3-})\) y nitrito\((\ce{NO2-})\) como aceptores finales de electrones, produciendo gas nitrógeno (N 2). Muchas bacterias que respiran aeróbicamente, incluyendo E. coli, cambian a usar nitrato como aceptor final de electrones y producen nitrito cuando los niveles de oxígeno se han agotado.
Los microbios que utilizan respiración anaeróbica suelen tener un ciclo de Krebs intacto, por lo que estos organismos pueden acceder a la energía de las moléculas NADH y FADH 2 formadas. Sin embargo, los respiradores anaeróbicos utilizan portadores ETS alterados codificados por sus genomas, incluyendo distintos complejos para la transferencia de electrones a sus aceptores finales de electrones. Se generan gradientes electroquímicos más pequeños a partir de estos sistemas de transferencia de electrones, por lo que se forma menos ATP a través de la respiración anaerobia.
Ejercicio\(\PageIndex{1}\)
¿Tanto la respiración aeróbica como la respiración anaeróbica utilizan una cadena de transporte de electrones?
Quimósmosis, fuerza motriz de protones y fosforilación oxidativa
En cada transferencia de un electrón a través del ETS, el electrón pierde energía, pero con algunas transferencias, la energía se almacena como energía potencial utilizándola para bombear iones de hidrógeno (H +) a través de una membrana. En las células procariotas, H + se bombea al exterior de la membrana citoplásmica (llamado espacio periplásmico en bacterias gramnegativas y grampositivas), y en las células eucariotas, se bombean desde la matriz mitocondrial a través de la membrana mitocondrial interna hacia el espacio intermembrana. Hay una distribución desigual de H + a través de la membrana que establece un gradiente electroquímico debido a que los iones H + están cargados positivamente (eléctricos) y hay una mayor concentración (química) en un lado de la membrana. Este gradiente electroquímico formado por la acumulación de H + (también conocido como protón) en un lado de la membrana en comparación con el otro se denomina fuerza motriz protónica (PMF). Debido a que los iones involucrados son H +, también se establece un gradiente de pH, siendo más ácido el lado de la membrana que tiene la mayor concentración de H +. Más allá del uso del PMF para hacer ATP, como se discute en este capítulo, el PMF también puede ser utilizado para impulsar otros procesos energéticamente desfavorables, incluyendo el transporte de nutrientes y la rotación de flagelos para la motilidad.
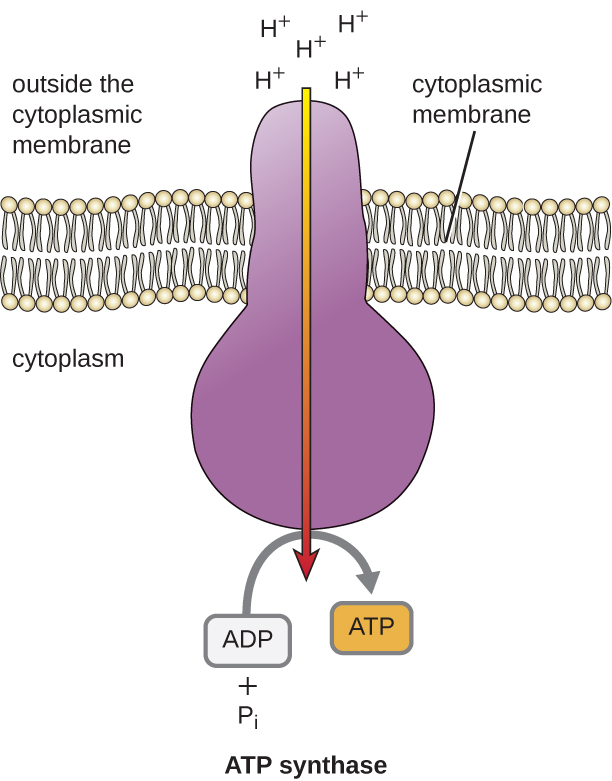
La energía potencial de este gradiente electroquímico generado por el ETS hace que el H + se difunda a través de una membrana (la membrana plasmática en células procariotas y la membrana interna en las mitocondrias en células eucariotas). Este flujo de iones de hidrógeno a través de la membrana, llamado quimiósmosis, debe ocurrir a través de un canal en la membrana a través de un complejo enzimático unido a membrana llamado ATP sintasa (Figura\(\PageIndex{1}\)). La tendencia al movimiento de esta manera es muy parecida al agua acumulada en un lado de una presa, moviéndose a través de la presa cuando se abre. La ATP sintasa (como una combinación de la ingesta y el generador de una presa hidroeléctrica) es una proteína compleja que actúa como un pequeño generador, girando por la fuerza del H + difundiéndose a través de la enzima, bajando su gradiente electroquímico desde donde hay muchos H + mutuamente repelentes a donde hay menos H +. En las células procariotas, H + fluye desde el exterior de la membrana citoplasmática hacia el citoplasma, mientras que en las mitocondrias eucariotas, H + fluye desde el espacio intermembrana a la matriz mitocondrial. El giro de las partes de esta máquina molecular regenera ATP a partir de ADP y fosfato inorgánico (P i) por fosforilación oxidativa, un segundo mecanismo para hacer ATP que cosecha la energía potencial almacenada dentro de un gradiente electroquímico.
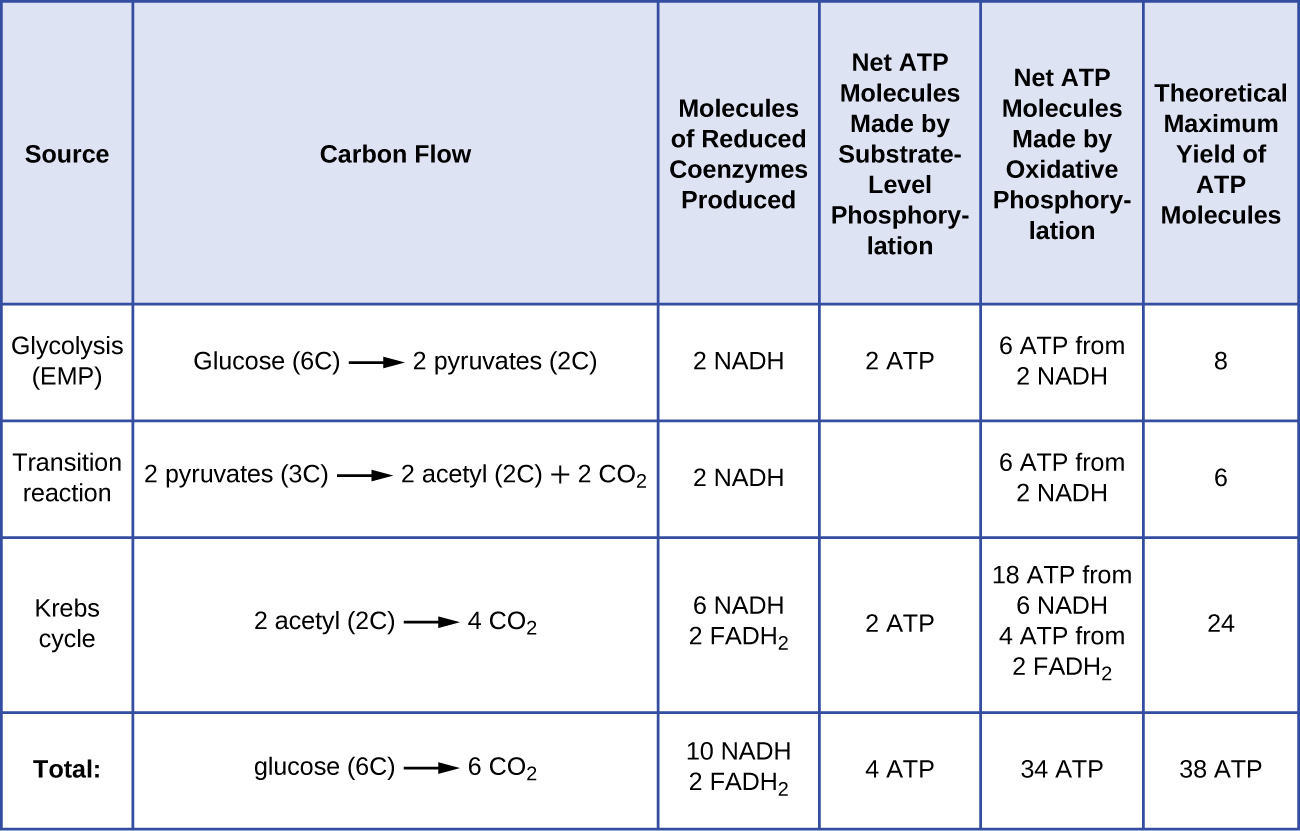
El número de moléculas de ATP generadas a partir del catabolismo de la glucosa varía. Por ejemplo, el número de iones hidrógeno que los complejos del sistema de transporte de electrones pueden bombear a través de la membrana varía entre diferentes especies de organismos. En la respiración aeróbica en mitocondrias, el paso de electrones de una molécula de NADH genera suficiente fuerza motriz protónica para formar tres moléculas de ATP por fosforilación oxidativa, mientras que el paso de electrones de una molécula de FADH 2 genera suficiente fuerza motriz protónica para producir solo dos Moléculas de ATP. Así, las 10 moléculas de NADH producidas por glucosa durante la glucólisis, la reacción de transición y el ciclo de Krebs transportan suficiente energía para producir 30 moléculas de ATP, mientras que las dos moléculas de FADH 2 producidas por glucosa durante estos procesos proporcionan suficiente energía para producir cuatro moléculas de ATP. En general, el rendimiento máximo teórico de ATP obtenido durante la respiración aeróbica completa de la glucosa es de 38 moléculas, siendo cuatro hechas por fosforilación a nivel de sustrato y 34 por fosforilación oxidativa (Figura\(\PageIndex{2}\)). En realidad, el rendimiento total de ATP suele ser menor, variando de una a 34 moléculas de ATP, dependiendo de si la célula está utilizando respiración aeróbica o respiración anaeróbica; en las células eucariotas, se gasta algo de energía para transportar intermedios desde el citoplasma hacia las mitocondrias, afectando el rendimiento de ATP.
La figura\(\PageIndex{2}\) resume los rendimientos máximos teóricos de ATP de diversos procesos durante la respiración aeróbica completa de una molécula de glucosa.
Ejercicio\(\PageIndex{1}\)
¿Cuáles son las funciones de la fuerza motriz protónica?
Resumen
- La mayor parte del ATP generado durante la respiración celular de la glucosa se produce por fosforilación oxidativa.
- Un sistema de transporte de electrones (ETS) está compuesto por una serie de complejos proteicos asociados a la membrana y portadores de electrones accesorios móviles asociados. El ETS está incrustado en la membrana citoplasmática de los procariotas y la membrana mitocondrial interna de los eucariotas.
- Cada complejo ETS tiene un potencial redox diferente, y los electrones se mueven de portadores de electrones con más potencial redox negativo a aquellos con más potencial redox positivo.
- Para llevar a cabo la respiración aeróbica, una célula requiere oxígeno como aceptor final de electrones. Una célula también necesita un ciclo completo de Krebs, una citocromo oxidasa apropiada y enzimas de desintoxicación con oxígeno para prevenir los efectos nocivos de los radicales de oxígeno producidos durante la respiración aeróbica.
- Los organismos que realizan respiración anaeróbica utilizan portadores alternativos del sistema de transporte de electrones para la transferencia final de electrones a los aceptores finales de electrones no oxigenados.
- Los microbios muestran una gran variación en la composición de sus sistemas de transporte de electrones, los cuales pueden ser utilizados con fines diagnósticos para ayudar a identificar ciertos patógenos.
- A medida que los electrones pasan del NADH y el FADH 2 a través de un ETS, el electrón pierde energía. Esta energía se almacena a través del bombeo de H + a través de la membrana, generando una fuerza motriz protónica.
- La energía de esta fuerza motriz protónica se puede aprovechar permitiendo que los iones de hidrógeno se difundan de nuevo a través de la membrana mediante la quimiósmosis usando ATP sintasa. A medida que los iones de hidrógeno se difunden a través de su gradiente electroquímico, los componentes de la ATP sintasa giran, produciendo ATP a partir de ADP y P i por fosforilación oxidativa.
- La respiración aeróbica forma más ATP (un máximo de 34 moléculas de ATP) durante la fosforilación oxidativa que la respiración anaeróbica (entre una y 32 moléculas de ATP).


