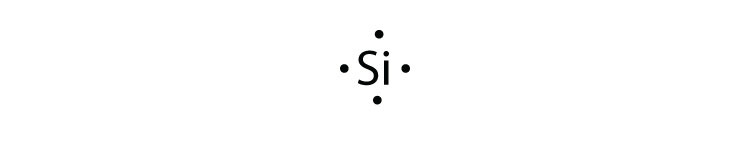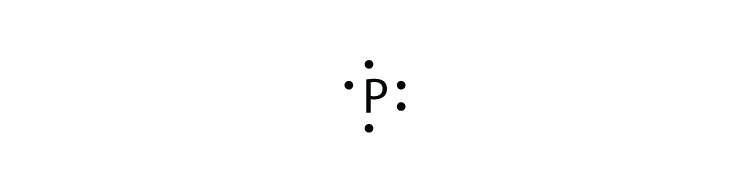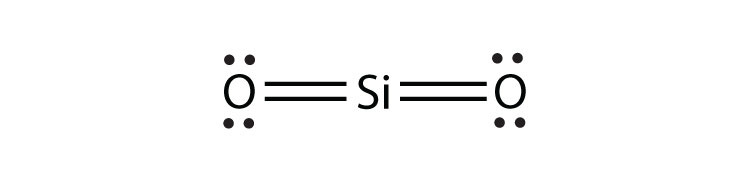9.E: Enlaces Químicos (Ejercicios)
- Page ID
- 74899
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)9.2: Diagramas de punto electrónico de Lewis
- Explica por qué los dos primeros puntos en un diagrama de puntos electrónicos de Lewis se dibujan en el mismo lado del símbolo atómico.
- ¿Es necesario que el primer punto alrededor de un símbolo atómico vaya a un lado particular del símbolo atómico?
- ¿Qué columna de la tabla periódica tiene diagramas de puntos electrónicos de Lewis con dos electrones?
- ¿Qué columna de la tabla periódica tiene diagramas de puntos electrónicos de Lewis que tienen seis electrones en ellos?
- Dibuja el diagrama de puntos electrónicos de Lewis para cada elemento.
- estroncio
- silicio
- Dibuja el diagrama de puntos electrónicos de Lewis para cada elemento.
- Krypton
- azufre
- Dibuja el diagrama de puntos electrónicos de Lewis para cada elemento.
- titanio
- fósforo
- Dibuja el diagrama de puntos electrónicos de Lewis para cada elemento.
- bromo
- galio
- Dibuja el diagrama de puntos electrónicos de Lewis para cada ion.
- Mg 2+
- S 2−
- Dibuja el diagrama de puntos electrónicos de Lewis para cada ion.
- En +
- Br −
- Dibuja el diagrama de puntos electrónicos de Lewis para cada ion.
- Fe 2+
- N 3−
- Dibuja el diagrama de puntos electrónicos de Lewis para cada ion.
- H +
- H −
RESPUESTAS
- Los dos primeros electrones en una capa de valencia son electrones s, que están emparejados.
- la segunda columna de la tabla periódica
-
-
-
- Mg 2+
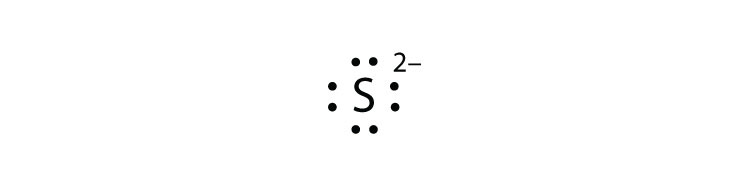
-
- Fe 2+

9.3: Transferencia de Electrones - Enlaces Iónicos
- Comentar sobre la posible formación del ion K 2+. ¿Por qué es poco probable su formación?
-
Comentar sobre la posible formación del ion Cl 2−. ¿Por qué es poco probable su formación?
-
¿Cuántos electrones tiene que perder un átomo de Ba para tener un octeto completo en su caparazón de valencia?
-
¿Cuántos electrones tiene que perder un átomo de Pb para tener un octeto completo en su caparazón de valencia?
-
¿Cuántos electrones tiene que ganar un átomo de Se para tener un octeto completo en su caparazón de valencia?
-
¿Cuántos electrones tiene que ganar un átomo de N para tener un octeto completo en su caparazón de valencia?
-
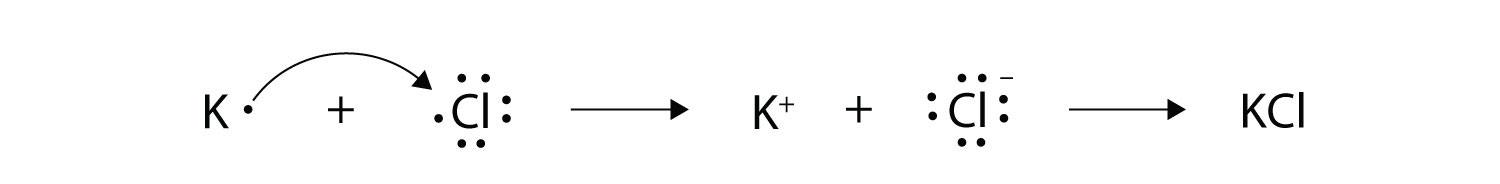
Con flechas, ilustran la transferencia de electrones para formar cloruro de potasio a partir de átomos de K y átomos de Cl.
-
Con flechas, ilustran la transferencia de electrones para formar sulfuro de magnesio a partir de átomos de Mg y átomos de S.
-
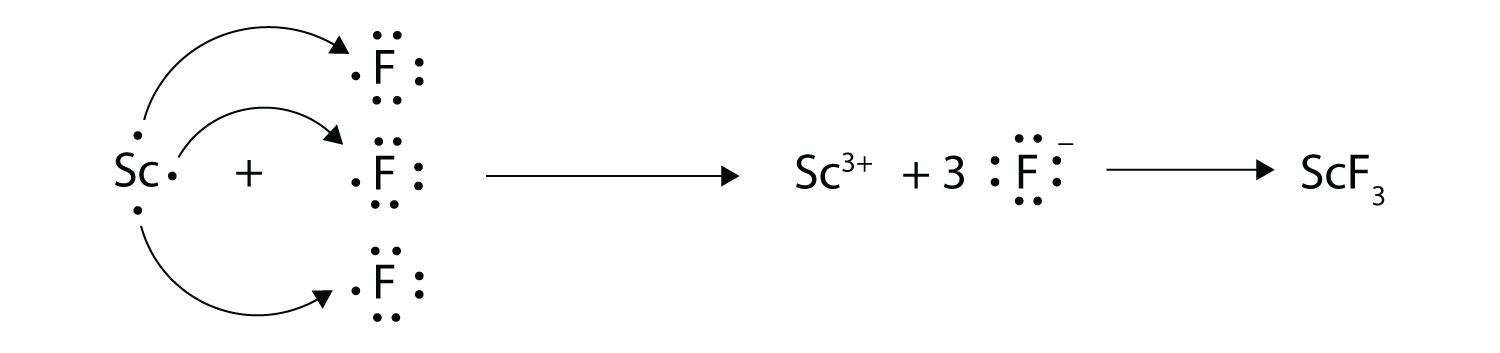
Con flechas, ilustran la transferencia de electrones para formar fluoruro de escandio a partir de átomos de Sc y átomos de F.
-
Con flechas, ilustran la transferencia de electrones para formar fosfuro de rubidio a partir de átomos de Rb y átomos de P.
-
¿Qué compuesto iónico tiene la energía de celosía más alta: Ki o MgO? ¿Por qué?
-
¿Qué compuesto iónico tiene la energía de celosía más alta, Ki o LiF? ¿Por qué?
- ¿Qué compuesto iónico tiene la energía de celosía más alta: Bas o MgO? ¿Por qué?
RESPUESTAS
- Es poco probable que se forme el ion K 2+ porque el ion K + ya satisface la regla del octeto y es bastante estable.
- dos
- dos
- MgO porque los iones tienen una carga de mayor magnitud
- MgO porque los iones son más pequeños
9.4: Enlaces covalentes
- ¿Cuántos electrones habrá en la capa de valencia de los átomos de H cuando haga un enlace covalente?
- ¿Cuántos electrones estarán en la capa de valencia de los átomos no H cuando hagan enlaces covalentes?
- ¿Cuál es el diagrama de puntos electrónicos Lewis de I 2? Circula los electrones alrededor de cada átomo para verificar que cada capa de valencia está llena.
- ¿Cuál es el diagrama de puntos electrónicos de Lewis de H 2 S? Circula los electrones alrededor de cada átomo para verificar que cada capa de valencia está llena.
- ¿Cuál es el diagrama de puntos electrónicos de Lewis de NCl 3? Circula los electrones alrededor de cada átomo para verificar que cada capa de valencia está llena.
- ¿Cuál es el diagrama de puntos electrónicos de Lewis de SiF 4? Circula los electrones alrededor de cada átomo para verificar que cada capa de valencia está llena.
- Dibuja el diagrama de puntos electrónicos de Lewis para cada sustancia.
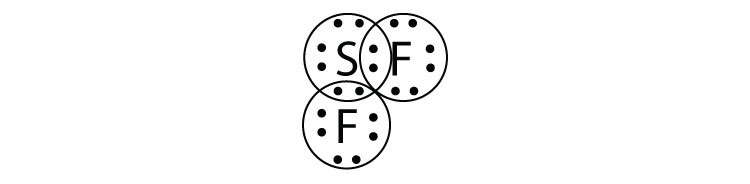
- SF 2
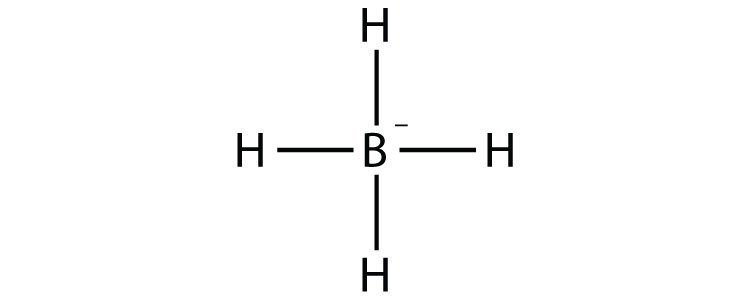
- BH 4 −
- Dibuja el diagrama de puntos electrónicos de Lewis para cada sustancia.
- PI 3
- OH −
- Dibuja el diagrama de puntos electrónicos de Lewis para cada sustancia.
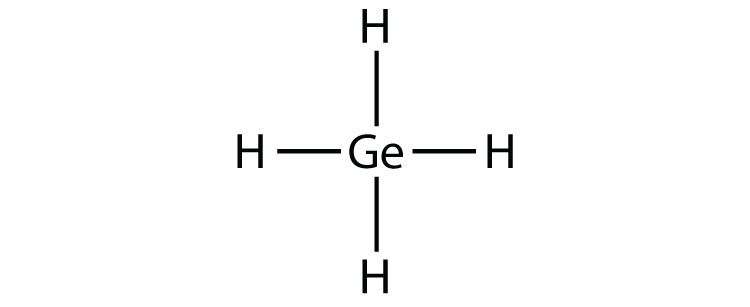
- GeH 4
- CLF
- Dibuja el diagrama de puntos electrónicos de Lewis para cada sustancia.
- ASf 3
- NH 4 +
- Dibuja el diagrama de puntos electrónicos de Lewis para cada sustancia. Es posible que se necesiten dobles o triples enlaces.
- SiO 2
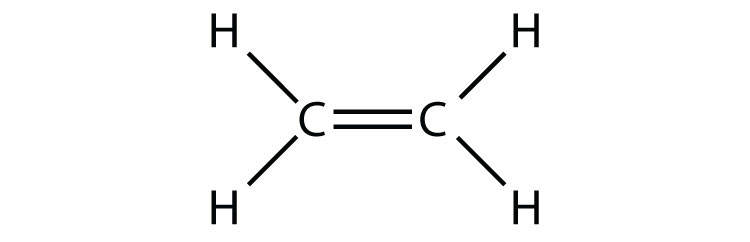
- C 2 H 4 (asumir dos átomos centrales)
- Dibuja el diagrama de puntos electrónicos de Lewis para cada sustancia. Es posible que se necesiten dobles o triples enlaces.
- CN −
- C 2 Cl 2 (asumir dos átomos centrales)
- Dibuja el diagrama de puntos electrónicos de Lewis para cada sustancia. Es posible que se necesiten dobles o triples enlaces.
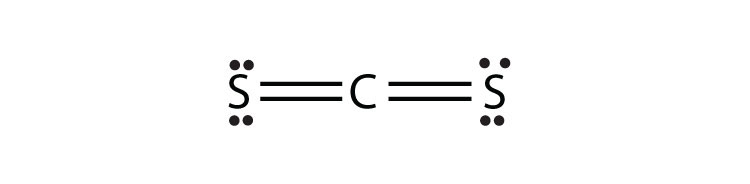
- CS 2
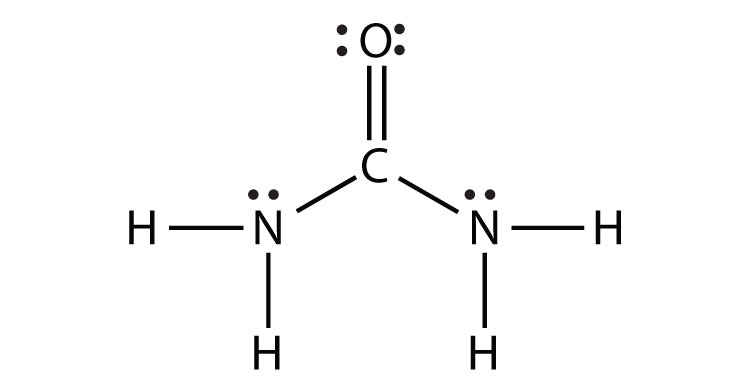
- NH 2 CONH 2 (supongamos que los átomos de N y C son los átomos centrales)
- Dibuja el diagrama de puntos electrónicos de Lewis para cada sustancia. Es posible que se necesiten dobles o triples enlaces.
- POCl
- HCOOH (supongamos que el átomo de C y un átomo de O son los átomos centrales)
RESPUESTAS
- dos
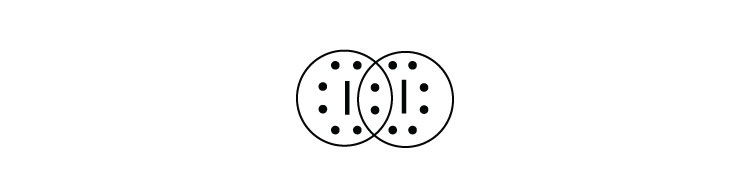
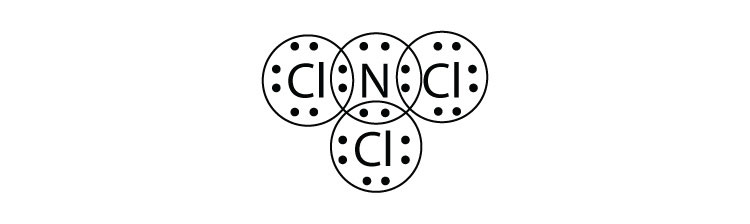
-
-
-
-
9.5: Otros aspectos de los enlaces covalentes
- Dé un ejemplo de un enlace covalente no polar. ¿Cómo sabes que es no polar?
- Dé un ejemplo de un enlace covalente polar. ¿Cómo sabes que es polar?
- ¿Cómo sabes qué lado de un enlace polar tiene la carga negativa parcial? Identificar el lado cargado negativamente de cada enlace polar.
- H—Cl
- H—S
- ¿Cómo sabes qué lado de un enlace polar tiene la carga positiva parcial? Identificar el lado cargado positivamente de cada enlace polar.
- H—Cl
- N-F
- Marcar el enlace entre los átomos dados como covalente no polar, covalente ligeramente polar, definitivamente covalente polar o probablemente iónico.
- H y C
- C y F
- K y F
- Marcar el enlace entre los átomos dados como covalente no polar, covalente ligeramente polar, definitivamente covalente polar o probablemente iónico.
- S y Cl
- P y O
- Cs y O
- ¿Qué enlace covalente es más fuerte, un enlace C-C o un enlace C-H?
- ¿Qué enlace covalente es más fuerte, un doble enlace O-O o un doble enlace N-N?
- Estimar el cambio de entalpía para esta reacción: N 2 + 3H 2 → 2NH 3 .Comience dibujando los diagramas de puntos electrónicos de Lewis para cada sustancia.
- Estimar el cambio de entalpía para esta reacción. Comienza dibujando los diagramas de puntos electrónicos de Lewis para cada sustancia: HN=NH + 2H 2 → 2NH 3
- Estimar el cambio de entalpía para esta reacción. Comienza dibujando los diagramas de puntos electrónicos de Lewis para cada sustancia: CH 4 + 2O 2 → CO 2 + 2H 2 O
- Estimar el cambio de entalpía para esta reacción. Comience dibujando los diagramas de puntos electrónicos de Lewis para cada sustancia: 4NH 3 + 3O 2 → 2N 2 + 6H 2 O
RESPUESTAS
- H—H; es no polar porque los dos átomos tienen las mismas electronegatividades (las respuestas variarán).
-
- Lado Cl
- Lado S
-
- covalente ligeramente polar
- definitivamente covalente polar
- probable iónica
- Enlace C—H
- −80 kJ
- −798 kJ
9.6: Violaciones a la Regla del Octeto
- ¿Por qué una molécula de electrones impares no puede satisfacer la regla del octeto?
- ¿Por qué un átomo de la segunda fila de la tabla periódica no puede formar moléculas de concha de valencia expandida?
- Dibuje un diagrama de puntos electrónicos de Lewis aceptable para estas moléculas que violen la regla del octeto.
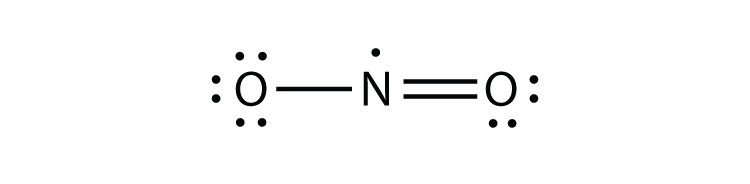
- NO 2
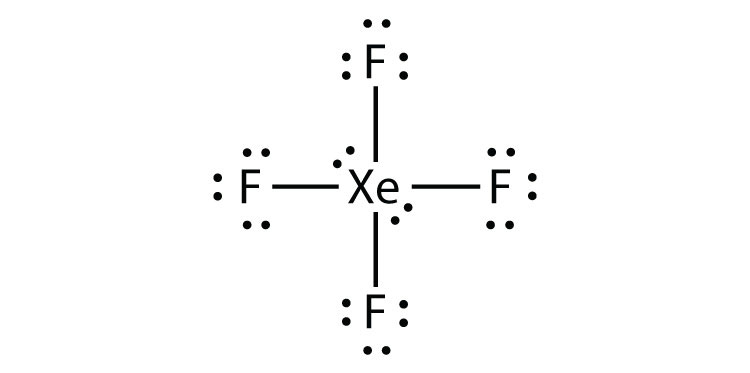
- XeF 4
- Dibuje un diagrama de puntos electrónicos de Lewis aceptable para estas moléculas que violen la regla del octeto.
- BCl 3
- ClO 2
- Dibuje un diagrama de puntos electrónicos de Lewis aceptable para estas moléculas que violen la regla del octeto.
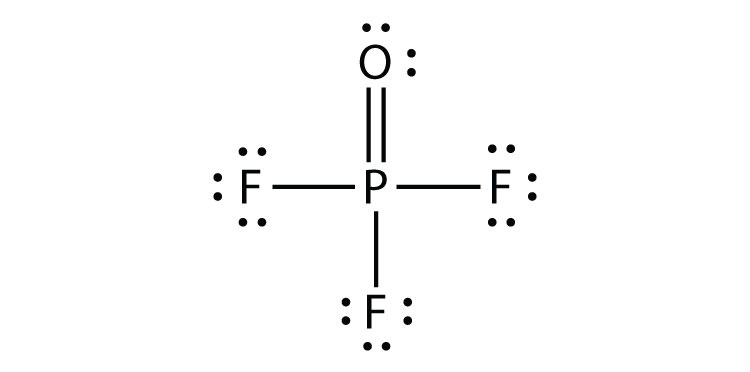
- POF 3
- CLF 3
- Dibuje un diagrama de puntos electrónicos de Lewis aceptable para estas moléculas que violen la regla del octeto.
- SF 4
- BeH 2
RESPUESTAS
- No hay manera de que todos los electrones puedan ser emparejados si hay un número impar de ellos.
-
-
9.7: Formas Moleculares
- ¿Cuál es la premisa básica detrás de VSEPR?
- ¿Cuál es la diferencia entre la geometría del grupo de electrones y la geometría molecular?
- Identificar la geometría del grupo electrónico y la geometría molecular de cada molécula.
- H 2 S
- POCl 3
- Identificar la geometría del grupo electrónico y la geometría molecular de cada molécula.
- CS 2
- H 2 S
- Identificar la geometría del grupo electrónico y la geometría molecular de cada molécula.
- HCN
- CCl 4
- Identificar la geometría del grupo electrónico y la geometría molecular de cada molécula.
- BI 3
- PH 3
- ¿Cuál es la geometría de cada especie?
- CN −
- PO 4 3−
- ¿Cuál es la geometría de cada especie?
- PO 3 3−
- NO 3 −
- ¿Cuál es la geometría de cada especie?
- COF 2
- C 2 Cl 2 (ambos átomos de C son átomos centrales y están unidos entre sí)
- ¿Cuál es la geometría de cada especie?
- CO 3 2−
- N 2 H 4 (ambos átomos de N son átomos centrales y están unidos entre sí)
RESPUESTAS
- Los pares de electrones se repelen entre sí.
-
- Geometría del grupo electrónico: tetraédrica; geometría molecular: doblada
- Geometría del grupo electrónico: tetraédrica; geometría molecular: tetraédrica
-
- geometría del grupo de electrones: lineal; geometría molecular: lineal
- Geometría del grupo electrónico: tetraédrica; geometría molecular: tetraédrica
-
- lineal
- tetraédrico
-
- plano trigonal
- lineal y lineal alrededor de cada átomo central
9.8 Ejercicios adicionales
- Explique por qué el hierro y el cobre tienen el mismo diagrama de puntos de electrones de Lewis cuando tienen diferentes números de electrones.
-
Nombra dos iones con el mismo diagrama de puntos de electrones de Lewis que el ion Cl −.
-
Con base en las tendencias conocidas, ¿qué compuesto iónico de la primera columna de la tabla periódica y la última columna de la tabla periódica debería tener la mayor energía de celosía?
-
Con base en las tendencias conocidas, ¿qué compuesto iónico de la primera columna de la tabla periódica y la última columna de la tabla periódica debería tener la energía de celosía más baja?
-
P 2 no es una forma estable de fósforo, pero si lo fuera, ¿cuál sería su probable diagrama de puntos de electrones de Lewis?
-
Se 2 no es una forma estable de selenio, pero si lo fuera, ¿cuál sería su probable diagrama de puntos de electrones de Lewis?
-
¿Cuáles son los diagramas de puntos electrónicos de Lewis de SO 2, SO 3 y SO 4 2−?
-
¿Cuáles son los diagramas de puntos electrónicos de Lewis de PO 3 3− y PO 4 3−?
-
¿Qué bono esperas que sea más polar, un bono O-H o un bono N-H?
-
¿Qué bono esperas que sea más polar, un bono O-F o un bono S—O?
-
Utilice energías de enlace para estimar el cambio de energía de esta reacción.
C 3 H 8 + 5O 2 → 3CO 2 + 4H 2 O -
Utilice energías de enlace para estimar el cambio de energía de esta reacción.
N 2 H 4 + O 2 → N 2 + 2H 2 O -
El etileno (C 2 H 4) tiene dos átomos centrales. Determinar la geometría alrededor de cada átomo central y la forma de la molécula general.
-
El peróxido de hidrógeno (H 2 O 2) tiene dos átomos centrales. Determinar la geometría alrededor de cada átomo central y la forma de la molécula general.
RESPUESTAS
- El hierro tiene d electrones que normalmente no se muestran en los diagramas de puntos electrónicos de Lewis.
-
-
LiF
-
-
Sería como N 2:
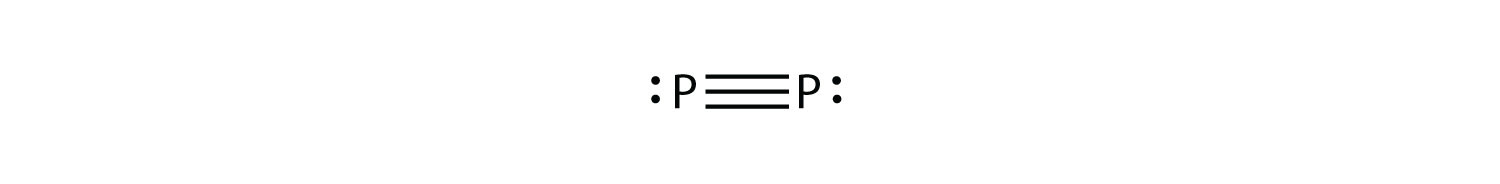
-
-
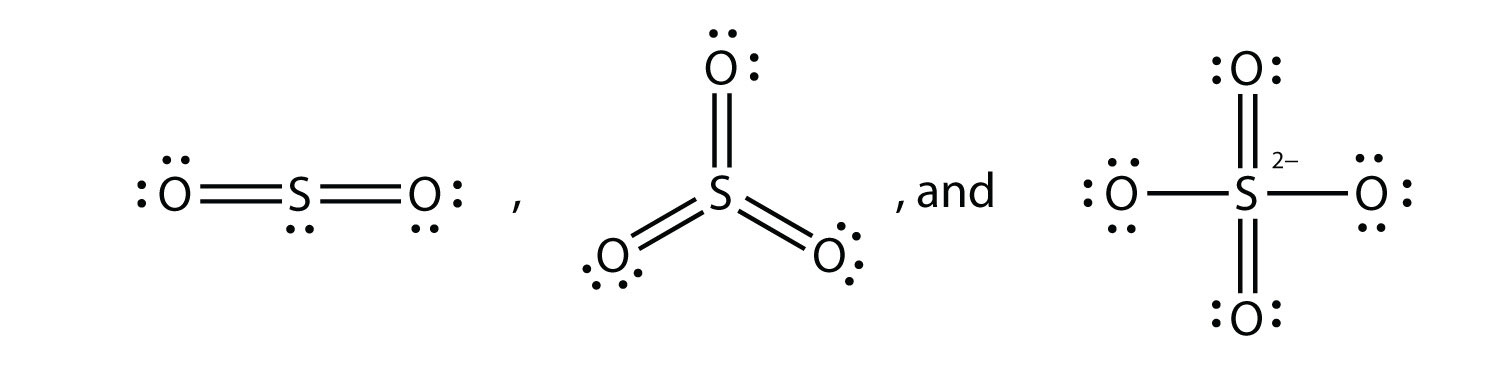
-
-
un enlace O—H
-
-
−2,000 kJ
-
-
plano trigonal alrededor de ambos átomos de C centrales