12.23: Ciclo de Nitrógeno
- Page ID
- 108102
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)
¿Qué pueden hacer las plantas de frijol que la mayoría de las otras plantas no pueden
No, no crecen tallos gigantes a las nubes. Las plantas de frijol y otras leguminosas (plantas que tienen sus semillas en vainas) pueden usar el nitrógeno en el aire para crecer. Se necesita la ayuda de bacterias amigas especiales en el suelo, y esta relación es única para las leguminosas.
El Ciclo del Nitrógeno
Como el agua y el carbono, el nitrógeno también se recicla repetidamente a través de la biosfera. Este proceso se llama el ciclo del nitrógeno. El nitrógeno es uno de los elementos más comunes en los organismos vivos. Es importante para crear tanto proteínas como ácidos nucleicos, como el ADN. El aire que respiramos es en su mayoría gas nitrógeno (N 2), pero, desafortunadamente, los animales y las plantas no pueden usar el nitrógeno cuando es un gas. De hecho, las plantas a menudo mueren por falta de nitrógeno incluso a través de que están rodeadas de abundante gas nitrógeno. El gas nitrógeno (N 2) tiene dos átomos de nitrógeno conectados por un triple enlace muy fuerte. La mayoría de las plantas y animales no pueden usar el nitrógeno en el gas nitrógeno porque no pueden romper ese triple enlace.
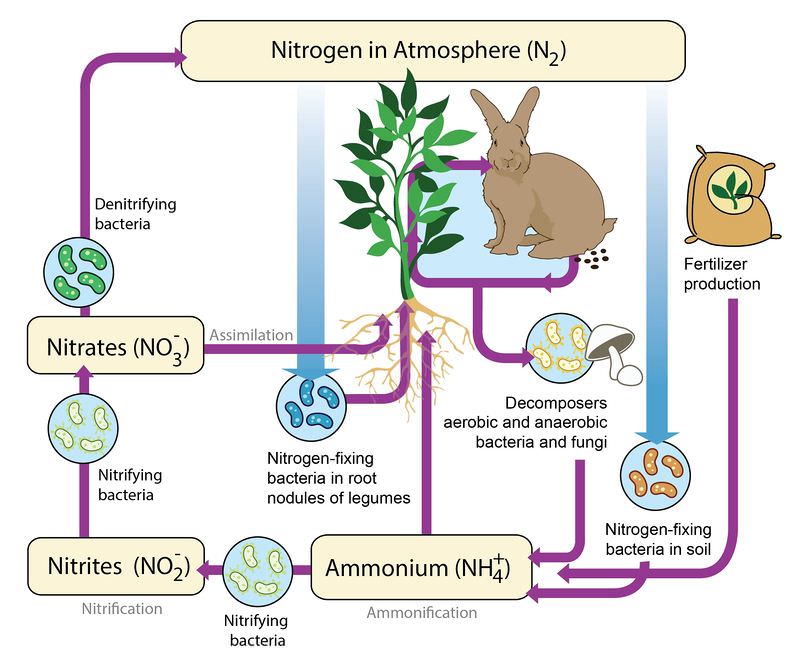
Para que las plantas hagan uso del nitrógeno, éste debe transformarse en moléculas que puedan utilizar. Esto se puede lograr de varias maneras diferentes (Figura a continuación).
- Relámpago: Cuando cae un rayo, el gas nitrógeno se transforma en nitrato (NO3-) que las plantas pueden usar.
- Fijación de nitrógeno: Las bacterias especiales fijadoras de nitrógeno también pueden transformar el gas nitrógeno en formas útiles. Estas bacterias viven en las raíces de las plantas de la familia de los guisantes. Convierten el gas nitrógeno en amonio (NH4+) (un proceso llamado amonificación). En ambientes acuáticos, las bacterias en el agua también pueden fijar el gas nitrógeno en amonio. El amonio puede ser utilizado por las plantas acuáticas como fuente de nitrógeno.
- El nitrógeno también es liberado al ambiente por organismos en descomposición o desechos en descomposición. Estos desechos liberan nitrógeno en forma de amonio.
El amonio en el suelo se puede convertir en nitrato mediante un proceso de dos etapas completado por dos tipos diferentes de bacterias. En forma de nitrato, el nitrógeno puede ser utilizado por las plantas a través del proceso de asimilación. Luego se pasa a los animales cuando comen las plantas.
Enviando Nitrógeno a la Atmósfera
Al volver a convertir el nitrato en gas nitrógeno, el proceso de desnitrificación, ocurre a través del trabajo de desnitrificar bacterias. Estas bacterias suelen vivir en pantanos y lagos. Ellos toman el nitrato y lo liberan de nuevo a la atmósfera como gas nitrógeno.
Al igual que el ciclo del carbono, las actividades humanas impactan en el ciclo del nitrógeno. Estas actividades humanas incluyen la quema de combustibles fósiles, que liberan gases de óxido de nitrógeno a la atmósfera. La liberación de óxido de nitrógeno de nuevo a la atmósfera conduce a problemas como la lluvia ácida.
Resumen
- El nitrógeno gaseoso se convierte en formas que pueden ser utilizadas por las plantas durante el proceso de fijación de nitrógeno.
- Las bacterias desnitrificantes vuelven a convertir el nitrato en nitrógeno gaseoso.
Revisar
- ¿Cómo utilizan los organismos vivos el nitrógeno?
- ¿Qué es la fijación de nitrógeno? Describa cómo sucede.
- ¿Cómo se convierte el nitrato en el suelo en gas nitrógeno?
- ¿Cómo se forma la lluvia ácida?

