10.4: Cohesión y Adhesión
- Page ID
- 128461
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)objetivos de aprendizaje
- Explicar los fenómenos de tensión superficial y acción capilar
Las fuerzas de atracción entre moléculas del mismo tipo se denominan fuerzas cohesivas. Los líquidos pueden, por ejemplo, mantenerse en recipientes abiertos porque las fuerzas cohesivas mantienen unidas las moléculas. Las fuerzas de atracción entre moléculas de diferentes tipos se denominan fuerzas adhesivas. Tales fuerzas hacen que las gotas líquidas se adhieran a los cristales de las ventanas, por ejemplo. En esta sección examinamos los efectos de las fuerzas cohesivas y adhesivas en líquidos.
Tensión superficial
La tensión superficial es una tendencia contractiva de la superficie de un líquido que le permite resistir una fuerza externa. Se muestra, por ejemplo, en la flotación de algunos objetos en la superficie del agua, aunque sean más densos que el agua, y en la capacidad de algunos insectos (por ejemplo, zancudas de agua) para correr sobre la superficie del agua. Esta propiedad es causada por la cohesión de moléculas similares y es responsable de muchos de los comportamientos de los líquidos.
Las fuerzas cohesivas entre las moléculas líquidas son responsables del fenómeno de la tensión superficial, como se muestra en. En la mayor parte del líquido, cada molécula es estirada por igual en todas las direcciones por las moléculas líquidas vecinas, lo que resulta en una fuerza neta de cero. Las moléculas en la superficie no tienen otras moléculas en todos los lados de ellas y por lo tanto son tiradas hacia adentro. Esto crea cierta presión interna y obliga a que las superficies líquidas se contraigan hasta el área mínima.

Diagrama de fuerzas de tensión superficial: Diagrama de las fuerzas sobre las moléculas de un líquido
La tensión superficial tiene la unidad de fuerza por unidad de longitud, o de energía por unidad de área. Las dos unidades son equivalentes. Sin embargo, cuando nos referimos a energía por unidad de área, utilizamos el término energía superficial, que es más general en cuanto se aplica tanto a sólidos como a líquidos.
Acción Capilar
La acción capilar, o capilaridad, es la capacidad de un líquido para fluir en espacios estrechos sin la ayuda de, y en oposición a, fuerzas externas como la gravedad. El efecto se puede observar en la extracción de líquidos entre los pelos de un pincel, en un tubo delgado, en materiales porosos como el papel, en algunos materiales no porosos como la fibra de carbono licuado, y en una celda. Ocurre debido a las fuerzas de atracción intermoleculares entre las superficies circundantes líquidas y sólidas. Si el diámetro del tubo es suficientemente pequeño, entonces la combinación de tensión superficial (que es causada por la cohesión dentro del líquido) y las fuerzas adhesivas entre el líquido y el recipiente actúan para levantar el líquido.
Con algunos pares de materiales, como el mercurio y el vidrio (ver), las fuerzas intermoleculares dentro del líquido superan las que se encuentran entre el sólido y el líquido, por lo que se forma un menisco convexo, y la acción capilar funciona a la inversa.
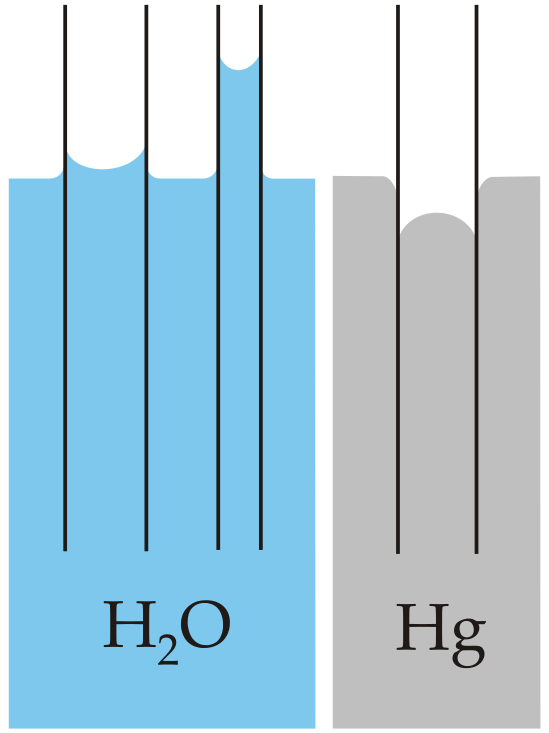
Capilaridad: Acción capilar del agua frente al mercurio, en cada caso con respecto al vidrio
Puntos Clave
- Las fuerzas de atracción entre moléculas del mismo tipo se denominan fuerzas cohesivas.
- Las fuerzas de atracción entre moléculas de diferentes tipos se denominan fuerzas adhesivas.
- La tensión superficial es una tendencia contractiva de la superficie de un líquido que le permite resistir una fuerza externa.
- La acción capilar, o capilaridad, es la capacidad de un líquido para fluir en espacios estrechos sin la ayuda de, y en oposición a, fuerzas externas como la gravedad.
Término Clave
- Presión: la cantidad de fuerza que se aplica sobre un área determinada dividida por el tamaño de esa área
- intermolecular: de una molécula a otra; entre moléculas
LICENCIAS Y ATRIBUCIONES
CONTENIDO CON LICENCIA CC, COMPARTIDO PREVIAMENTE
- Curación y Revisión. Proporcionado por: Boundless.com. Licencia: CC BY-SA: Atribución-CompartirIgual
CC CONTENIDO LICENCIADO, ATRIBUCIÓN ESPECÍFICA
- Colegio OpenStax, Colegio de Física. 17 de septiembre de 2013. Proporcionado por: OpenStax CNX. Ubicado en: http://cnx.org/content/m42197/latest/?collection=col11406/1.7. Licencia: CC BY: Atribución
- Colegio OpenStax, Colegio de Física. 17 de septiembre de 2013. Proporcionado por: OpenStax CNX. Ubicado en: http://cnx.org/content/m42197/latest/?collection=col11406/1.7. Licencia: CC BY: Atribución
- Tensión superficial. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Surface_Tension. Licencia: CC BY-SA: Atribución-CompartirIgual
- Colegio OpenStax, Colegio de Física. 17 de septiembre de 2013. Proporcionado por: OpenStax CNX. Ubicado en: http://cnx.org/content/m42197/latest/?collection=col11406/1.7. Licencia: CC BY: Atribución
- Acción capilar. Proporcionado por: Wikipedia. Ubicado en: http://en.Wikipedia.org/wiki/Capillary_action. Licencia: CC BY-SA: Atribución-CompartirIgual
- Tensión superficial. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Surface_Tension. Licencia: CC BY-SA: Atribución-CompartirIgual
- Adhesión. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Adhesión. Licencia: CC BY-SA: Atribución-CompartirIgual
- Cohesión (química). Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Cohesion_ (química). Licencia: CC BY-SA: Atribución-CompartirIgual
- Tensión superficial. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Surface_Tension. Licencia: CC BY-SA: Atribución-CompartirIgual
- intermolecular. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/intermolecular. Licencia: CC BY-SA: Atribución-CompartirIgual
- Presión. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/Pressure. Licencia: CC BY-SA: Atribución-CompartirIgual
- Archivo:Capillarity.svg - Wikipedia, la enciclopedia libre. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/w/index. php*title=file:capillarity.svg&page=1. Licencia: CC BY-SA: Atribución-CompartirIgual
- Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/w/index. php*title=file:wassermolek%C 3% Bcleintr%C 3% B6pfchen.svg&page=1. Licencia: Dominio Público: No Conocido Derechos de Autor


