3.6: Eficiencia Carnot
- Page ID
- 82065
Una expresión general para la eficiencia de un motor térmico se puede escribir como
\[ Efficiency = \dfrac{Work}{Heat \, Energy \, (hot)} \]
Sabemos que toda la energía que se pone en el motor tiene que salir ya sea como trabajo o calor residual. Por lo que el trabajo es igual a Calor a Alta temperatura menos Calor rechazado a Baja temperatura. Por lo tanto, esta expresión se convierte
\[ Efficiency = \dfrac{Q_{hot} - Q_{cold}}{Q_hot} \]
donde\( Q_{hot} \) es la entrada de calor a alta temperatura y\( Q_{cold} \) es el calor rechazado a baja temperatura. El símbolo\( \eta \) (letra griega eta) se utiliza a menudo para la eficiencia esta expresión se puede reescribir como:
\[ \eta ' \, (\%) = 1 - \dfrac{Q_{cold}}{Q_{hot}} * 100\% \]
La ecuación anterior se multiplica por 100 para expresar la eficiencia como porcentaje.
El ingeniero francés Sadi Carnot demostró que la relación de Q caliente a Q frío debe ser la misma que la relación de temperaturas de calor a alta temperatura y el calor rechazado a baja temperatura. Entonces esta ecuación, también llamada Carnot Efficiency, puede simplificarse como:
\[ \eta ' \, (\%) = 1 - \dfrac{T_{cold}}{T_{hot}} * 100\% \]
Nota
A diferencia de las ecuaciones anteriores, las posiciones de\( T_{cold} \) y\( T_{hot} \) se invierten.
La Eficiencia Carnot es la máxima eficiencia teórica que se puede obtener cuando el motor térmico está funcionando entre dos temperaturas:
- La temperatura a la que opera el reservorio de alta temperatura (T h ot).
- La temperatura a la que opera el depósito de baja temperatura (T c viejo).
En el caso de un automóvil, las dos temperaturas son:
- La temperatura de los gases de combustión dentro del motor (T h ot).
- La temperatura a la que se agotan los gases del motor (T frío).
El siguiente video explica cómo funcionan los motores de automóviles.
Entonces, ¿por qué deberíamos operar los automóviles con bajas eficiencias?
No es que no podamos lograr altas temperaturas, pero no tenemos los materiales del motor que puedan soportar la alta temperatura. De hecho, no dejamos que los gases del motor vayan al máximo que pueden ir incluso ahora y en su lugar tratamos de mantener el motor fresco haciendo circular el refrigerante.
Entonces estamos quitando el calor de los gases (bajando así la T caliente) y haciendo que el motor funcione a temperaturas más frías para que el motor esté protegido -pero bajando la eficiencia de un automóvil.
Información Adicional
Una analogía son los impuestos. Cuanto más dinero ganes (calor), más dinero se grava (frío), dejándote con menos dinero para llevar a casa (eficiencia). No obstante, si pudieras ganar más dinero (calor) y encontrar la manera de tener menos impuestos sacados (mejor material del motor), tendrías más dinero para llevar a casa (eficiencia).
La Figura 3.6.1 muestra dos escalas de temperatura. La escala etiquetada como “CALIENTE”, muestra el rango de temperaturas para la combustión de gases en un motor de automóvil. La báscula etiquetada como “FRÍO”, muestra el rango de temperaturas a las que se agotan los gases del motor del automóvil.
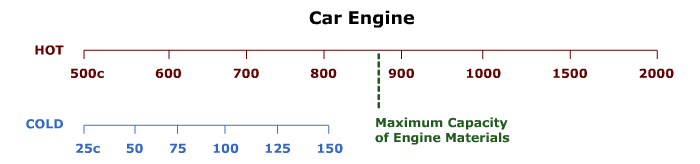
Figura 3.6.1. Básculas de temperatura fría y caliente en un motor típico de automóvil
En el Cuadro 3.6.1 se enumeran las eficiencias en función de las temperaturas frías y calientes.
Cuadro 3.6.1. Eficiencia del motor del automóvil (en%)
| Caliente 500°C |
Caliente 600°C |
Caliente 700°C |
Caliente 800°C |
Caliente 900°C |
Caliente 1000°C |
Caliente 1500°C |
Caliente 2000°C |
|
|---|---|---|---|---|---|---|---|---|
| Frío 150°C |
45 | 52 | 57 | 61 | 64 | 67 | 76 | 81 |
| Frío 125°C |
49 | 54 | 59 | 63 | 66 | 69 | 78 | 82 |
| Frío 100°C |
52 | 57 | 62 | 65 | 68 | 71 | 79 | 84 |
| Frío 75°C |
55 | 60 | 64 | 68 | 70 | 73 | 80 | 85 |
| Frío 50°C |
58 | 63 | 67 | 70 | 72 | 75 | 82 | 86 |
| Frío 25°C |
61 | 66 | 69 | 72 | 75 | 77 | 83 | 87 |
Problemas de ejemplo
Ejemplo 1
Para una caldera de servicio de carbón, la temperatura del vapor de alta presión (T caliente) sería de aproximadamente 540°C y T fría, la temperatura del agua de la torre de enfriamiento, sería de aproximadamente 20°C Calcular la eficiencia Carnot de la planta de energía.
- Contestar
-
La eficiencia del carnot depende de las altas temperaturas y bajas temperaturas entre las que opera el motor térmico. Se nos dan ambas temperaturas. Sin embargo, primero es necesario convertir las temperaturas a Kelvin.
\[ T_{hot} = 540 + 273 = 813 K \nonumber\]
\[ T_{cold} = 20 + 273 = 293 K \nonumber\]
Usando la ecuación 3.6.4,
\[ \eta = (1 - \dfrac{293}{813}) * 100\% = 64\% \nonumber\]
De la fórmula Carnot Efficiency, se puede inferir que un máximo del 64% de la energía del combustible puede ir a generación. Para que la eficiencia de Carnot sea lo más alta posible, se debe aumentar la T caliente o disminuir la T fría (temperatura de rechazo de calor).
Para problemas de práctica extra, refiérase a este enlace.


