8.4: Gas Natural y Gas Natural Sintético como Materias Primas para Combustibles Líquidos
( \newcommand{\kernel}{\mathrm{null}\,}\)
8.4 Gas Natural y Gas Natural Sintético como Materias Primas para Combustibles Líquidos
En la Lección 4, discutimos la gasificación en profundidad. También discutimos brevemente el uso de gas de síntesis para hacer líquidos. En la Lección 8, entraremos en un poco más de profundidad. Este tipo de procesos se denominan licuefacción indirecta.
El objetivo principal de la gasificación es producir un gas de síntesis compuesto principalmente por monóxido de carbono (CO) e hidrógeno (H 2). Después de la gasificación, el producto necesita ser limpiado para eliminar cualquier líquido, y hay varias reacciones que se pueden hacer para cambiar la relación H 2 /CO o para hacer diferentes productos. Aquí es donde comenzaremos esta lección.
La Figura 8.8 (a, b y c) muestra las tres fases diferentes del proceso por las que debe pasar el gas. La primera fase (Figura 8a) es el gasificador y separación de productos gaseosos, líquidos y sólidos. La biomasa no es carbono puro, y todas las corrientes contendrán una variedad de otros compuestos que pueden no ser deseados o pueden ser dañinos.
Los sólidos son removidos por un ciclón o un precipitador electrostático. Las partículas son similares a lo que se ve en la combustión: partículas ungasificadas o parcialmente gasificadas. Algunos materiales minerales/cenizas también pueden estar en los sólidos. Se utiliza un separador para eliminar los líquidos, principalmente alquitranes y agua que deben separarse y procesarse para su uso. La fracción de agua se puede utilizar para hacer reaccionar adicionalmente los compuestos orgánicos, y los alquitranes se pueden destilar y hacer reaccionar de manera similar a los procesos de licuefacción directa que describimos en secciones anteriores. En cualquier caso, el agua debe ser tratada antes de su eliminación.
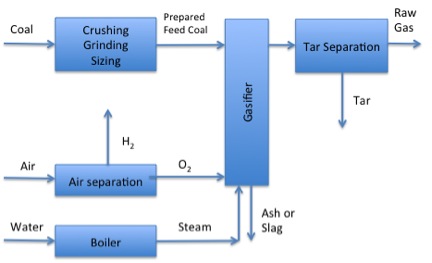
- Haga clic aquí para ver una alternativa de texto de la Figura 8.8a
-
Fase 1 de Gasificación:
El carbón es triturado, molido y dimensionado en presencia de hidrógeno. A continuación el carbón de alimentación preparado entra en el gasificado donde hay vapor de una caldera y mucho gas oxígeno. Se eliminan las cenizas y la escoria, y los productos restantes pasan a la separación de alquitrán donde el gas crudo se separa del alquitrán.
Crédito: Dra. Caroline B. Clifford
Los gases también pueden contener gases no deseados. Tres gases que deben eliminarse de la fase gaseosa son amoníaco (NH 3), dióxido de carbono (CO 2) y sulfuro de hidrógeno (H 2 S). Son corrosivos y/o tóxicos y necesitan ser removidos. Los gases ácidos (H 2 S y CO 2) se denominan gases ácidos porque pueden disolverse en agua y producir ácidos débiles que pueden ser corrosivos para los metales. Existe una gama de procesos que pueden separar los gases ácidos. Un método típico para eliminar estos gases nocivos se llama el proceso Rectisol (Figura 8.8b). Tanto H 2 S como CO 2 son solubles en metanol, mientras que H 2 y CO no lo son. En el esquema simplificado de la Figura 8.10b, hay dos partes en el proceso, un absorbedor y un regenerador. El gas crudo entra en el absorbedor y entra en contacto con la solución pobre de metanol. El gas purificado sale por la parte superior, y la solución rica en gases absorbidos no deseados va al regenerador; los gases ácidos se separan luego del metanol para que una solución de metanol pobre salga por el fondo para ser reciclada para su uso en el absorbedor. El H 2 S en el gas ácido puede quemarse o hacerse reaccionar con SO 2 para formar azufre sólido, que se utiliza para la fabricación de productos químicos. El CO 2 sale de la pila pero también podría capturarse si se ponen en marcha los procesos para capturarlo.
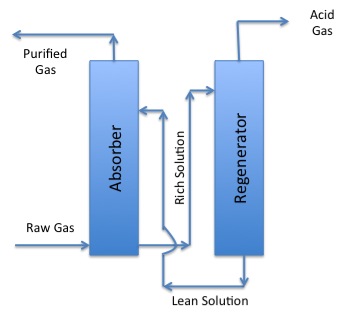
- Haga clic aquí para ver una alternativa de texto de la Figura 8.8b
-
Fase 2 de Gasificación:
El gas crudo de la fase uno ingresa al absorbedor y se elimina el gas purificado. Entonces la solución rica restante entra en el regenerador. El gas ácido se separa en el regenerador y la solución pobre restante regresa al absorbedor
Crédito: Dra. Caroline B. Clifford
La relación H 2 /CO puede no ser ideal para reacciones de síntesis aguas abajo. La Figura 8.8c muestra un proceso para usar la reacción de desplazamiento agua-gas para cambiar la relación de H2 /CO.
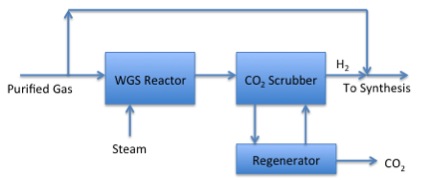
- Haga clic aquí para ver una alternativa de texto de la Figura 8.8c
-
Fase 3 de Gasificación:
El gas purificado y el vapor van a un reactor WHS. De ahí ingresan a un depurador de CO2 que puede enviar el gas al regenerador para eliminar CO2 adicional después de eso el gas puede regresar al depurador y con gas hidrógeno proceder a la síntesis.
Crédito: Dra. Caroline B. Clifford
Idealmente, la corriente de gas que sale del gasificador seguida de una unidad Rectisol podría ser razonablemente pura H 2 y CO. El desplazamiento agua-gas puede cambiar la relación de H 2 /CO. La reacción se muestra a continuación:
CO + H 2 O→CO 2 + H 2
Esta sería la manera de hacer menos CO y más H 2, pero la reacción puede ir a la inversa para hacer más CO y menos H 2 también. A partir de la gasificación del carbón, queremos desplazarlo a la derecha tal como está escrito. Las ventajas incluyen:
- que es un proceso de equilibrio;
- puede cambiar la reacción en otra dirección aprovechando el Principio de LeChatlier;
- con el mismo número de moles en ambos lados, la posición de equilibrio es independiente de la presión, sin necesidad de compresión o liberación de presión del reactor de desplazamiento;
- se puede adaptar a cualquier presión de funcionamiento.
La principal desventaja de la reacción de desplazamiento agua-gas es que es una fábrica de CO 2! Solo hay algunas formas de separar CO 2, como un depurador de monoetilamina (MEA). Se puede separar el CO 2 a una concentración del 99%, lo que sería ideal para CCS. Otra cosa a considerar es que no necesitamos separar toda la corriente de gas y desplazarla; solo necesitamos hacer lo suficiente para obtener la relación H 2 /CO donde queremos que esté. Una vez que lleguemos a este punto, podremos estar listos para hacer alguna síntesis de líquidos.


