3.6: Sensores de composición
- Page ID
- 85362
Introducción
Existen muchas herramientas analíticas útiles, como análisis fotométrico, análisis electrométrico, cromatografía, espectrometría de masas, conductividad térmica y diversas mediciones de propiedades físicas (densidad y gravedad específica), que pueden ser utilizadas para determinar la composición de las mezclas. Se dispone de una amplia gama de métodos para medir la composición, por lo que es importante elegir el mejor método dado un conjunto de condiciones. El primer paso es decidir entre medir las propiedades físicas o químicas para determinar la composición. Si elige medir una propiedad física, asegúrese de que sea única para el componente deseado de la mezcla y le permitirá determinar con precisión la composición. El objetivo de este artículo es explicar los diversos métodos analíticos y herramientas utilizadas para determinar la composición de una muestra dada. Después de leer esto, deberías poder determinar qué método de medición de la composición es el más apropiado para una circunstancia dada.
Tipos de Pruebas: On-line v Off-line
El análisis en línea es el monitoreo continuo de la composición de una muestra, la cual se encuentra bajo la influencia de un sistema de control y dirigida por un actuador que puede responder y regular las condiciones de operación en tiempo real de tal manera que se mantengan los puntos de ajuste deseados. Las pruebas en línea se pueden realizar en línea o mediante pruebas de flujo deslizante. En las pruebas en línea, el sensor se conecta directamente a la línea y proporciona retroalimentación a través de un transmisor. Por otro lado, en las pruebas de flujo de deslizamiento, una corriente lateral del proceso corre a lo largo de la línea principal. Tal aparato se parece mucho a la configuración de un bypass. Las condiciones del proceso de la corriente de deslizamiento se pueden manipular continuamente para facilitar la obtención de las mediciones. Similar a las pruebas en línea, el sensor se conecta directamente a la corriente de deslizamiento y proporciona retroalimentación a través de un transmisor. Las ventajas del análisis en línea incluyen una retroalimentación inmediata y continua que responde a los cambios en las condiciones del proceso. La principal desventaja de las pruebas en línea es que suelen ser mucho más complicadas y costosas que las pruebas fuera de línea. Además, las pruebas fuera de línea son más robustas y tienen aplicaciones más variadas, mientras que las pruebas en línea pueden no funcionar en todas las situaciones. Las pruebas en línea evitan la producción continua de productos no deseados, con una respuesta inmediata y corrección del material defectuoso.
El análisis fuera de línea implica la extracción de una muestra del proceso o reacción, y su posterior prueba en una máquina que puede estar ubicada en una ubicación alejada de la línea de proceso en un laboratorio. En este caso, se retira manualmente una muestra que posteriormente se envía al analizador de composición. Se examinan los resultados del análisis y luego se envían al sistema de control o actuador para realizar los ajustes correspondientes. El análisis en línea es comparable a las pruebas fuera de línea, siendo la principal diferencia que en las pruebas en línea, las muestras se analizan en una máquina que está al lado de la línea de proceso. Esto reduce en gran medida el tiempo perdido en el transporte de la muestra, aunque todavía permite la posibilidad de introducir contaminantes en la muestra. En el análisis fuera de línea, algunas de las desventajas incluyen el tiempo muerto de la muestra, que es el tiempo perdido durante el transporte, la variabilidad de las ubicaciones de las pruebas de la muestra y el tiempo de retraso para los ajustes que se realizarán en el proceso. En el análisis fuera de línea, el tiempo de rezago entre la extracción de la muestra del sistema y la recepción de los resultados de la prueba podría ocasionar pérdidas significativas a la empresa, ya que se produce el producto defectuoso y el proceso no se corrige hasta que se reciben los resultados. Este prolongado procesamiento defectuoso podría derivar en la acumulación de pérdidas por valor de miles de dólares, lo que podría haberse evitado si se estableciera un sistema de análisis en línea.
Si bien ambos métodos son ampliamente utilizados en la industria, hay un impulso hacia más pruebas en línea. Un artículo publicado en 2003 instando a las compañías farmacéuticas a adoptar más pruebas analíticas en proceso, como las pruebas en línea, avalado por la Administración de Alimentos y Medicamentos refleja esta tendencia. Esto ha sido parte de un esfuerzo más amplio de la FDA para alentar a las empresas a avanzar hacia mejores prácticas de fabricación. Si bien las pruebas en línea pueden ser comparativamente costosas de instalar al principio, los ahorros del proceso no solo recuperarían los costos asociados con la instalación, sino que también evitarían pérdidas significativas. Muchas empresas han adoptado técnicas de fabricación ajustada, y una de sus características distintivas es corregir un defecto lo antes posible en el proceso de producción, no permitiendo que los productos defectuosos pasen al siguiente paso de procesamiento. Permitir que los productos defectuosos se perpetúen a través del sistema puede incluso contaminar otros materiales no defectuosos en el proceso de producción.
Estándares y curvas de calibración
Antes de discutir las diferentes formas de medir la composición de una muestra, es necesario entender que los sensores de composición utilizan estándares o curvas de calibración para medir una composición desconocida contra una (s) conocida (s). El estándar puede ser un estándar interno con el que se comparan todas las demás mediciones, como una celda de referencia o una serie de estándares utilizados para crear una curva de calibración. Con una curva de calibración, se miden una serie de estándares conocidos con el sensor y la señal producida por el sensor se grafica en el eje y de una gráfica; la información conocida sobre cada muestra se grafica en el eje x. A partir de esta información, se puede desarrollar una relación entre la salida de señal del sensor y la cantidad conocida que está tratando de medir. Los datos medidos para la muestra desconocida se pueden comparar gráficamente con la curva de calibración o usando la ecuación escrita para describir la curva. Usando esta información, la medición realizada por el sensor puede interpretarse como una medición útil de la composición del porcentaje en peso, porcentaje en volumen, porcentaje molar, etc.
Análisis fotométrico
El análisis fotométrico es la medición de la intensidad de la luz visible y otras ondas electromagnéticas (EM). A través de la medición de estos valores, la composición de muestras o flujos se puede determinar de diversas maneras diferentes. Una amplia gama de dispositivos fotométricos basados en muchos principios diferentes se utilizan en la industria de la ingeniería química para este propósito. Algunos de los instrumentos más comunes se tratan en este artículo.
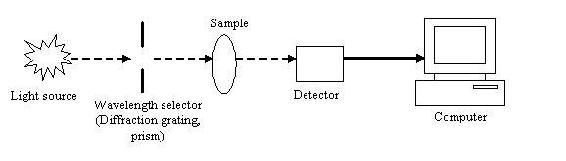
Tipos de fotómetros
Un fotómetro es cualquier tipo de instrumento utilizado para medir las características de la luz. Hay dos categorías amplias de fotómetros: dispersivos y no dispersivos.
Fotómetros dispersivos
En fotómetros dispersivos, la luz de la fuente se dispersa y una banda espectral estrecha se dirige selectivamente a la muestra y al detector. Un monocromador suele ser la herramienta que realiza esta función. El elemento dispersante del monocromador puede ser una rejilla de difracción, prisma y filtros de interferencia. Las rejillas de difracción son las más comunes; para cada posición de la rejilla pasa una banda estrecha de luz dispersa a través de una rendija de salida. Los dispositivos dispersivos pueden escanear a través de un espectro y realizar mediciones a varias longitudes de onda. Esta capacidad les permite ser utilizados para el análisis de múltiples componentes.
Fotómetros
no dispersivos Los fotómetros no dispersivos utilizan un filtro de paso de banda estrecha para bloquear una gran cantidad de radiación no deseada. Hacen mediciones a longitudes de onda discretas seleccionadas. El filtro pasa la radiación a las longitudes de onda de referencia y medición seleccionadas. El filtro de longitud de onda de referencia selecciona una banda donde ninguno de los componentes presentes en una corriente de proceso absorbe radiación; el filtro de longitud de onda de medición se selecciona para que coincida con la banda de absorción del componente que se está analizando. La relación de la luz transmitida en las longitudes de onda de referencia y medición es medida por el fotómetro. Los fotómetros no dispersivos se utilizan generalmente para medir un solo componente en la corriente del proceso.
Un ejemplo de tal dispositivo es el analizador de Infrarrojos No Dispersivos (NDIR) que se utiliza frecuentemente para medir las concentraciones de ciertos gases en un flujo de gas mixto. El analizador NDIR utiliza un gas no absorbente de referencia como O 2, Cl 2 y N 2 y lo compara con un gas de muestra como CO, CO 2, SO 2, CH 4, etc. se utilizan haces de radiación infrarroja: un haz de referencia para el gas no absorbente y un haz de análisis para la muestra.
Espectrofotómetros
Los espectrofotómetros son ampliamente utilizados como sensores de composición. Los espectrofotómetros son fotómetros que miden la intensidad de la luz a longitudes de onda específicas. Existen muchos tipos diferentes de espectrofotómetros, y normalmente se categorizan en función de los rangos de longitudes de onda que monitorean: ultravioleta (280-380 nm), luz visible (400-700 nm), infrarroja (0.7-1000 µm) o microondas (1-300 mm). Otras distinciones importantes son la técnica de medición, el método de obtención del espectro y la fuente de variación de intensidad.
El espectro de emisión registrado por el espectrofotómetro consiste típicamente en una serie de picos estrechos de diferentes alturas, también conocidos como líneas espectrales. La altura o amplitud de esas líneas puede estar relacionada con la concentración o abundancia del material específico a través de una curva de calibración y su posición en el espectro distingue los componentes del material. Si bien existen numerosos métodos para obtener un espectro, la aplicación más común de un espectrofotómetro es para la medición de la absorción de luz.
Absorción
El grado de absorción de las ondas electromagnéticas que exhiben los componentes de la muestra es una característica distintiva que puede ser utilizada para revelar la composición de la muestra. La absorción se relaciona con la inversa de la transmitancia por:
\[A=\log \left(\frac{1}{T}\right) \nonumber \]
donde\(A\) está la Absorbancia (Unidad de Absorbancia, AU) y\(T\) es la Transmitancia (como porcentaje).
Los espectrofotómetros basados en absorción tienen una fuente de radiación que emitirá un rango específico de ondas EM para ser absorbidas por la muestra midiendo la intensidad de la luz que pasa a través de la muestra. Una relación útil utilizada para determinar cuantitativamente la concentración de una especie absorbente en solución es la Ley Beer-Lambert:
\[A=-\log \left(\frac{I}{I_{0}}\right)=\epsilon\, c \, L \nonumber \]
donde
- I = Intensidad de la luz incidente a una longitud de onda particular
- I 0 = Intensidad de la luz transmitida
- épsilon = absortividad molar o coeficiente de extinción (1/M * cm)
- c = concentración de la especie absorbente
- L = longitud de trayectoria a través de la muestra
Según la Ley Beer-Lambert, la absorbancia de una solución es directamente proporcional a su concentración. El épsilon constante es una propiedad molecular fundamental para un disolvente dado. Se puede encontrar a partir de tablas de referencias o determinarse a través de la construcción de una curva de calibración. La Ley Beer-Lambert es útil para caracterizar muchos compuestos, pero no es válida para todas las especies. Por ejemplo, moléculas complejas muy grandes como los colorantes orgánicos a menudo exhiben una relación polinómica de segundo orden entre absorbancia y concentración.
Dos dispositivos ampliamente utilizados que miden la absorbancia de muestras son los espectrofotómetros ultravioleta e infrarrojo.
Espectrofotómetros Ultravioleta (UV)
La espectrofotometría UV es un método útil para detectar y cuantificar sustancias en solución. Ciertos compuestos en estado gaseoso o líquido absorben la radiación ultravioleta, dando como resultado picos de absorción que pueden correlacionarse con grupos funcionales específicos. Estas especies incluyen compuestos aromáticos y carbonílicos en sustancias orgánicas e iones de metales de transición en solución. Esta propiedad es útil para categorizar y medir la composición de este tipo de muestras, sin embargo esta propiedad no puede ser utilizada como una prueba específica para un compuesto dado. La naturaleza del disolvente, el pH de la solución, la temperatura, las altas concentraciones de electrolitos y la presencia de sustancias interferentes pueden influir en los espectros de absorción de los compuestos, al igual que las variaciones en el ancho de hendidura en el espectrofotómetro. Muchos solventes orgánicos tienen una absorción UV significativa y por lo tanto agregarán picos a las especies disueltas en ellos. La polaridad del disolvente, la alta concentración de electrolitos y el pH pueden afectar el espectro de absorción de un compuesto orgánico al provocar la protonación o desprotonación del compuesto. La temperatura también puede hacer que las moléculas complejas cambien en la conformación y también pueden alterar las propiedades del disolvente utilizado. Las variaciones en el ancho de la hendidura alterarán el ancho de banda efectivo, distorsionando las mediciones de longitud
Los componentes básicos del analizador general son la fuente de luz UV, el portamuestras, los filtros ópticos y el detector (típicamente un fototubo). Los filtros ópticos (típicamente un monocromador o rejilla de difracción) separan las longitudes de onda de la luz que atraviesa la muestra y aseguran que solo las longitudes de onda deseadas lleguen al detector.
La mayoría de los analizadores UV son fotómetros dispersivos que también funcionan en el espectro de luz visible y se denominan espectrofotómetros UV-Vis. Dado que estos instrumentos se encuentran generalmente en laboratorios, generalmente se utilizan para análisis fuera de línea. Sin embargo, hay máquinas UV en línea y sensores disponibles para mediciones en línea en tiempo real de las corrientes de flujo del proceso. Espectrofotómetros UV utilizados en muchas industrias para diversas aplicaciones.
Espectrofotómetros infrarrojos (IR)
La espectroscopia infrarroja se basa en el hecho de que existen frecuencias específicas a las que los enlaces moleculares rotan o vibran cuando se exponen a niveles discretos de energía de radiación. Un haz de luz infrarroja pasa a través de la muestra, ya sea una longitud de onda a la vez con un haz monocromático o usando un instrumento de transformada de Fourier que mide todas las longitudes de onda a la vez. La inspección de la luz transmitida revela cuánta energía se absorbió en cada longitud de onda, luego se grafican estos datos (ver ejemplo a continuación). Esta gráfica permite que la frecuencia de las vibraciones se asocie a un tipo de unión particular. Los espectros de absorción IR característicos obtenidos para una muestra pueden ser utilizados para identificar el compuesto, mientras que la amplitud de absorbancia es proporcional a la concentración del analito. Los analizadores IR se utilizan para analizar compuestos gaseosos o líquidos que pueden absorber ondas IR. Los componentes del sistema son generalmente similares a los de un espectrofotómetro UV, con la excepción de la fuente de luz IR.
Los instrumentos IR se han utilizado regularmente en un entorno de laboratorio fijo desde hace décadas. Existen técnicas de IR tanto dispersivas como no dispersivas. Más recientemente, los fabricantes de instrumentos han reducido significativamente sus requisitos de tamaño y potencia. Además de los sensores IR en línea para flujos de proceso, la instrumentación portátil está disponible para el análisis de campo, como el monitoreo de gases de chimenea. Otra tecnología relativamente moderna, el Espectrómetro Infrarrojo por Transformada de Fourier (FTIR), es ampliamente utilizado en la industria hoy en día debido a su alta sensibilidad y amplio rango de aplicación. Por ejemplo, el análisis FTIR se utiliza en la cuantificación de peróxidos orgánicos nocivos en lubricantes y combustibles.
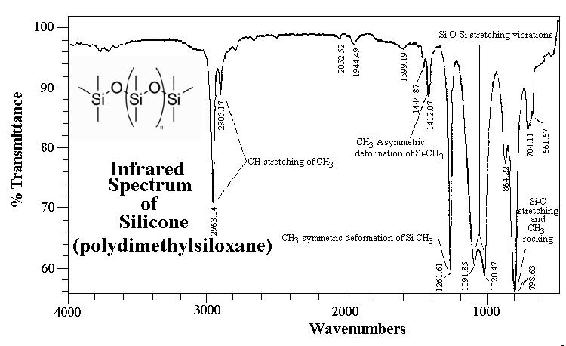
Radiación
En lugar de medir la absorción de luz, muchos espectrofotómetros miden la radiación de las ondas EM. Las muestras pueden irradiar ondas EM en muchas formas tales como calor, luminiscencia, fluorescencia y fosforescencia. La medición de dicha radiación se emplea a menudo en áreas biológicas y farmacéuticas debido a su alta sensibilidad y especificidad. Por ejemplo, se utilizan espectrofotómetros de fluorescencia para analizar la presencia y concentración de compuestos biológicos diana. Se introducen moléculas de sonda fluorescente en la muestra que se unirán selectivamente a la molécula biológica de interés y el dispositivo detectará y medirá la cantidad de radiación fluorescente. En estos experimentos, se deben medir los estándares apropiados para calibrar adecuadamente la radiación medida con la concentración de la muestra. Adicionalmente, la contaminación de la muestra puede afectar los patrones de radiación.
Ejemplos de otras técnicas que utilizan las ondas EM de radiación incluyen espectroscopía de emisión de llama, emisión de rayos X inducida por partículas y fluorescencia de rayos X. Estos métodos se utilizan estrictamente para el análisis de laboratorio.
Fotometría con Luz Visible
La manera en que ciertos materiales interactúan con la luz visible se puede utilizar para analizar la composición del material de muestra. Los refractómetros, turbidímetros y medidores de opacidad son todos analizadores que utilizan este principio.
Refractometría
La teoría detrás de la refractometría es que la luz visible se dobla (o refracta) cuando pasa por dos medios opacos de diferentes densidades. La Ley de Snell relaciona el ángulo de incidencia α con el índice refractivo η por:
\[\frac{n_{1}}{n_{2}}=\frac{\alpha_{2}}{\alpha_{1}} \nonumber \]
α 1, α 2 = ángulos de incidencia
η 1, η 2 = índices de refracción de los dos medios (sin unidades)
Alternativamente, se puede usar el ángulo crítico para analizar la composición. El ángulo crítico se define como el ángulo de incidencia que produce una refracción de 90 o con respecto a la normal de la interfaz es decir α 2 = 0 o. Así, la Ley de Snell se convierte en:
\[\frac{n_{1}}{n_{2}}=\frac{1}{\sin \alpha_{c}} \nonumber \]
α c = ángulo crítico
Por favor refiérase al diagrama a continuación.
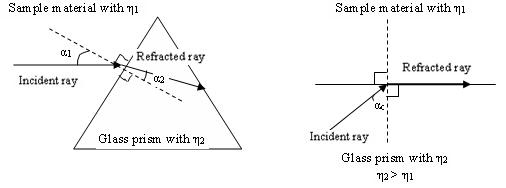
Diferentes materiales tendrán diferentes índices de refracción; el índice de refracción experimental medido puede compararse con una lista de valores de índice de refracción en un banco de datos. Los refractómetros de proceso continuo o en línea generalmente miden los cambios en el ángulo crítico en una interfaz vidrio-muestra causados por las variaciones en las concentraciones de composición. Los refractómetros se utilizan en numerosas industrias como la industria alimentaria, química, metalúrgica debido a su alta precisión y repetibilidad, bajo mantenimiento y fácil instalación. Un ejemplo es el uso de un refractómetro para monitorear la cantidad de concentrado de jugo en el jugo.
Turbidímetros
Los turbidímetros miden la turbidez, o claridad de la muestra, de los fluidos. Un haz de luz pasa a través del analizador y si el agua, u otra sustancia química que se va a probar, es “pura”, entonces la luz viajaría sin ser perturbada. Sin embargo, si la muestra contiene sólidos o partículas suspendidos, la luz interactuaría con las partículas haciendo que las partículas absorban la luz y la reflejen en diferentes direcciones. Un ejemplo es el humo en el aire que le da al aire un aspecto nebuloso.
La mayoría de los turbidímetros modernos son nefelómetros. Los nefelómetros o turbidímetros nefelométricos miden la luz dispersa reflejada en las partículas suspendidas en la muestra. Este instrumento contiene una fuente de luz, algún tipo de recipiente para contener la muestra y fotodetectores para detectar la luz dispersada. Una lámpara de filamento de tungsteno se usa más comúnmente como fuente de luz. Si las partículas suspendidas, típicamente medidas en nanómetros, son menores que la longitud de onda que la luz incidente, la luz reflejada se dispersa por igual en todas las direcciones. Si las partículas son mayores que la longitud de onda de la luz incidente, el patrón de dispersión se enfocará lejos de la luz incidente.
Los nefelómetros se suelen utilizar cuando los sólidos están presentes en la muestra en pequeñas concentraciones. Cuando hay alta turbidez en una muestra, se produce dispersión múltiple y es posible que el turbidímetro ya no pueda analizar el fluido. Las desventajas de los nefelómetros incluyen ser propensos al ensuciamiento e incapacidad de analizar fluidos que tienen altas concentraciones de partículas sólidas.
Los turbidímetros son importantes para la industria, específicamente para plantas químicas, refinerías de petróleo y plantas de tratamiento de aguas residuales. Por ejemplo, los nefelómetros se utilizan para detectar los contaminantes en el agua en el monitoreo de la calidad del agua.
Monitores de Opacidad
Los monitores de opacidad miden la atenuación de la luz debido a la dispersión y absorción por la muestra. La atenuación se define como la disminución en la intensidad y amplitud del haz de luz medido en comparación con el haz de luz emitido. Los monitores de opacidad difieren de los turbidímetros en que analizan muestras midiendo el porcentaje de transmisión de la fuente de luz que pasa a través de la muestra y NO la dispersión de la fuente de luz. Una aplicación común es la medición de la densidad de humo en chimeneas. La densidad del contaminante o partícula se expresa como porcentaje de opacidad, porcentaje de transmitancia o densidad óptica.
% opacidad = 100 x opacidad = 100 —% transmitancia
Análisis electrométrico
El análisis electrométrico utiliza los principios de la electroquímica para analizar la composición de diferentes muestras.
Celdas de Conductividad
Las celdas de conductividad miden la capacidad de un líquido para conducir una corriente eléctrica. Dado que los líquidos conducen corriente debido a la presencia de iones, la composición se puede determinar midiendo la concentración de los iones presentes. Las celdas de conductividad determinan la concentración a partir de la definición de conductividad molar (lambda). La conductividad molar es una propiedad que puede ser influenciada por la temperatura. También varía con la concentración si el químico que se mide es un electrolito débil. Se define por la siguiente ecuación:
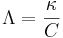
- λ = conductividad molar [S m 2 /kmol]
- κ = conductividad [S]
- C = concentración [kmol/ m 3]
Dado que es difícil medir directamente la conductividad, las celdas de conductividad miden la resistencia (R) de un líquido de muestra entre dos electrodos cuando se aplica una pequeña corriente. La resistencia se relaciona con la conductividad por la siguiente ecuación:
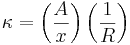
- κ = conductividad [S]
- A = área del electrodo [m 2]
- x = distancia entre electrodos [m]
- R = resistencia [ohm, Ω]
Tenga en cuenta que el área del electrodo, A, y la distancia entre los dos electrodos, x, son fijos para un sensor en particular y a menudo se expresan como una constante de celda (k c).
El siguiente diagrama de flujo muestra cómo se determina la composición en términos de concentración:
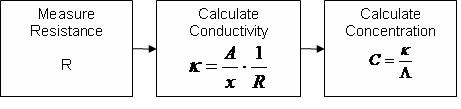
Las celdas de conductividad se pueden utilizar en el sistema de flujo e instalarse directamente en el sistema de tuberías. Las celdas de conductividad pueden venir en tres tipos: sonda de dos electrodos, sonda de múltiples electrodos o una sonda sin contacto y sin electrodo (toroidal). La sonda de dos electrodos es uno de los tipos más comunes y normalmente usa carbono o acero inoxidable como electrodos. El electrodo múltiple sondado tiene dos, cuatro o seis electrodos. Esta sonda tiene la ventaja de reducir los errores debidos a la polarización (reacción electroquímica en la superficie del electrodo) y el ensuciamiento. Finalmente, la sonda toroidal no tiene electrodos y en su lugar mide la corriente de CA en un circuito cerrado de solución utilizando dos toroides incrustados (un núcleo magnético con alambre envuelto alrededor de él para hacer un inductor). La sonda sin electrodos es buena para soluciones que tienden a tener problemas de polarización o ensuciamiento aceitoso. Las celdas de conductividad en línea son adecuadas para temperaturas de hasta 480K y presiones de hasta 1700 kN/ m 2.
Dado que la concentración se encuentra a partir de la conductividad molar, que es una propiedad del fluido que depende fuertemente de la temperatura, un sensor de temperatura a menudo se empareja con una celda de conductividad por lo que los efectos de la temperatura se pueden explicar en los cálculos de concentración.
Las celdas de conductancia se usan mejor en aplicaciones donde un solo tipo de ion está presente en una solución diluida. Las concentraciones más altas conducen a complicaciones que no pueden ser descritas por la relación lineal simplista entre concentración y conductividad, ya que la conductividad molar comienza a variar con concentraciones más altas de electrolitos débiles.
Electrodos selectivos de iones
Electrodo de pH
El electrodo de pH se usa comúnmente tanto en el laboratorio como en el entorno industrial. Este electrodo es sensible a la concentración de los iones H +. El electrodo de pH básicamente mide la diferencia de potencial entre una solución de referencia y la muestra. Consulte la sección del sensor de pH para obtener ejemplos y más información sobre la teoría relevante.
Otros electrodos selectivos de iones
Los electrodos también pueden ser específicos de otros iones como: Na +, K +, Ag +, ClO 4, BF 4, SO 2 y CO 2. La sensibilidad iónica de un electrodo depende principalmente del método de separación de iones en la solución. El mayor problema con los electrodos selectivos de iones es el problema de la falta de suficiente selectividad para el ion deseado, y la posterior interferencia por otros iones con propiedades químicas similares al ion deseado. La mayoría de los electrodos utilizan una membrana para separar un ion específico, aunque existen otras técnicas. Los electrodos selectivos de iones se pueden dividir en las siguientes tres categorías según el modo de separación: membrana sólida (vidrio o cristalina), membrana líquida (intercambiador iónico clásico con un portador neutro o cargado) y membrana en un electrodo especial (sensor de gas o electrodo enzimático). Ejemplos de electrodos selectivos de iones utilizados en la industria incluyen sensores de nitrato para el tratamiento de aguas residuales o monitoreo de la calidad de los ríos, sensores de hidrazina y sodio para agua de calderas, y sensores de cloro y flúor para plantas de tratamiento de agua.
Sensores de Potencial de Oxidación-Reducción (ORP)
Los sensores ORP, o también llamados sensores Redox, pueden determinar la concentración de iones que existen en dos estados de oxidación diferentes en solución. Por ejemplo, este tipo de electrodo se puede utilizar para analizar la composición de una solución con iones Fe 2+ y Fe 3+. Este tipo de electrodo mide el potencial causado por la capacidad de reducción u oxidación de una solución.
Este tipo de sensor mide directamente el potencial eléctrico que indica la fuerza reductora u oxidante de una solución. El poder reductor u oxidante de una solución depende de si el estado de oxidación mayor o menor es el preferido por el ion.
Cuando un ion favorece el estado de oxidación más alto (o tiene propiedades reductoras), los iones tienden a ceder electrones y el electrodo se vuelve más cargado negativamente.
Cuando un ion favorece el estado de oxidación inferior (o tiene propiedades oxidantes), los iones tienden a ganar electrones y el electrodo se vuelve más cargado positivamente.
Al comprar un sensor ORP de un proveedor, muchos modelos ya vienen empaquetados con un sensor de pH, ya que estas dos mediciones a menudo son monitoreadas para mantener un proceso funcionando en las condiciones adecuadas. Por ejemplo, en la industria de piscinas y spas, es importante monitorear tanto la concentración de desinfectantes en el agua con un sensor ORP, como medir el pH del agua.
Sensores Polarográficos
Los sensores polágrafos funcionan realizando electrólisis con dos tipos de electrodos: uno que es polarizable y otro que no lo es. Operan de manera muy similar a los voltámetros, pero con voltámetros el potencial se cambia de manera controlada y se mide el voltaje. El sistema más antiguo de medición polarográfica utilizó electrodos de mercurio de caída. Aquí el principio es que la tensión superficial del mercurio cambia con la cantidad de carga que se aplica entre la parte superior e inferior del electrodo, y este cambio de tensión superficial se puede ver en cómo el peso de las gotas de mercurio varía con el tiempo.
Los tipos más modernos de polarografía utilizan dos tipos diferentes de metales que están conectados en una solución con electrolitos, y los electrones se moverán hacia el metal más cargado positivamente. Este movimiento de electrones induce una corriente, que finalmente se detiene una vez que las cargas están equilibradas (polarizadas). Si todas las cargas están equilibradas dentro del sistema, no fluirá corriente. Por lo tanto, se aplica un pequeño potencial a un sensor polarográfico para que exista una corriente para que el sensor mida.
La muestra que se analiza necesita tener la capacidad de despolarizar el sistema, o inclinar el saldo de cargas. El ion de interés cruza una membrana selectiva y reacciona mediante una reacción de oxidación/reducción con una superficie metálica (a menudo llamada electrodo de medición). La reacción entre el ion y el electrodo provoca una distribución desigual de las cargas. Una vez que un sistema es despolarizado, el potencial del sistema aumenta ya que una región más positiva y otra más negativa existe por separado. El aumento en el potencial hace que la corriente fluya, que es la señal medida por el sensor. Esto crea una gráfica que muestra la relación entre la corriente aplicada y el potencial medido. Una desventaja de este tipo de herramienta de medición es que esta gráfica requiere una curva de calibración para interpretar los datos, por lo que el análisis de composición mediante polarografía no se puede hacer en línea. La ventaja de este tipo de método es que es altamente preciso y muy reproducible.
A continuación se muestra un esquema básico de un sensor polarográfico.
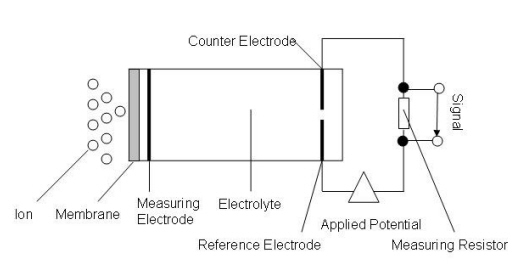
Los sensores polágrafos son los más utilizados para evaluar contaminantes en el aire como Cl 2, HCl, HBr y HF. También se puede utilizar para medir O 2 y otros gases inertes en humos.
Sensores Cerámicos de Alta Temperatura
Este tipo de sensores tienen una sección calentada de óxido de circonio (ZrO 2), también conocida como zirconia, que está ligeramente dopada con itria (Y 2 O 3). Esta estructura reticular estable es capaz de medir la conducción de iones de oxígeno a altas temperaturas. Este sensor se utiliza exclusivamente para medir O 2 y a menudo se usa para medir la composición de O 2 en los gases de combustión.
Cromatografía
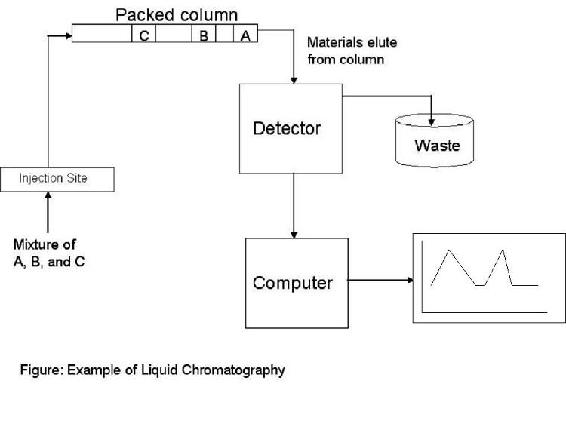
La cromatografía es un conjunto de métodos físicos utilizados para separar y así analizar mezclas complejas. La cromatografía consiste en una fase móvil, generalmente un gas o un líquido, y una fase estacionaria, típicamente un sólido o un líquido. Estas dos fases se combinan en una columna de la fase estacionaria basada en el tipo de cromatografía que se desea completar (es decir, Gas-líquido, Gas-sólido, Líquido) para separar la mezcla. El tiempo de retención de un componente es el tiempo antes de que el componente eluya de la columna. El tiempo de retención y el orden de elución se basan en la interacción relativa entre cada soluto y cada fase. Cuanto más fuerte sea la interacción del soluto con la fase móvil, en relación con la fase estacionaria, más pronto se eluirá el soluto de la columna. La interacción soluto-fase es una función de las cargas de las moléculas, la absorción de la fase estacionaria y la solubilidad relativa.
La cromatografía por sí misma no detecta sustancias, sino que se acopla rutinariamente con una unidad de detección. Cada sustancia se detecta a medida que sale del cromatógrafo. El tiempo de retención para cada sustancia puede compararse entonces con un estándar para determinar qué sustancias estaban en la mezcla. Para sustancias desconocidas, el orden de elución puede determinar algunas propiedades de la sustancia. Por ejemplo, una sustancia que inicialmente eluye después del etanol en una columna no polar es menos polar que el etanol. Sin embargo, otros detectores de composición son mucho más adecuados para el análisis de sustancias desconocidas.
La cromatografía es el proceso de detección de composición más utilizado para el análisis en línea de muestras dentro de una mezcla compleja. Debido a su precisión, la cromatografía se usa comúnmente para separar o purificar muestras dentro de las industrias química o bioquímica. Dependiendo del tipo de cromatografía utilizada, incluso se pueden analizar mezclas delicadas como proteínas. Sin embargo, la cromatografía es principalmente útil cuando hay algunas expectativas para los componentes en una mezcla; la cromatografía no es la mejor para una muestra completamente desconocida, pero es útil para detectar la composición de una corriente de proceso donde la mayoría de los componentes son conocidos y existe un estándar adecuado.
Tipos de Cromatografía
Cromatografía Gas-Líquida (
GLC) GLC es uno de los tipos más comunes de cromatografía. Se le conoce comúnmente como GC (cromatografía de gases). En una serie típica, la mezcla líquida a analizar se agrega al sistema y se vaporiza antes de ingresar a la columna. Un gas portador, a menudo Helio, transporta la muestra vaporizada a través de una columna. La columna puede estar empaquetada con fase estacionaria, o bien la columna puede tener un diámetro muy pequeño en cuyo caso está revestida con fase estacionaria (tubo capilar). La fase móvil gaseosa corre a través de la fase estacionaria dentro de la columna a diversas velocidades determinadas por la volatilidad relativa y afinidad a la fase estacionaria. Cuanto más tiempo pase una molécula de muestra en la fase gaseosa, más rápido se eluirá de la columna. Por esta razón, la temperatura y la identidad química del recubrimiento en la fase estacionaria son dos variables importantes que pueden necesitar ser manipuladas para recibir una separación clara de los componentes en la mezcla. En general, una temperatura más baja dará como resultado una mejor separación pero tiempos de elución más largos y dispersión de la muestra debido a los efectos del flujo. El uso eficiente de este aparato requiere un equilibrio entre estos efectos competidores.
La GC es relativamente simple de usar para un técnico; un cromatógrafo de gases calibrado puede ejecutar varias muestras sin una gran cantidad de preparación de muestras. La cromatografía de gases funciona bien en sustancias que se vaporizan por debajo de 300°C y están libres de iones; sin embargo, no funciona bien en sustancias que se descomponen por debajo de 300°C.
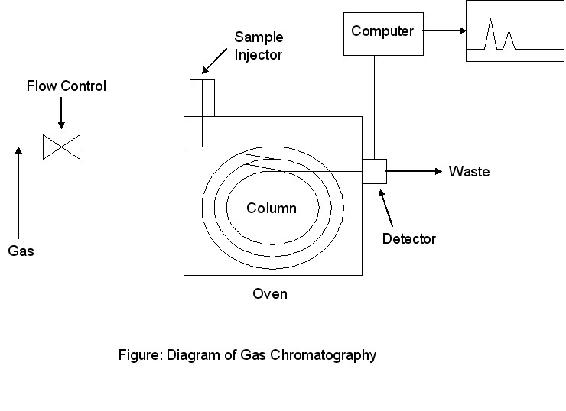
Cromatografía Gas-Sólido (GSC)
GSC utiliza una fase móvil gaseosa que corre a través de una fase estacionaria sólida absorbente (por ejemplo, gel de sílice o alúmina) dentro de la columna de vidrio según lo determinado por absorción. Este método opera siguiendo los mismos principios que la cromatografía gas-líquido. Se usa más comúnmente con gases (a diferencia de una sustancia vaporizada) y con hidrocarburos de bajo peso molecular.
La cromatografía líquida (LC)
LC analiza líquidos de baja volatilidad dentro de una fase estacionaria sólida. La separación se produce a partir de la adsorción/desorción debido a que los solutos tienen diferentes grados de atracción hacia la fase estacionaria, típicamente debido a que la fase estacionaria tiene diferente polaridad que la fase móvil. Es común usar una mezcla de solventes para separar con precisión las mezclas. La cromatografía líquida se utiliza en varias industrias, incluyendo las industrias farmacéutica y petroquímica.
Espectrometría de Masas
La espectrometría de masas se encuentra entre las herramientas de detección composicional más precisas y, en consecuencia, una de las más caras. La idea básica se ilustra a continuación:
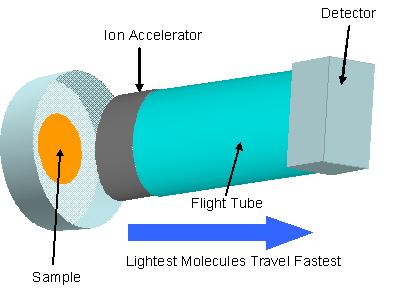
Una muestra se ioniza, esto se puede realizar mediante varias técnicas, los iones se someten a una fuerza eléctrica y se aceleran a través de un tubo. Debido a que la fuerza eléctrica aplicada a cada molécula es la misma, una aceleración de moléculas a través del tubo depende de su masa (F=mA). La aceleración también depende de cualquier carga en la molécula debido a fuerzas magnéticas atractivas o repulsivas. Al final del tubo, un detector calcula el tiempo de vuelo para cada una de las moléculas.
La espectrometría de masas es esencialmente una herramienta para crear un espectro de distintas relaciones masa/carga. Se utiliza muy a menudo después de técnicas de separación por cromatografía para servir como técnica de identificación de moléculas.
Componentes MS
Hay 3 componentes fundamentales para la espectrometría de masas: una fuente de iones, un analizador de masas y un detector.
La fuente de iones es el componente responsable de ionizar la muestra. Hay muchos métodos diferentes, incluida la ionización química, eléctrica o láser. La selección de la fuente de iones adecuada depende de las características de la muestra (fase, biológicamente activa, etc.).
El analizador de masas es la técnica y herramienta utilizada para diferenciar los iones en un espectro basado en la relación masa/carga. La técnica descrita anteriormente es la técnica de tiempo de vuelo. Otro método común es un analizador de masas de campo sectorial donde las moléculas se aceleran a través de un tubo y se aplica una fuerza magnética perpendicular a la dirección de vuelo de las moléculas. Las moléculas se desviarán a diferentes magnitudes dependiendo de su tamaño.
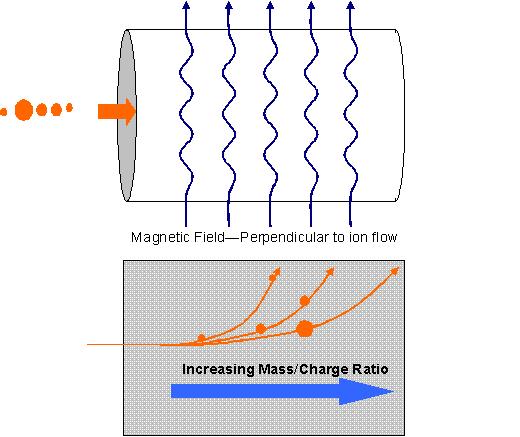
El detector generalmente amplifica los cambios en una corriente eléctrica que ocurren cuando las moléculas golpean el detector.
Conductividad Térmica para Gases
Los cambios en la conductividad térmica pueden ser utilizados para detectar variaciones en una mezcla de gases. Cuando hay una fuente de calor, los gases y el vapor conducirán el calor. El cambio de calor entre la fuente y los gases se estabilizará a una temperatura común. La temperatura depende principalmente de la conductividad térmica y por lo tanto de la composición del gas.
El equipo típico para analizadores de conductividad térmica incluye: una celda de referencia, una celda de muestra, una fuente de calor combinada (filamentos de alambre o termistores) y detector. La celda de muestra y la celda de referencia generalmente se colocan en un soporte donde se puede montar el detector. La referencia es una celda idéntica de la celda de muestra, a través de la cual fluirá un gas conocido. La resistencia del detector de referencia será constante y la resistencia muestra-detector variará dependiendo de la composición. La resistencia es una función de la temperatura y la salida del puente detector será una función de la composición de la muestra.
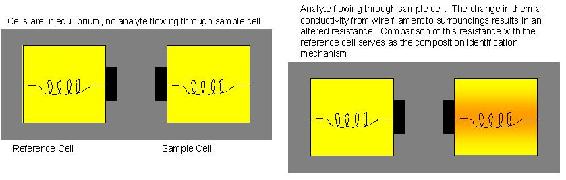
La conductividad térmica, como la espectrometría de masas, a menudo se usa en combinación con cromatografía de gases
Mediciones físicas de la propiedad
Las propiedades físicas pueden ser utilizadas para medir indirectamente la composición, pero esta técnica no es tan versátil como las descritas anteriormente, ya que sólo se aplica a un número limitado de circunstancias. La ventaja de usar propiedades físicas para medir indirectamente la composición es que este tipo de medidas suelen ser más baratas que los tipos de sensores descritos anteriormente.
Densidad y Gravedad Específica
Las mediciones de densidad y gravedad específica requieren una mezcla binaria con al menos una fase fluida para realizar mediciones precisas. Dada la temperatura y presión, la densidad de un gas se puede encontrar usando la ley de gas ideal o alguna otra relación, y dado que la densidad es una función de la composición, la composición se puede medir indirectamente. Ver Termodinámica para más información. La gravedad específica es simplemente la relación de densidad del agua sobre la densidad del componente no compresible en las mismas condiciones físicas, lo que significa que es simplemente una medición adimensional de la densidad.
A continuación se describen cuatro dispositivos de medición diferentes para encontrar densidad.
Columna de Líquido
En una columna de líquido, se utilizan las mediciones de presión en una columna para determinar la densidad. La columna puede estar abierta a la atmósfera, donde se mide la presión manométrica en la parte inferior de la columna de altura fija. O bien, la columna puede estar cerrada, en cuyo caso la medición de presión diferencial se realiza entre la parte inferior de la columna de altura fija y en la parte superior de la columna inmediatamente por debajo de la superficie del líquido.
Desplazamiento — Hidrómetro
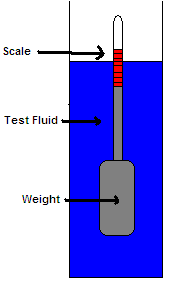
Un hidrómetro suele estar hecho de vidrio y consiste en un vástago cilíndrico y una bombilla ponderada con mercurio o granalla de plomo para que flote en posición vertical. El líquido a ensayar se vierte en un frasco alto, y el hidrómetro se baja suavemente en el líquido hasta que flota libremente. Se anota el punto en el que la superficie del líquido toca el tallo del hidrómetro. Los hidrómetros suelen contener una escala de papel dentro del tallo, de manera que la gravedad específica se puede leer directamente.
El funcionamiento del hidrómetro se basa en el principio de Arquímedes de que un sólido suspendido en un líquido será flotado por una fuerza igual al peso del líquido desplazado. Así, cuanto menor sea la densidad de la sustancia, menor se hundirá el hidrómetro.
Medición directa de masa
Con esta técnica, el fluido pasa continuamente a través de un tubo en forma de U, donde el tubo oscila a su frecuencia natural. Un dispositivo electroquímico golpea el tubo periódicamente en la porción curva del tubo. El cambio de frecuencia entre el impacto electroquímico y la frecuencia natural es proporcional a los cambios en la densidad que se correlaciona con la composición de la sustancia.
Medidores de Densidad de Radiación La radiación
gamma dentro de una tubería/recipiente se utiliza para determinar la densidad del líquido. A continuación se muestra un diagrama de la configuración.
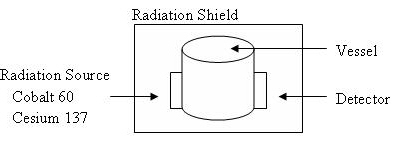
Si la longitud del camino para la fuente de radiación es inferior a 610 mm entonces se usa cesio 137. Por encima de 610mm, se utiliza cobalto 60. El detector suele ser un medidor de ionización. La densidad es una función de la absorción de la radiación que se está detectando. Se debe tener en cuenta la descomposición del recipiente al calibrar
Viscosidad
Consulte la sección Sensor de viscosidad del sitio web de control de procesos para obtener información en profundidad.
Gráficas integrales
- Para gráficos simples y fáciles de leer que resumen las ventajas y desventajas de cada tipo de sensor, por favor siga estos enlaces para obtener una versión PDF de cada gráfico.
Medios:Fotométrico sensors.pdf
Medios:Medición Electroanalítica Techniques.pdf
Medios:Otros tipos de medición Techniques.pdf
- Para ver gráficos de resumen completos que incluyen más sensores no discutidos en el artículo, por favor siga los enlaces aquí para obtener una versión PDF de estos gráficos de resumen.
Medios:ComposicionesSensoresGeneral.pdf
Medios:ComposicionesSensoresSphysical.pdf
Medios:ComposiciónSensoresquemical.pdf
Medios:ComposiciónSensorSelectrical.pdf
Ejemplo Aplicado: Espectrómetro Mars Pathfinder
El Mars Pathfinder utiliza un espectrómetro de rayos X Alpha Proton para identificar los químicos que componen la superficie marciana. La increíble herramienta dispara rayos X en la superficie del planeta y utiliza un detector de retrodispersión para recolectar las partículas alfa, protones y rayos X característicos de elementos específicos. Estos eventos de dispersión específicos de átomos permiten a los científicos de la NASA determinar la composición de la superficie.
Su supervisor lo puso a cargo de monitorear las emisiones de una vieja pila de humo que la planta acaba de reabrir para mantenerse al día con la demanda de productos. Es importante medir la cantidad de humo y oxígeno que sale de la pila. Elija los tipos adecuados de sensores para instalar y tenga en cuenta que el contenido de la pila sale a temperaturas muy altas.
Solución
Para monitorear la densidad de humo se podría instalar un monitor de opacidad que mida la absoprción y dispersión de la luz. Consulte Sensor Asmebly en este sitio web Ensamblaje de monitor de opacidad para obtener un diagrama esquemático básico.
Para monitorear la concentración de oxígeno se podría instalar ya sea un sensor polarográfico o un sensor cerámico de alta temperatura porque ambos tipos de sensores son específicos de la partícula O 2. El sensor cerámico de alta temperatura es más adecuado para esta aplicación ya que las emisiones salen a altas temperaturas.
Usted es el encargado de calibrar una nueva celda de conductividad adquirida por la compañía. La celda de conductividad se utilizará para medir la concentración de NaCl en los reactivos iniciales. El NaCl tiene una conductividad molar de 12.6 Sm 2/kmol. Las dimensiones de las celdas son las siguientes: el área de las celdas (A) es de 100 m 2 y la distancia entre las celdas (x) es de 0.25 m. Calcular la concentración necesaria para producir una resistencia de 10 ohmios en el sensor.
Solución
Haciendo referencia a la sección Celda de Conductividad, la ecuación se puede organizar para encontrar la concentración:
\[\text{concentration} = \dfrac{\text{conductivity}}{\text{.olar conductivity}} \nonumber \]
Desconocido = conductividad
\[\begin{align*} \text { conductivity } & =\left(\frac{A}{x}\right)\left(\frac{1}{R}\right) \\[4pt] &=\left(\frac{100}{0.25}\right)\left(\frac{1}{10}\right) \\[4pt] &= 40 \end{align*} \nonumber \]
Vuelva a enchufar en la ecuación inicial
concentración = conductividad/conductividad molar
concentración = 40/12.6
concentración = 3.17 kmol
Referencias
- Richardson, JF. Coulson & Richardson's Ingeniería Química Vol. 3, Oxford: Butterworth-Heinemann. ISBN 0080410030
- Perry, GH; Verde, DW. Manual de ingeniería química de Perry 7a edición, Nueva York: Mcgraw-Hill ISBN 0070498415
- Entonces, Peter; Dong, CY. Espectrofotometría de Fluorescencia Enciclopedia de Ciencias de la Vida, Londres: McMillan
- Ingeniería OMEGA. Medición de Turbidez.
- Especialidades Analíticas. Sensores Electroquímicos
- Shimadzu. Cuantificación de Peróxidos Orgánicos Usando FTIR y ATR.
- Diccionario Merriam-Webster.
- Wikipedia, Espectrometría de Masas
- Berg, Jeremy M.; Tymoczko, John L.; Stryer, Lubert. Bioquímica, Sexta Edición. W.H. Freeman y Compañía.
- Wilks, Paul. Monitoreo de procesos: ¿En línea, en línea o flujo deslizante?.
- Thayer, Ann M. CONOCE THY PROCESO:El impulso normativo para la analítica de procesos establece nuevos objetivos para la fabricación farmacéutica.
- Randall, Willis C. PAT Pendiente.
- Instrumentos ABB. Tipos de Sensores de Composición Industrial disponibles para su compra.
- Topac Inc. Celdas de Conductividad.
- Wroblewski, Wojciech. Electrodos selectivos de iones.
- Departamento de Ingeniería Química en Case Western Reserve. Enciclopedia de Electroquímica.
- Diseño y Conceptos Básicos del Turbidímetro. www.epa.gov/ogwdw/mdbp/pdf/turbidity/chap_11.pdf
Contributores
Autores: (Septiembre 14,2006) Nicole Blan, Jessica Nunn, Pamela Anne Roxas, Cynthia Sequerah
Stewards: (27 de septiembre de 2007) Eric Gauthier, Kevin Lin, Matt Naughton, Rebecca Rutishauser
Anclajes: (26 de septiembre de 2007) Megan Boekeloo, Stacy Young


