18.7: La ocurrencia, preparación y propiedades del nitrógeno
- Page ID
- 1958
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Habilidades para desarrollar
- Describir las propiedades, la preparación y los usos del nitrógeno.
La mayoría del nitrógeno puro proviene de la destilación fraccionada del aire líquido. La atmósfera consiste en 78% de nitrógeno en volumen. Esto significa que hay más de 20 millones de toneladas de nitrógeno en cada milla cuadrada de la superficie terrestre. El nitrógeno es un componente de las proteínas y del material genético (ADN/ARN) de todas las plantas y los animales.
En condiciones normales, el nitrógeno es un gas incoloro, inodoro e insípido. Hierve a 77 K y se congela a 63 K. El nitrógeno líquido es un refrigerante útil porque es económico y tiene un punto de ebullición bajo. El nitrógeno no es muy reactivo porque tiene un fuerte triple enlace entre los átomos de nitrógeno. Las únicas reacciones comunes a temperatura ambiente ocurren con el litio para formar Li3N, con ciertos complejos de metales de transición y con hidrógeno u oxígeno en bacterias fijadoras de nitrógeno. La falta de reactividad del nitrógeno hace que algunas bacterias puedan sintetizar compuestos de nitrógeno usando el gas nitrógeno atmosférico como fuente, esto es uno de los eventos químicos más interesantes de nuestro planeta. Este proceso es un tipo de fijación de nitrógeno. En este caso, la fijación de nitrógeno es el proceso en el que los organismos convierten el nitrógeno atmosférico en sustancias químicas biológicamente útiles. La fijación de nitrógeno también ocurre cuando un rayo atraviesa el aire, esto causa que el nitrógeno molecular reaccione con el oxígeno para formar los óxidos de nitrógeno, que luego son transportados a la tierra.
La fijación del nitrógeno
Todos los organismos vivos necesitan los compuestos que contienen el nitrógeno para sobrevivir. Desafortunadamente, la mayoría de estos organismos no pueden absorber el nitrógeno de su fuente más abundante: la atmósfera. El nitrógeno atmosférico consiste en moléculas de N2, que no son muy reactivas debido al fuerte triple enlace de nitrógeno-nitrógeno. Sin embargo, algunos organismos pueden superar este problema usando un proceso conocido como la fijación de nitrógeno, que se muestra en la Figura \(\PageIndex{1}\).

Figura \(\PageIndex{1}\): Todos los organismos vivos necesitan el nitrógeno. Algunos microorganismos pueden procesar el nitrógeno atmosférico usando la fijación del nitrógeno. (crédito "raíces": modificación del trabajo por el Departamento de Agricultura de los Estados Unidos; crédito "nódulos de raíz": modificación del trabajo por Louisa Howard)
La fijación del nitrógeno es el proceso en el que los organismos convierten el nitrógeno atmosférico en sustancias químicas biológicamente útiles. Hasta hoy en día, el único tipo de organismos biológicos capaces de fijar el nitrógeno son los microorganismos. Estos organismos usan enzimas llamadas nitrogenasas, que contienen hierro y molibdeno. Muchos de estos microorganismos viven en relación simbiótica con las plantas. El ejemplo más conocido es la presencia de los rizobios en los nódulos radiculares de las leguminosas.
Se necesitan grandes volúmenes de nitrógeno atmosférico para producir el amoníaco, el principal material de partida usado para la preparación de grandes cantidades de otros compuestos que contienen el nitrógeno. La mayoría de los demás usos del nitrógeno elemental dependen de su inactividad. Es útil cuando un proceso químico requiere una atmósfera inerte. Los alimentos enlatados y los embutidos no se pueden oxidar en una atmósfera de nitrógeno puro por eso retienen un mejor sabor y color, y se echan a perder con menos rapidez cuando se sellan en el nitrógeno en vez del aire. Esta tecnología permite que los productos frescos estén disponibles durante todo el año, independientemente de la temporada de cultivo.
Hay compuestos que contienen el nitrógeno en todos sus estados de oxidación desde 3− a 5+. Una gran parte de la química del nitrógeno involucra las reacciones de oxidación-reducción. Algunos metales activos (como los metales alcalinos y los metales alcalinotérreos) pueden reducir el nitrógeno para formar los nitruros metálicos. En el resto de esta sección, examinaremos la química del nitrógeno y el oxígeno.
Hay óxidos de nitrógeno bien caracterizados en los que el nitrógeno exhibe cada uno de sus números de oxidación positivos desde 1+ a 5+. Cuando el nitrato de amonio se calienta cuidadosamente se forma el óxido nitroso (óxido de dinitrógeno) y el vapor de agua. Un calentamiento más fuerte genera el gas nitrógeno, el gas oxígeno y el vapor de agua. Esta reacción no se debe intentar porque puede ser muy explosiva. En 1947, hubo una gran explosión de nitrato de amonio en Texas City, Texas, y, en 2013, hubo otra gran explosión en West, Texas. En los últimos 100 años, han ocurrido casi 30 desastres similares en todo el mundo, lo que resultó en la pérdida de muchas vidas. En esta reacción de oxidación-reducción, el nitrógeno del ion nitrato oxida el nitrógeno del ion amonio. El óxido nitroso, que se muestra en la Figura \(\PageIndex{2}\), es un gas incoloro que posee un olor agradable y un sabor dulce. Se usa como un anestésico para operaciones menores, especialmente en la odontología, donde se conoce como "gas de la risa".
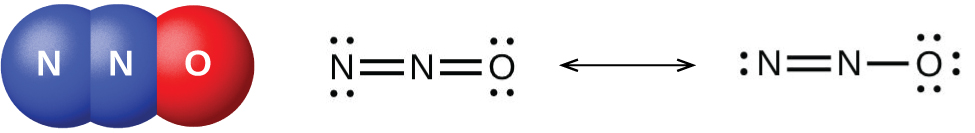
Figura \(\PageIndex{2}\): El óxido nitroso, N2O, es un anestésico que tiene estas estructuras moleculares (izquierda) y de resonancia (derecha).
Se forman bajos rendimientos de óxido nítrico, NO, cuando se calienta el nitrógeno y el oxígeno juntos. El NO también se forma cuando los relámpagos atraviesan el aire durante las tormentas eléctricas. Quemando el amoniaco es el método comercial para preparar el óxido nítrico. En el laboratorio, la reducción del ácido nítrico es el mejor método para la preparación del óxido nítrico. Cuando el cobre reacciona con el ácido nítrico diluido, el principal producto de la reducción es el óxido nítrico:
\[\ce{3Cu}(s)+\ce{8HNO3}(aq)⟶\ce{2NO}(g)+\ce{3Cu(NO3)2}(aq)+\ce{4H2O}(l)\]
El óxido nítrico gaseoso es el óxido de nitrógeno más térmicamente estable y es la más simple molécula térmicamente estable con un electrón desapareado. Es uno de los contaminantes atmosféricos generados por los motores de combustión interna. Resulta de la reacción del nitrógeno atmosférico y el oxígeno durante el proceso de la combustión.
A temperatura ambiente, el óxido nítrico es un gas incoloro que consiste en moléculas diatómicas. Como ocurre muchas veces con las moléculas que contienen un electrón desapareado, dos moléculas se combinan para formar un dímero emparejando sus electrones desapareados para formar un enlace. Tanto el NO líquido como el sólido contienen dímeros de N2O2, como el que se muestra en la Figura \(\PageIndex{3}\). La mayoría de las sustancias con electrones no apareados exhiben color al absorber la luz visible; sin embargo, el NO es incoloro porque la absorción de luz no se encuentra en la región visible del espectro.
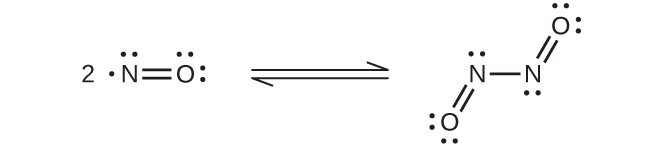
Figura \(\PageIndex{3}\): Esta figura muestra el equilibrio entre NO y N2O2. La molécula N2O2 puede absorber la luz.
El enfriamiento de una mezcla con partes iguales del óxido nítrico y el dióxido de nitrógeno a -21 °C produce el trióxido de dinitrógeno, un líquido de color azul que consisten en moléculas de N2O3 (Figura \(\PageIndex{4}\)). El trióxido de dinitrógeno existe solo en los estados líquido y sólido. Cuando se calienta, regresa a una mezcla de NO y NO2.
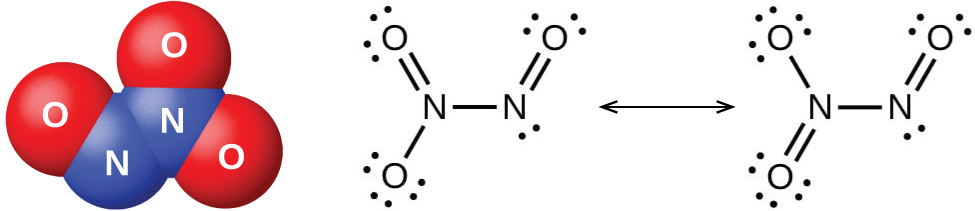
Figura \(\PageIndex{4}\): El trióxido de dinitrógeno, N2O3, solo existe en los estados líquido y sólido y tiene estas estructuras moleculares (izquierda) y de resonancia (derecha).
Es posible preparar el dióxido de nitrógeno en el laboratorio mediante la calentamiento del nitrato de un metal pesado o reduciendo el ácido nítrico concentrado con el cobre metálico, como se muestra en la Figura \(\PageIndex{5}\). Comercialmente, es posible preparar el dióxido de nitrógeno mediante la oxidación del óxido nítrico con el aire.

Figura \(\PageIndex{5}\): La reacción del cobre metálico con el HNO3 concentrado produce una solución de Cu(NO3)2 y humo de NO2 de color marrón. (crédito: modificación del trabajo de Mark Ott)
La molécula de dióxido de nitrógeno (Figura \(\PageIndex{6}\)) contiene un electrón desapareado, que es responsable por su color y paramagnetismo. También es responsable por la dimerización del NO2. A bajas presiones o altas temperaturas, el dióxido de nitrógeno es de color marrón oscuro. Este color es causado por la presencia de la molécula NO2. A bajas temperaturas, el color desaparece casi por completo cuando se forma el tetraóxido de dinitrógeno, N2O4. A temperatura ambiente, existe un equilibrio:
\[\ce{2NO2}(g)⇌\ce{N2O4}(g) \hspace{20px} K_P=6.86\]
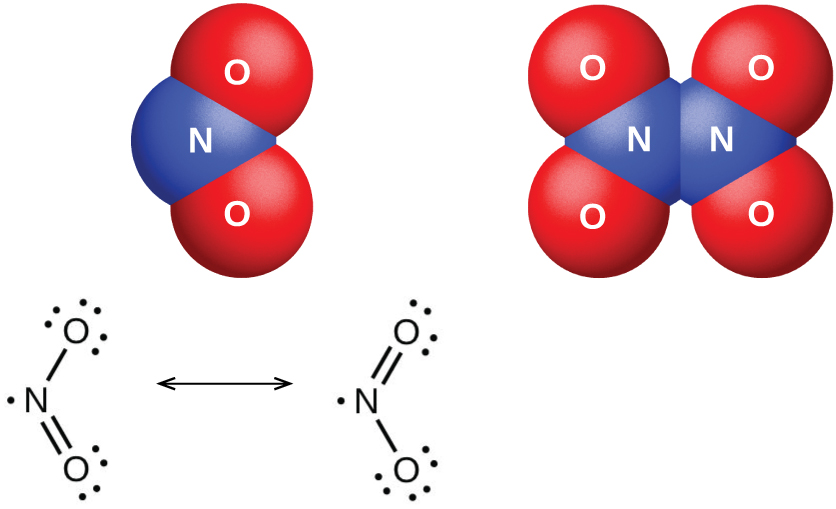
Figura \(\PageIndex{6}\): Se muestran las estructuras moleculares y de resonancia para el dióxido de nitrógeno (NO2, izquierda) y el tetraóxido de dinitrógeno (N2O4, derecha) en la figura de arriba.
Pentóxido de dinitrógeno, N2O5 (Figura \(\PageIndex{7}\)), es un sólido blanco que se forma por la deshidratación del ácido nítrico por el óxido de fósforo (V) (decoxido de tetrafosforo):
\[\ce{P4O10}(s)+\ce{4HNO3}(l)⟶\ce{4HPO3}(s)+\ce{2N2O5}(s)\]
Es inestable a temperaturas más altas que a temperaturas ambientes y se descompone en N2O4 y O2.
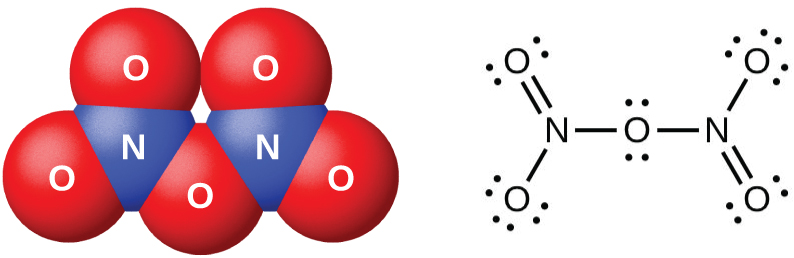
Figura \(\PageIndex{7}\): Esta imagen muestra la estructura molecular y una estructura de resonancia de una molécula de pentóxido de dinitrógeno, N2O5.
Los óxidos de nitrógeno (III), nitrógeno (IV) y nitrógeno (V) reaccionan con el agua y forman los oxiácidos que contienen el nitrógeno. El óxido de nitrógeno (III), N2O3, es el anhídrido del ácido nitroso; El HNO2 se forma cuando el N2O3 reacciona con el agua. No existen los oxiácidos estables que contienen el nitrógeno con un estado de oxidación de 4+; por eso el óxido de nitrógeno (IV), NO2, se descompone en una de dos formas cuando reacciona con el agua. En el agua fría, se forma una mezcla de HNO2 y HNO3. A temperaturas más altas, se formarán HNO3 y NO. El óxido de nitrógeno (V), N2O5, es el anhídrido del ácido nítrico; El HNO3 se produce cuando el N2O5 reacciona con el agua:
\[\ce{N2O5}(s)+\ce{H2O}(l)⟶\ce{2HNO3}(aq)\]
Los óxidos de nitrógeno poseen comportamiento de oxidación-reducción extenso. El óxido nitroso se parece al oxígeno en su comportamiento cuando se calienta con sustancias combustibles. El N2O es un agente oxidante fuerte que se descompone cuando se calienta para formar el nitrógeno y el oxígeno. Debido a que un tercio del gas liberado es oxígeno, el óxido nitroso favorece la combustión mejor que el aire (un quinto de oxígeno). En el laboratorio, tiras finas de madera explotan en llamas cuando se introduce en una botella de este gas. El óxido nítrico actúa como oxidante y como reductor. Por ejemplo:
\[\textrm{oxidizing agent: }\ce{P4}(s)+\ce{6NO}(g)⟶\ce{P4O6}(s)+\ce{3N2}(g)\]
\[\textrm{reducing agent: }\ce{Cl2}(g)+\ce{2NO}(g)⟶\ce{2ClNO}(g)\]
El dióxido de nitrógeno (o el tetraóxido de dinitrógeno) es un buen agente oxidante. Por ejemplo:
\[\ce{NO2}(g)+\ce{CO}(g)⟶\ce{NO}(g)+\ce{CO2}(g)\]
\[\ce{NO2}(g)+\ce{2HCl}(aq)⟶\ce{NO}(g)+\ce{Cl2}(g)+\ce{H2O}(l)\]
Resumen
El nitrógeno puede tener estados de oxidación desde 3- a 5+. Debido a la estabilidad del triple enlace N≡N, se necesita mucha energía para producir los compuestos a partir del nitrógeno molecular. Los metales activos como los metales alcalinos y los metales alcalinotérreos pueden reducir el nitrógeno para formar los nitruros metálicos. Los óxidos de nitrógeno y los hidruros de nitrógeno también son sustancias importantes.
Glosario
- la fijación del nitrógeno
- la formación de compuestos nitrogenados a partir del nitrógeno molecular
Contribuyentes y atribuciones
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


