18.11: La ocurrencia, preparación y propiedades de los halógenos
- Page ID
- 1962
Habilidades para desarrollar
- Describir la preparación, las propiedades y los usos de los halógenos.
- Describir las propiedades, la preparación y los usos de los compuestos halógenos
Los elementos del grupo 17 son los halógenos. Estos elementos son el flúor, cloro, bromo, yodo y astato. Estos elementos son demasiado reactivos para aparecer libremente en la naturaleza, pero sus compuestos están extensamente distribuidos. Los cloruros son los más abundantes; aunque los fluoruros, bromuros y yoduros son menos comunes, están razonablemente disponibles. En esta sección, examinaremos la presencia, la preparación y las propiedades de los halógenos. Después, examinaremos los compuestos de halógeno con los metales representativos, seguido por un estudio de los interhalógenos. Esta sección concluirá con algunas aplicaciones de los halógenos.
La ocurrencia y preparación de los halógenos
Todos los halógenos se encuentran en el agua de mar como iones de haluro. La concentración del ion cloruro es de 0.54 M; el de los otros haluros es menos que 10–4 M. El fluoruro también se encuentra en minerales como CaF2, Ca(PO4)3F y Na3AlF6. El cloruro también se encuentra en el Gran Lago Salado y el Mar Muerto, y en extensos lechos de sal que contienen NaCl, KCl o MgCl2. Parte del cloro en el cuerpo humano está presente como el ácido clorhídrico, que es un componente del ácido del estómago. Los compuestos de bromo se encuentran en el Mar Muerto y en las salmueras subterráneas. Los compuestos de yodo se encuentran en pequeñas cantidades en el salitre de Chile, las salmueras subterráneas y las algas marinas. El yodo se necesita para el funcionamiento de la glándula tiroides.
Las mejores fuentes de los halógenos (excepto el yodo) son las sales de haluros. Los iones de haluro se pueden oxidar para liberar moléculas de halógeno diatómico mediante varios métodos, dependiendo de la facilidad de oxidación del ion haluro. El fluoruro es el halógeno más difícil de oxidar, mientras que el yoduro es el más fácil.
El método principal usado para la preparación del flúor es la oxidación electrolítica. El procedimiento de electrólisis más común es la utilización de una mezcla fundida de fluoruro de hidrógeno y potasio, KHF2 y fluoruro de hidrógeno anhidro. La electrólisis causa que el HF se descomponga, formando el gas flúor en el ánodo e hidrógeno en el cátodo. Es necesario mantener los dos gases separados para evitar que reaccionen y causen una explosiva para reformar el fluoruro de hidrógeno.
Casi todo el cloro comercial proviene de la electrólisis del ión cloruro en soluciones acuosas de cloruro de sodio; este es el proceso de cloroalcalino discutido en el capítulo previo. El cloro también es un producto de la producción electrolítica de los metales como el sodio, el calcio y el magnesio a partir de sus cloruros fundidos. El cloro también se puede producir por la oxidación química del ión cloruro en una solución ácida con agentes oxidantes fuertes como el dióxido de manganeso (MnO2) o el dicromato de sodio (Na2Cr2O7). La reacción con el dióxido de manganeso es:
\[\ce{MnO}_{2(s)}+\ce{2Cl^-}_{(aq)}+\ce{4H_3O^+}_{(aq)}⟶\ce{Mn}^{2+}_{(aq)}+\ce{Cl}_{2(g)}+\ce{6H_2O}_{(l)} \tag{\(\PageIndex{1}\)}\]
La preparación comercial del bromo involucra la oxidación del ion bromuro por el cloro:
\[\ce{2Br^-}_{(aq)}+\ce{Cl}_{2(g)}⟶\ce{Br}_{2(l)}+\ce{2Cl^-}_{(aq)} \tag{\(\PageIndex{2}\)}\]
El cloro es un agente oxidante más fuerte que el bromo. Este método es importante para la producción de casi todo el bromo doméstico.
Un poco del yodo proviene de la oxidación del cloruro de yodo, ICl o el ácido yódico, \(\ce{H10_3}\). La preparación comercial del yodo usa la reducción del yodato de sodio, \(\ce{NaIO_3}\), una impureza en los depósitos de salitre de Chile, con hidrogenosulfito de sodio:
\[\ce{2IO^-}_{3(aq)}+\ce{5HSO^-}_{3(aq)}⟶\ce{3HSO^-}_{4(aq)}+\ce{2SO^{2-}}_{4(aq)}+\ce{H_2O}_{(l)}+\ce{I}_{2(s)} \tag{\(\PageIndex{3}\)}\]
Las propiedades de los halógenos
El flúor es un gas de color amarillo pálido, el cloro es un gas de color amarillo verdoso, del bromo es un líquido de color marrón rojizo oscuro y el yodo es un sólido cristalino de color negro grisáceo. El bromo líquido tiene una alta presión de vapor y el vapor rojizo se puede ver fácilmente en la Figura \(\PageIndex{1}\). Los cristales de yodo tienen una presión de vapor notable. Cuando se calientan despacio, estos cristales se subliman y forman un vapor de hermoso color violeta intenso.

Figura \(\PageIndex{1}\): El cloro es un gas de color amarillo verdoso pálido (izquierda), el bromo gaseoso es de color naranja intenso (centro) y el yodo gaseoso es de color púrpura (derecha). (El flúor es tan reactivo que es demasiado peligroso para manipular). (crédito: Sahar Atwa)
El bromo es solo un poco soluble en el agua, pero es miscible en casi todos los solventes menos polares (o apolares) como el cloroformo, el tetracloruro de carbono y el disulfuro de carbono, formando soluciones que varían de colores desde amarillo a marrón rojizo, según la concentración.
El yodo es soluble en el cloroformo, el tetracloruro de carbono, el disulfuro de carbono y muchos hidrocarburos, produciendo soluciones de color violeta con moléculas de I2. El yodo se disuelve solo un poco en el agua, produciendo soluciones de color marrón. Es bastante soluble en soluciones acuosas de yoduros, con los que forma soluciones de color marrón. Estas soluciones de color marrón se deben a que las moléculas de yodo tienen orbitales de valencia d vacíos y pueden actuar como ácidos de Lewis débiles hacia el ion yoduro. La ecuación para la reacción reversible del yodo (ácido de Lewis) con el ion yoduro (base de Lewis) para formar el ion triyoduro, \(\ce{I3-}\), es:
\[\ce{I}_{2(s)}+\ce{I^-}_{(aq)}⟶\ce{I^-}_{3(aq)} \tag{\(\PageIndex{4}\)} \]
Cuanto más fácil sea oxidar el ion haluro, más difícil será que el halógeno actúe como el agente oxidante. El flúor generalmente oxida un elemento a su estado de oxidación más alto, mientras que los halógenos más pesados no pueden hacer esto. Por ejemplo, cuando el exceso de flúor reacciona con el azufre, se forma \(\ce{SF_6}\). El cloro produce \(\ce{SCl_2}\) y el bromo, \(\ce{S_2Br_2}\). El yodo no reacciona con el azufre.
El flúor es el agente oxidante más fuerte de los elementos conocidos. Puede espontáneamente oxidar la mayoría de los demás elementos; por lo tanto, la reacción inversa, la oxidación de los fluoruros, es muy difícil de lograr. El flúor reacciona directamente y forma los fluoruros binarios con todos los elementos excepto los gases nobles más ligeros (He, Ne y Ar). El flúor es un agente oxidante tan fuerte que muchas sustancias se encienden al contactarlo. Las gotas de agua se encienden en el flúor y forman \(\ce{O_2}\), \(\ce{OF_2}\), \(\ce{H_2O_2}\), \(\ce{O_3}\) y \(\ce{HF}\). La madera y el asbesto se encienden y se queman en el gas flúor. La mayoría de los metales calientes arden vigorosamente en el flúor. Sin embargo, es posible manipular el flúor en recipientes de cobre, hierro o níquel porque una capa adherente de la sal de fluoruro pasiva sus superficies. El flúor es el único elemento que reacciona directamente con el xenón, un gas noble.
Aunque es un agente oxidante fuerte, el cloro es menos activo que el flúor. Mezclando el cloro e hidrógeno en la oscuridad hace que la reacción entre los elementos sea demasiadamente lenta. La exposición de la mezcla a la luz causa que los dos elementos reaccionen explosivamente. El cloro también es menos activo hacia los metales que el flúor, y las reacciones de oxidación normalmente requieren temperaturas más altas. El sodio fundido se enciende en el cloro. El cloro reacciona con la mayoría de los no metales (C, N2 y O2 son excepciones notables), formando compuestos moleculares covalentes. El cloro generalmente reacciona con los compuestos que contienen solo carbono e hidrógeno (hidrocarburos) mediante la adición de enlaces múltiples o por sustitución.
En el agua fría, el cloro pasa por una reacción de descomposición:
\[\ce{Cl}_{2(aq)}+\ce{2H_2O}_{(l)}⟶\ce{HOCl}_{(aq)}+\ce{H_3O^+}_{(aq)}+\ce{Cl^-}_{(aq)} \tag{\(\PageIndex{5}\)} \]
Una mitad de los átomos de cloro se oxidan al estado de oxidación 1+ (el ácido hipocloroso) y la otra mitad se reducen al estado de oxidación 1− (el ion cloruro). Esta descomposición es incompleta, por eso el agua con el cloro es una mezcla en equilibrio de moléculas de cloro, moléculas de ácido hipocloroso, iones de hidronio e iones de cloruro. Cuando se expone a la luz, esta solución pasa por una descomposición fotoquímica:
\[\ce{2HOCl}_{(aq)}+\ce{2H_2O}_{(l)}\xrightarrow{\ce{sunlight}} \ce{2H_3O^+}_{(aq)}+\ce{2Cl^-}_{(aq)}+\ce{O}_{2(g)} \tag{\(\PageIndex{6}\)} \]
El cloro no metálico es más electronegativo que cualquier otro elemento excepto el flúor, el oxígeno y el nitrógeno. En general, los elementos muy electronegativos son buenos agentes oxidantes; por eso, esperaríamos que el cloro elemental oxidara todos los demás elementos excepto estos tres (y los gases nobles no reactivos). Su propiedad oxidante, de hecho, es responsable para su uso principal. Por ejemplo, el cloruro de fósforo (V), un intermedio importante en la preparación de las insecticidas y armas químicas, se fabrica usando la oxidación del fósforo con cloro:
\[\ce{P}_{4(s)}+\ce{10Cl}_{2(g)}⟶\ce{4PCl}_{5(l)} \tag{\(\PageIndex{7}\)} \]
También se usa una gran cantidad de cloro para oxidar y destruir los materiales orgánicos o biológicos en la depuración y blanqueo del agua.
Las propiedades químicas del bromo son similares a las del cloro, aunque el bromo es el agente oxidante más débil y su reactividad es menos que la del cloro.
El yodo es el halógeno menos reactivo. Es el agente oxidante más débil y el ion yoduro es el ion haluro que se oxida más fácilmente. El yodo reacciona con los metales, pero a veces se requiere el calentamiento. No oxida otros iones de haluro.
En comparación con los otros halógenos, el yodo reacciona solo un poco con el agua. Las trazas de yodo en el agua reaccionan con una mezcla de almidón e ión yoduro, formando un color azul intenso. Esta reacción es una prueba muy sensible que muestra la presencia del yodo en el agua.
Los haluros de los metales representativos
Se han preparado miles de sales de los metales representativos. Los haluros binarios son una subclase importante de sales. Una sal es un compuesto iónico compuesto de cationes y aniones, distintos de los iones de hidróxido u óxido. En general, es posible preparar estas sales a partir de los metales o de óxidos, hidróxidos o carbonatos. Discutiremos los tipos de reacciones generales para la preparación de sales a través de las reacciones usadas para preparar los haluros binarios.
Los compuestos binarios de un metal con halógenos se llaman los haluros. La mayoría de los haluros binarios son iónicos. Sin embargo, el mercurio, los elementos del grupo 13 con estados de oxidación de 3+, el estaño (IV) y el plomo (IV) forman haluros binarios covalentes. La reacción directa de un metal y un halógeno produce el haluro del metal correspondiente. Ejemplos de estas reacciones de oxidación-reducción incluyen:
\[\ce{Cd}_{(s)}+\ce{Cl}_{2(g)}⟶\ce{CdCl}_{2(s)} \tag{\(\PageIndex{8}\)}\]
Video \(\PageIndex{1}\): Las reacciones de los metales alcalinos con los halógenos elementales son muy exotérmicas y, a veces, bastante violentas. En condiciones controladas, ofrecen demostraciones interesantes para los estudiantes de química. Puede ver el calentamiento inicial del sodio que elimina la capa de hidróxido de sodio, peróxido de sodio y aceite mineral residual para exponer la superficie reactiva. La reacción con el cloro gaseoso procede fácilmente.
Si un metal puede presentar dos estados de oxidación, pueda ser necesario controlar la estequiometría para producir el haluro con el estado de oxidación más bajo. Por ejemplo, la preparación del cloruro de estaño (II) requiere una proporción de 1: 1 de Sn a \(\ce{Cl_2}\), mientras que la preparación del cloruro de estaño (IV) requiere una proporción de 1: 2:
\[\ce{Sn}_{(s)}+\ce{Cl}_{2(g)}⟶\ce{SnCl}_{2(s)} \tag{\(\PageIndex{8}\)}\]
\[\ce{Sn}_{(s)}+\ce{2Cl}_{2(g)}⟶\ce{SnCl}_{4(l)} \tag{\(\PageIndex{9}\)}\]
Los metales representativos activos, aquellos que son más fáciles de oxidar que el hidrógeno, reaccionan con los haluros de hidrógeno gaseosos para producir los haluros metálicos e hidrógeno. La reacción del zinc con el fluoruro de hidrógeno es:
\[\ce{Zn}_{(s)}+\ce{2HF}_{(g)}⟶\ce{ZnF}_{2(s)}+\ce{H}_{2(g)} \tag{\(\PageIndex{10}\)}\]
Los metales representativos activos también reaccionan con soluciones de haluros de hidrógeno para formar el hidrógeno y las soluciones de los correspondientes haluros. Ejemplos de estas reacciones incluyen:
\[\ce{Cd}_{(s)}+\ce{2HBr}_{(aq)}⟶\ce{CdBr}_{2(aq)}+\ce{H}_{2(g)} \tag{\(\PageIndex{11}\)}\]
\[\ce{Sn}_{(s)}+\ce{2HI}_{(aq)}⟶\ce{SnI}_{2(aq)}+\ce{H}_{2(g)} \tag{\(\PageIndex{12}\)}\]
Los hidróxidos, carbonatos y algunos óxidos reaccionan con las soluciones de haluros de hidrógeno para producir soluciones de sales de haluros. Se pueden preparar sales adicionales usando la reacción de estos hidróxidos, carbonatos y óxidos con una solución acuosa de otros ácidos:
\[\ce{CaCo}_{3(s)}+\ce{2HCl}_{(aq)}⟶\ce{CaCl}_{2(aq)}+\ce{CO}_{2(g)}+\ce{H_2O}_{(l)} \tag{\(\PageIndex{13}\)}\]
\[\ce{TlOH}_{(aq)}+\ce{HF}_{(aq)}⟶\ce{TlF}_{(aq)}+\ce{H_2O}_{(l)} \tag{\(\PageIndex{14}\)}\]
Algunos haluros y muchas de las otras sales de los metales representativos son insolubles. Se pueden preparar estas sales solubles usando las reacciones de metátesis que ocurre cuando se mezclan las soluciones de las sales solubles (Figura \(\PageIndex{2}\)). Las reacciones de la metátesis se discuten en el capítulo sobre la estequiometría de las reacciones químicas.

Figura \(\PageIndex{2}\): El HgI2 sólido se forma cuando se mezclan soluciones de KI y Hg(NO3)2. (crédito: Sahar Atwa).
Varios haluros se encuentran en grandes cantidades en la naturaleza. Las salmueras oceánicas y subterráneas contienen muchos haluros. Por ejemplo, el cloruro de magnesio en el océano es la fuente de iones de magnesio que se usan en la producción del magnesio. Grandes depósitos subterráneos de cloruro de sodio, como la mina de sal que se muestra en la Figura \(\PageIndex{3}\), ocurren en muchas partes del mundo. Estos depósitos sirven como fuentes de sodio y cloro en casi todos los demás compuestos que contienen estos elementos. El proceso de cloroalcalino es un ejemplo.

Figura \(\PageIndex{3}\): Los depósitos subterráneos del cloruro de sodio se encuentran en todo el mundo y a veces se extraen. Este es un túnel en la mina de sal de Kłodawa en Polonia. (crédito: Jarek Zok).
Los interhalógenos
Los compuestos que se forman a partir de dos o más halógenos diferentes se llaman los interhalógenos. Las moléculas de los interhalógenos consisten en un átomo del halógeno más pesado unido por enlaces simples a un número impar de átomos del halógeno más ligero. Las estructuras de IF3, IF5 y IF7 se muestran en la Figura \(\PageIndex{4}\). Las fórmulas para los otros interhalógenos que provienen de la reacción de los respectivos halógenos, se encuentran en la Tabla \(\PageIndex{1}\).
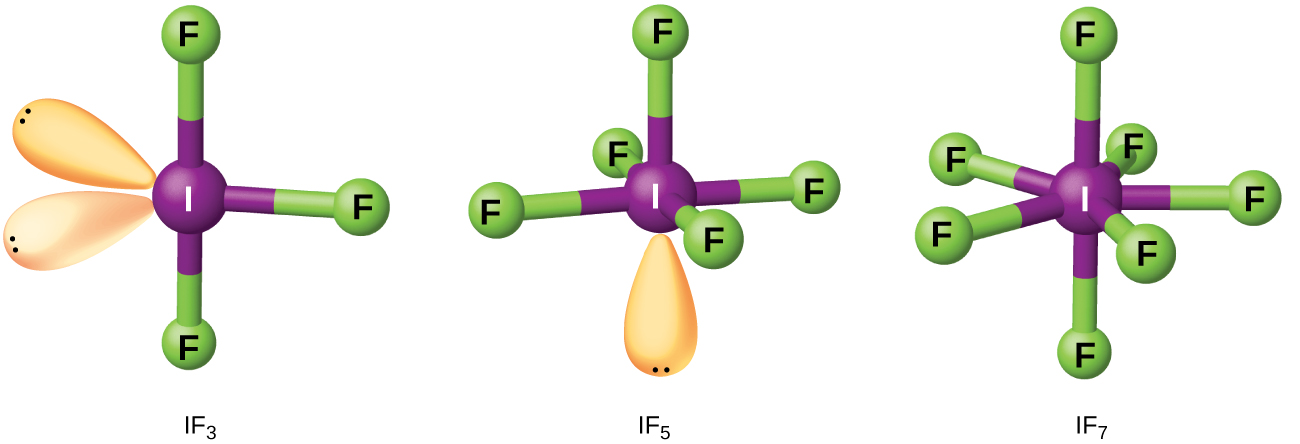
Figura \(\PageIndex{4}\): La estructura de IF3 tiene la forma de T (izquierda), IF5 es piramidal cuadrada (centro) y IF7 es bipiramidal pentagonal (derecha).
Observe en la Tabla \(\PageIndex{1}\) que el flúor puede oxidar el yodo a su estado de oxidación máximo, 7+, mientras que el bromo y el cloro, que son más difíciles de oxidar, alcanzan solo el estado de oxidación 5+. Un estado de oxidación 7+ es el límite para los halógenos. Debido a que los halógenos más pequeños se agrupan alrededor de uno más grande, el número máximo de átomos más pequeños posibles aumenta cuando aumenta el radio del átomo más grande. Muchos de estos compuestos son inestables y la mayoría son extremadamente reactivos. Los interhalógenos reaccionan como los haluros componentes; por ejemplo, los fluoruros de halógeno son agentes oxidantes más fuertes que los cloruros de halógeno.
| YX | YX3 | YX5 | YX7 |
|---|---|---|---|
| BrCl(g) | |||
| BrF(g) | BrF3(l) | BrF5(l) | |
| ClF(g) | ClF3(g) | ClF5(g) | |
| IBr(s) | |||
| ICl(l) | ICl3(s) | ||
| IF(s) | IF3(s) | IF5(l) | IF7(g) |
Los polihaluros iónicos de los metales alcalinos, como KI3, KICl2, KICl4, CsIBr2 y CsBrCl2, que contienen un anión compuesto por al menos tres átomos de halógeno, están relacionados con los interhalógenos. Como se vio en un capítulo anteriormente, la formación del anión polihaluro \(\ce{I_3^-}\) es responsable por la solubilidad del yodo en soluciones acuosas que contienen un ion yoduro.
Las aplicaciones
El ion fluoruro y los compuestos de flúor tienen muchos usos importantes. Los compuestos de carbono, hidrógeno y flúor reemplazan los freones (compuestos de carbono, cloro y flúor) como refrigerantes. El teflón es un polímero compuesto por unidades de –CF2CF2–. El ion fluoruro se agrega a los suministros de agua y a algunas pastas dentales como SnF2 o NaF para combatir las caries. El fluoruro parcialmente convierte los dientes de Ca5(PO4)3(OH) en Ca5(PO4)3F.
El cloro es un blanqueador importante para la pulpa de la madera y la tela del algodón. El cloro reacciona con el agua para formar el ácido hipocloroso, que oxida las sustancias coloreadas a incoloras. Grandes cantidades de cloro son importantes en la cloración de los hidrocarburos (reemplazando el hidrógeno con el cloro) para producir los compuestos como el tetracloruro (CCl4), cloroformo (CHCl3) y cloruro de etilo (C2H5Cl), y en la producción del cloruro de polivinilo (PVC) y otros polímeros. El cloro también es importante porque mata bacterias en los suministros de agua de la comunidad.
El bromo es importante en la producción de ciertos tintes y los bromuros de sodio y potasio se usan como sedantes. A un punto, el bromuro de plata susceptible a la luz era un componente de la película fotográfica.
El yodo en una solución alcohólica con el yoduro de potasio es un antiséptico (tintura de yodo). Las sales de yoduro son esenciales para el funcionamiento correcto de la glándula tiroides; una deficiencia de yodo puede causar el desarrollo de bocio. La sal de mesa yodada contiene 0.023% de yoduro de potasio. El yoduro de plata es útil en la siembra de nubes para inducir la lluvia; fue importante en la producción de las películas fotográficas y el yodoformo, CHI3, es un antiséptico.
Resumen
Los halógenos forman haluros con elementos menos electronegativos. Los haluros de los metales varían de iónicos a covalentes; los haluros de los no metales son covalentes. Los interhalógenos se forman usando la combinación de dos o más halógenos diferentes. Todos los metales representativos reaccionan directamente con los halógenos elementales o con soluciones de ácidos hidrohálicos (HF, HCl, HBr y HI) para producir los haluros metálicos representativos. Otras preparaciones de laboratorio involucran la adición de los ácidos hidrohálicos acuosos a compuestos que contienen tales aniones básicos, como hidróxidos, óxidos o carbonatos.
Contribuyentes y Atribuciones
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


