4.8: Conformaciones de Ciclohexanos Monosustituidos
- Page ID
- 76371
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Objetivo de aprendizaje
- dibujar conformadores de ciclohexano monosustituidos (solo silla)
- correlacionar energías de conformaciones con diagramas de energía rotacional y predecir las conformaciones más estables para butano, alcanos superiores, ciclohexano, ciclohexanos monosustituidos y ciclohexanos disustituidos
Introducción
Debido a que los enlaces axiales son paralelos entre sí, los sustituyentes más grandes que el hidrógeno generalmente sufren una mayor aglomeración estérica cuando están orientados axiales en lugar de ecuatoriales. En consecuencia, los ciclohexanos sustituidos adoptarán preferencialmente conformaciones en las que los sustituyentes mayores asumen orientación ecuatorial.
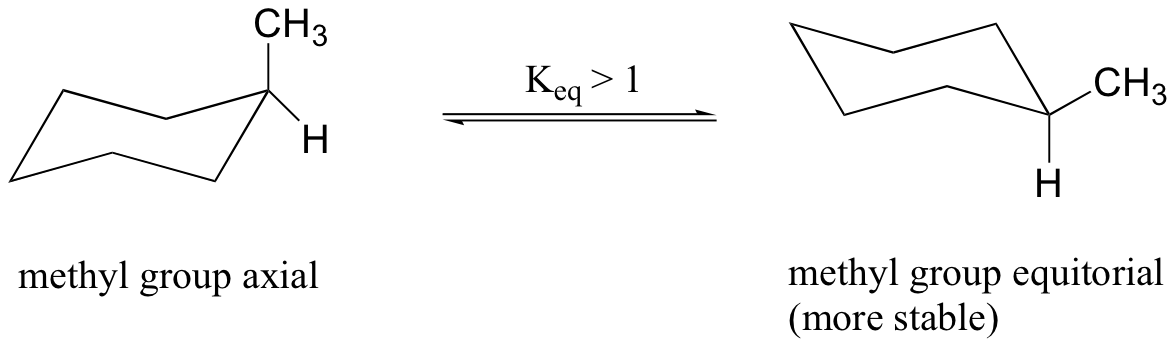
Cuando el grupo metilo en la estructura anterior ocupa una posición axial sufre hacinamiento estérico por los dos hidrógenos axiales ubicados en el mismo lado del anillo. La conformación en la que el grupo metilo es ecuatorial es más estable, y así el equilibrio se encuentra en esta dirección.

Al examinar posibles estructuras para los ciclohexanos monosustituidos, es útil seguir dos principios:
- Las conformaciones de las sillas son generalmente más estables que otras posibilidades.
- Los sustituyentes en los conformadores de silla prefieren ocupar posiciones ecuatoriales debido al aumento del impedimento estérico de las ubicaciones axiales.
Mediciones experimentales de impedimento estérico
El impedimento estérico relativo experimentado por diferentes grupos sustituyentes orientados en una ubicación axial versus ecuatorial en ciclohexano puede ser determinado por el equilibrio conformacional del compuesto. La constante de equilibrio correspondiente está relacionada con la diferencia de energía entre los conformadores y la recolección de dichos datos permite evaluar la tendencia relativa de los sustituyentes a existir en una ubicación ecuatorial o axial.
Al observar los valores energéticos de la tabla, es claro que el “tamaño” aparente de un sustituyente (en términos de su preferencia por la orientación ecuatorial sobre la axial) está influenciado por su ancho y longitud de enlace al ciclohexano, como lo demuestra el hecho de que un grupo vinilo axial está menos obstaculizado que el etilo, y el yodo ligeramente menos que el cloro.
| Sustentante | \(-\Delta{G}^o\)kcal/mol | Sustentante | \(-\Delta{G}^o\)kcal/mol |
|---|---|---|---|
| \(\ce{CH_3\bond{-}}\) | \ (-\ Delta {G} ^o\) kcal/mol” style="text-align:center; ">1.7 | \(\ce{O_2N\bond{-}}\) | \ (-\ Delta {G} ^o\) kcal/mol” style="text-align:center; ">1.1 |
| \(\ce{CH_2H_5\bond{-}}\) | \ (-\ Delta {G} ^o\) kcal/mol” style="text-align:center; ">1.8 | \(\ce{N#C\bond{-}}\) | \ (-\ Delta {G} ^o\) kcal/mol” style="text-align:center; ">0.2 |
| \(\ce{(CH_3)_2CH\bond{-}}\) | \ (-\ Delta {G} ^o\) kcal/mol” style="text-align:center; ">2.2 | \(\ce{CH_3O\bond{-}}\) | \ (-\ Delta {G} ^o\) kcal/mol” style="text-align:center; ">0.5 |
| \(\ce{(CH_3)_3C\bond{-}}\) | \ (-\ Delta {G} ^o\) kcal/mol” style="text-align:center; ">\(\geq 5.0\) | (CH 3) 3 C- | \ (-\ Delta {G} ^o\) kcal/mol” style="text-align:center; ">0.7 |
| \(\ce{F\bond{-}}\) | \ (-\ Delta {G} ^o\) kcal/mol” style="text-align:center; ">0.3 | F- | \ (-\ Delta {G} ^o\) kcal/mol” style="text-align:center; ">1.3 |
| \(\ce{Cl\bond{-}}\) | \ (-\ Delta {G} ^o\) kcal/mol” style="text-align:center; ">0.5 | \(\ce{C_6H_5\bond{-}}\) | \ (-\ Delta {G} ^o\) kcal/mol” style="text-align:center; ">3.0 |
| \(\ce{Br\bond{-}}\) | \ (-\ Delta {G} ^o\) kcal/mol” style="text-align:center; ">0.5 | \ (-\ Delta {G} ^o\) kcal/mol” style="text-align:center; "> | |
| \(\ce{I\bond{-}}\) | \ (-\ Delta {G} ^o\) kcal/mol” style="text-align:center; ">0.5 | \ (-\ Delta {G} ^o\) kcal/mol” style="text-align:center; "> |
Ejercicio
1. En la molécula, ciclohexil etino hay poca cepa estérica, ¿por qué?
- Contestar
-
1.
El grupo etino es lineal y por lo tanto no afecta a los hidrógenos en las posiciones 1,3 para decir en la medida en que lo haría un grupo más voluminoso o doblado (por ejemplo, grupo eteno). Esto lleva a una menor tensión en la molécula.

Colaboradores y Atribuciones
Dr. Dietmar Kennepohl FCIC (Professor of Chemistry, Athabasca University)
Prof. Steven Farmer (Sonoma State University)
- Robert Bruner (http://bbruner.org)
Organic Chemistry With a Biological Emphasis by Tim Soderberg (University of Minnesota, Morris)

