10.10: Una introducción a la síntesis de múltiples pasos
- Page ID
- 76008
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Objetivo de aprendizaje
- utilizar el análisis retrosintético para diseñar una síntesis multietapa con regioquímica y estereoquímica correctas utilizando las reacciones estudiadas hasta la fecha
Introducción
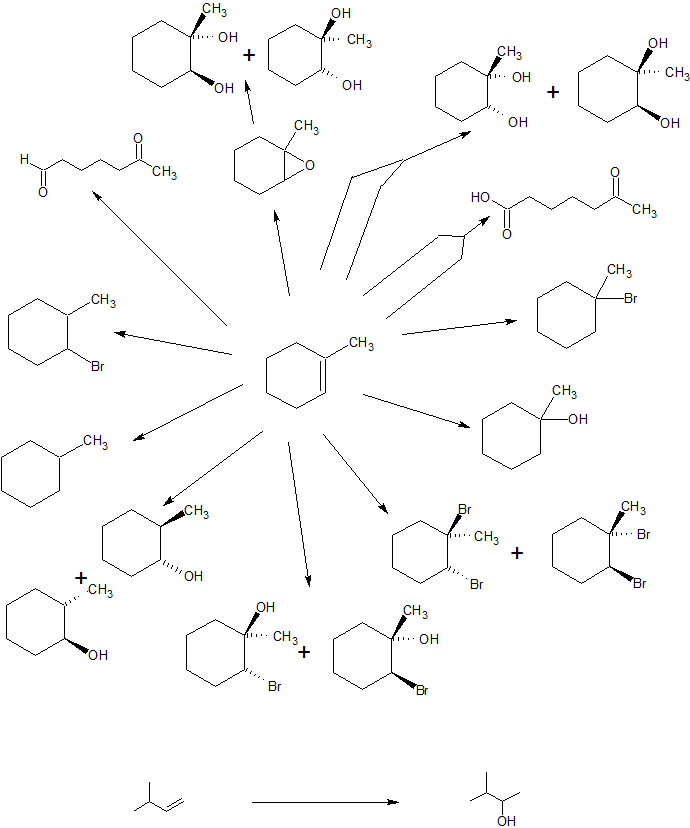
El estudio de la química orgánica introduce a los estudiantes a una amplia gama de reacciones interrelacionadas. Los alquenos, por ejemplo, pueden convertirse en alcanos, alcoholes, haluros de alquilo, epóxidos, glicoles y boranos estructuralmente similares; escindirse en aldehídos, cetonas y ácidos carboxílicos más pequeños; y agrandarse por adición de carbocationes y radicales así como cicloadiciones. La mayoría de estas reacciones se muestran en el Mapa de Reacciones de Alqueno a continuación. Todos estos productos pueden transformarse posteriormente en una gran cantidad de nuevos compuestos que incorporan una amplia variedad de grupos funcionales. En consecuencia, la concepción lógica de una síntesis de múltiples etapas para la construcción de un compuesto designado a partir de un material de partida específico se convierte en uno de los problemas más desafiantes que se pueden plantear. Los mapas de reacción de grupos funcionales como el siguiente para alquenos pueden ser útiles en el diseño de síntesis de múltiples etapas. Puede ser útil construir y diseñar sus propios mapas de reacción para cada grupo funcional estudiado.
Mapa - Reacción alqueno
Nota: Los reactivos para cada transformación química se han omitido intencionadamente para que este mapa pueda ser utilizado como herramienta de estudio. Las respuestas se proporcionan al final de esta sección como parte de los ejercicios.
Sintesis Simple de Múltiples Pasos
Una secuencia de uno o dos pasos de reacciones simples no es tan difícil de deducir. Por ejemplo, la síntesis de meso-3,4-hexanodiol a partir de 3-hexino puede ocurrir por más de una vía de múltiples etapas.
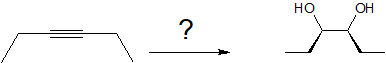
Un enfoque sería reducir el alquino a cis o trans-3-hexeno antes de emprender la formación de glicol. La hidroxilación de permanaganato o tetroóxido de osmio de cis-3-hexeno formaría el isómero meso deseado.
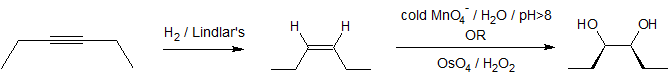
A partir del trans-3-hexeno, sería necesario epoxidar primero el alqueno con un perácido seguido de la apertura del anillo con hidrólisis ácida o básica.

Las síntesis multipaso más largas requieren un análisis y un pensamiento cuidadosos, ya que hay que considerar muchas opciones. Al igual que un ajedrecista experto que evalúa los pros y los contras de los movimientos potenciales de largo alcance, el químico debe evaluar el éxito potencial de varias vías de reacción posibles, centrándose en el alcance y las limitaciones que constreñen cada una de las reacciones individuales que se emplean. La habilidad se adquiere por la práctica, la experiencia y, a menudo, el ensayo y error.
Pensándolo a través con 3 ejemplos
Los siguientes tres ejemplos ilustran estrategias para desarrollar síntesis multipaso a partir de las reacciones estudiadas en los diez primeros capítulos de este texto. Es útil buscar sistemáticamente cambios estructurales comenzando con la cadena de carbono y hacer una lluvia de ideas sobre las reacciones de conversión de grupos funcionales relevantes. La retrosíntesis es el enfoque de trabajar hacia atrás desde el producto hasta el material de partida.
En el primer ejemplo, se nos pide sintetizar 1-butanol a partir del acetileno.
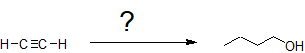
La cadena carbonada duplica su tamaño, lo que indica una reacción de acetiluro S N 2 con un haluro de alquilo. La formación de alcohol primario a partir de una reacción de hidratación de alquenos anti-Markovnikov (hidroboración-oxidación) es más probable que una reacción de sustitución. Aplicando la retrosíntesis, trabajamos hacia atrás del alcohol al alqueno y al alquino a partir de una reacción de acetiluro que inicialmente construye la cadena de carbono.
Retro-Síntesis
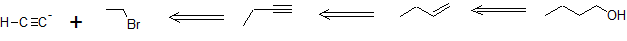
Trabajando hacia adelante, especificamos los reactivos necesarios para cada transformación identificada a partir de la retrosíntesis. El bromuro de etilo también debe derivarse del acetileno por lo que se combinan múltiples rutas de reacción como se muestra a continuación.
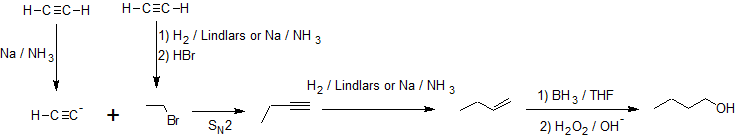
En el segundo ejemplo, se nos pide sintetizar 1,2-dibromobutano a partir del acetileno.
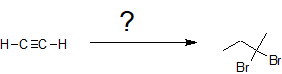
Una vez más se produce un incremento en la longitud de la cadena carbonada que indica una reacción de acetilido S N 2 con un haluro de alquilo similar al primer ejemplo. La hidrohalogenación puede ser sutil de discernir porque los átomos de hidrógeno no se muestran en las estructuras de la línea de enlace. Al comparar las fórmulas químicas de 1-butino con 1,2-dibromobutano, hay una diferencia de dos átomos de H y dos átomos de Br, lo que indica hidrohalogenación y no halogenación. La adición de ambos átomos de bromo al mismo átomo de carbono también respalda la idea de que la hidrohalogenación ocurre en un alquino y no en un alqueno. La formación del dihaluro geminal también indica hidrohalogenación en lugar de halogenatioína porque la halogenación produce dihaluros vecinales. Con esta visión, la retrosíntesis indica la siguiente serie de transformaciones químicas.
Retro-Síntesis
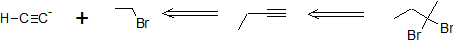
Trabajando hacia adelante, especificamos los reactivos necesarios para cada transformación.
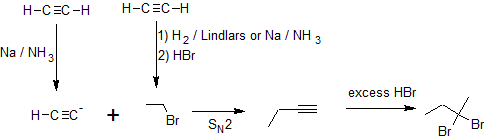
En el tercer ejemplo, se nos pide producir 6-oxoheptanal a partir de metilciclohexano.
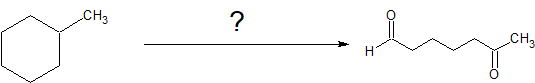
Contando los carbonos, el material de partida y el producto contienen siete átomos de carbono y hay una reacción de escisión de un alqueno en condiciones reductoras. Un aspecto importante que falta de esta reacción es un buen grupo de salida (LG). Los alcanos son químicamente bastante aburridos. Podemos quemarlos como combustible o realizar halogenación de radicales libres para crear haluros de alquilo con excelentes grupos salientes. Con estas observaciones, es razonable la siguiente retrosíntesis.
Retro-Síntesis
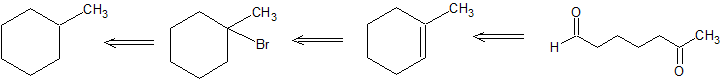
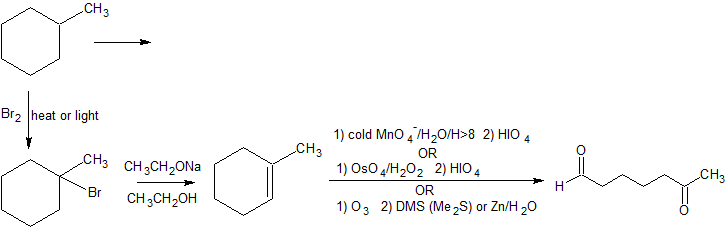
Trabajando hacia adelante, especificamos los reactivos necesarios para cada reacción. Para la halogenación inicial por radicales libres del alcano, tenemos la opción de cloro (Cl2) o bromo (Br2). Debido a que el metilciclohexano tiene varias clasificaciones diferentes de carbonos, la selectividad de Br2 es más importante que la reactividad más rápida de Cl2. Una base fuerte con calor se puede utilizar para el segundo paso para seguir un mecanismo E2 y formar 1-metilciclohexeno. El grupo aldehído en el producto final indica una escisión oxidativa suave por cualquiera de varias vías de reacción. Estas reacciones se pueden combinar en la siguiente síntesis de múltiples etapas.
Mapas de reacción para construir dominio de conversión de grupos funcionales
Después de trabajar con los ejemplos anteriores, podemos ver lo importante que es memorizar todas las reacciones grupales funcionales estudiadas en los diez primeros capítulos. Podemos aplicar el conocimiento de estas reacciones a la sabiduría de las síntesis de varios pasos.
Tenga en cuenta: Los reactivos para cada transformación química se han omitido intencionalmente para que estos mapas puedan ser utilizados como herramientas de estudio. Las respuestas se proporcionan al final de esta sección como parte de los ejercicios.
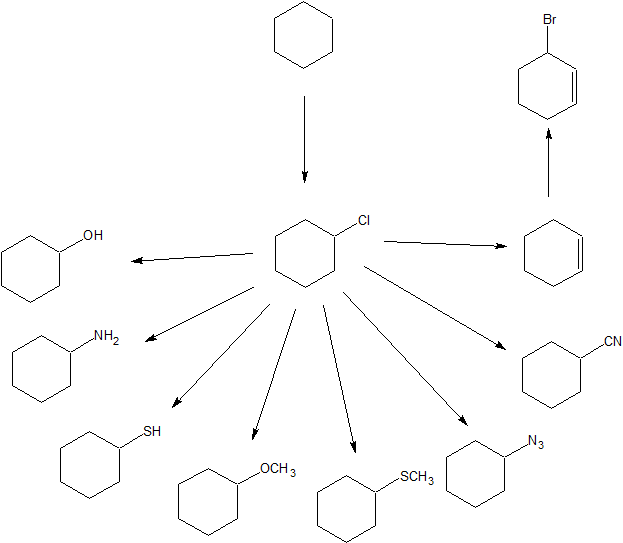
Mapa de Reacción de Alcano y Halogen
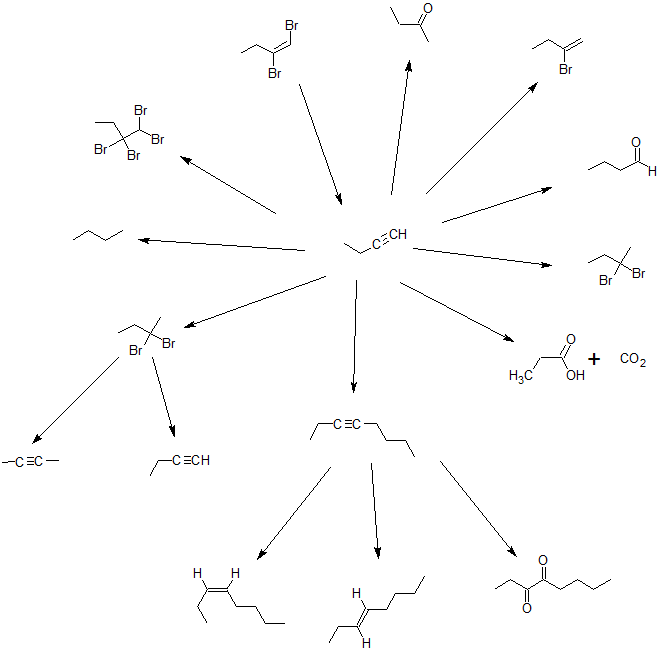
Mapa - Reacción alquino
Ejercicio
1. Comenzando en 3-hexino predecir rutas sintéticas para lograr:
a) trans -3-hexeno
b) 3,4-dibromohexano
c) 3-hexanol.
2. Partiendo de acetileno y cualquier haluros de alquilo se propone una síntesis para hacer
a) pentanal
b) hexano.
- Contestar
-
1.

2.
.png)
Colaboradores y Atribuciones
Dr. Dietmar Kennepohl FCIC (Professor of Chemistry, Athabasca University)
Prof. Steven Farmer (Sonoma State University)
William Reusch, Professor Emeritus (Michigan State U.), Virtual Textbook of Organic Chemistry

