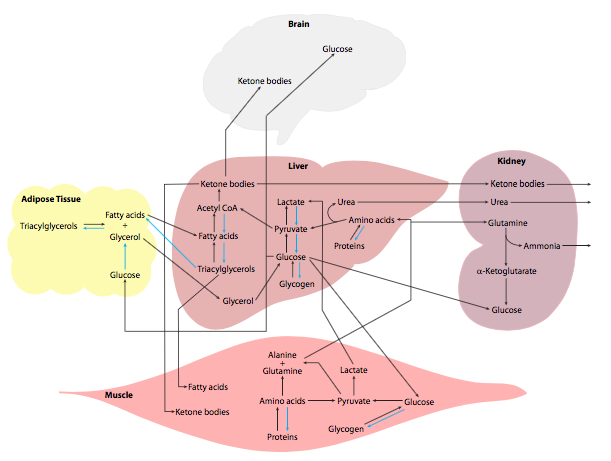
5.9: Degradación de aminoácidos
- Page ID
- 52975
Las proteínas son descompuestas por una variedad de proteasas que hidrolizan los enlaces peptídicos para generar péptidos y aminoácidos más pequeños. Aquellos aminoácidos que no se utilizan para la construcción de nuevas proteínas se pueden descomponer aún más para entrar en los procesos metabólicos discutidos en este capítulo.
Existe una gran variedad de proteasas, clasificadas en uno de los seis grupos (a partir de 2008): serina proteasas, metaloproteasas, proteasas de ácido aspártico, cisteína proteasas, treonina proteasas y proteasas de ácido glutámico. Todos ellos trabajan formando un nucleófilo en su sitio activo para atacar al grupo carbonilo peptídico. Difieren en la construcción de sus sitios activos, y la especificidad de las secuencias diana a ser escindidas. La base de datos MEROPS (http://merops.sanger.ac.uk/) enumera cientos de enzimas y sus sitios específicos de reconocimiento. Al igual que con otras enzimas, el reconocimiento se basa en la formación de enlaces de hidrógeno estabilizantes entre la enzima y la diana. En el caso de las proteasas, muchos de los importantes enlaces estabilizantes deben formarse justo alrededor del sitio de escisión, conduciendo así a secuencias de reconocimiento específicas.
Aunque a menudo se piensa en la escisión como una forma de destruir la actividad de una proteína, de hecho, la escisión específica de partes inhibidoras de una proteína puede activarla. Un ejemplo destacado de esto (la cascada de caspasas) se discute en la sección de apoptosis del capítulo del ciclo celular.
Algunas proteasas son secretadas y hacen su trabajo extracelularmente. Estas incluyen enzimas digestivas como pepsina, tripsina y quimotripsina, así como proteasas del torrente sanguíneo como la trombina y la plasmina que ayudan a controlar la coagulación. El sistema inmunitario también utiliza proteasas para destruir células y virus invasores.
En su conversión a intermedios metabólicos, los aminoácidos primero experimentan desaminación. El objetivo principal de la desaminación es excretar el exceso de nitrógeno (como urea) y luego usar o convertir (en glucosa) el esqueleto de carbono restante. Esta desaminación es un proceso de dos partes: el primer paso para la desaminación suele ser una transaminación catalizada por una aminotransferasa, en la que el grupo amino del aminoácido se transfiere a α-cetoglutarato que luego produce un nuevo α-cetoácido del aminoácido y glutamato.
El grupo amino del glutamato podría luego transferirse al oxaloacetato para formar α-ceto-glutarato y aspartato. Esa serie de transaminaciones transforma el aminoácido original, pero no elimina el nitrógeno del grupo amino. La vía alternativa es la desaminación del glutamato por glutamato deshidrogenasa, la cual genera α-cetoglutarato y amoníaco, utilizando ya sea NAD + o NADP como agente oxidante.
Los aminoácidos se descomponen en uno de los siguientes siete intermedios metabólicos: piruvato, acetil-CoA, acetoacetato, a-cetoglutarato, succinil-CoA, fumarato y oxaloacetato de la siguiente manera: 1) Ala, Cys, Gly, Ser, Thr, Trp se descomponen en piruvato; 2) Ile, Leu, Lys, Thr a acetil-CoA; 3) Leu, Lys, Thr a acetil-CoA; 3) Leu, Lys, Thr ys, Phe, Trp, Tyr a acetoacetato; 4) Arg, Glu, Gln, His, Pro a α-cetoglutarato; 5) Ile, Met, Val a succinil-CoA; 6) Asp, Phe, Tyr a fumarato; 7) Asn, Asp a oxaloacetato.