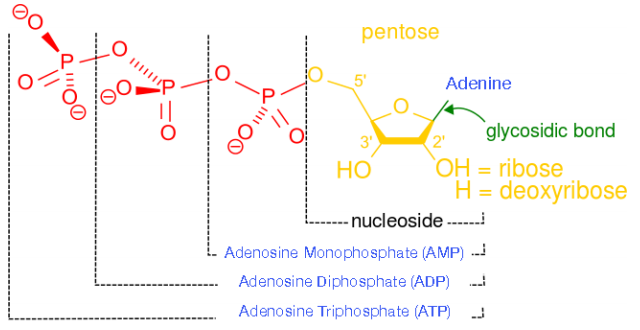
2.6: Fosforilaciones celulares
- Page ID
- 53699
La formación de trifosfatos es esencial para satisfacer las necesidades energéticas inmediatas de la célula para síntesis, movimiento y señalización. En un día dado, un ser humano promedio usa más que su peso corporal en trifosfatos. Dado que los trifosfatos son la “moneda” que satisface las necesidades inmediatas de la célula, es importante entender cómo se hacen los trifosfatos. Existen tres mecanismos de fosforilación: 1) nivel de sustrato; 2) oxidativo; y 3) fotofosforilación. Los consideramos aquí individualmente.
Fosforilación a nivel de sustrato
El tipo de fosforilación más fácil de entender es el que ocurre a nivel de sustrato. Este tipo de fosforilación implica la síntesis directa de ATP a partir de ADP y un intermedio reactivo, típicamente una molécula que contiene fosfato de alta energía. La fosforilación a nivel de sustrato es un contribuyente relativamente menor a la síntesis total de trifosfatos por las células. Un ejemplo de fosforilación del sustrato proviene de la glucólisis.
\[\ce{Phosphoenolpyruvate (PEP) + ADP <=> Pyuvate + ATP}\]
Esta reacción tiene una muy negativa\(ΔG^{o'}\) (-31.4 kJ/mol), lo que indica que el PEP contiene más energía que el ATP, favoreciendo así energéticamente la síntesis de ATP. También se pueden preparar otros trifosfatos por fosforilación a nivel de sustrato. Por ejemplo, el GTP se puede sintetizar mediante la siguiente reacción del ciclo del ácido cítrico
\[\ce{Succinyl-CoA + GDP + P_i <=> Succinate + GTP + CoA-SH}\]
Los trifosfatos pueden intercambiarse fácilmente en fosforilaciones a nivel de sustrato catalizadas por la enzima Nucleósido Difosfato Quinasa (NDPK). Una forma generalizada de las reacciones catalizadas por esta enzima es la siguiente:
\[\ce{XTP + YDP <=> XDP + YTP}\]
donde\(\ce{X}\) puede ser adenosina, citidina, uridina, timidina o guanosina y\(\ce{Y}\) puede ser cualquiera de estas también. Por último, una forma inusual de sintetizar ATP por fosforilación a nivel de sustrato es la catalizada por la adenilato quinasa
\[\ce{2 ADP <=> ATP + AMP}\]
Esta reacción es un medio importante para generar ATP cuando la célula no tiene otras fuentes de energía. La acumulación de AMP resultante de esta reacción activa enzimas, como la fosfofructoquinasa, de la glucólisis, que catalizarán reacciones para dar a la célula la energía adicional necesaria.
Transporte de electrones/fosforilación oxidativa
Las mitocohondrias se llaman las centrales eléctricas de la célula porque la mayor parte del ATP de una célula se produce allí, en un proceso denominado fosforilación oxidativa. El mecanismo por el cual se produce ATP en la fosforilación oxidativa es uno de los procesos más interesantes en toda la biología. Tiene tres consideraciones primarias. El primero es eléctrico: los electrones de portadores de energía reducida, como NADH y FADH2, ingresan a un sistema de transporte de electrones a través de complejos proteicos que contienen hierro. Como se ve en la figura de la siguiente página, los electrones se mueven de un complejo a otro, no muy diferente de la forma en que podrían moverse a través de un circuito eléctrico.
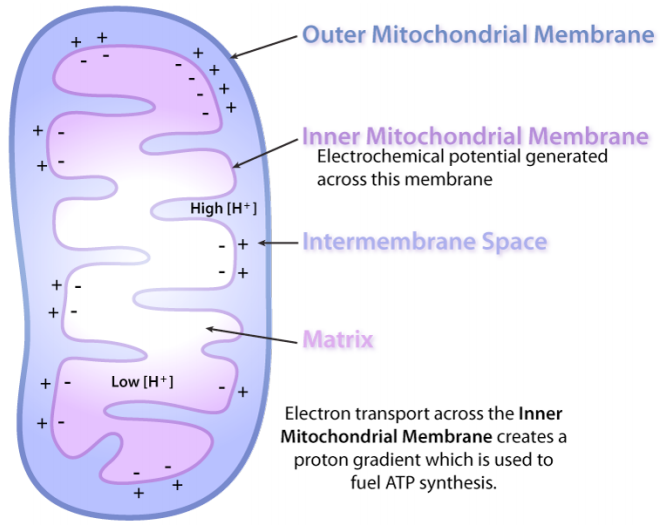
La siguiente consideración surge como un fenómeno secundario. Cuando los electrones pasan a través de los complejos I, III y IV, los protones se mueven desde la matriz mitocondrial (dentro de la mitocondria) y se depositan en el espacio intermembrana (entre las membranas interna y externa de la mitocondria). El efecto de esta redistribución es aumentar el potencial eléctrico y químico a través de la membrana. Los estudiantes pueden pensar en el proceso como “cargar la batería”.
Al igual que una batería cargada, el potencial que surge del diferencial de protones a través de la membrana se puede usar para hacer cosas. Esta es la tercera consideración. En la mitocondria, lo “cosa” que hace el gradiente de protones es crear ATP a partir de ADP y Pi (fosfato inorgánico). Este proceso requiere energía y se logra mediante el movimiento de protones a través de un complejo proteico en la membrana mitocondrial interna. El complejo proteico es una enzima que tiene varios nombres, incluyendo Complejo V, PTAS (Proton Translocating ATP Synthase) y ATP Synthase. Central para su función es el movimiento de protones a través de él (desde afuera de nuevo hacia la matriz). Los protones solo se moverán a través de ATP Sintasa si su concentración es mayor fuera de la membrana interna que en la matriz.
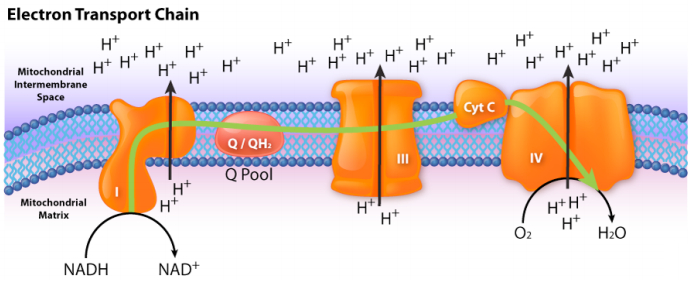
En resumen, el sistema de transporte de electrones carga la batería para la fosforilación oxidativa bombeando protones fuera de la mitocondria. La membrana interna intacta de la mitocondria mantiene los protones fuera, excepto aquellos que vuelven a entrar a través de ATP Sintasa. La ATP Sintasa permite que los protones vuelvan a entrar en la matriz mitocondrial y cosechar su energía para producir ATP.
ATP Sintasa
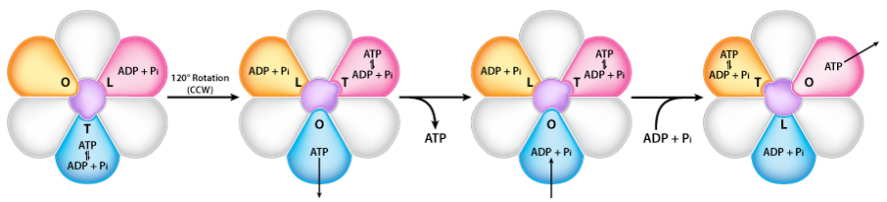
La ATP Sintasa en sí es una nanomáquina increíble que produce ATP usando un gradiente de protones que fluye a través de él desde el espacio intermembrana de regreso a la matriz. No es fácil representar en una sola imagen lo que hace la sintasa. La figura de la derecha ilustra la naturaleza de múltiples subunidades de esta proteína de membrana, que actúa como una turbina en una presa hidroeléctrica. El movimiento de protones a través de la ATP Sintasa hace que gire como una turbina, y el giro es necesario para hacer ATP.
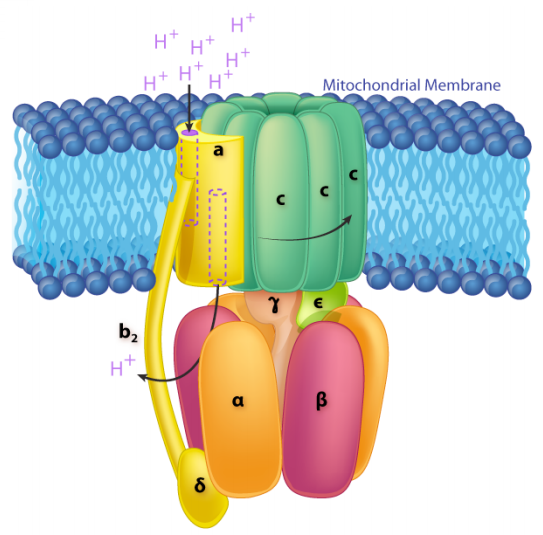
En ATP Sintasa, el componente de hilado es la porción de membrana (anillo c) del tallo F0. Las proteínas del anillo c están unidas al tallo gamma-épsilon, que se proyecta en la cabeza F1 de la estructura del hongo. La cabeza F1 contiene la capacidad catalítica para producir ATP. La cabeza F1 es de estructura hexamérica con proteínas alfa y beta emparejadas dispuestas en un trímero de dímeros. El movimiento de la proteína gamma dentro del trímero alfa-beta hace que cada conjunto de proteínas beta cambie la estructura ligeramente en tres formas diferentes llamadas Loose, Tight y Open (L, T, O). Cada una de estas formas tiene una función. La forma suelta se une\(\ce{ADP}\) y\(\ce{P_i}\). La forma apretada los “aprieta” para formar el ATP. La forma abierta libera el ATP en la matriz mitocondrial. Así, como resultado del exceso de protones en el espacio intermembrana, se produce ATP.
Fotofosforilación
El tercer tipo de fosforilación para producir ATP se encuentra únicamente en las células que realizan la fotosíntesis. Este proceso es similar a la fosforilación oxidativa de varias maneras. Una diferencia primaria es la última fuente de energía para la síntesis de ATP. En la fosforilación oxidativa, la energía proviene de electrones producidos por la oxidación de moléculas biológicas. En el caso de la fotosíntesis, la energía proviene de la luz del sol.
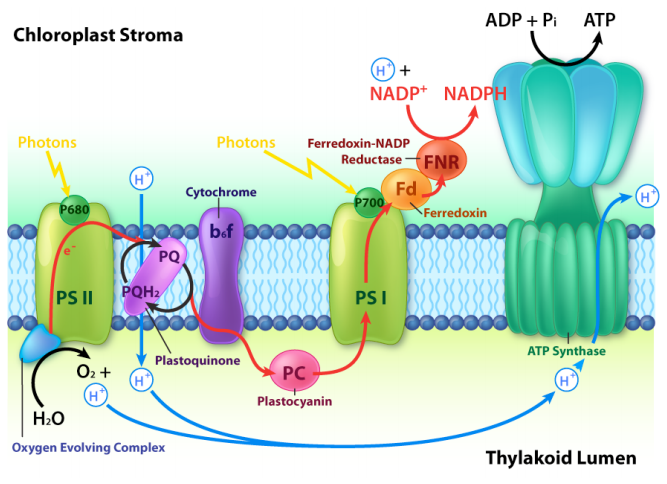
Los fotones del sol interactúan con moléculas de clorofila en centros de reacción en los cloroplastos de plantas o membranas de bacterias fotosintéticas. Un esquema del proceso se muestra arriba. Las similitudes de la fotofosforilación con la fosforilación oxidativa incluyen:
- una cadena de transporte de electrones
- creación de un gradiente de protones
- recolección de energía del gradiente de protones haciendo ATP
con la ayuda de una ATP sintasa. Algunas de las diferencias incluyen:
- la fuente de los electrones —\(\ce{H2O}\) para la fotosíntesis versus\(\ce{NADH/FADH2}\) para la fosforilación oxidativa
- dirección del bombeo de protones: hacia el espacio tilacoideo de los cloroplastos versus fuera de la matriz de la mitocondria
- movimiento de protones durante la síntesis de ATP — fuera del espacio tilacoide en la fotosíntesis versus hacia la matriz mitocondrial
- naturaleza del aceptor de electrones terminal —\(\ce{NADP^{+}}\) en la fotosíntesis versus\(\ce{O2}\) en la fosforilación oxidativa.
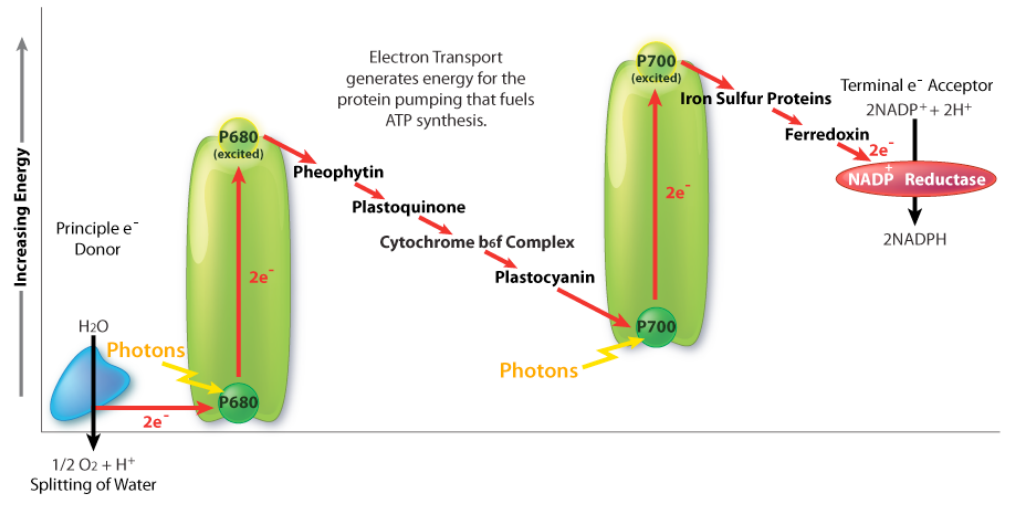
Transporte de electrones en cloroplastos vs mitocondrias
De alguna manera, el movimiento de electrones en los cloroplastos durante la fotosíntesis es opuesto al del transporte de electrones en las mitocondrias. En la fotosíntesis, el agua es la fuente de electrones y su destino final es\(\ce{NADPH}\). En las mitocondrias,\(\ce{NADH/ FADH2}\) son fuentes de electrones y\(\ce{H2O}\) es su destino final.
¿Cómo hacen los sistemas biológicos que los electrones vayan en ambos sentidos? Parecería ser el equivalente a ir y venir de un lugar en particular mientras siempre se va cuesta abajo, ya que los electrones se moverán según el potencial. La respuesta es la energía capturada de los fotones, que eleva los electrones en la fotosíntesis a una energía donde se mueven “cuesta abajo” hacia su\(\ce{NADPH}\) destino en un esquema en forma de Z. El movimiento de electrones a través de este esquema en las plantas requiere energía de fotones en dos lugares para “levantar” suficientemente la energía de los electrones. Por último, cabe señalar que la fotosíntesis en realidad tiene dos fases, referidas como el ciclo de luz (descrito anteriormente) y el ciclo oscuro, que es un conjunto de reacciones químicas que capta\(\ce{CO2}\) de la atmósfera y la “fija”, en última instancia, en glucosa. El ciclo oscuro también se conoce como el Ciclo Calvino.


