6.8: Metabolismo del colesterol
- Page ID
- 53924
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)La vía de biosíntesis del colesterol es larga y requiere cantidades significativas de energía reductora y ATP, razón por la cual se incluye aquí. El colesterol tiene papeles importantes en el cuerpo en las membranas. También como precursor de hormonas esteroides y ácidos biliares y su precursor metabólico inmediato, el 7-deshidrocolesterol, es un precursor de la vitamina D. La vía que conduce al colesterol se conoce como la vía isoprenoide y las ramas de la misma conducen a otras moléculas incluyendo otras vitaminas liposolubles.
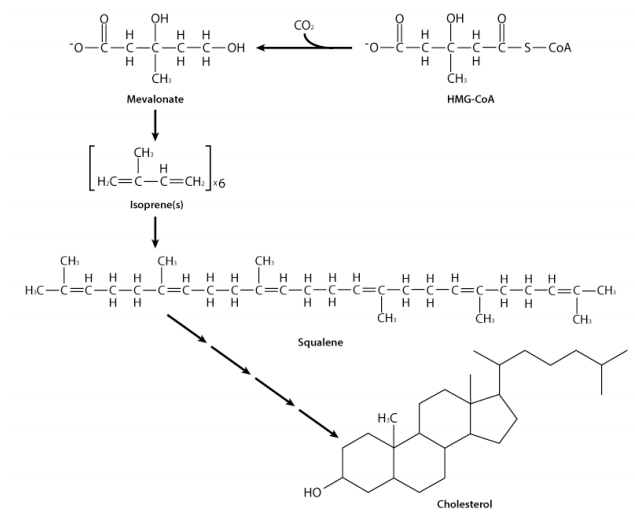
A partir de HMG-CoA, la enzima HMG-CoA reductasa cataliza la formación de mevalonato. La reacción requiere NADPH y da como resultado la liberación de la coenzima A y parece ser uno de los pasos reguladores más importantes en la vía de síntesis. La enzima está regulada tanto por la inhibición por retroalimentación (el colesterol la inhibe) como por la modificación covalente (la fosforilación la inhibe). La síntesis de la enzima también está regulada transcripcionalmente. Cuando los niveles de colesterol bajan, la transcripción del gen aumenta.
El mevalonato se fosforila dos veces y luego se descarboxila para producir el intermedio de cinco carbonos conocido como isopentenil-pirofosfato (IPP). IPP se convierte fácilmente en dimetilalilpirofosfato (DMAPP). Estos dos compuestos de cinco carbonos, también llamados isoprenos, son los bloques de construcción para la síntesis de colesterol y compuestos relacionados. Esta vía se conoce como la vía isoprenoide. Se procede en la dirección del colesterol comenzando con la unión de IPP y DMAPP para formar geranil-pirofosfato. El geranil-pirofosfato se combina con otro IPP para hacer farnesil-pirofosfato, un compuesto de 15 carbonos. Dos farnesil-pirofosfatos se unen para crear el compuesto de 30 carbonos conocido como escualeno. El escualeno, en un complicado reordenamiento que implica reducción y oxígeno molecular forma un intermedio cíclico conocido como lanosterol que se asemeja al colesterol. La conversión de lanosterol en colesterol es un proceso largo que involucra 19 etapas que ocurren en el retículo endoplásmico.
Al ramificarse a partir del colesterol, se puede formar la Vitamina D o las hormonas esteroides, que incluyen los progestágenos, andrógenos, estrógenos, mineralocorticoides y los glucocorticoides. La molécula de rama para todos estos es el metabolito del colesterol (y progestágeno) conocido como pregnenalona. Los progestágenos son precursores de todas las demás clases.
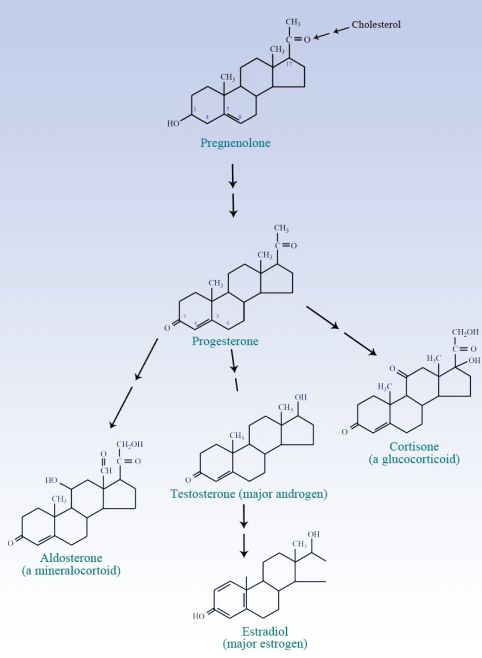
Los estrógenos se derivan de los andrógenos en una interesante reacción que requirió la formación de un anillo aromático. La enzima que cataliza esta reacción se conoce como aromatasa y es de importancia médica. El crecimiento de algunos tumores es estimulado por los estrógenos, por lo que se prescriben inhibidores de la aromatasa para prevenir la formación de estrógenos y ralentizar el crecimiento tumoral. Cabe señalar que la síntesis de otras vitaminas liposolubles y clorofila también se ramifica a partir de la vía de síntesis de isoprenoides en el geranilpirofosfato. La unión de dos geranilgeranilpirofosfatos ocurre en plantas y bacterias y conduce a la síntesis de licopeno, que a su vez es un precursor del betacaroteno, el precursor final de la vitamina A. Las vitaminas E y K, así como la clorofila también se sintetizan a partir de geranilgeranilpirofosfato.
Metabolismo del ácido biliar
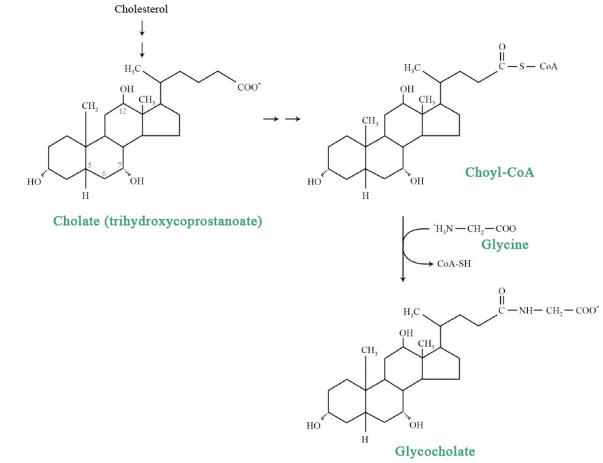
Otra vía del colesterol conduce a los ácidos biliares polares, los cuales son importantes para la solubilización de la grasa durante la digestión. Convertir el colesterol muy no polar en un ácido biliar implica la oxidación del carbono terminal en la cadena lateral de los anillos. Otras alteraciones para aumentar la polaridad de estos compuestos incluyen la hidroxilación de los anillos y el enlace a otros compuestos polares.
Los ácidos biliares comunes incluyen ácido cólico, ácido quenodesoxicólico, ácido glicólico, ácido taurocólico y ácido desoxicólico. Otro dato importante sobre los ácidos biliares es que su síntesis reduce la cantidad de colesterol disponible y promueve la captación de LDL por el hígado. Normalmente los ácidos biliares se reciclan eficientemente dando como resultado una reducción limitada de los niveles de colesterol Sin embargo, los inhibidores del reciclaje promueven la reducción de los niveles de colesterol.