8.4: Fermentación
- Page ID
- 54683
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Objetivos de aprendizaje
- Definir la fermentación y explicar por qué no requiere oxígeno
- Describir las vías de fermentación y sus productos finales y dar ejemplos de microorganismos que utilizan estas vías
- Comparar y contrastar fermentación y respiración anaeróbica
Muchas células son incapaces de llevar a cabo la respiración debido a una o más de las siguientes circunstancias:
- La célula carece de una cantidad suficiente de cualquier aceptor de electrones final inorgánico apropiado para llevar a cabo la respiración celular.
- La célula carece de genes para hacer complejos apropiados y portadores de electrones en el sistema de transporte de electrones.
- La célula carece de genes para producir una o más enzimas en el ciclo de Krebs.
Mientras que la falta de un aceptor de electrones final inorgánico apropiado es ambientalmente dependiente, las otras dos condiciones están genéticamente determinadas. Así, muchos procariotas, incluyendo miembros del género clínicamente importante Streptococcus, son permanentemente incapaces de respirar, incluso en presencia de oxígeno. Por el contrario, muchos procariotas son facultativos, lo que significa que, si las condiciones ambientales cambian para proporcionar un aceptor de electrones final inorgánico apropiado para la respiración, los organismos que contienen todos los genes requeridos para hacerlo cambiarán a la respiración celular para el metabolismo de la glucosa porque la respiración permite una producción mucho mayor de ATP por molécula de glucosa.
Si no se produce respiración, el NADH debe ser reoxidado a NAD + para su reutilización como portador de electrones para la glucólisis, el único mecanismo de la célula para producir cualquier ATP, para continuar. Algunos sistemas vivos utilizan una molécula orgánica (comúnmente piruvato) como aceptor final de electrones a través de un proceso llamado fermentación. La fermentación no implica un sistema de transporte de electrones y no produce directamente ningún ATP adicional más allá del producido durante la glucólisis por fosforilación a nivel de sustrato. Los organismos que realizan la fermentación, llamados fermentadores, producen un máximo de dos moléculas de ATP por glucosa durante la glucólisis. En la tabla\(\PageIndex{1}\) se comparan los aceptores de electrones finales y los métodos de síntesis de ATP en respiración aeróbica, respiración anaeróbica y fermentación. Nótese que el número de moléculas de ATP que se muestran para la glucólisis asume la vía Embden-Meyerhof-Parnas. Se indica el número de moléculas de ATP producidas por fosforilación a nivel de sustrato (SLP) versus fosforilación oxidativa (OP).
| Tipo de Metabolismo | Ejemplo | Aceptor Final de Electrones | Vías involucradas en la síntesis de ATP (tipo de fosforilación) | Rendimiento máximo de moléculas de ATP |
|---|---|---|---|---|
| Respiración aeróbica | Pseudomonas aeruginosa | \(\ce{O2}\) |
Glucólisis EMP (SLP) Ciclo Krebs (SLP) Transporte de electrones y quimiósmosis (OP): |
2 2 34 |
| Total | 38 | |||
| Respiración anaeróbica | Paracoccus denitrificans |
\(\ce{NO3-}\),\(\ce{SO4^{-2}}\),\(\ce{Fe^{+3}}\),\(\ce{CO2}\), otros inorgánicos |
Glucólisis EMP (SLP) Ciclo Krebs (SLP) Transporte de electrones y quimiósmosis (OP): |
2 2 1—32 |
| Total | 5 — 36 | |||
| Fermentación | Candida albicans |
Organics (generalmente piruvato) |
Glucólisis EMP (SLP) Fermentación |
2 0 |
| Total | 2 |
Los procesos de fermentación microbiana han sido manipulados por humanos y se utilizan ampliamente en la producción de diversos alimentos y otros productos comerciales, incluyendo productos farmacéuticos. La fermentación microbiana también puede ser útil para identificar microbios con fines de diagnóstico.
La fermentación por algunas bacterias, como las del yogur y otros productos alimenticios agriados, y por los animales en los músculos durante el agotamiento del oxígeno, es la fermentación del ácido láctico. La reacción química de la fermentación de ácido láctico es la siguiente:
\[\ce{Pyruvate + NADH \leftrightarrow lactic\: acid + NAD+}\]
Las bacterias de varios géneros grampositivos, incluyendo Lactobacillus, Leuconostoc y Streptococcus, se conocen colectivamente como bacterias del ácido láctico (LAB), y diversas cepas son importantes en la producción de alimentos. Durante la producción de yogur y queso, el ambiente altamente ácido generado por la fermentación con ácido láctico desnaturaliza las proteínas contenidas en la leche, haciendo que ésta se solidifique. Cuando el ácido láctico es el único producto de fermentación, se dice que el proceso es la fermentación homoláctica; tal es el caso de Lactobacillus delbrueckii y S. thermophiles utilizados en la producción de yogurt. Sin embargo, muchas bacterias realizan fermentación heteroláctica, produciendo una mezcla de ácido láctico, etanol y/o ácido acético, y CO 2 como resultado, debido a su uso de la vía de pentosa fosfato ramificada en lugar de la vía EMP para la glucólisis. Un fermentador heteroláctico importante es Leuconostoc mesenteroides, que se utiliza para agriar verduras como pepinos y repollo, produciendo encurtidos y chucrut, respectivamente.
Las bacterias del ácido láctico también son importantes médicamente. La producción de ambientes de bajo pH dentro del cuerpo inhibe el establecimiento y crecimiento de patógenos en estas áreas. Por ejemplo, la microbiota vaginal está compuesta en gran parte por bacterias del ácido láctico, pero cuando estas bacterias se reducen, la levadura puede proliferar, provocando una infección por levaduras. Adicionalmente, las bacterias del ácido láctico son importantes para mantener la salud del tracto gastrointestinal y, como tales, son el componente principal de los probióticos.
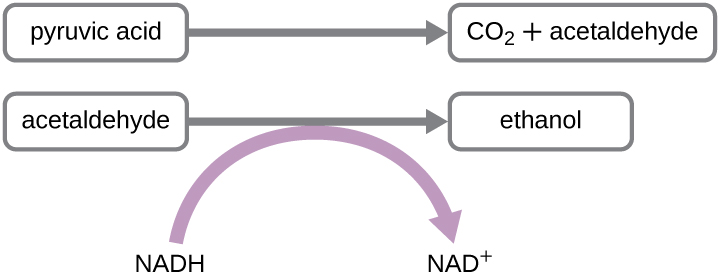
Otro proceso de fermentación familiar es la fermentación alcohólica, que produce etanol. La reacción de fermentación de etanol se muestra en la Figura\(\PageIndex{1}\). En la primera reacción, la enzima piruvato descarboxilasa elimina un grupo carboxilo del piruvato, liberando gas CO 2 mientras produce la molécula de dos carbonos acetaldehído. La segunda reacción, catalizada por la enzima alcohol deshidrogenasa, transfiere un electrón de NADH a acetaldehído, produciendo etanol y NAD +. La fermentación etanólica de piruvato por la levadura Saccharomyces cerevisiae se utiliza en la producción de bebidas alcohólicas y también hace que los productos de pan suban debido a la producción de CO 2. Fuera de la industria alimentaria, la fermentación de etanol de productos vegetales es importante en la producción de biocombustibles.
Más allá de la fermentación del ácido láctico y la fermentación alcohólica, muchos otros métodos de fermentación ocurren en procariotas, todos con el propósito de asegurar un suministro adecuado de NAD + para la glucólisis (Tabla\(\PageIndex{2}\)). Sin estas vías, la glucólisis no ocurriría y no se cosecharía ATP de la descomposición de la glucosa. Cabe señalar que la mayoría de las formas de fermentación además de la fermentación homoláctica producen gas, comúnmente CO 2 y/o gas hidrógeno. Muchos de estos diferentes tipos de vías de fermentación también se utilizan en la producción de alimentos y cada uno da como resultado la producción de diferentes ácidos orgánicos, contribuyendo al sabor único de un determinado producto alimenticio fermentado. El ácido propiónico producido durante la fermentación del ácido propiónico contribuye al sabor distintivo del queso suizo, por ejemplo.
Varios productos de fermentación son importantes comercialmente fuera de la industria alimentaria. Por ejemplo, los disolventes químicos como la acetona y el butanol se producen durante la fermentación de acetona-butanol-etanol. Los compuestos farmacéuticos orgánicos complejos utilizados en antibióticos (p. ej., penicilina), vacunas y vitaminas se producen a través de la fermentación ácida mixta. Los productos de fermentación se utilizan en el laboratorio para diferenciar diversas bacterias con fines de diagnóstico. Por ejemplo, las bacterias entéricas son conocidas por su capacidad para realizar la fermentación ácida mixta, reduciendo el pH, lo que puede detectarse mediante un indicador de pH. De igual manera, también se puede detectar la producción bacteriana de acetoína durante la fermentación de butanodiol. La producción de gas a partir de la fermentación también se puede observar en un tubo Durham invertido que atrapa el gas producido en un cultivo de caldo.
Los microbios también se pueden diferenciar según los sustratos que pueden fermentar. Por ejemplo, E. coli puede fermentar lactosa, formando gas, mientras que algunos de sus parientes gramnegativos cercanos no pueden. La capacidad de fermentar el alcohol de azúcar sorbitol se utiliza para identificar la cepa patógena enterohemorrágica O157:H7 de E. coli ya que, a diferencia de otras cepas de E. coli, es incapaz de fermentar sorbitol. Por último, la fermentación de manitol diferencia el Staphylococcus aureus fermentador de manitol de otros estafilococos no fermentadores de manitol.
| Pathway | Productos Finales | Ejemplo Microbios | Productos Comerciales |
|---|---|---|---|
| Acetona-butanol-etanol | Acetona, butanol, etanol, CO 2 | Clostridium acetobutylicum | Solventes comerciales, alternativa a gasolina |
| Alcohol | Etanol, CO 2 | Cándida, Saccharomyces | Cerveza, pan |
| Butanodiol | Ácido fórmico y láctico; etanol; acetoína; 2,3 butanediol; CO 2; gas hidrógeno | Klebsiella, Enterobacter | Chardonnay |
| Ácido butírico | Ácido butírico, CO 2, gas hidrógeno | Clostridium butyricum | Mantequilla |
| Ácido láctico | Ácido láctico | Estreptococos, Lactobacillus | chucrut, yogur, queso |
| Ácido mixto | Ácidos acético, fórmico, láctico y succínico; etanol, CO 2, gas hidrógeno | Escherichia, Shigella | Vinagre, cosmética, farmacéutica |
| Ácido propiónico | Ácido acético, ácido propiónico, CO 2 | Propionibacterium, Bifidobacterium | Queso Suizo |
Ejercicio\(\PageIndex{1}\)
¿Cuándo un microbio metabólicamente versátil realizaría la fermentación en lugar de la respiración celular?
Identificación de bacterias mediante el uso de paneles de prueba API
La identificación de un aislado microbiano es esencial para el diagnóstico adecuado y el tratamiento adecuado de los pacientes. Los científicos han desarrollado técnicas que identifican bacterias de acuerdo a sus características bioquímicas. Típicamente, o bien examinan el uso de fuentes específicas de carbono como sustratos para la fermentación u otras reacciones metabólicas, o identifican productos de fermentación o enzimas específicas presentes en las reacciones. En el pasado, los microbiólogos han utilizado tubos de ensayo individuales y placas para realizar pruebas bioquímicas. Sin embargo, los científicos, especialmente aquellos en laboratorios clínicos, ahora utilizan con mayor frecuencia paneles de plástico, desechables y multitest que contienen una serie de tubos de reacción en miniatura, cada uno típicamente incluye un sustrato específico y un indicador de pH. Después de la inoculación del panel de prueba con una pequeña muestra del microbio en cuestión y la incubación, los científicos pueden comparar los resultados con una base de datos que incluye los resultados esperados para reacciones bioquímicas específicas para microbios conocidos, permitiendo así una rápida identificación de un microbio de muestra. Estos paneles de prueba han permitido a los científicos reducir costos al tiempo que mejoran la eficiencia y reproducibilidad al realizar un mayor número de pruebas simultáneamente.
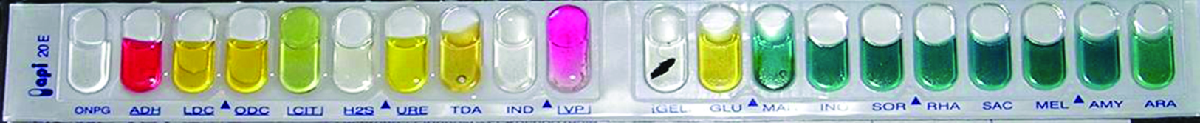
Muchos paneles de análisis bioquímicos miniaturizados comerciales cubren una serie de grupos clínicamente importantes de bacterias y levaduras. Uno de los paneles de prueba más antiguos y populares es el panel de índice de perfil analítico (API) inventado en la década de 1970. Una vez que se ha realizado alguna caracterización básica de laboratorio de una cepa determinada, como determinar la morfología Gram de la cepa, se puede utilizar una tira reactiva apropiada que contiene de 10 a 20 pruebas bioquímicas diferentes para diferenciar cepas dentro de ese grupo microbiano. Actualmente, las diversas tiras API pueden ser utilizadas para identificar rápida y fácilmente más de 600 especies de bacterias, tanto aeróbicas como anaerobias, y aproximadamente 100 tipos diferentes de levaduras. Con base en los colores de las reacciones cuando están presentes productos finales metabólicos, debido a la presencia de indicadores de pH, se crea un perfil metabólico a partir de los resultados (Figura\(\PageIndex{2}\)). Luego, los microbiólogos pueden comparar el perfil de la muestra con la base de datos para identificar el microbio específico.
Enfoque Clínico: Parte 2
Muchos de los síntomas de Hannah son consistentes con varias infecciones diferentes, incluyendo influenza y neumonía. Sin embargo, sus reflejos lentos junto con su sensibilidad a la luz y rigidez del cuello sugieren alguna posible afectación del sistema nervioso central, tal vez indicando meningitis. La meningitis es una infección del líquido cefalorraquídeo (LCR) alrededor del cerebro y la médula espinal que causa inflamación de las meninges, las capas protectoras que cubren el cerebro. La meningitis puede ser causada por virus, bacterias u hongos. Aunque todas las formas de meningitis son graves, la meningitis bacteriana es particularmente grave. La meningitis bacteriana puede ser causada por varias bacterias diferentes, pero la bacteria Neisseria meningitidis, un diplococo gramnegativo en forma de frijol, es una causa común y conduce a la muerte dentro de 1 a 2 días en 5% a 10% de los pacientes.
Dada la posible gravedad de los padecimientos de Hannah, su médico aconsejó a sus padres que la llevaran al hospital de la capital gambiana de Banjul y allí le hicieran la prueba y la trataran por posible meningitis. Después de un viaje de 3 horas hasta el hospital, Hannah fue ingresada de inmediato. Los médicos tomaron una muestra de sangre y le realizaron una punción lumbar para analizar su LCR. También inmediatamente la iniciaron en un curso del antibiótico ceftriaxona, el medicamento de elección para el tratamiento de la meningitis causada por N. meningitidis, sin esperar los resultados de las pruebas de laboratorio.
Ejercicio\(\PageIndex{2}\)
- ¿Cómo se podrían utilizar las pruebas bioquímicas para confirmar la identidad de N. meningitidis?
- ¿Por qué los médicos de Hannah decidieron administrar antibióticos sin esperar los resultados de la prueba?
Conceptos clave y resumen
- La fermentación utiliza una molécula orgánica como aceptor final de electrones para regenerar NAD + a partir de NADH para que la glicólisis pueda continuar.
- La fermentación no implica un sistema de transporte de electrones, y el proceso de fermentación no produce ATP directamente. Los fermentadores producen muy poco ATP, solo dos moléculas de ATP por molécula de glucosa durante la glucólisis.
- Los procesos de fermentación microbiana se han utilizado para la producción de alimentos y productos farmacéuticos, y para la identificación de microbios.
- Durante la fermentación del ácido láctico, el piruvato acepta electrones del NADH y se reduce a ácido láctico. Los microbios que realizan fermentación homoláctica producen solo ácido láctico como producto de fermentación; los microbios que realizan fermentación heteroláctica producen una mezcla de ácido láctico, etanol y/o ácido acético, y CO 2.
- La producción de ácido láctico por la microbiota normal impide el crecimiento de patógenos en ciertas regiones del cuerpo y es importante para la salud del tracto gastrointestinal.
- Durante la fermentación de etanol, el piruvato se descarboxila primero (liberando CO 2) a acetaldehído, que luego acepta electrones del NADH, reduciendo el acetaldehído a etanol. La fermentación de etanol se utiliza para la producción de bebidas alcohólicas, para hacer subir productos de pan y para la producción de biocombustibles.
- Los productos de fermentación de las vías (por ejemplo, la fermentación del ácido propiónico) proporcionan sabores distintivos a los productos alimenticios. La fermentación se utiliza para producir solventes químicos (fermentación acetona-butanol-etanol) y productos farmacéuticos (fermentación ácida mixta).
- Los tipos específicos de microbios pueden distinguirse por sus vías de fermentación y productos. Los microbios también pueden diferenciarse de acuerdo con los sustratos que son capaces de fermentar.


