1.10: Resolución de Problemas - Conversiones de Unidades y Estimación de Respuestas
- Page ID
- 72968
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)- Convertir un valor reportado en una unidad a un valor correspondiente en una unidad diferente.
La capacidad de convertir de una unidad a otra es una habilidad importante. Por ejemplo, una enfermera con comprimidos de aspirina de 50 mg que debe administrar 0.2 g de aspirina a un paciente necesita saber que 0.2 g equivale a 200 mg, por lo que se necesitan 4 tabletas. Afortunadamente, existe una manera sencilla de convertir de una unidad a otra.
Factores de conversión
Si aprendiste las unidades SI y prefijos descritos anteriormente, entonces sabes que 1 cm es 1/100 de metro.
\[ 1\; \rm{cm} = \dfrac{1}{100} \; \rm{m} \nonumber \]
o
\[100\; \rm{cm} = 1\; \rm{m} \nonumber \]
Supongamos que dividimos ambos lados de la ecuación por 1 m (tanto el número como la unidad):
\[\mathrm{\dfrac{100\:cm}{1\:m}=\dfrac{1\:m}{1\:m}} \nonumber \]
Siempre y cuando realicemos la misma operación en ambos lados del signo de iguales, la expresión sigue siendo una igualdad. Mira el lado derecho de la ecuación; ahora tiene la misma cantidad en el numerador (la parte superior) que en el denominador (la parte inferior). Cualquier fracción que tenga la misma cantidad en el numerador y el denominador tiene un valor de 1:

Sabemos que 100 cm es de 1 m, por lo que tenemos la misma cantidad en la parte superior e inferior de nuestra fracción, aunque se expresa en diferentes unidades. Una fracción que tiene cantidades equivalentes en el numerador y el denominador pero expresada en diferentes unidades se denomina factor de conversión.
Aquí hay un ejemplo sencillo. ¿Cuántos centímetros hay en 3.55 m? Quizás puedas determinar la respuesta en tu cabeza. Si hay 100 cm en cada metro, entonces 3.55 m equivale a 355 cm. Para resolver el problema de manera más formal con un factor de conversión, primero escribimos la cantidad que nos dan, 3.55 m. Luego multiplicamos esta cantidad por un factor de conversión, que es lo mismo que multiplicarla por 1. Podemos escribir 1 como\(\mathrm{\frac{100\:cm}{1\:m}}\) y multiplicar:
\[ 3.55 \; \rm{m} \times \dfrac{100 \; \rm{cm}}{1\; \rm{m}} \nonumber \]
El 3.55 m puede pensarse como una fracción con un 1 en el denominador. Debido a que m, la abreviatura de metros, aparece tanto en el numerador como en el denominador de nuestra expresión, cancelan:
\[\dfrac{3.55 \; \cancel{\rm{m}}}{ 1} \times \dfrac{100 \; \rm{cm}}{1 \; \cancel{\rm{m}}} \nonumber \]
El paso final es realizar el cálculo que queda una vez canceladas las unidades:
\[ \dfrac{3.55}{1} \times \dfrac{100 \; \rm{cm}}{1} = 355 \; \rm{cm} \label{Ex1} \]
En la respuesta final, omitimos el 1 en el denominador. Así, por un procedimiento más formal, encontramos que 3.55 m equivale a 355 cm. Una descripción generalizada de este proceso es la siguiente:
\[\text{quantity (in old units)} \times \text{conversion factor} = \text{quantity (in new units)} \nonumber \]
Quizás se pregunte por qué usamos un procedimiento aparentemente complicado para una conversión sencilla. En estudios posteriores, los problemas de conversión que encontrarás no siempre serán tan sencillos. Si puedes dominar la técnica de aplicar factores de conversión, podrás resolver una gran variedad de problemas.
En el ejemplo anterior (Ecuación\ ref {Ex1}), se utilizó la fracción\(\frac{100 \; \rm{cm}}{1 \; \rm{m}}\) como factor de conversión. ¿El factor de conversión\(\frac{1 \; \rm m}{100 \; \rm{cm}}\) también es igual a 1? Sí, lo hace; tiene la misma cantidad en el numerador que en el denominador (salvo que se expresan en diferentes unidades). ¿Por qué no usamos ese factor de conversión? Si hubiéramos utilizado el segundo factor de conversión, la unidad original no habría cancelado, y el resultado no tendría sentido. Esto es lo que habríamos conseguido:
\[ 3.55 \; \rm{m} \times \dfrac{1\; \rm{m}}{100 \; \rm{cm}} = 0.0355 \dfrac{\rm{m}^2}{\rm{cm}} \nonumber \]
Para que la respuesta sea significativa, tenemos que construir el factor de conversión en una forma que haga que la unidad original se cancele. La figura\(\PageIndex{1}\) muestra un mapa conceptual para construir una conversión adecuada.

Cifras significativas en conversiones
¿Cómo afectan los factores de conversión a la determinación de cifras significativas? Los números en los factores de conversión basados en cambios de prefijo, como kilogramos a gramos, no se consideran en la determinación de cifras significativas en un cálculo debido a que los números en dichos factores de conversión son exactos. Los números exactos son números definidos o contados, no números medidos, y pueden considerarse como que tienen un número infinito de cifras significativas. (Es decir, 1 kg es exactamente 1,000 g, por la definición de kilo-.) Los números contados también son exactos. Si hay 16 alumnos en un aula, el número 16 es exacto. En contraste, los factores de conversión que provienen de mediciones (como la densidad, como veremos en breve) o son aproximaciones tienen un número limitado de cifras significativas y deben tenerse en cuenta al determinar las cifras significativas de la respuesta final.
- El volumen promedio de sangre en un macho adulto es de 4.7 L. ¿Cuál es este volumen en mililitros?
- Un colibrí puede aletear sus alas una vez en 18 ms. ¿Cuántos segundos hay en 18 ms?
Solución
- Empezamos con lo que nos dan, 4.7 L. Queremos cambiar la unidad de litros a mililitros. Hay 1,000 mL en 1 L. A partir de esta relación, podemos construir dos factores de conversión:
\[ \dfrac{1\; \rm{L}}{1,000\; \rm{mL}} \; \text{ or } \; \dfrac{1,000 \; \rm{mL}}{1\; \rm{L}} \nonumber \]
Utilizamos el factor de conversión que cancelará la unidad original, litros, e introducimos la unidad a la que estamos convirtiendo, que es mililitros. El factor de conversión que hace esto es el de la derecha.

\[ 4.7 \cancel{\rm{L}} \times \dfrac{1,000 \; \rm{mL}}{1\; \cancel{\rm{L}}} = 4,700\; \rm{mL} \nonumber \]
Debido a que los números en el factor de conversión son exactos, no los consideramos a la hora de determinar el número de cifras significativas en la respuesta final. Así, reportamos dos cifras significativas en la respuesta final.
- Podemos construir dos factores de conversión a partir de las relaciones entre milisegundos y segundos:
\[ \dfrac{1,000 \; \rm{ms}}{1\; \rm{s}} \; \text{ or } \; \dfrac{1\; \rm{s}}{1,000 \; \rm{ms}} \nonumber \]
Para convertir 18 ms a segundos, elegimos el factor de conversión que cancelará milisegundos e introducirá segundos. El factor de conversión de la derecha es el adecuado. Establecimos la conversión de la siguiente manera:

\[ 18 \; \cancel{\rm{ms}} \times \dfrac{1\; \rm{s}}{1,000 \; \cancel{\rm{ms}}} = 0.018\; \rm{s} \nonumber \]
Los valores numéricos del factor de conversión no afectan nuestra determinación del número de cifras significativas en la respuesta final.
Realiza cada conversión.
- 101,000 ns a segundos
- 32.08 kg a gramos
- Contestar a
-
\[ 101,000 \cancel{\rm{ns}} \times \dfrac{1\; \rm{s}}{1,000,000,000\; \cancel{\rm{ns}}} = 0.000101\; \rm{s} \nonumber \]
- Respuesta b
-
\[ 32.08 \cancel{\rm{kg}} \times \dfrac{1,000 \; \rm{g}}{1\; \cancel{\rm{kg}}} = 32,080\; \rm{g} \nonumber \]
Factores de conversión a partir de diferentes unidades
Los factores de conversión también se pueden construir para convertir entre diferentes tipos de unidades. Por ejemplo, la densidad se puede utilizar para convertir entre la masa y el volumen de una sustancia. Considera el mercurio, que es un líquido a temperatura ambiente y tiene una densidad de 13.6 g/mL. La densidad nos dice que 13.6 g de mercurio tienen un volumen de 1 mL. Podemos escribir esa relación de la siguiente manera:
13.6 g de mercurio = 1 mL de mercurio
Esta relación se puede utilizar para construir dos factores de conversión:
\[\mathrm{\dfrac{13.6\:g}{1\:mL}\:and\:\dfrac{1\:mL}{13.6\:g}} \nonumber \]
¿Cuál usamos? Depende, como es habitual, de las unidades que necesitamos cancelar e introducir. Por ejemplo, supongamos que queremos conocer la masa de 16 mL de mercurio. Usaríamos el factor de conversión que tiene mililitros en la parte inferior (para que la unidad de mililitros cancele) y gramos en la parte superior para que nuestra respuesta final tenga una unidad de masa:
\[ \begin{align*} \mathrm{16\:\cancel{mL}\times\dfrac{13.6\:g}{1\:\cancel{mL}}} &= \mathrm{217.6\:g} \\[4pt] &\approx \mathrm{220\:g} \end{align*} \nonumber \]
En el último paso, limitamos nuestra respuesta final a dos cifras significativas porque la cantidad de volumen tiene sólo dos cifras significativas; el 1 en la unidad de volumen se considera un número exacto, por lo que no afecta el número de cifras significativas. El otro factor de conversión sería útil si se nos diera una masa y se nos pidiera encontrar volumen, como lo ilustra el siguiente ejemplo.
La densidad se puede utilizar como factor de conversión entre masa y volumen.
Un termómetro de mercurio para medir la temperatura de un paciente contiene 0.750 g de mercurio. ¿Cuál es el volumen de esta masa de mercurio?
Solución
Debido a que estamos comenzando con gramos, queremos usar el factor de conversión que tiene gramos en el denominador. La unidad gramo cancelará algebraicamente, y se introducirán mililitros en el numerador.
\[ \begin{align*} 0.750 \; \cancel{\rm{g}} \times \dfrac{1\; \rm{mL}}{13.6 \; \cancel{\rm{g}}} &= 0.055147 \ldots \; \rm{mL} \\[4pt] &\approx 0.0551\; \rm{mL} \end{align*} \nonumber \]
Hemos limitado la respuesta final a tres cifras significativas.
¿Cuál es el volumen de 100.0 g de aire si su densidad es 1.3 g/L?
- Contestar
-
\[100.0 \cancel{\rm{g}} \times \dfrac{1\; \rm{L}}{1.3\; \cancel{\rm{g}}} = 76.92307692\; \rm{L} ≈ 77 L \nonumber \]
Debido a que la densidad (1.3 g/L) tiene solo 2 cifras significativas, estamos redondeando la respuesta final a 2 cifras significativas.
Resolución de problemas con múltiples conversiones
En ocasiones tendrás que realizar más de una conversión para obtener la unidad deseada. Por ejemplo, supongamos que desea convertir 54.7 km en milímetros. Puedes memorizar la relación entre kilómetros y milímetros, o puedes hacer la conversión en dos pasos. La mayoría de la gente prefiere convertir en pasos.
Para hacer una conversión paso a paso, primero convertimos la cantidad dada a la unidad base. En este ejemplo, la unidad base son metros. Sabemos que hay 1,000 m en 1 km:
\[ 54.7\; \cancel{\rm{km}} \times \dfrac{1,000 \; \rm{m}}{1\; \cancel{\rm{km}}} = 54,700\; \rm{m} \nonumber \]
Después tomamos el resultado (54.700 m) y lo convertimos a milímetros, recordando que hay\(1,000\; \rm{mm}\) para cada\(1\; \rm{m}\):
\[ \begin{align*} 54,700 \; \cancel{\rm{m}} \times \dfrac{1,000 \; \rm{mm}}{1\; \cancel{\rm{m}}} &= 54,700,000 \; \rm{mm} \\[4pt] &= 5.47 \times 10^7\; \rm{mm} \end{align*} \nonumber \]
Hemos expresado la respuesta final en notación científica.
Como atajo, ambos pasos de la conversión se pueden combinar en una sola expresión de varios pasos:
Mapa Conceptal

Cálculo
\[ \begin{align*} 54.7\; \cancel{\rm{km}} \times \dfrac{1,000 \; \cancel{\rm{m}}}{1\; \cancel{\rm{km}}} \times \dfrac{1,000 \; \rm{mm}}{1\; \cancel{\rm{m}}} &= 54,700,000 \; \rm{mm} \\[4pt] &= 5.47 \times 10^7\; \rm{mm} \end{align*} \nonumber \]
En cada paso, se cancela la unidad anterior y se produce la siguiente unidad en la secuencia, cancelando cada unidad sucesiva hasta que solo quede la unidad necesaria en la respuesta.
Cualquiera de los métodos, un paso a la vez o todos los pasos juntos, es aceptable. Si haces todos los pasos juntos, la restricción para el número adecuado de cifras significativas debe hacerse después del último paso. Siempre y cuando las matemáticas se realicen correctamente, deberías obtener la misma respuesta sin importar qué método uses.
Convierta 58.2 ms en megaseconds en un cálculo de varios pasos.
Solución
Primero, convierta la unidad dada (ms) a la unidad base, en este caso, segundos y luego convierta segundos en la unidad final, megaseconds:
Mapa Conceptal
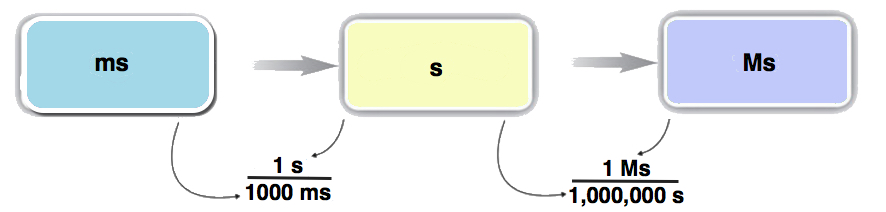
Cálculo
\[ \begin{align*} 58.2 \; \cancel{\rm{ms}} \times \dfrac{\cancel{1 \rm{s}}}{1,000\; \cancel{\rm{ms}}} \times \dfrac{1\; \rm{Ms}}{1,000,000\; \cancel{ \rm{s}}} &=0.0000000582\; \rm{Ms} \\[4pt] &= 5.82 \times 10^{-8}\; \rm{Ms} \end{align*} \nonumber \]
Ninguno de los factores de conversión afecta el número de cifras significativas en la respuesta final.
Convierta 43.007 mg a kilogramos en un cálculo de varios pasos.
- Contestar
-
\[ \begin{align*} 43.007 \; \cancel{\rm{mg}} \times \dfrac{\cancel{1 \rm{g}}}{1,000\; \cancel{\rm{mg}}} \times \dfrac{1\; \rm{kg}}{1,000\; \cancel{ \rm{g}}} &=0.000043007\; \rm{kg} \\[4pt] &= 4.3007 \times 10^{-5}\; \rm{kg} \end{align*} \nonumber \].
Ninguno de los factores de conversión afecta el número de cifras significativas en la respuesta final.
Un farmacéutico dispensa medicamentos que han sido recetados por un médico. Aunque eso puede sonar sencillo, los farmacéuticos en Estados Unidos deben tener un doctorado en farmacia y estar licenciados por el estado en el que trabajan. La mayoría de los programas de farmacia requieren cuatro años de educación en una escuela de farmacia especializada.
Los farmacéuticos deben conocer mucha química y biología para que puedan entender los efectos que los medicamentos (que son químicos, después de todo) tienen en el cuerpo. Los farmacéuticos pueden asesorar a los médicos sobre la selección, dosis, interacciones y efectos secundarios de los medicamentos. También pueden asesorar a los pacientes sobre el uso adecuado de sus medicamentos, incluyendo cuándo y cómo tomar medicamentos específicos adecuadamente. Los farmacéuticos se pueden encontrar en farmacias, hospitales y otras instalaciones médicas.
Curiosamente, un nombre anticuado para farmacéutico es químico, que se usaba cuando antes los farmacéuticos hacían mucha preparación de medicamentos, o compuestos. En los tiempos modernos, los farmacéuticos rara vez componen sus propios medicamentos, pero su conocimiento de las ciencias, incluida la química, les ayuda a brindar valiosos servicios en apoyo de la salud de todos.
Llave para llevar
- Una unidad se puede convertir a otra unidad del mismo tipo con un factor de conversión.
Ejercicios de Revisión de Conceptos
- ¿Cómo se determina qué cantidad en un factor de conversión va en el denominador de la fracción?
- Indicar los lineamientos para determinar cifras significativas al utilizar un factor de conversión.
- Escribe un mapa conceptual (un plan) de cómo convertirías\(1.0 \times 10^{12}\) nano litros (nL) a kilo litros (kL).
RESPUESTAS
- La unidad que desea cancelar del numerador va en el denominador del factor de conversión.
- Los números exactos que aparecen en muchos factores de conversión no afectan el número de cifras significativas; de lo contrario, se aplican las reglas normales de multiplicación y división para cifras significativas.
- Mapa conceptual: Convertir los dados (nanolitros, nL) a litros; luego convertir litros a kilolitros.


