16.2: La masa, la energía y la teoría de la relatividad
- Page ID
- 127422
Objetivos de aprendizaje
Al final de esta sección, podrás:
- Explicar cómo la materia puede convertirse en energía
- Describir las partículas que componen los átomos
- Describir el núcleo de un átomo
- Entender las fuerzas nucleares que mantienen unidos a los átomos
- Rastrear las reacciones nucleares en el interior solar
Como hemos visto, la energía no puede ser creada ni destruida, sino que sólo se convierte de una forma a otra. Una de las notables conclusiones derivadas por Albert Einstein (ver el cuadro de Albert Einstein a continuación) cuando desarrolló su teoría de la relatividad es que la materia también puede considerarse una forma de energía y puede convertirse en energía. Además, la energía también se puede convertir en materia. Esto parecía contradecir lo que los humanos habían aprendido a lo largo de miles de años al estudiar la naturaleza. La materia es algo que podemos ver y tocar, mientras que la energía es algo que los objetos tienen cuando hacen cosas como moverse o calentarse. La idea de que la materia o la energía se pueden convertir entre sí parecía tan indignante como decir que podrías acelerar un auto girando el parachoques a más velocidad, o que podrías crear un asiento delantero más grande al ralentizar tu auto. Eso sería bastante difícil de creer; sin embargo, el universo en realidad funciona algo así.
Convertir la materia en energía
La notable equivalencia entre materia y energía se da en una de las ecuaciones más famosas:
\[E=mc^2\label{Eq1}\]
En esta ecuación, E significa energía,\(m\) significa masa, y\(c\), la constante que relaciona las dos, es la velocidad de la luz (\(3 × 10^8\)metros por segundo). Obsérvese que la masa es una medida de la cantidad de materia, por lo que la significación de esta ecuación es que la materia se puede convertir en energía y la energía se puede convertir en materia. Comparemos esta ecuación de convertir materia y energía con algunas ecuaciones de conversión comunes que tienen la misma forma:
\[\text{inches }= \text{ feet} \times 12 \nonumber\]
o
\[\text{cents }= \text{ dollars} \times 100 \nonumber\]
Así como cada fórmula de conversión permite calcular la conversión de una cosa en otra, cuando convertimos la materia en energía, consideramos cuánta masa tiene la materia. El factor de conversión en este caso resulta no ser ni 12 ni 100, como en nuestros ejemplos, sino otra cantidad constante: la velocidad de la luz al cuadrado. Tenga en cuenta que la materia no tiene que viajar a la velocidad de la luz (o la velocidad de la luz al cuadrado) para que se produzca esta conversión. El factor de\(c^2\) es solo el número que mostró Einstein debe ser utilizado para relacionar masa y energía.
Observe que esta fórmula no nos dice cómo convertir la masa en energía, así como la fórmula para centavos no nos dice dónde cambiar monedas por un billete de dólar. Las fórmulas simplemente nos dicen cuáles son los valores equivalentes si logramos hacer la conversión. Cuando Einstein derivó por primera vez su fórmula en 1905, nadie tenía la menor idea de cómo convertir la masa en energía de ninguna manera práctica. El propio Einstein intentó desalentar la especulación de que la conversión a gran escala de la masa atómica en energía sería factible en un futuro próximo. Hoy, como resultado de los desarrollos en física nuclear, regularmente convertimos la masa en energía en centrales eléctricas, armas nucleares y experimentos de física de alta energía en aceleradores de partículas.
Debido a que la velocidad de la luz al cuadrado (\(c^2\)) es una cantidad muy grande, la conversión de incluso una pequeña cantidad de masa da como resultado una cantidad muy grande de energía. Por ejemplo, la conversión completa de 1 gramo de materia (aproximadamente 1/28 onza, o aproximadamente 1 clip) produciría tanta energía como la quema de 15,000 barriles de petróleo.
Los científicos pronto se dieron cuenta de que la conversión de la masa en energía es la fuente del calor y la luz del Sol. Con la\(E = mc^2\) ecuación de Einstein, podemos calcular que la cantidad de energía irradiada por el Sol podría ser producida por la conversión completa de alrededor de 4 millones de toneladas de materia en energía dentro del Sol cada segundo. Destruir 4 millones de toneladas por segundo suena mucho en comparación con las cosas terrenales, pero ten en cuenta que el Sol es un reservorio muy grande de materia. De hecho, veremos que el Sol contiene masa más que suficiente para destruir cantidades tan enormes de materia y seguir brillando a su ritmo actual durante miles de millones de años.
Pero saber todo eso todavía no nos dice cómo se puede convertir la masa en energía. Para entender el proceso que realmente ocurre en el Sol, necesitamos explorar un poco más la estructura del átomo.
ALBERT EINSTEIN
Durante gran parte de su vida, Albert Einstein (Figura\(\PageIndex{1}\)) fue uno de los famosos más reconocidos de su época. Extraños lo detuvieron en la calle, y la gente de todo el mundo le pidió avales, consejos y asistencia. De hecho, cuando Einstein y la gran estrella de cine Charlie Chaplin se conocieron en California, descubrieron que compartían sentimientos similares sobre la pérdida de privacidad que vino con la fama. El nombre de Einstein era una palabra familiar a pesar de que la mayoría de la gente no entendía las ideas que le habían hecho famoso.
Einstein nació en 1879 en Ulm, Alemania. Cuenta la leyenda que no le fue bien en la escuela (incluso en aritmética), y desde entonces miles de estudiantes han intentado justificar una mala calificación al referirse a esta historia. Por ay, como muchas leyendas, esta no es verdad. Los registros indican que aunque tendió a rebelarse contra el estilo de enseñanza autoritario en boga en Alemania en ese momento, Einstein era un buen estudiante.
Después de graduarse del Instituto Politécnico Federal en Zurich, Suiza, Einstein al principio tuvo problemas para conseguir un trabajo (incluso como profesor de secundaria), pero finalmente se convirtió en examinador en la Oficina Suiza de Patentes. Trabajando en su tiempo libre, sin el beneficio de un ambiente universitario pero utilizando su magnífica intuición física, escribió cuatro artículos en 1905 que finalmente transformarían la forma en que los físicos miraban el mundo.
Uno de ellos, que le valió a Einstein el Premio Nobel en 1921, estableció parte de los cimientos de la mecánica cuántica: la rica, desconcertante y notable teoría del reino subatómico. Pero su trabajo más importante presentó la teoría especial de la relatividad, un reexamen del espacio, el tiempo y el movimiento que agregó un nuevo nivel de sofisticación a nuestra comprensión de esos conceptos. La famosa ecuación E = mc 2 fue en realidad una parte relativamente menor de esta teoría, agregada en un artículo posterior.
En 1916, Einstein publicó su teoría general de la relatividad, que fue, entre otras cosas, una descripción fundamentalmente nueva de la gravedad (ver Agujeros Negros y Espacio-tiempo curvo). Cuando esta teoría fue confirmada por mediciones de la “flexión de la luz estelar” durante un eclipse de 1919 (el titular del New York Times decía, “Lights All Askew in the Heavens”), Einstein se hizo mundialmente famoso.
En 1933, para escapar de la persecución nazi, Einstein dejó su cátedra en Berlín y se estableció en Estados Unidos en el recién creado Instituto de Estudios Avanzados de Princeton. Permaneció allí hasta su muerte en 1955, escribiendo, dando conferencias y defendiendo una variedad de causas intelectuales y políticas. Por ejemplo, accedió a firmar una carta escrita por Leo Szilard y otros científicos en 1939, alertando al presidente Roosevelt sobre los peligros de permitir que la Alemania nazi desarrolle primero la bomba atómica. Y en 1952, a Einstein se le ofreció la segunda presidencia de Israel. Al declinar la posición, dijo: “Sé un poco de la naturaleza y casi nada de los hombres.

Partículas Elementales
Los componentes fundamentales de los átomos son el protón, el neutrón y el electrón (ver La estructura del átomo).
Los protones, neutrones y electrones no son de ninguna manera todas las partículas que existen. Primero, para cada tipo de partícula, existe una antipartícula correspondiente pero opuesta. Si la partícula lleva una carga, su antipartícula tiene la carga opuesta. El antielectrón es el positrón, que tiene la misma masa que el electrón pero está cargado positivamente. De igual manera, el antiprotón tiene una carga negativa. Lo notable de tal antimateria es que cuando una partícula entra en contacto con su antipartícula, las partículas originales son aniquiladas, y se producen cantidades sustanciales de energía en forma de fotones.
Dado que nuestro mundo está hecho exclusivamente de partículas ordinarias de materia, la antimateria no puede sobrevivir por mucho tiempo. Pero las antipartículas individuales se encuentran en los rayos cósmicos (partículas que llegan a la cima de la atmósfera terrestre desde el espacio) y pueden crearse en aceleradores de partículas. Y, como veremos en un momento, la antimateria se crea en el núcleo del Sol y otras estrellas.
Los fanáticos de la ciencia ficción pueden estar familiarizados con la antimateria de las series de televisión y películas de Star Trek. El Starship Enterprise es impulsado por la cuidadosa combinación de materia y antimateria en la sala de máquinas del barco. Según\(E=mc^2\), la aniquilación de materia y antimateria puede producir una enorme cantidad de energía, pero evitar que el combustible de antimateria toque el barco antes de que sea necesario debe ser un gran problema. ¡No es de extrañar que Scotty, el ingeniero jefe del programa de televisión original, siempre se viera preocupado!
En 1933, el físico Wolfgang Pauli (Figura) sugirió que podría haber otro tipo de partícula elemental. La energía parecía desaparecer cuando se producían ciertos tipos de reacciones nucleares, violando la ley de conservación de la energía. Pauli se mostró reacio a aceptar la idea de que una de las leyes básicas de la física estaba equivocada, y sugirió un “remedio desesperado”. Quizás una partícula tan lejana no detectada, a la que se le dio el nombre de neutrino (“pequeño neutro”), se llevó la energía “faltante”. Sugirió que los neutrinos eran partículas con masa cero, y que al igual que los fotones, se movían con la velocidad de la luz.

El elusivo neutrino no se detectó hasta 1956. La razón por la que fue tan difícil de encontrar es que los neutrinos interactúan muy débilmente con otra materia y por lo tanto son muy difíciles de detectar. La tierra es más transparente a un neutrino que el panel de vidrio más delgado y limpio para un fotón de luz. De hecho, la mayoría de los neutrinos pueden pasar completamente a través de una estrella o planeta sin ser absorbidos. Como veremos, este comportamiento de los neutrinos los convierte en una herramienta muy importante para estudiar el Sol. Desde la predicción de Pauli, los científicos han aprendido mucho más sobre el neutrino. Ahora sabemos que hay tres tipos diferentes de neutrinos, y en 1998, se descubrió que los neutrinos tenían una cantidad minúscula de masa. En efecto, es tan pequeño que los electrones son al menos 500.000 veces más masivos. La investigación en curso se centra en determinar la masa de neutrinos con mayor precisión, y aún puede resultar que uno de los tres tipos es sin masa. Volveremos al tema de los neutrinos más adelante en este capítulo.
Algunas de las propiedades del protón, electrón, neutrón y neutrino se resumen en la Tabla\(\PageIndex{1}\). (Otras partículas subatómicas han sido producidas por experimentos con aceleradores de partículas, pero no juegan un papel en la generación de energía solar).
| Partícula | Masa (kg) | Cargar |
|---|---|---|
| Protón | 1.67265 × 10 −27 | +1 |
| Neutrón | 1.67495 × 10 −27 | 0 |
| Electron | 9.11 × 10 −31 | −1 |
| Neutrino | <2 × 10 −36 (incierto) | 0 |
El Núcleo Atómico
El núcleo de un átomo no es sólo una colección suelta de partículas elementales. Dentro del núcleo, las partículas se mantienen unidas por una fuerza muy poderosa llamada la fuerza nuclear fuerte. Se trata de una fuerza de corto alcance, solo capaz de actuar sobre distancias aproximadamente del tamaño del núcleo atómico. Un experimento de pensamiento rápido muestra lo importante que es esta fuerza. Echa un vistazo a tu dedo y considera los átomos que lo componen. Entre ellos se encuentra el carbono, uno de los elementos básicos de la vida. Enfoca tu imaginación en el núcleo de uno de tus átomos de carbono. Contiene seis protones, que tienen una carga positiva, y seis neutrones, que son neutros. Así, el núcleo tiene una carga neta de seis positivos. Si tan sólo estuviera actuando la fuerza eléctrica, los protones en este y cada átomo de carbono se encontrarían muy repulsivos y se alejarían volando.
La fuerza nuclear fuerte es una fuerza atractiva, más fuerte que la fuerza eléctrica, y mantiene las partículas del núcleo fuertemente unidas entre sí. Vimos antes que si bajo la fuerza de la gravedad una estrella “se encoge” —acercando sus átomos— se libera energía gravitacional. De la misma manera, si las partículas se unen bajo la fuerte fuerza nuclear y se unen para formar un núcleo atómico, parte de la energía nuclear se libera. La energía entregada en tal proceso se llama la energía de unión del núcleo.
Cuando se libera dicha energía de unión, el núcleo resultante tiene una masa ligeramente menor que la suma de las masas de las partículas que se juntaron para formarlo. En otras palabras, la energía proviene de la pérdida de masa. Este ligero déficit de masa es sólo una pequeña fracción de la masa de un protón. Pero debido a que cada bit de masa perdida puede proporcionar mucha energía (recuerde, E = mc 2), esta liberación de energía nuclear puede ser bastante sustancial.
Las mediciones muestran que la energía de unión es mayor para los átomos con una masa cercana a la del núcleo de hierro (con un número combinado de protones y neutrones igual a 56) y menor tanto para los núcleos más ligeros como para los más pesados. El hierro, por lo tanto, es el elemento más estable: dado que cede la mayor cantidad de energía cuando se forma, requeriría la mayor cantidad de energía para descomponerlo de nuevo en sus partículas componentes.
Lo que esto significa es que, en general, cuando los núcleos atómicos ligeros se unen para formar uno más pesado (hasta el hierro), se pierde masa y se libera energía. Esta unión de núcleos atómicos se llama fusión nuclear.
La energía también se puede producir dividiendo los núcleos atómicos pesados en otros más ligeros (hasta el hierro); este proceso se llama fisión nuclear. La fisión nuclear fue el proceso que aprendimos a usar primero, en bombas atómicas y en reactores nucleares utilizados para generar energía eléctrica y, por lo tanto, puede ser más familiar para usted. La fisión también ocurre a veces de manera espontánea en algunos núcleos inestables a través del proceso de radiactividad natural. Pero la fisión requiere núcleos grandes y complejos, mientras que sabemos que las estrellas están compuestas predominantemente por núcleos pequeños y simples. Entonces debemos buscar primero la fusión para explicar la energía del Sol y las estrellas (Figura\(\PageIndex{3}\)).
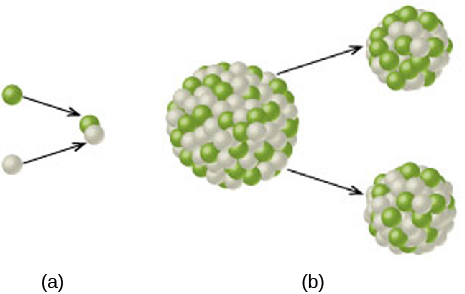
Atracción nuclear versus repulsión eléctrica
Hasta el momento, parece que tenemos una receta muy atractiva para producir la energía emitida por el Sol: “enrollar” algunos núcleos y unirlos a través de la fusión nuclear. Esto hará que pierdan parte de su masa, que luego se convierte en energía. Sin embargo, cada núcleo, incluso hidrógeno simple, tiene protones, y todos los protones tienen cargas positivas. Ya que las cargas similares se repelen a través de la fuerza eléctrica, cuanto más cerca nos acercamos dos núcleos entre sí, más se repelen. Es cierto que si podemos conseguirlos a una “distancia de ataque” de la fuerza nuclear, entonces se unirán con una atracción mucho más fuerte. Pero esa distancia impactante es muy pequeña, aproximadamente del tamaño de un núcleo. ¿Cómo podemos acercar los núcleos lo suficiente como para participar en la fusión?
La respuesta resulta ser el calor, un calor tremendo, que acelera los protones lo suficiente como para superar las fuerzas eléctricas que intentan mantener separados a los protones. Dentro del Sol, como vimos, el elemento más común es el hidrógeno, cuyo núcleo contiene sólo un solo protón. Dos protones solo pueden fusionarse en regiones donde la temperatura es mayor a unos 12 millones de K, y la velocidad de los protones promedio alrededor de 1000 kilómetros por segundo o más. (¡En unidades anticuadas, eso es más de 2 millones de millas por hora!)
En nuestro Sol, tales temperaturas extremas se alcanzan sólo en las regiones cercanas a su centro, que tiene una temperatura de 15 millones de K. Los cálculos muestran que casi toda la energía del Sol se genera dentro de unos 150.000 kilómetros de su núcleo, o dentro de menos del 10% de su volumen total.
Incluso a estas altas temperaturas, es sumamente difícil obligar a dos protones a combinarse. En promedio, un protón rebotará de otros protones en el núcleo abarrotado del Sol durante unos 14 mil millones de años, a razón de 100 millones de colisiones por segundo, antes de que se fusione con un segundo protón. Esto es, sin embargo, sólo el tiempo promedio de espera. Algunos de los enormes números de protones en la región interior del Sol son “afortunados” y solo toman algunas colisiones para lograr una reacción de fusión: son los protones responsables de producir la energía que irradia el Sol. Dado que el Sol tiene alrededor de 4.5 mil millones de años, la mayoría de sus protones aún no han estado involucrados en reacciones de fusión.
Reacciones nucleares en el interior del sol
El Sol, entonces, aprovecha la energía contenida en los núcleos de los átomos a través de la fusión nuclear. Veamos lo que sucede con más detalle. En lo profundo del Sol, un proceso de tres pasos toma cuatro núcleos de hidrógeno y los fusiona para formar un solo núcleo de helio. El núcleo de helio es ligeramente menos masivo que los cuatro núcleos de hidrógeno que se combinan para formarlo, y esa masa se convierte en energía.
El paso inicial requerido para formar un núcleo de helio a partir de cuatro núcleos de hidrógeno se muestra en la Figura\(\PageIndex{4}\). A las altas temperaturas dentro del núcleo del Sol, dos protones se combinan para formar un núcleo de deuterio, que es un isótopo (o versión) de hidrógeno que contiene un protón y un neutrón. En efecto, uno de los protones originales se ha convertido en neutrón en la reacción de fusión. La carga eléctrica tiene que conservarse en las reacciones nucleares, y se conserva en ésta. Un positrón (electrón de antimateria) emerge de la reacción y se lleva la carga positiva originalmente asociada con uno de los protones.
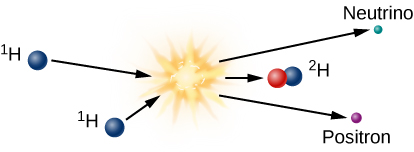
Al ser antimateria, este positrón colisionará instantáneamente con un electrón cercano, y ambos serán aniquilados, produciendo energía electromagnética en forma de fotones de rayos gamma. Este rayo gamma, que ha sido creado en el centro del Sol, se encuentra en un mundo abarrotado de núcleos y electrones que se mueven rápidamente. El rayo gamma choca con partículas de materia y transfiere su energía a una de ellas. La partícula luego emite otro fotón de rayos gamma, pero a menudo el fotón emitido tiene un poco menos de energía que el que fue absorbido.
Tales interacciones suceden a los rayos gamma una y otra y otra vez a medida que avanzan lentamente hacia las capas externas del Sol, hasta que su energía se reduce tanto que ya no son rayos gamma sino rayos X (recuerden lo que aprendiste en El Espectro Electromagnético). Posteriormente, a medida que los fotones pierden aún más energía a través de colisiones en el abarrotado centro del Sol, se convierten en fotones ultravioleta.
Para cuando llegan a la superficie del Sol, la mayoría de los fotones han renunciado a la energía suficiente para ser luz ordinaria, y son la luz solar que vemos proveniente de nuestra estrella. (Para ser precisos, cada fotón de rayos gamma se convierte finalmente en muchos fotones separados de luz solar de baja energía). Entonces, la luz solar emitida por el Sol hoy tuvo su origen como un rayo gamma producido por reacciones nucleares profundas en el núcleo del Sol. El tiempo que requieren los fotones para llegar a la superficie depende de qué tan lejos viaje un fotón en promedio entre colisiones, y el tiempo de viaje depende de qué modelo del complicado interior solar aceptemos. Las estimaciones son algo inciertas pero indican que la emisión de energía desde la superficie del Sol puede demorar su producción en el interior en 100.000 años hasta tanto como 1,000,000 años.
Además del positrón, la fusión de dos átomos de hidrógeno para formar deuterio da como resultado la emisión de un neutrino. Debido a que los neutrinos interactúan tan poco con la materia ordinaria, los producidos por las reacciones de fusión cercanas al centro del Sol viajan directamente a la superficie del Sol y luego al espacio, en todas las direcciones. Los neutrinos se mueven casi a la velocidad de la luz, y escapan del Sol unos dos segundos después de ser creados.
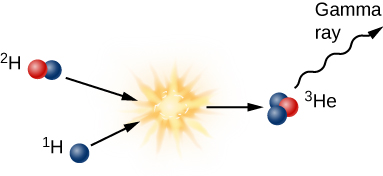
El segundo paso para formar helio a partir de hidrógeno es agregar otro protón al núcleo de deuterio para crear un núcleo de helio que contenga dos protones y un neutrón (Figura\(\PageIndex{5}\)). En el proceso, nuevamente se pierde algo de masa y se emite más radiación gamma. Tal núcleo es helio porque un elemento se define por su número de protones; cualquier núcleo con dos protones se llama helio. Pero esta forma de helio, que llamamos helio-3 (y escribimos en taquigrafía como\(^3 \text{He}\)) no es el isótopo que vemos en la atmósfera del Sol o en la Tierra. Ese helio tiene dos neutrones y dos protones y de ahí se llama helio-4 (\(^4 \text{He}\)).
Para llegar al helio-4 en el Sol, el helio-3 debe combinarse con otro helio-3 en el tercer paso de fusión (ilustrado en la Figura\(\PageIndex{6}\)). Obsérvese que de este paso quedan dos protones energéticos; cada uno de ellos sale de la reacción listo para chocar con otros protones y para iniciar de nuevo el paso 1 en la cadena de reacciones.
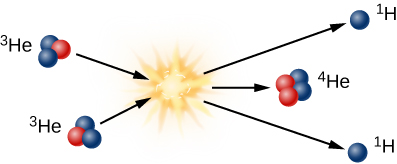
Estas animaciones de reacciones protón-protón muestran los pasos necesarios para la fusión del hidrógeno en helio en el Sol.
Visite el reactor de fusión Tokamak en el Laboratorio General Atomics en San Diego, CA, para un recorrido de 8 minutos.
La cadena protón-protón
Las reacciones nucleares en el Sol que hemos estado discutiendo pueden describirse sucintamente a través de las siguientes fórmulas nucleares:
\[\begin{aligned} ^1 \text{H}+ ~ ^1 \text{H} \rightarrow ~ ^2 \text{H}+ \text{e}^++v \\ ^2 \text{H}+ ~ ^1 \text{H} \rightarrow ~ ^3 \text{He}+ \gamma \\ ~ ^3 \text{He}+ ~ ^3 \text{He} \rightarrow ~ ^4 \text{He}+ ~ ^1 \text{H}+ ~ ^1 \text{H} \end{aligned} \nonumber\]
Aquí, los superíndices indican el número total de neutrones más protones en el núcleo,\(\text{e}^+\) es el positrón,\(v\) es el neutrino, e\(\gamma\) indica que se emiten rayos gamma. Tenga en cuenta que el tercer paso requiere dos núcleos de helio-3 para comenzar; los dos primeros pasos deben ocurrir dos veces antes de que pueda ocurrir el tercer paso.
Si bien, como discutimos, el primer paso en esta cadena de reacciones es muy difícil y generalmente lleva mucho tiempo, los otros pasos ocurren más rápidamente. Después de que se forma el núcleo de deuterio, sobrevive un promedio de sólo unos 6 segundos antes de ser convertido en\(^3 \text{He}\). Alrededor de un millón de años después de eso (en promedio), el\(^3 \text{He}\) núcleo se combinará con otro para formar\(^4 \text{He}\).
Podemos calcular la cantidad de energía que generan estas reacciones calculando la diferencia en las masas inicial y final. Las masas de átomos de hidrógeno y helio en las unidades normalmente utilizadas por los científicos son\(1.007825u\) y\(4.00268u\), respectivamente. (La unidad de masa,\(u\), se define como 1/12 la masa de un átomo de carbono, o aproximadamente la masa de un protón.) Aquí, incluimos la masa de todo el átomo, no solo del núcleo, porque los electrones también están involucrados. Cuando el hidrógeno se convierte en helio, se crean dos positrones (recuerden, el primer paso ocurre dos veces), y estos se aniquilan con dos electrones libres, sumando a la energía producida.
\[ \begin{aligned} 4 \times 1.007825 & =4.03130u \text{ (mass of initial hydrogen atoms)} \\ ~ & −4.00268u \text{ (mass of final helium atoms)} \\ ~ & =0.02862u \text{ (mass lost in the transformation)} \end{aligned} \nonumber\]
La masa perdida,\(0.02862u\), es 0.71% de la masa del hidrógeno inicial. Así, si 1 kilogramo de hidrógeno se convierte en helio, entonces la masa del helio es solo 0.9929 kilogramo, y 0.0071 kilogramo de material se convierte en energía. La velocidad de la luz (\(c\)) es de 3 × 108 metros por segundo, por lo que la energía liberada por la conversión de solo 1 kilogramo de hidrógeno en helio es:
\[\begin{array}{l} E=mc^2 \\ E=0.0071 \text{ kg} \times \left( 3 \times 10^8 \text{ m/s} \right)^2=6.4 \times 10^{14} \text{ J} \end{array} \nonumber\]
Esta cantidad, la energía liberada cuando un solo kilogramo (2.2 libras) de hidrógeno se somete a fusión, abastecería toda la electricidad utilizada por el hogar típico estadounidense durante aproximadamente 17,000 años.
Para producir la luminosidad del Sol de 4 × 10 26 vatios, unos 600 millones de toneladas de hidrógeno deben convertirse en helio cada segundo, de las cuales alrededor de 4 millones de toneladas se convierten de la materia en energía. Por muy grandes que sean estos números, el almacenamiento de hidrógeno (y por lo tanto de energía nuclear) en el Sol es aún más enorme, y puede durar mucho tiempo, de hecho, miles de millones de años.
A las temperaturas dentro de las estrellas con masas menores a aproximadamente 1.2 veces la masa de nuestro Sol (una categoría que incluye al Sol mismo), la mayor parte de la energía es producida por las reacciones que acabamos de describir, y este conjunto de reacciones se llama la cadena protón-protón (o a veces, la p-p cadena). En la cadena protón-protón, los protones chocan directamente con otros protones para formar núcleos de helio.
En las estrellas más calientes, otro conjunto de reacciones, llamado ciclo carbono-nitrógeno-oxígeno (CNO), logra el mismo resultado neto. En el ciclo de CNO, los núcleos de carbono e hidrógeno chocan para iniciar una serie de reacciones que forman nitrógeno, oxígeno y, en última instancia, helio. Los núcleos de nitrógeno y oxígeno no sobreviven sino que interactúan para formar carbono nuevamente. Por lo tanto, el resultado es el mismo que en la cadena protón-protón: cuatro átomos de hidrógeno desaparecen, y en su lugar, se crea un solo átomo de helio. El ciclo CNO juega sólo un papel menor en el Sol pero es la principal fuente de energía para las estrellas con masas mayores que alrededor de la masa del Sol.
Para que veas que hemos resuelto el acertijo que tanto preocupaba a los científicos a finales del siglo XIX. El Sol puede mantener su alta temperatura y producción de energía durante miles de millones de años a través de la fusión del elemento más simple del universo, el hidrógeno. Debido a que la mayor parte del Sol (y las otras estrellas) está hecho de hidrógeno, es un “combustible” ideal para alimentar una estrella. Como se discutirá en los siguientes capítulos, podemos definir a una estrella como una bola de gas capaz de conseguir que su núcleo se caliente lo suficiente como para iniciar la fusión de hidrógeno. Hay bolas de gas que carecen de la masa requerida para hacer esto (Júpiter es un ejemplo local); como tantos aspirantes en Hollywood, nunca serán estrellas.
Fusión en la Tierra
¿No sería maravilloso si pudiéramos duplicar el mecanismo de energía del Sol de manera controlada en la Tierra? (Ya lo hemos duplicado de manera incontrolada en bombas de hidrógeno, pero esperamos que nuestros almacenes de estos nunca se utilicen). La energía de fusión tendría muchas ventajas: utilizaría hidrógeno (o deuterio, que es hidrógeno pesado) como combustible, y hay hidrógeno abundante en los lagos y océanos de la Tierra. El agua se distribuye mucho más uniformemente en todo el mundo que el petróleo o el uranio, lo que significa que unos pocos países ya no tendrían una ventaja energética sobre los demás. Y a diferencia de la fisión, que deja subproductos peligrosos, los núcleos que resultan de la fusión son perfectamente seguros.
El problema es que, como vimos, se necesitan temperaturas extremadamente altas para que los núcleos superen su repulsión eléctrica y se sometan a fusión. Cuando las primeras bombas de hidrógeno explotaron en pruebas en la década de 1950, los “fusibles” para calentarlos lo suficiente eran bombas de fisión. Las interacciones a tales temperaturas son difíciles de mantener y controlar. Para hacer poder de fusión en la Tierra, después de todo, tenemos que hacer lo que hace el Sol: producir temperaturas y presiones lo suficientemente altas como para obtener núcleos de hidrógeno en términos íntimos entre sí.
La Unión Europea, Estados Unidos, Corea del Sur, Japón, China, Rusia, Suiza e India están colaborando en el Reactor Experimental Termonuclear Internacional (ITER), un proyecto para demostrar la viabilidad de la fusión controlada (Figura). La instalación se está construyendo en Francia. La construcción requerirá más de 10,000,000 de componentes y 2000 trabajadores para el montaje. Aún no se ha determinado la fecha de inicio de operaciones.
El ITER se basa en el diseño Tokamak, en el que un gran contenedor en forma de rosquilla está rodeado por imanes superconductores para confinar y controlar los núcleos de hidrógeno en un campo magnético fuerte. Los experimentos de fusión anteriores han producido alrededor de 15 millones de vatios de energía, pero sólo por uno o dos segundos, y han requerido 100 millones de vatios para producir las condiciones necesarias para lograr la fusión. El objetivo de ITER es construir el primer dispositivo de fusión capaz de producir 500 millones de vatios de energía de fusión hasta por 1000 segundos. El desafío es mantener el deuterio y el tricio, que participarán en las reacciones de fusión, lo suficientemente calientes y densos, durante el tiempo suficiente para producir energía.

Conceptos clave y resumen
La energía solar es producida por interacciones de partículas, es decir, protones, neutrones, electrones, positrones y neutrinos. Específicamente, la fuente de la energía del Sol es la fusión de hidrógeno para formar helio. La serie de reacciones necesarias para convertir hidrógeno en helio se denomina cadena protón-protón. Un átomo de helio es aproximadamente 0.71% menos masivo que los cuatro átomos de hidrógeno que se combinan para formarlo, y esa masa perdida se convierte en energía (con la cantidad de energía dada por la fórmula\(E = mc^2\)).
Glosario
- fisión
- descomponer los núcleos atómicos más pesados en núcleos más ligeros
- fusión
- acumulación de núcleos atómicos más pesados a partir de núcleos más ligeros
- neutrino
- partícula fundamental que no tiene carga y una masa que es pequeña en relación con un electrón; rara vez interactúa con la materia ordinaria y viene en tres tipos diferentes
- positrón
- partícula con la misma masa que un electrón, pero cargada positivamente
- cadena protón-protón
- serie de reacciones termonucleares por las cuales los núcleos de hidrógeno se construyen en núcleos de helio


