5.1: Coloides del Suelo
- Page ID
- 89005
Objetivos de aprendizaje
- Medir los efectos de diferentes cationes sobre las propiedades coloidales.
- Identificar los componentes del suelo que controlan el intercambio iónico.
- Determinar la capacidad de intercambio catiónico de horizontes de suelo seleccionados.
Los coloides consisten en minerales arcillosos y materia orgánica, y desempeñan papeles críticos en las propiedades químicas, físicas y biológicas del suelo. Los coloides son de tamaño muy pequeño. La mayoría de las cargas en el suelo provienen de coloides, lo que los hace importantes para la capacidad de intercambio catiónico, la capacidad de amortiguación y la retención de nutrientes como Ca 2+, K +, Mg 2+, etc. Además, el pequeño tamaño de los coloides conduce a áreas superficiales muy altas, lo que facilita reacciones químicas y proporciona hábitat para microbios. Algunas arcillas se expanden y contraen con los cambios en la humedad del suelo. La fuerza de las arcillas expandidas puede ser considerable y comúnmente causar fallas estructurales en cimientos de casas y muros de sótanos, carreteras y puentes, y otras estructuras artificiales. Otras arcillas no se expanden, y hacen sustancias ideales para alfarería de barro, o techos de tejas. La fracción de materia orgánica de los coloides son importantes para el desarrollo de la estructura del suelo, o como fuente de alimento para los organismos del suelo. Las propiedades del suelo atribuidas a los coloides son numerosas, y serán el foco de las siguientes actividades de laboratorio.
Materiales
- Placas de Petri
- Vasos
- Espátulas
- Caolinita pura
- Bentonita pura
- Caliper
- Batería de 6V
- Alambres de cobre sólidos, 2 totales, 25 cm de largo
- Pinzas de cocodrilo para los cables
- Toallas de papel
- Tubos de ensayo
- Frascos
- Buretas
- Dispensadores con tapa de botella para dispensar 10 mL
- Solución de indicador de fenolftaleína
- Solución de cloruro de aluminio, 1 M
- Solución de cloruro de potasio, 1 M
- Solución de cloruro de sodio, 1 M
- Solución de cloruro de calcio, 1 M
- Solución de hidróxido de sodio, 0.01 M
- Soluciones de extracto CEC de suelo simulado
- Horizonte E de Norfolk, HCl 0.002 M
- 10 mL de extracto representan 1 g de suelo
- Horizonte de Norfolk Bt, HCl 0.005 M
- 10 mL de extracto representan 1 g de suelo
- Horizonte Cecil Ap, 0.010 M HCl
- 10 mL de extracto representan 1 g de suelo
- Cecil Bt Horizon, 0.007 M HCl
- 10 mL de extracto representan 1 g de suelo
- Whitestore Bt Horizon, 0.015 M HCl
- 10 mL de extracto representan 0.5 g de suelo
Lectura Recomendada
- Introducción a la Sorción de Constituyentes Químicos en Suelos (Thompson y Goyne, 2012)
- Capacidad de Intercambio Catiónico y Saturación de Bases (Sonon et al., 2017)
Asignación Prelab
Usando las lecturas recomendadas y la introducción a este laboratorio, considere las preguntas que se enumeran a continuación. Estas definiciones/preguntas proporcionarán un resumen conciso de los principales conceptos a abordar en el laboratorio. También servirán de base para el cuestionario posterior al laboratorio y son útiles notas de estudio para los exámenes.
- Definir el término “coloide del suelo”. ¿Cuáles son los principales tipos de coloides de suelo?
- Describir las fuentes de carga en los coloides del suelo.
- Definir la capacidad de intercambio catiónico.
- ¿Qué unidades se utilizan para expresar la capacidad de intercambio catiónico?
- Enumere la cantidad general de capacidad de intercambio catiónico aportada por caolinita, montmorillonita (esmectita) y humus.
- Definir porcentaje de saturación base. ¿Qué cationes suelen considerarse cationes base? Técnicamente hablando no son bases. ¿Por qué se les llama cationes base?
Introducción
Las partículas coloidales extremadamente pequeñas (menores de 0.001 mm) de arcilla y humus controlan muchas propiedades químicas y físicas importantes del suelo. Esta porción del suelo a menudo se llama la “fracción activa”. El pequeño tamaño de los coloides da como resultado una gran superficie por unidad de peso, y su estructura iónica resulta en una carga eléctrica neta. El tipo, cantidad y mineralogía de coloides influirán fuertemente en la mayoría de las decisiones de manejo de la tierra. Por ejemplo, un suelo que es 40% de arcilla que consiste principalmente en esmectita (una arcilla de contracción 2:1) podría tener limitaciones para construir caminos, o construir cimientos debido al desplazamiento del suelo a medida que el suelo se moja y se seca. Sin embargo, dicho suelo podría ser altamente productivo para la agricultura de cultivos en hileras, debido a la alta cantidad de carga que facilita la retención de nutrientes como Ca 2+, K +, Mg 2+, etc. Por el contrario, un suelo, como un Oxisol que tiene 80% de arcilla tiene coloides que son principalmente óxidos de aluminio y hierro, que no se encogen ni se hinchan, y tienen una baja cantidad de carga. Así, el suelo sería muy adecuado para la construcción de cimientos. Sin embargo, la alta capacidad de fijación de fósforo y la limitada capacidad de retener cationes base limitan la productividad del suelo para la agricultura en hileras.
El intercambio iónico es una de las características más significativas de las fracciones de arcilla y humus. La capacidad de las partículas para atraer o adsorber cationes se denomina capacidad de intercambio catiónico. Esta capacidad permite que el suelo sirva como almacén de nutrientes vegetales como potasio, calcio y magnesio. Esta capacidad de intercambio reactivo también permite que el suelo sirva como filtro o medio de tratamiento para la aplicación terrestre de materiales de desecho.
Determinación de la capacidad de intercambio catiónico
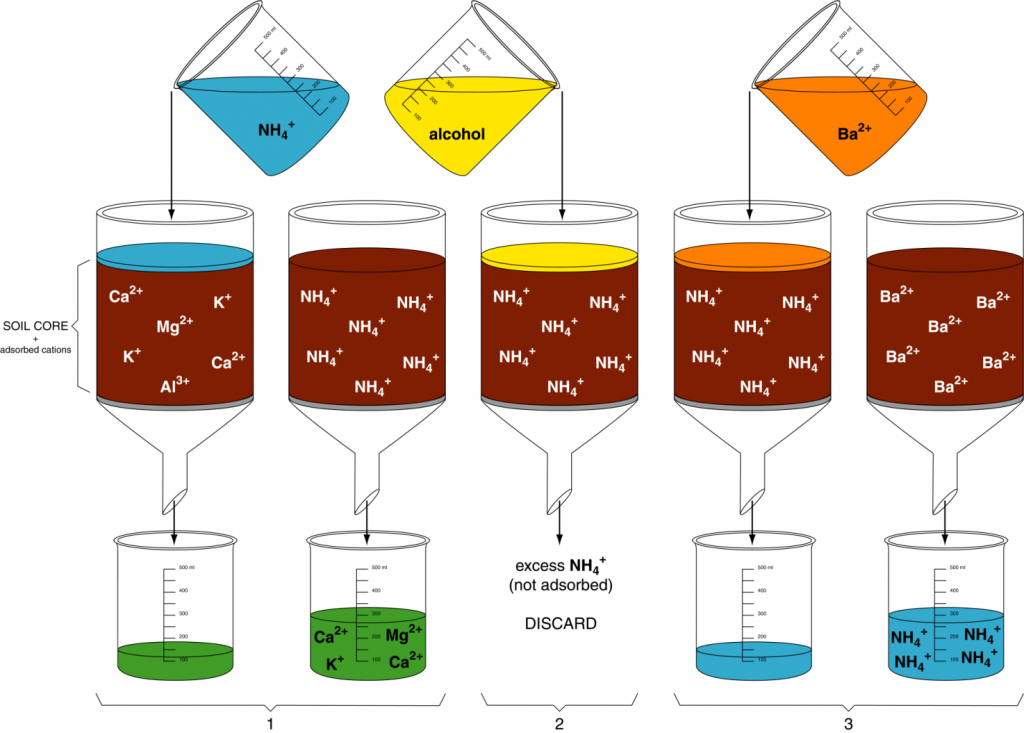
La capacidad de intercambio catiónico (cantidad de cationes que un suelo puede adsorber por unidad de peso, CEC) se puede determinar mediante un proceso de desplazamiento simple (Figura 13.1). En el paso 1, una muestra de suelo se satura primero con un catión simple como NH 4 + por lo que todos los sitios de carga negativa están ocupados por NH 4 +. En la etapa 2, se elimina el exceso de NH 4 + (es decir, no en sitios de intercambio) mediante lixiviación con alcohol etílico. En el paso 3, se utiliza otro catión como Ba 2+ para desplazar a todos los NH 4 +. El NH 4 + se recoge en el filtrado y se mide. La cantidad de NH 4 + recolectada de la muestra es la cantidad de cationes que el suelo puede contener, es decir, CEC.
Muchos cationes podrían ser utilizados en el paso 1 del método de desplazamiento. Los laboratorios de suelo suelen utilizar el ion amonio. Sin embargo, en esta actividad, se utilizará H + como catión saturante. Por lo tanto, determinaremos la cantidad de H + extraído en el filtrado. Después, usando esa cantidad, calcularás el CEC para cada muestra de suelo.
El cálculo de CEC utiliza el concepto de moles de carga. En química, un mol de un elemento es la cantidad del elemento con un peso en gramos numéricamente igual a su peso atómico. Por ejemplo, el peso atómico de K es 39.1, por lo que un mol de K pesa 39.1 g Un mol de cualquier elemento contiene 6.02 x 10 23 átomos del elemento. De igual manera, un mol de carga es de 6.02 x 10 23 cargas. Si K existe como catión en solución (K +), entonces una solución que contenga un mol de K contendría 6.02 x 10 23 cargas positivas.
El número de cargas positivas en el filtrado es así igual al número de cargas negativas en los sitios de intercambio en la muestra de suelo. Por lo tanto, su tarea es determinar el número de cargas en el filtrado. Cada ion H + tiene una carga positiva, por lo que al determinar la cantidad de H + en el filtrado, se puede determinar el número de cargas positivas en el filtrado y por extensión, el número de cargas negativas en los sitios de intercambio en la muestra de suelo.
Actividad 1: Demostración de Características de Encogimiento-O
En un laboratorio anterior, llenaste dos placas de Petri con suspensiones de bentonita y caolinita y las dejaste a un lado para que se sequen. Recupere esas placas de Petri y realice los siguientes pasos:
![]() Medir la altura y el radio de los discos de bentonita y caolinita, y registrar los resultados en la Tabla 13.1.
Medir la altura y el radio de los discos de bentonita y caolinita, y registrar los resultados en la Tabla 13.1.
![]() Calcular el volumen de cada disco, y registrar los resultados en la Tabla 13.1.
Calcular el volumen de cada disco, y registrar los resultados en la Tabla 13.1.
![]() Calcular y registrar el porcentaje de cambio de volumen en cada muestra en relación con el volumen original (volumen interior de la placa de Petri vacía).
Calcular y registrar el porcentaje de cambio de volumen en cada muestra en relación con el volumen original (volumen interior de la placa de Petri vacía).
Cuadro 13.1. Mediciones de Encogimiento y Cambios de Volumen
| Muestra | Radio (cm) | Altura (cm) | Volumen (cm^3) | % de cambio de volumen |
|---|---|---|---|---|
| Plato Petri vacío | N/A | |||
| Caolinita | ||||
| Bentonita |
![]() Si estuvieras construyendo una casa con sótano, ¿preferirías que el mineral arcilloso dominante del suelo en tu lote sea caolinita o bentonita? Explique.
Si estuvieras construyendo una casa con sótano, ¿preferirías que el mineral arcilloso dominante del suelo en tu lote sea caolinita o bentonita? Explique.
Actividad 2. Demostraciones de Carga Coloide
Usando la suspensión restante de la Actividad 1, tu instructor demostrará carga coloidal a la clase. En esta demostración, dos cables con pinzas de cocodrilo están unidos a una batería de 6V: un cable al terminal positivo y el otro al terminal negativo. Los dos alambres se insertan luego en la suspensión y se dejan reaccionar durante aproximadamente 15 minutos.
![]() Describe lo que observas cuando se retiran los cables de la lechada, y explica el fenómeno que causa esto.
Describe lo que observas cuando se retiran los cables de la lechada, y explica el fenómeno que causa esto.
Actividad 3: Demostración de Floculación y Dispersión
Como ya saben, la mayoría de las arcillas del suelo tienen una carga negativa que es neutralizada en diversos grados por los cationes adsorbidos. Los floculados o agregados se forman más rápidamente y son más estables cuando el coloide del suelo es neutralizado más completamente por el catión adsorbido. La cantidad de neutralización está relacionada con el tamaño de iones, valencia y concentración. Realice el siguiente experimento para probar el efecto de diversos iones sobre la floculación de una arcilla de suelo dispersa.
- Llene 5 tubos de ensayo hasta 1/2 llenos con la suspensión de arcilla dispersa. El tubo de ensayo 5, que contiene la suspensión de arcilla original, se reservará para su uso como cheque.
- Agrega 10 gotas de 1 M AlCl 3 al tubo de ensayo número 1.
- Agrega 10 gotas de KCl 1 M al tubo de ensayo 2.
- Añadir 10 gotas de NaCl 1 M al tubo de ensayo 3.
- Agrega 10 gotas de CaCl 1 M 2 al tubo de ensayo 4.
- Agitar cada suspensión a fondo.
- Observe y registre el tiempo que comienza la floculación en cada tubo.
- Continuar observando a lo largo del resto del periodo de clase y anotar el tamaño relativo y las tasas de sedimentación de los flóculos.
![]() Registre sus observaciones en la Tabla 13.2.
Registre sus observaciones en la Tabla 13.2.
Cuadro 13.2. Efecto de los cationes sobre la floculación de una suspensión de arcilla.
| Catión añadido | Tamaño relativo y tasas de sedimentación de los flóculos |
|---|---|
| K+ | |
| Na+ | |
| Ca2+ | |
| Al3+ | |
| Comprobar |
Actividad 4. Determinar la CEC mediante la sustitución de cationes adsorbidos.
En esta actividad, valorarás el filtrado con una solución 0.01 molar de NaOH usando fenolftaleína como indicador. La fenolftaleína cambia de incolora a rosa tenue cuando la cantidad de iones OH — añadidos a través del NaOH es igual a la cantidad de iones H + en la solución (es decir, cuando el pH se eleva a 7). Para esta actividad, supongamos que las muestras de suelo han sido extraídas y los filtrados ya están disponibles para su análisis.
- Colocar 10 ml de cada filtrado en matraces separados de 125 ml. Esta cantidad de 10 ml es la cantidad de filtrado de 1.0 gramo de suelo.
- Añadir 10 gotas del indicador de fenolftaleína.
- Valorar el extracto con la solución de NaOH hasta un punto final rosado tenue. La valoración debe hacerse con mucho cuidado para obtener resultados significativos. Si pones demasiado NaOH en el matraz y obtienes un color rosa brillante, desecha la solución y repite el proceso. En la siguiente tabla, registrar los mililitros de solución de NaOH utilizados para lograr el punto final.
![]() Calcula la CCA y registra tus datos en la Tabla 13.3.
Calcula la CCA y registra tus datos en la Tabla 13.3.
Aquí hay un ejemplo de cómo calcular la CEC, suponiendo que se requirieron 2.5 mL de NaOH para lograr un punto final. La reacción que se produce durante la titulación es
\[\text{NaOH}+\text{H}^{+}\rightarrow\text{Na}^{+}+\text{H}_2\text{O} \nonumber\]
Así, un mol de NaOH reacciona con un mol de H +. Por lo tanto, en el punto final de fenolftaleína, se agregaron moles de NaOH = moles de H+ en solución.
La solución de NaOH 0.01 molar contiene 1 cmol de carga por litro (1 cmol c/L). Por lo tanto 2.5 mL NaOH contiene
\[\text{cmol}_\text{c}\text{ of NaOH}=2.5\text{ mL NaOH}\times\frac{1\text{ L}}{1000\text{ mL}}\times\frac{0.01\text{ mol NaOH}}{1\text{ L}}\times\frac{1\text{ mol}_\text{c}}{1\text{ mol NaOH}}\times \frac{100\text{ cmol}_\text{c}}{1\text{ mol}_\text{c}}= 0.0025\text{ mol}_\text{c}\text{ NaOH} \nonumber\]
Así, la CCA es
\[\frac{\text{cmol}_\text{c}}{\text{kg soil}}= \frac{0.0025\text{ cmol}_\text{c}}{1\text{ g soil}}\times\frac{1000\text{ g soil}}{1\text{ kg soil}}= \frac{2.5cmolc}{\text{kg soil}} \nonumber\]
Cuadro 13.3. Cálculos de la CEC.
| Extracto | Molaridad de NaOH | Mililitros de NaOH usados | Wt. De suelo | CEC | % Arcilla |
|---|---|---|---|---|---|
| Norfolk E | 0.01 | 1 g | 9 | ||
| Norfolk Bt | 0.01 | 1 g | 37 | ||
| Cecil Ap | 0.01 | 1 g | 13 | ||
| Cecil Bt | 0.01 | 1 g | 51 | ||
| Tienda Blanca Bt | 0.01 | 0.5 g | 57 |
![]() Utilizando los datos del Cuadro 13.3, construir una gráfica en la Figura 13.2 con porcentaje de arcilla en el eje X y CEC en el eje Y. Etiquetar los ejes y trazar todos los datos. Dibuja una línea a través de los puntos de la gráfica para el Norfolk E, Norfolk Bt y Cecil Bt, y responde las siguientes preguntas:
Utilizando los datos del Cuadro 13.3, construir una gráfica en la Figura 13.2 con porcentaje de arcilla en el eje X y CEC en el eje Y. Etiquetar los ejes y trazar todos los datos. Dibuja una línea a través de los puntos de la gráfica para el Norfolk E, Norfolk Bt y Cecil Bt, y responde las siguientes preguntas:
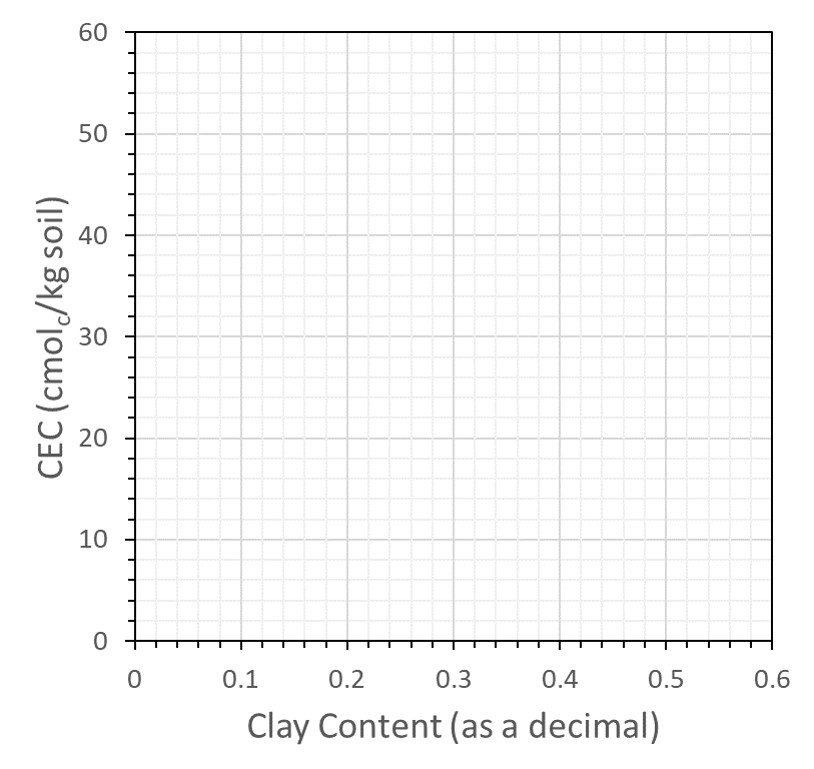
![]() De los cuatro factores principales que afectan a la CEC del suelo (cantidad de arcilla, tipo de arcilla, cantidad de humus, pH), ¿cuál es el responsable de este incremento lineal en la CEC?
De los cuatro factores principales que afectan a la CEC del suelo (cantidad de arcilla, tipo de arcilla, cantidad de humus, pH), ¿cuál es el responsable de este incremento lineal en la CEC?
![]() La pendiente de la línea representa el cambio en la CEC dividido por el cambio en el contenido de arcilla. Al expresar el contenido de arcilla como una fracción (por ejemplo, 30% arcilla = 0.30 kg arcilla/kg suelo), la pendiente se vuelve
La pendiente de la línea representa el cambio en la CEC dividido por el cambio en el contenido de arcilla. Al expresar el contenido de arcilla como una fracción (por ejemplo, 30% arcilla = 0.30 kg arcilla/kg suelo), la pendiente se vuelve
\[\text{Slope}=\frac{\Delta\frac{\text{ cmol}_\text{c}}{\text{kg soil}}}{\Delta\frac{\text{kg clay}}{\text{kg soil}}}=\frac{\text{max CEC}-\text{min CEC}}{\text{max clay}-\text{min clay}}=\text{______}\frac{\text{ cmol}_\text{c}}{\text{kg clay}} \nonumber\]
![]() La pendiente calculada es la CEC sobre una base arcillosa. Usando esa pendiente (cmol c/kg arcilla), utilice la Figura 13.2 para determinar el tipo de arcilla en los suelos Norfolk y Cecil.
La pendiente calculada es la CEC sobre una base arcillosa. Usando esa pendiente (cmol c/kg arcilla), utilice la Figura 13.2 para determinar el tipo de arcilla en los suelos Norfolk y Cecil.
![]() La línea que has dibujado no pasa por el origen, lo que indica que un suelo sin arcilla seguiría teniendo CEC. ¿Cómo podría ser esto posible?
La línea que has dibujado no pasa por el origen, lo que indica que un suelo sin arcilla seguiría teniendo CEC. ¿Cómo podría ser esto posible?
![]() La muestra de horizonte Cecil Ap cae justo por encima de la línea que dibujaste en la pregunta #1, sin embargo, ambas muestras de Cecil fueron tomadas del mismo perfil. ¿Cómo se puede explicar esta diferencia en la CEC?
La muestra de horizonte Cecil Ap cae justo por encima de la línea que dibujaste en la pregunta #1, sin embargo, ambas muestras de Cecil fueron tomadas del mismo perfil. ¿Cómo se puede explicar esta diferencia en la CEC?
![]() El CEC para el horizonte White Store Bt tampoco cae en la línea para el suelo de Norfolk y Cecil. Explique qué puede ser diferente acerca de los coloides en el suelo White Store Bt.
El CEC para el horizonte White Store Bt tampoco cae en la línea para el suelo de Norfolk y Cecil. Explique qué puede ser diferente acerca de los coloides en el suelo White Store Bt.
Ejemplo Cálculos de Capacidad de Intercambio Catiónico
Supongamos que un suelo tiene un CEC de 1.0 cmol c/kg. ¿Cuántos kg de Ca 2+ se pueden adsorber en una hectárea de suelo a una profundidad de 20 cm? Asumir una densidad aparente de 1.4 Mg/m 3.
Volumen de suelo = profundidad del área:
\[\text{Soil volume}=10,000\text{ m}^2\times0.2\text{ m}=2,000\text{ m}^3 \nonumber\]
Peso del suelo = volumen de densidad:
\[\text{Soil weight}=1.4\frac{\text{Mg}}{\text{m}^3}×2,000\text{ m}^3=2,800\text{ Mg}=2,800,000\text{ kg} \nonumber\]
Debido a que Ca tiene una valencia de 2, un mol de Ca tiene 2 moles de carga:
\[\frac{2\text{ mol}_\text{c}}{1\text{ mol Ca}|^{2+}} \nonumber\]
El suelo puede adsorber 1.0 cmol c/kg. La cantidad de Ca requerida para suministrar esta cantidad de cargo es
\[\frac{1\text{ cmol}_\text{c}}{\text{kg soil}}\times\frac{1\text{ cmol Ca}^{2+}}{2\text{ cmol}_\text{c}}=\frac{0.5\text{ cmol Ca}^{2+}}{\text{kg soil}} \nonumber\]
El peso atómico del Ca es 40.078, por lo que el suelo puede adsorberse
\[\frac{0.5\text{ cmol Ca}^{2+}}{\text{kg soil}}\times\frac{1\text{ mol Ca}^{2+}}{100\text{ cmol Ca}^{2+}}\times\frac{40.078\text{g Ca}^{2+}}{1\text{mol Ca}^{2+}}=\frac{0.20\text{ g Ca}^{2+}}{\text{kg soil}} \nonumber\]
La cantidad de Ca adsorbida en el volumen total del suelo es
\[\frac{0.20\text{ g Ca}^{2+}}{\text{ kg soil}}\times\frac{2,800,000\text{ kg soil}}{1\text{ ha}}\times\frac{1\times\text{ kg Ca}^{2+}}{1000\text{ g Ca}^{2+}}=\frac{560\text{ kg Ca}^{2+}}{ha} \nonumber\]
En el problema anterior, ¿cuánto Al 3+ podría ser adsorbido por el suelo?
Debido a que la valencia de Al es 3, un mol de Al tiene 3 moles de carga. Así, el suelo, que tiene 1 cmol c/kg, puede adsorber
\[\frac{1\text{ cmol}_\text{c}}{\text{kg soil}}× \frac{1\text{cmol Al}^{3+}}{3\text{ cmol}_\text{c}}=\frac{0.33\text{ cmol Al}^{3+}}{\text{kg soil}} \nonumber\]
El peso atómico de Al es 26.981538 por lo que el suelo puede adsorberse
\[\frac{0.33\text{ cmol Al}^{3+}}{\text{kg soil}}\times\frac{1\text{ mol Al}^{3+}}{100\text{ cmol Al}^{3+}}\times\frac{26.982\text{ g Al}^{3+}}{1\text{ mol Al}^{3+}}=\frac{0.09\text{ g Al}^{3+}}{\text{kg soil}} \nonumber\]
La cantidad de Al adsorbida en el volumen total del suelo es
\[\frac{0.09\text{ g Al}^{3+}}{\text{ kg soil}}\times\frac{2,800,000\text{ kg soil}}{1\text{ ha}}\times\frac{1\times\text{ kg Al}^{3+}}{1000\text{ g Al}^{3+}}=\frac{252\text{ kg Al}^{3+}}{ha} \nonumber\]
Cálculos de capacidad de intercambio catiónico
Calcular cuántos kg/ha de los siguientes cationes podría adsorber este suelo (con una CEC de 1 cmol c/kg).
![]() Mg 2+, con un peso atómico de 24.305:
Mg 2+, con un peso atómico de 24.305:
![]() Na +, con un peso atómico de 22.990:
Na +, con un peso atómico de 22.990:
![]() H +, con un peso atómico de 1.008:
H +, con un peso atómico de 1.008:
![]() K +, con un peso atómico de 39.098:
K +, con un peso atómico de 39.098:
Cálculos de Saturación Base
Ca 2+, Mg 2+, K + y Na + se denominan cationes básicos porque cuando están en solución, la solución es básica. En contraste, H + y Al 3+ se consideran cationes ácidos porque disminuyen el pH de la solución.
Por lo tanto, la saturación de base es
\[\text{Percent base saturation}=\frac{\text{ cmol}_\text{c}\text{ of base cations}}{\text{total CEC of the soil}}\times100\text{%} \nonumber\]
Un suelo alcalino encontrado en una región semiárida podría tener las siguientes características de intercambio catiónico (por kg de suelo):
- 9.0 cmol c Ca 2+
- 2.5 cmol c Mg 2+
- 0.5 cmol c K +
- 2.0 cmol c Al 3+
- 2.0 cmol c H +
![]() Si estos cationes son los únicos en los sitios de intercambio de este suelo, ¿cuál es el porcentaje de saturación base?
Si estos cationes son los únicos en los sitios de intercambio de este suelo, ¿cuál es el porcentaje de saturación base?
Actividad 5. Cálculo versus estimación de CEC
Hay dos formas de calcular la CEC: el método de la suma de cationes y el método de mineralogía.
El método de la suma de cationes
Si tiene un análisis de suelo donde se listan las cantidades de todos los cationes en el suelo, simplemente sumando todas esas cantidades intercambiables dará como resultado el CEC que encontró en los problemas anteriores.
El Método “Mineralogía”
Como sabes por tu lectura y discusión en clase, los minerales arcillosos tienen una gama de valores para la CEC. Si se conoce la mineralogía de la fracción arcillosa (es decir, el tipo y las cantidades de cada mineral arcilloso), entonces se puede aproximar la CEC.
Para facilitar estos cálculos, el Cuadro 13.4 contiene valores representativos para que CEC los use en todos los cálculos de esta clase a menos que se indique lo contrario. En la naturaleza, sin embargo, estos coloides del suelo tendrán un rango de valores.
Cuadro 13.4. CCA típica de diversos coloides de suelo.
| Tipo mineral o coloide | CEC de coloide puro |
|---|---|
| cmolc/kg | |
| caolinita | 10 |
| ilita | 30 |
| montmorillonita/esmectita | 100 |
| vermiculita | 150 |
| humus | 200 |
Como ejemplo de este enfoque de mineralogía para los cálculos de la CEC, considere un suelo que tenga 100% arcilla donde la arcilla sea 100% caolinita. La CCA sería entonces de 10 cmol c/kg. Si un suelo contiene solo 10% de caolinita (o 10 kg de arcilla en 100 kg de suelo), sin embargo, esta arcilla contribuiría
\[\text{Total CEC of the soil}=\frac{10\text{ cmol}_\text{c}}{\text{kg clay}}\times\frac{10\text{ kg clay}}{100\text{ kg soil}}=\frac{1.0\text{ cmol}_\text{c}}{\text{kg soil}} \nonumber\]
Un suelo de pradera contiene 30% de arcilla. Esta fracción del tamaño de arcilla es predominantemente montmorillonita. El suelo también contiene 5% de humus (materia orgánica).
![]() Utilizando el método de mineralogía, ¿cuál es la capacidad de intercambio catiónico (CEC) aportada por la arcilla?
Utilizando el método de mineralogía, ¿cuál es la capacidad de intercambio catiónico (CEC) aportada por la arcilla?
![]() ¿Cuál es la capacidad estimada de intercambio catiónico (CEC) aportada por el humus?
¿Cuál es la capacidad estimada de intercambio catiónico (CEC) aportada por el humus?
![]() ¿Cuál es el total estimado de CEC de este suelo?
¿Cuál es el total estimado de CEC de este suelo?
Los siguientes son datos reales de laboratorio para el suelo en el ejemplo:
Cuadro 13.5. Datos de cationes intercambiables
| Acidez intercambiable | Bases Intercambiables | Bases Intercambiables | Bases Intercambiables | Bases Intercambiables |
|---|---|---|---|---|
| H+ + Al3+ | Ca2+ | Mg2+ | K+ | Na+ |
| —cmolc/kg— | —cmolc/kg— | —cmolc/kg— | —cmolc/kg— | —cmolc/kg— |
| 14.0 | 29 | 10 | 5.5 | 1.5 |
![]() Calcular el CEC a partir de los datos de la tabla utilizando el método de suma de cationes.
Calcular el CEC a partir de los datos de la tabla utilizando el método de suma de cationes.
![]() ¿Cuál es el porcentaje de saturación base?
¿Cuál es el porcentaje de saturación base?
![]() Si quisieras sustituir el Na + por Ca 2+, ¿cuántos kilogramos de Ca 2+ por 2,800,000 kg de suelo necesitarías?
Si quisieras sustituir el Na + por Ca 2+, ¿cuántos kilogramos de Ca 2+ por 2,800,000 kg de suelo necesitarías?
Asignación: Cuestionario en línea
Un cuestionario para este laboratorio estará disponible en línea. Por favor acceda a él según lo indique su instructor.


