3.2: Conductores de punto cuántico/ molécula única
- Page ID
- 84372
Como vimos en el Capítulo 2, un punto cuántico es un conductor 0-d; sus electrones están confinados en todas las dimensiones. Un buen ejemplo de un punto cuántico es una sola molécula que se aísla en el espacio. Podemos aproximar nuestro punto cuántico o molécula por un pozo cuadrado que confina electrones en todas las dimensiones. Una consecuencia de este confinamiento es que los niveles de energía en el punto cuántico aislado o molécula son discretos. Típicamente, sin embargo, el modelo simple de partículas en una caja no genera estimaciones suficientemente precisas de los niveles de energía discretos en el punto. Más bien, el material en el punto cuántico o la estructura de la molécula define los niveles de energía reales.
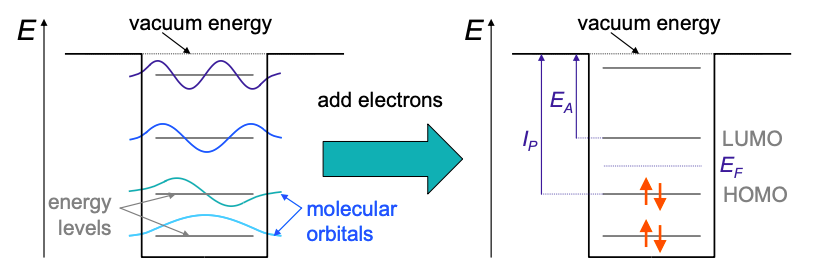
La Figura 3.2.1 muestra un pozo cuadrado típico con sus niveles de energía. Supondremos que estos niveles de energía ya han sido determinados con precisión. Cada nivel de energía corresponde a un orbital molecular diferente. Los niveles de energía de los estados unidos dentro del pozo se miden con respecto a la Energía de Vacío, típicamente definida como la energía potencial de un electrón libre en un vacío. Tenga en cuenta que si hay un campo eléctrico, la energía de vacío variará con la posición.
A continuación le agregamos electrones a la molécula. Cada nivel de energía toma dos electrones, uno de cada giro. El orbital molecular más alto ocupado (HOMO) y el orbital molecular desocupado más bajo (LUMO) son particularmente importantes. En la mayoría de los materiales químicamente estables, el HOMO está completamente lleno; los HOMO parcialmente llenos generalmente mejoran la reactividad ya que tienden a aceptar o donar electrones fácilmente.
Anteriormente afirmamos que el transporte de carga se produce sólo en estados parcialmente llenos. Esto se logra mejor agregando electrones al LUMO, o restando electrones del HOMO. Modificar la población de electrones en todos los demás estados requiere mucha más energía. De ahí que ignoraremos todos los orbitales moleculares excepto el HOMO y el LUMO.
La Figura 3.2.1 también define el Potencial de Ionización (IP) de una molécula como la energía de unión de un electrón en el HOMO. La energía de unión de los electrones en el LUMO se define como la Afinidad Electrónica (EA) de la molécula.