2.3: Contaminantes con uso específico
- Page ID
- 70514
2.3. Contaminantes con uso específico
2.3.1. Productos de Protección de Cultivos
Autor: Kees van Gestel
Críticos: Steven Droge, Peter Dohmen
Objetivos de inclinación:
Deberías ser capaz de:
- describir el papel de los productos de protección de cultivos en la agricultura
- mencionan diferentes tipos de plaguicidas y sus diferentes grupos objetivo.
- distinguir y mencionar importantes grupos químicos de plaguicidas
- relacionados con la química
- relacionados con el modo de acción - describir los principales componentes incluidos en una formulación comercial de un producto de protección de cultivos junto a la sustancia o principios activos.
Palabras clave: Insecticidas, Herbicidas, Fungicidas, Sustancias activas, Formulaciones
Introducción
Los productos de protección de cultivos se utilizan en la agricultura. El objetivo principal de la agricultura es el suministro de alimentos. Para ello, la agricultura tiene como objetivo reducir la competencia por otras plantas (no agrícolas) y la pérdida de cultivo por herbívoros o enfermedades. Una herramienta importante para lograrlo es el uso de químicos, como los productos de protección de cultivos (CPP). En consecuencia, los CPP se introducen intencionalmente en el ambiente y representan una de las mayores fuentes de sustancias químicas xenobióticas en el ambiente. Estos químicos son, por definición, efectivos contra el organismo diana, a menudo ya en dosis bastante bajas, pero también pueden ser tóxicos para organismos no diana, incluidos los humanos. El uso de pesticidas, también llamados Productos de Protección de Cultivos (CPP) o a menudo también Productos de Protección Vegetal (PPP, este último término puede ser engañoso para herbicidas que pretenden reducir todas las plantas excepto las plantas de cultivo), por lo tanto, está estrictamente regulado en la mayoría de los países. Los principales pesticidas utilizados en los mayores volúmenes a nivel mundial son herbicidas all s, insecticidas y fungicidas. Como se muestra en el Cuadro 1, los plaguicidas se utilizan contra un gran número de enfermedades y plagas.
Cuadro 1. Clasificación de plaguicidas según lo que se supone que deben controlar
|
Tipo de pesticida |
Target |
|
acaricidas |
contra ácaros y arañas (incl. miticidas) |
|
algicidas |
contra algas |
|
altelmínticos (vermicidas) |
contra parásitos |
|
antibióticos |
contra bacterias y virus (incl. bactericidas) |
|
bactericidas |
contra bacterias |
|
fungicidas |
contra hongos |
|
herbicidas |
contra malezas |
|
insecticidas |
contra insectos |
|
acaricidas |
contra ácaros |
|
molusquicidas |
contra babosas y caracoles |
|
nematicidas |
contra nematodos |
|
reguladores del crecimiento vegetal |
retardar o acelerar el crecimiento de las plantas |
|
repelentes |
ahuyentar plagas (por ejemplo, insectos, aves) |
|
rodenticidas |
contra roedores |
Formulaciones
Un producto pesticida generalmente consiste en una o más sustancias activas, que son traídas al mercado en una formulación comercial (polvo en aerosol, granulado, producto líquido etc.). La formulación se utiliza para facilitar el manejo práctico y la aplicación del químico, pero también para potenciar su efecto o su seguridad de uso. El principio activo puede, por ejemplo, ser un químico sólido, mientras que la aplicación requiere que se pulveriza. O la sustancia activa se degrada rápidamente bajo la influencia de la luz solar y por lo tanto tiene que ser encapsulada. Uno de los tipos de formulación más utilizados es una emulsión concentrada, que puede ser rociada directamente después de la dilución con agua. En esta formulación, la sustancia activa se disuelve en una matriz oleosa y se agrega un detergente como emulsionante para hacer que el aceite sea miscible con agua. De esta manera, la sustancia activa se vuelve rápidamente disponible después de la pulverización. En las denominadas formulaciones de liberación lenta, la sustancia activa se encapsula en microcápsulas permeables, de las cuales se libera lentamente. Otro componente de una formulación puede ser un sinergista, lo que aumenta la eficacia de la sustancia activa, por ejemplo bloqueando enzimas que metabolizan la sustancia activa. Aquí una descripción general de los componentes principales de la formulación:
- Disolventes: para facilitar el manejo y aplicación de las sustancias activas, suelen disolverse. Para un compuesto altamente soluble en agua, este disolvente puede ser solo agua; sin embargo, la mayoría de los compuestos tienen baja solubilidad en agua y, por lo tanto, se disuelven en solventes orgánicos.
- Emulsionante, detergentes, dispersantes: se utiliza para proporcionar una mezcla homogénea de la sustancia activa en la solución acuosa de pulverización.
- Portador: formulaciones sólidas, tales como gránulos humectables (WG). Todas las formulaciones en polvo humectables (WP) a menudo usan materiales inertes como arcilla (caolinita) como vehículo.
- Agente humectante: ayudan a proporcionar una película homogénea en la superficie de la planta.
- Adyuvante: puede ayudar a aumentar la absorción de la sustancia activa en la planta.
- Constituyentes menores:
- Agente anticongelante: para mantener estable la formulación también en condiciones de almacenamiento en frío.
- Agente antiespumante: algunos de los formulantes pueden dar lugar a la formación de espuma durante la aplicación, lo cual no es deseado.
- Conservante, biocida: para prevenir la degradación biológica de la sustancia activa o de los formulantes durante el almacenamiento.
- Existen numerosos componentes adicionales específicos adicionales para fines específicos como colores, retenes, pegatinas, etc.
Se utilizan cuatro tipos de nomenclatura en el caso de los plaguicidas:
1. El nombre comercial, por ejemplo Calypso ®, que es dado por el fabricante. La misma sustancia activa a menudo se vende con más de un nombre comercial diferente (en consecuencia, el uso de nombres comerciales únicamente no es una descripción suficiente de la sustancia problema en la literatura científica).
2. El nombre en clave, que es el nombre “común” de la sustancia activa. Calypso ® 480 SC, por ejemplo, es una suspensión concentrada que contiene 480 g/L del principio activo tiacloprid.
3. El nombre químico de la sustancia activa. El tiacloprid es [3- [(6-cloropiridin-3-il) metil] -1,3-tiazolidin-2-iliden] cianamida.
4. El nombre del grupo químico al que pertenece la sustancia activa, en caso de tiacloprid: neonicotinoides.
Clases químicas
Los pesticidas representan bastantes grupos diferentes de productos químicos. Los pesticidas incluyen productos químicos inorgánicos (como el cobre utilizado como fungicida), químicos sintéticos orgánicos y biológicos (compuestos orgánicos naturales). Se pueden usar pesticidas del mismo grupo químico contra diferentes organismos de plagas, como los compuestos organoestánnicos (ver más abajo). Algunos químicos tienen un amplio modo de acción: muchos desinfectantes del suelo, como el metamo-sodio, matan nematodos, hongos, insectos del suelo y malezas. Otros pesticidas son más selectivos, como los neonicotinoides que actúan únicamente sobre los insectos, o muy selectivos, como el regulador del crecimiento de insectos fenoxicarb, que se usa contra los rodillos de hojas sin afectar a sus enemigos naturales. La selectividad de un pesticida también indica en qué medida las especies no objetivo pueden verse afectadas por su aplicación (efectos secundarios). El manejo integrado de plagas (IPM) tiene como objetivo un sistema de protección de cultivos lo más sustentable posible mediante la combinación de agentes biológicos (depredadores del organismo plaga) utilizando productos químicos que tienen un modo de acción selectivo. Tales sistemas están recibiendo hoy en día un interés creciente en diferentes cultivos agrícolas.
Se presentan con más detalle algunos grupos de plaguicidas que se utilizaron o aún son ampliamente utilizados. Sus modos de acción se discuten en el Capítulo 4.
- Hidrocarburos clorados
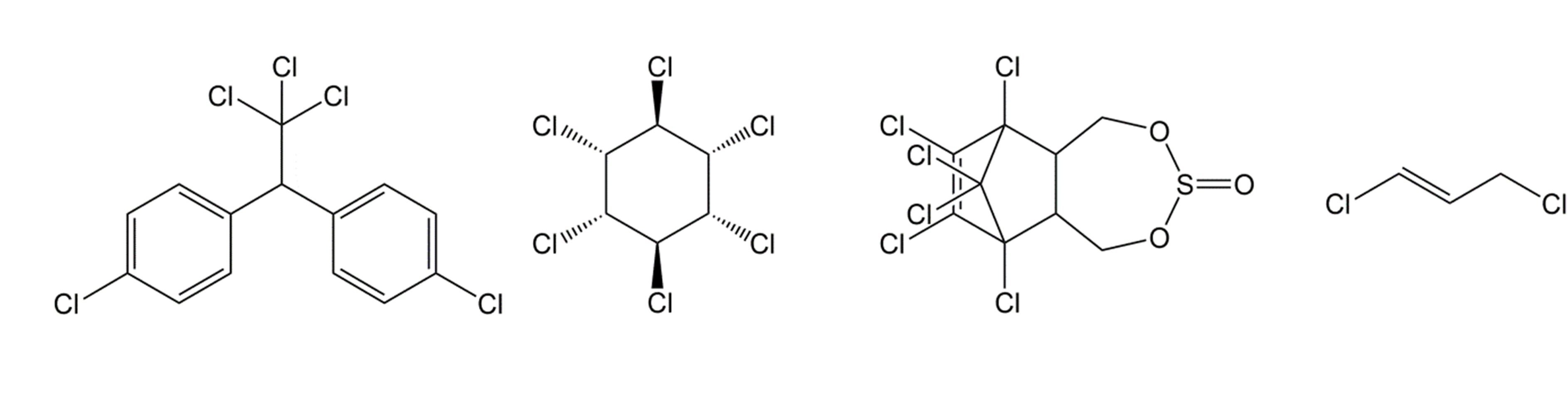
El representante más conocido de este grupo es el DDT (dicloro-difenil tricloroetano; Figura 1), que fue descubierto en 1939 por el entomólogo suizo Paul Hermann Müller y parecía ser un pesticida ideal: era efectivo, barato y fácil de producir y permaneció activo durante un largo periodo de tiempo. Como remedio contra la Malaria y otras enfermedades transmitidas por insectos, ha salvado millones de vidas humanas. Sin embargo, la alta persistencia del DDT, su fuerte bioacumulación y sus efectos sobre las poblaciones de aves han desencadenado la búsqueda de alternativas y su prohibición en la mayoría de los países occidentales. Pero en algunos países en desarrollo, debido a la falta de alternativas adecuadas para un control efectivo de la malaria, el DDT sigue en uso para matar los mosquitos de la malaria.
Otros representantes de los hidrocarburos clorados son el lindano, también llamado gamma-hexaclorociclohexano (Figura 1), y los ciclodienos que incluyen los “drinos” (aldrina, dieldrina, endrina, Ver Sección 2.1) y endosulfán (Figura 1). Debido a su alta persistencia y potencial bioacumulativo, la mayoría de los plaguicidas organoclorados han sido prohibidos.
Los hidrocarburos halogenados volátiles se utilizaron a menudo como desinfectantes del suelo. Estos compuestos fueron inyectados en el suelo, y actuaron como nematicida pero también mataron hongos, insectos del suelo y malezas. Un ejemplo es 1,3-dicloropropeno (Figura 1).
- Organofosfatos
Los organofosfatos son ésteres de ácido fosfórico y constituyen importantes moléculas biológicas como los ácidos nucleicos (ADN) o ATP. Dentro del contenido de pesticidas esto se refiere principalmente a un grupo de moléculas de organofosfato que interfieren con la acetilcolinesterasa. Los gases nerviosos, producidos para la guerra química (p. ej., Sarín), también pertenecen a los organofosfatos. Son mucho menos persistentes y por lo tanto se introdujeron como alternativas para los hidrocarburos clorados. La estructura molecular común de los organofosfatos es un triéster de fosfato, fosfonato, fosfortionato, fosfortiolato, fosforditionato o fosforamidato (Figura 2). Con dos de los tres enlaces éster, un grupo metilo o etilo se une al átomo de P, mientras que el tercer enlace éster se une al grupo restante o “grupo saliente”.
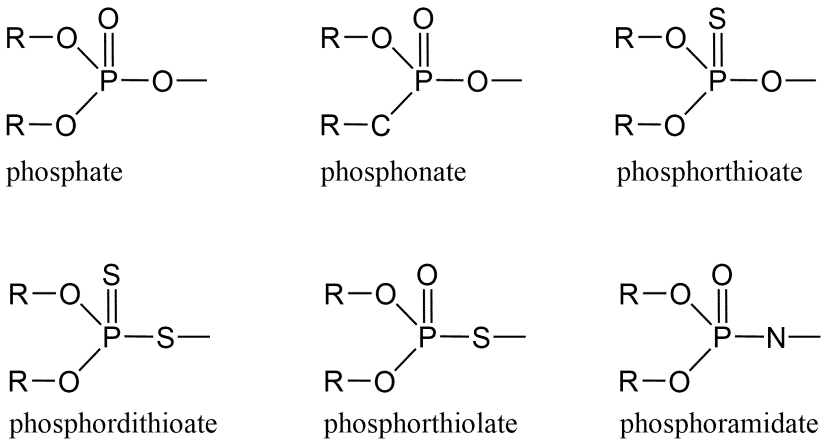
Dependiendo de la identidad de este último grupo, se pueden distinguir tres subgrupos:
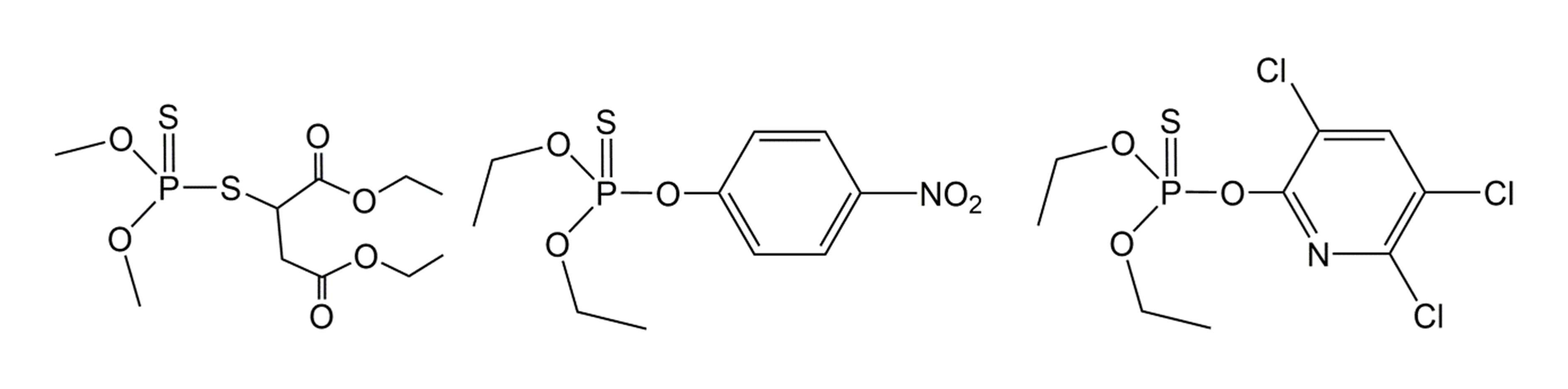
1. Organofosfatos alifáticos, incluyendo malatión (Figura 3) y una serie de químicos sistémicos.
2. Fenil-organofosfatos, que son más estables que los alifáticos pero también menos solubles en agua, como el paratión (ya no permitido en Europa; Figura 3).
3. Organofosfatos heterocíclicos, incluidos los químicos con un anillo aromático que contiene un átomo de nitrógeno como el clorpirifos (Figura 3).
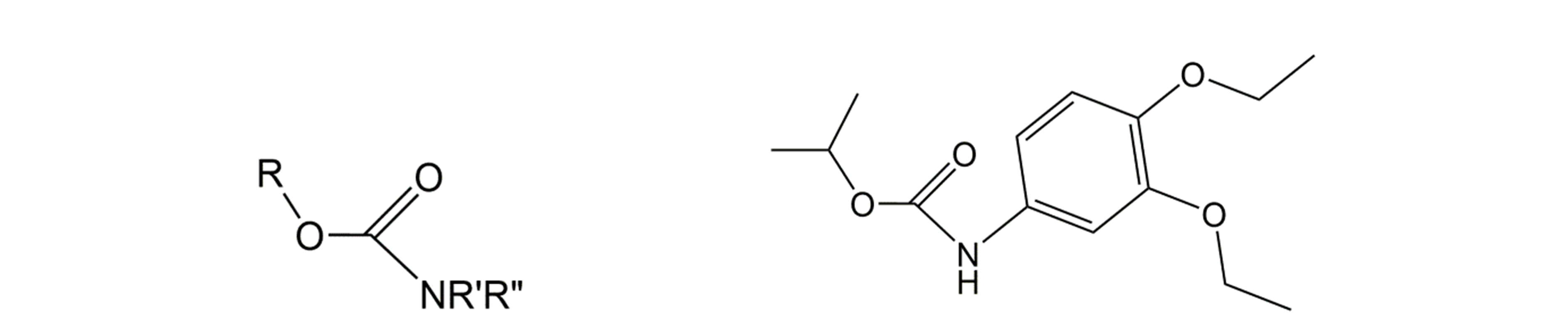
- Carbatos
Cuando los organofosfatos se derivan del ácido fosfórico, los carbamatos se derivan del carbamato (Figura 4). Su modo de acción es similar al de los organofosfatos. El uso de representantes mayores de este grupo, como aldicarb, carbarilo, carbofurano y propoxur, ya no está permitido en Europa, pero el dietofencarb (Figura 4), oxamilo y metomilo siguen en uso.
- Piretroides
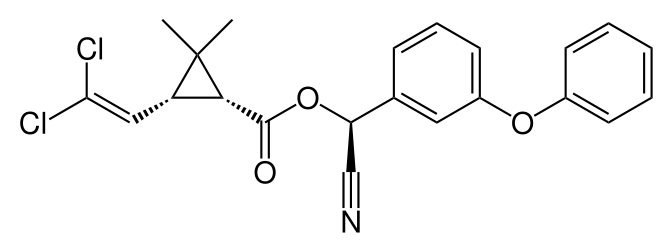
Una serie de pesticidas modernos se derivan de productos naturales. Los piretroides se basan en piretro, un insecticida natural de flores de la margarita persa de ojos de buey, Chrysanthemum roseum. Típico para la estructura molecular de los piretroides es el grupo ciclopropano-carboxilo (la estructura triangular), que está conectado con un grupo aromático a través de un enlace éster (Figura 5). El pireto se degrada rápidamente bajo la influencia de la luz solar. Los piretroides sintéticos, que son mucho más estables y por lo tanto utilizados a gran escala contra muchos insectos diferentes, incluyen cipermetrina (Figura 5), deltametrina, lambda-cihalotrina, fluvalinato y esfenvalerato.
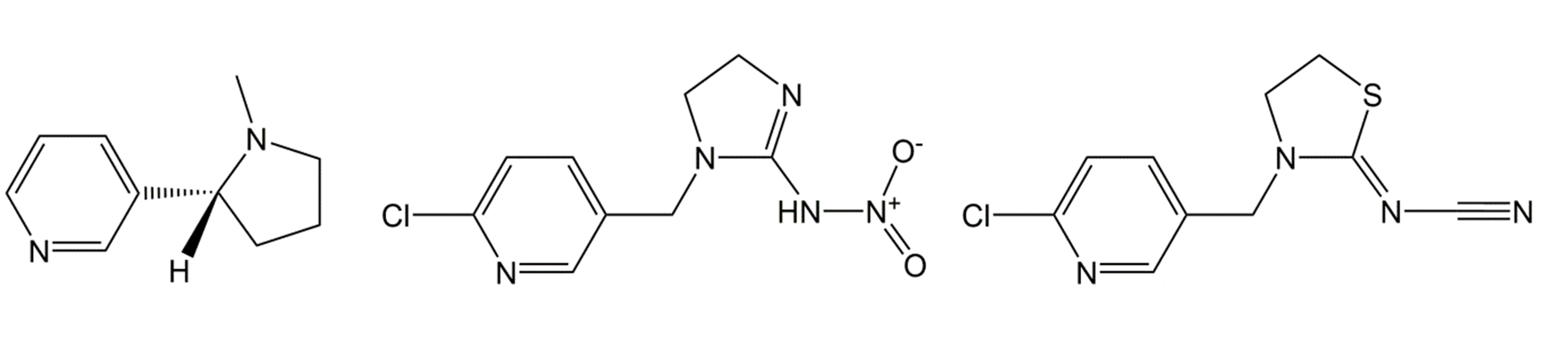
Neonicotinoides
A partir del compuesto natural nicotina, que actúa como insecticida natural contra herbívoros vegetales, pero que fue prohibido como insecticida debido a su alta toxicidad humana, en la década de 1980 se ha desarrollado un nuevo grupo de insecticidas más específicos, los neonicotinoides (Figura 6). Varios neonicotinoides (e.g., imidacloprid, tiametoxam) son sistémicos. Esto significa que son absorbidos por la planta y ejercen su efecto desde el interior de la planta, ya sea sobre el organismo plaga (fungicidas sistémicos o insecticidas) o sobre la propia planta (herbicidas sistémicos). Los neonicotinoides sistémicos se aplican ampliamente como aderezo de semillas en cultivos principales como maíz y girasol. Otros compuestos se utilizan principalmente en aplicaciones de pulverización, por ejemplo en el cultivo de frutos (tiacloprid, acetamiprid, etc.). Si bien los neonicotinoides son más selectivos y por lo tanto preferidos sobre las clases más antiguas de insecticidas como organofosfatos, carbamatos y piretroides, en los últimos años se han vuelto objeto de debate por sus efectos secundarios sobre las abejas melíferas y otros polinizadores.
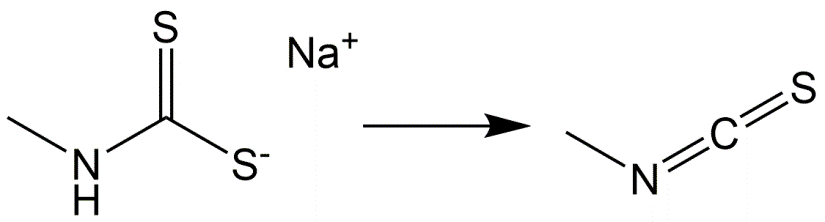
- Isotiocianatos
Los isotiocianatos se utilizaron a gran escala como desinfectante del suelo contra nematodos, hongos y malezas. La gran cantidad de químicos con diferente origen químico pertenecientes a los isotiocianatos tienen en común que forman isotiocianato en el suelo. Un representante de este grupo es el metamo-sodio (Figura 7).
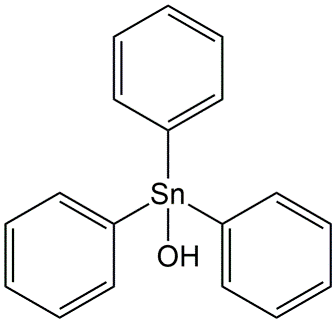
- Compuestos organoestánnicos
Se utilizó hidróxido de fentín (Figura 8) como fungicida contra Phytophthora (causante de la enfermedad de la papa). Se utilizaron compuestos de tributilestaño (TBT) como agente antiincrustante (algicida) en barcos. El TBTC (cloruro de tributilestaño) es extremadamente tóxico para los mariscos, como las ostras, y por esta razón está prohibido en muchos países. El óxido de fenbutatina se utilizó como acaricida contra los ácaros en árboles frutales (cloruro de tributilestaño).
- Rianoides
También indicados como insecticidas de diamida, este grupo incluye compuestos sintéticos químicamente distintos como clorantraniliprol (Figura 9), flubendiamida y ciantraniliprol, que actúan sobre el receptor de rianodina y se utilizan contra insectos masticadores y chupadores.
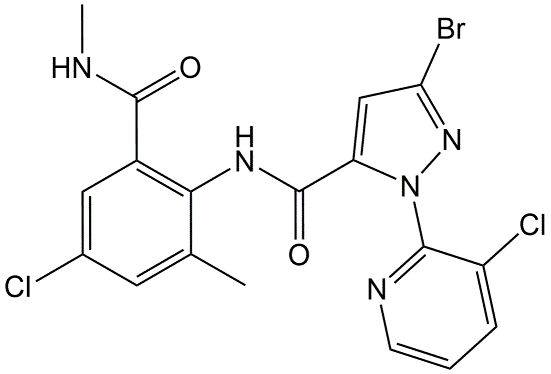
- Ácidos fenoxi acéticos
Los ácidos fenoxiacéticos son herbicidas sistémicos, ejerciendo su acción después de la absorción por la hoja y translocación por toda la planta. Especialmente las plantas con hojas anchas orientadas horizontalmente son sensibles a estos herbicidas. El 2,4-D (Figura 10) es el representante más conocido de este grupo.
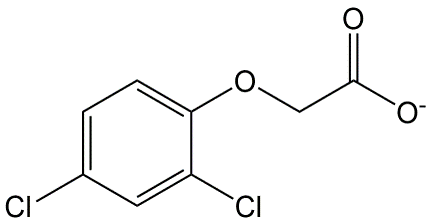
- Triazinas
Las triazinas son compuestos heterocíclicos de nitrógeno, cuya estructura se caracteriza por un anillo aromático en el que tres átomos de carbono han sido reemplazados por átomos de nitrógeno. Las triazinas generalmente se aplican al suelo antes de la germinación de las semillas. El uso de varios compuestos (atrazina, simazina) ha sido prohibido en Europa, mientras que otros como la metribuzina y la terbutilazina (Figura 11) siguen en uso.
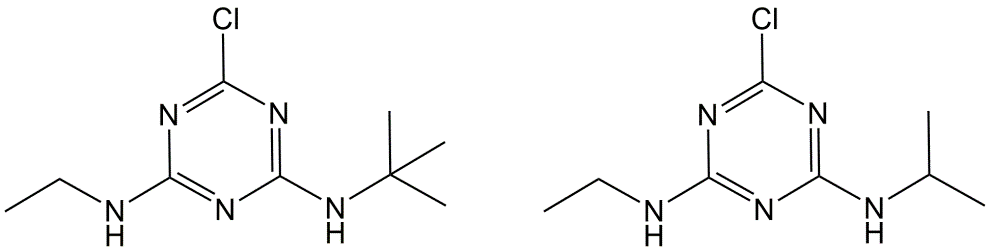
- Bipiridilos
Este grupo contiene los herbicidas diquat y paraquat (Figura 12) los cuales actúan principalmente como herbicidas de contacto. Esto significa que dañan la planta sin ser retomados. En el suelo, se inactivan rápidamente por una fuerte unión a las partículas del suelo. El uso de paraquat ya no está permitido en Europa, pero el diquat sigue en uso.
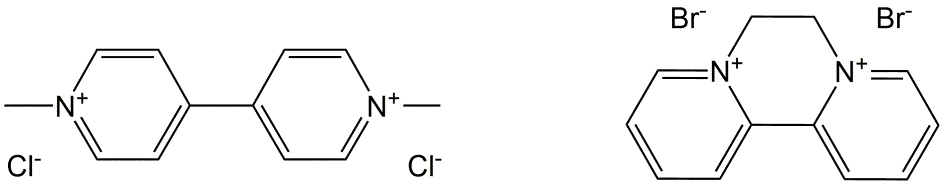
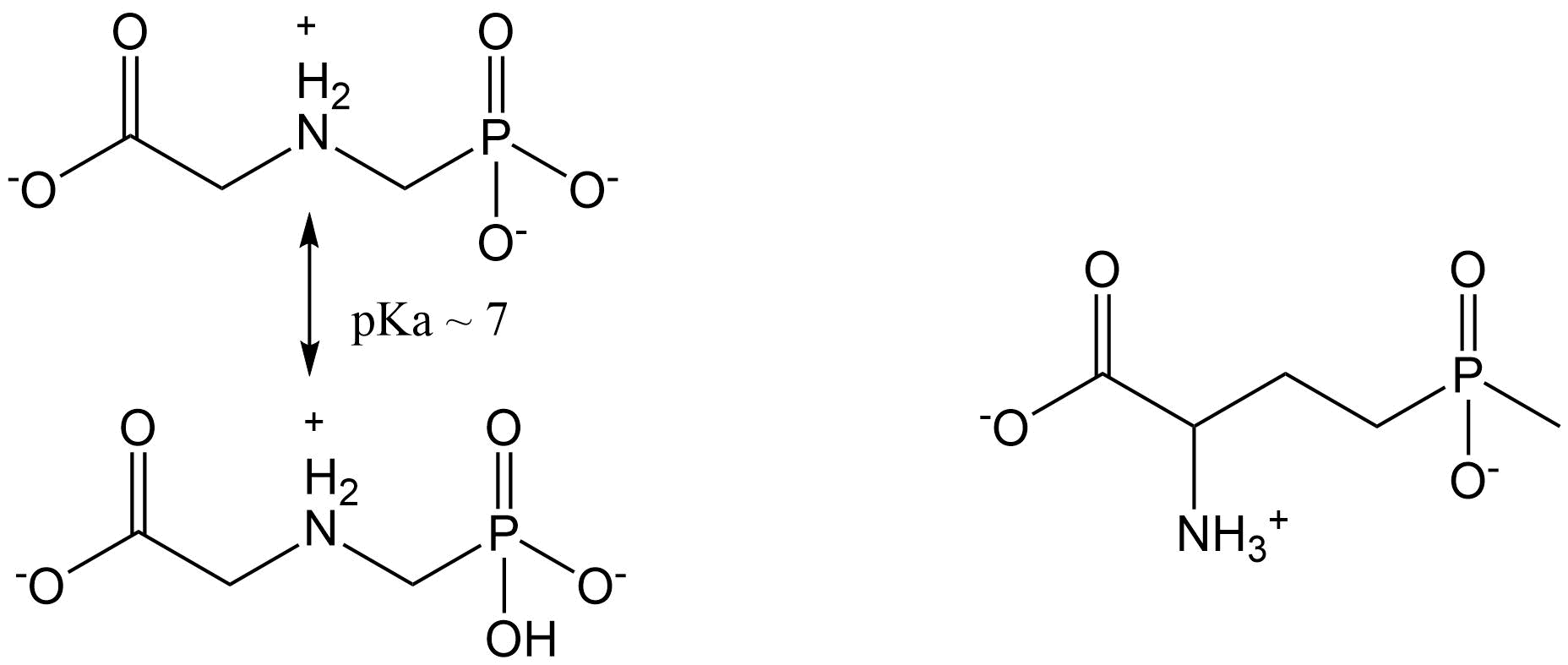
- Glifosato y Glufosinato
Como alternativa a los herbicidas antes mencionados, se desarrollaron glifosato y posteriormente glufosinato. Se trata de herbicidas sistémicos de amplio espectro con una estructura química relativamente simple (Figura 13). Su baja toxicidad para otros organismos provocó que los productores de pesticidas introdujeran cultivos genéticamente modificados (por ejemplo, soja, maíz, colza oleaginosa y algodón) que contienen genes incorporados para la resistencia contra estos herbicidas de amplio espectro. Este tipo de resistencia permite al agricultor utilizar el herbicida sin dañar el cultivo. Por esta razón, los ambientalistas temen un uso irrestricto de estos herbicidas, lo que de hecho es el caso especialmente para el glifosato (más conocido bajo el nombre de formulación Roundup ®).
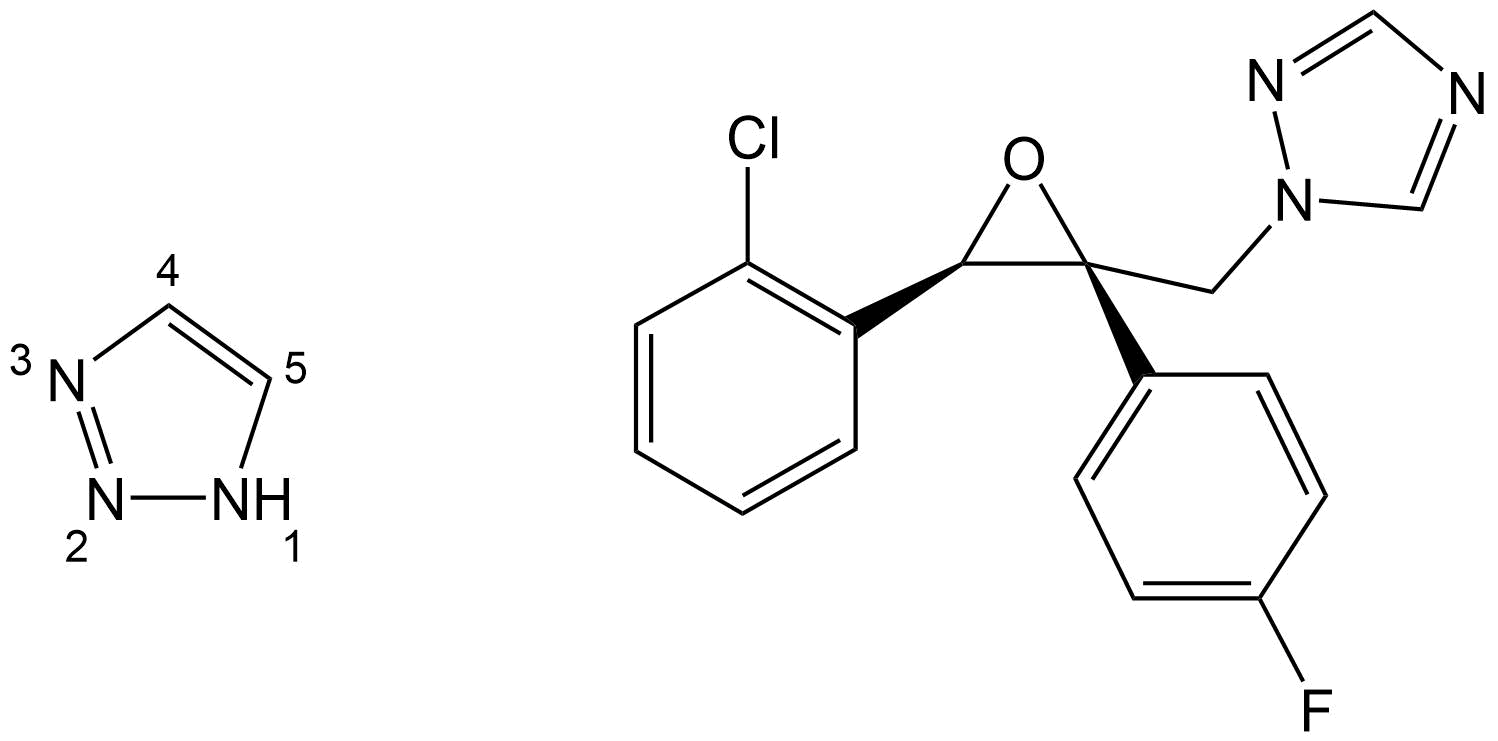
- Triazoles
Varios fungicidas modernos comparten un grupo de triazol (Figura 14). Estos fungicidas han ganado importancia debido a problemas con la resistencia de los hongos frente a otras clases de fungicidas. Los miembros de este grupo son, por ejemplo, epoxiconazol, propiconazol y tebuconazol.
- Plaguicidas biológicos
Los pesticidas biológicos se producen en organismos vivos como metabolitos secundarios para protegerse contra depredadores, herbívoros, parásitos o competencia. Pueden ser altamente efectivos y actuar a bajas concentraciones (alta toxicidad), pero a diferencia de algunos pesticidas sintéticos suelen ser suficientemente biodegradables. Compuestos como el piretro o la estrobilurina se producen dentro de la planta o dentro del hongo y así se protegen contra la fotólisis u otra degradación ambiental. Además, el organismo vivo puede producir cantidades adicionales del metabolito secundario bajo demanda. Sin embargo, cuando se usa como pesticida aplicado como aerosol, la molécula necesita ser modificada para mejorar su estabilidad (por ejemplo contra la fotólisis) para permanecer suficientemente activa durante un período de tiempo suficiente. En consecuencia, los derivados sintéticos de estas moléculas biológicas suelen ser más estables, menos biodegradables. Ejemplos son el insecticida Bt, que contiene una endotoxina altamente tóxica para los insectos producida por la bacteria Bacillus thuringiensis, y avermectinas, moléculas complejas sintetizadas por la bacteria Streptomyces avermitilis. Las avermectinas actúan como insecticidas, acaricidas y tienen propiedades antihelmínticas. En la naturaleza, se han encontrado ocho formas diferentes de avermectina. La ivermectina es una estructura ligeramente modificada que se sintetiza y comercializa comercialmente. Otros compuestos que pertenecen a este grupo son la milbemectina y la emamectina.
Las plantas genéticamente modificadas que contienen un gen que codifica la toxina producida por la bacteria Bacillus thuringiensis (o Bt) son otro ejemplo de modificación genética que se aplica en la agricultura y producen cultivos resistentes a insectos.
Referencias:
Base de datos de plaguicidas
Los pesticidas sistémicos son fácilmente absorbidos por las plantas y distribuidos internamente en todos los tejidos de las plantas. ¿Qué espera con respecto a la solubilidad en agua de los plaguicidas sistémicos?
- Muy Bajo
- Muy alto
¿Por qué los insecticidas sistémicos se aplican como aderezo de semillas, tan dosificados en el suelo, peligrosos para las abejas melíferas y otros polinizadores?
Un pesticida con una sustancia activa que apenas es soluble en agua se introduce al mercado en una formulación comercial. ¿Qué componentes deben estar presentes en la formulación para permitir la aplicación homogénea del pesticida por pulverización?
Nombrar tres grupos importantes de insecticidas y mencionar una propiedad o característica típica.
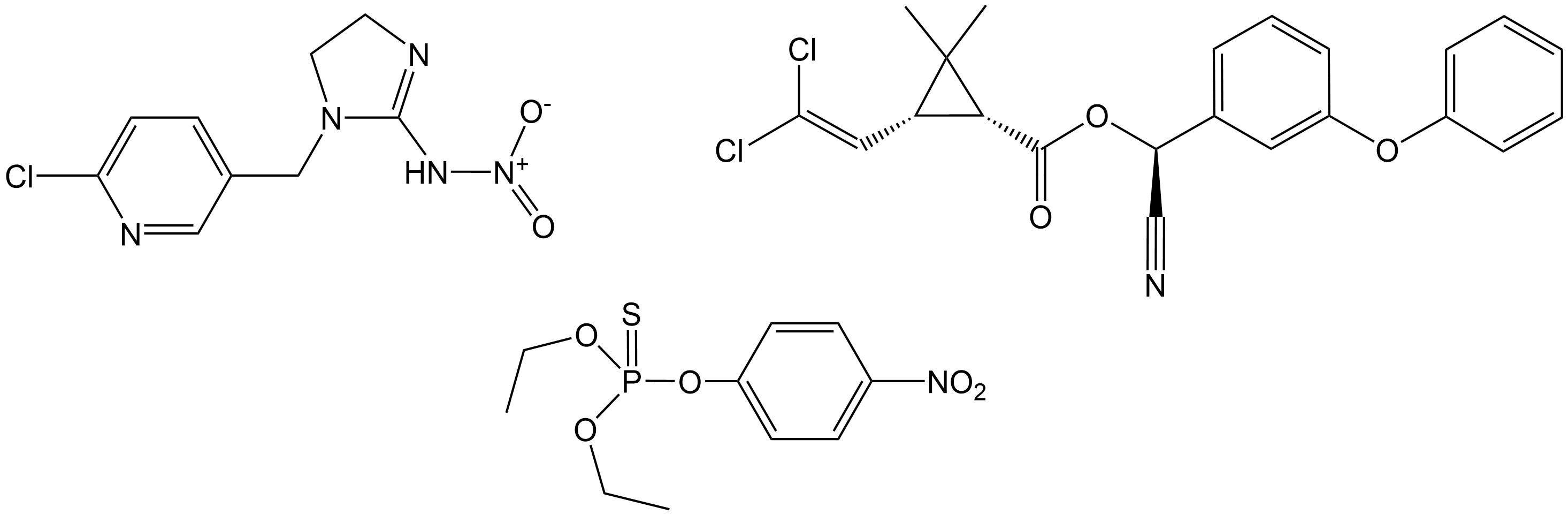
- Las figuras muestran tres estructuras químicas. Indicar cuál de estos productos químicos es
- Un organofosfato (círculo)
- Un piretroide (triángel)
- Un neonicotinoide (cuadrado)
2.3.2. Biocidas
Autor: Thomas Wagner
Críticos: Steven Droge, Kevin Thomas
Objetivos de aprendizaje:
Deberías ser capaz de:
- Comprender el propósito del uso de biocidas
- Distinguir diferentes grupos de biocidas
- Comprender la legislación relativa a la producción y uso de biocidas
- Comprender el impacto potencial de los biocidas en los ecosistemas
Palabras clave: Biocidas, tipos de productos, Regulación de Productos Biocidas (BPR), impacto ambiental
Introducción
La legislación europea describe a un biocida como “sustancia química o microorganismo destinado a destruir, disuadir, inofensivo o ejercer un efecto controlador sobre cualquier organismo dañino por medios químicos o biológicos”. La Agencia de Protección Ambiental de Estados Unidos (EPA), una agencia independiente del gobierno federal estadounidense para proteger el medio ambiente, define a los biocidas como “un grupo diverso de sustancias venenosas que incluyen conservantes, insecticidas, desinfectantes y pesticidas utilizados para el control de organismos que son perjudiciales para la salud humana o animal o que causen daños a productos naturales o manufacturados”. La definición de la EPA incluye los plaguicidas (Capítulo 2.3.1). En la literatura científica y no científica, la distinción entre biocidas, pesticidas y productos fitosanitarios suele ser vaga.
Los biocidas se utilizan a nuestro alrededor:
- La pasta de dientes que usaste esta mañana contiene biocidas para conservar la pasta de dientes
- El agua que usaste para enjuagarte la boca está preparada con biocidas para la desinfección
- La ropa que llevas puesta está impregnada de biocidas para evitar olores
- La comida que comiste en el desayuno podría haber contenido biocidas para conservar la comida
- Los materiales de construcción a su alrededor tienen recubrimientos superficiales que contienen biocidas para evitar la degradación biológica del material
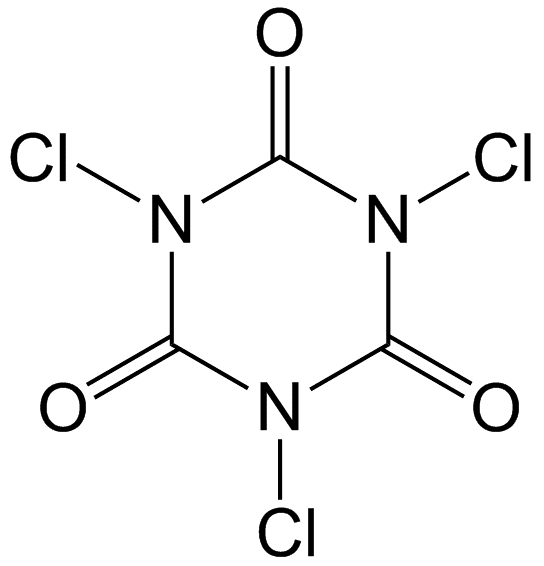
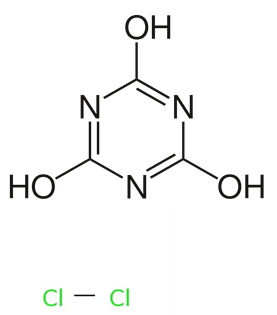
Un biocida contiene una 'sustancia activa', que es la sustancia química que es tóxica para su organismo objetivo, y a menudo contiene 'cosustancias no activas', lo que podría ayudar a alcanzar los parámetros deseados del producto, como viscosidad, pH, color, olor o aumentar su manejo o efectividad. La combinación de sustancias activas y sustancias no activas juntas constituye el 'biocida'. Un ejemplo de un biocida bien conocido es TriChlor, que contiene cloro de sustancia activa que se utiliza para desinfectar piscinas. Debido a que no es práctico almacenar gas cloro para el tratamiento de piscinas, se agregan tabletas TriChlor al agua de la piscina. El tricloro es ácido tricloroisocianúrico (Figura 1). Cuando se disuelven en agua, los átomos de Cl son reemplazados por átomos de H, formando cloro (Cl -) y ácido cianúrico (Figura 2). El cloro libre es capaz de desinfectar la piscina.
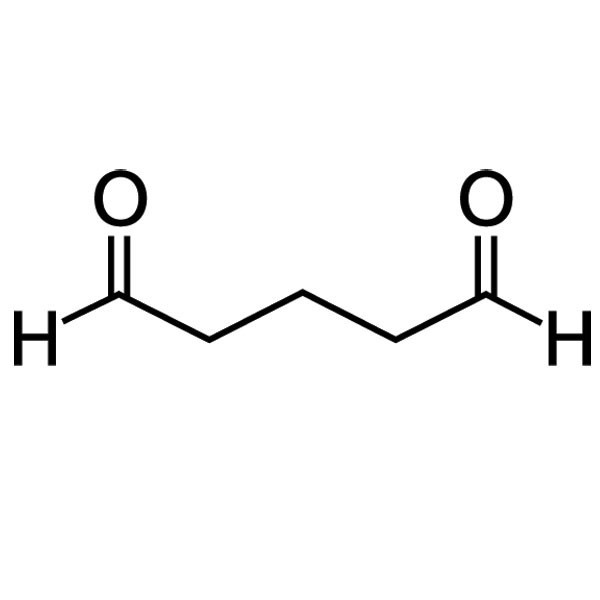
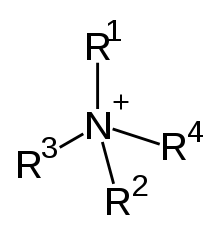
Un biocida también puede contener múltiples sustancias biológicamente activas para mejorar su efectividad, como AQUCAR™ 742 producido por DuPont. Contiene glutaraldehído (Figura 3) y compuestos de amonio cuaternario (Figura 4) que tienen un efecto tóxico sinérgico sobre los microorganismos que están presentes en los yacimientos petrolíferos y podrían formar biopelículas en los ductos.
Tipos de productos
Los biocidas son clasificados en 22 tipos de producto diferentes por la Agencia Europea de Sustancias Químicas (ECHA) (Cuadro 1). Es posible que una sustancia activa pueda clasificarse en más de un tipo de producto.
Cuadro 1. La clasificación de biocidas en 22 tipos de productos (www.echa.europe.eu)
|
Grupo principal 1: Desinfectantes y biocidas generales |
|
Tipo de producto 1 - Biocidas para la higiene humana |
|
Tipo de producto 2 - Área privada y área de salud pública desinfectantes y otros biocidas |
|
Tipo de producto 3 - Biocidas de higiene veterinaria |
|
Tipo de producto 4 - Desinfectantes para alimentos y piensos |
|
Tipo de producto 5 - Desinfectantes de agua potable |
|
Grupo principal 2: Conservantes |
|
Tipo de producto 6 - Conservantes en lata |
|
Tipo de producto 7 - Conservantes de película |
|
Tipo de producto 8 - Conservantes para madera |
|
Tipo de producto 9 - Conservantes de fibra, cuero, caucho y materiales poliméricos |
|
Tipo de producto 10 - Conservantes de albañ |
|
Tipo de producto 11 - Conservantes para sistemas de enfriamiento líquido y procesamiento |
|
Tipo de producto 12 - Slimicides |
|
Tipo de producto 13 - Conservantes fluidos para la metalmecánica |
|
Grupo principal 3: Control de plagas |
|
Tipo de producto 14 - Raticidas |
|
Tipo de producto 15 - Avidicides |
|
Tipo de producto 16 - Molusquicidas |
|
Tipo de producto 17 - Piscicidas |
|
Tipo de producto 18 - Insecticidas, acaricidas y productos para el control de otros artrópodos |
|
Tipo de producto 19 - Repelentes y atrayentes |
|
Tipo de producto 20 - Control de otros vertebrados |
|
Grupo principal 4: Otros biocidas |
|
Tipo de producto 21 - Productos antiincrustantes |
|
Tipo de producto 22 - Fluidos de embalsamamiento y taxidermistas |
Legislación
En Europa, los biocidas están autorizados para su producción y uso por el Reglamento de Productos Biocidas (BPR, Reglamento (UE) 528/2012) de la ECHA. El BPR 'tiene como objetivo mejorar el funcionamiento del mercado de biocidas en la UE, al tiempo que garantiza un alto nivel de protección para los seres humanos y el medio ambiente'. (echa.europe.eu/legislación). Se trata de un marco regulatorio alternativo al de los productos fitosanitarios, gestionados por la Autoridad Europea de Seguridad Alimentaria (EFSA). Todos los biocidas pasan por un amplio proceso de autorización antes de ser permitidos en el mercado. La valoración de un nuevo activo inicia con la evaluación de un producto por parte de las autoridades de un estado miembro de la ECHA, tras lo cual el Comité de Biocidas de la ECHA forma dictamen. La Comisión Europea toma entonces la decisión de aprobar o rechazar la nueva sustancia activa con base en el dictamen de la ECHA. Esta aprobación se otorga por un máximo de 10 años y debe renovarse una vez que llegue al final del periodo de registro. El BPR tiene criterios estrictos para nuevas sustancias activas, y cumplir con los siguientes 'criterios de exclusión' dará como resultado que la nueva sustancia activa no sea aprobada:
- Carcinógenos, mutágenos y sustancias reprotóxicas categorías 1A o 1B según regulación CLP
- Disruptores endocrinos
- Sustancias persistentes, bioacumulativas y tóxicas (PBT)
- Sustancias muy persistentes y muy bioacumulativas (VPb)
En casos muy especiales, se permitirán nuevas sustancias activas en el mercado al cumplir con estos criterios de exclusión, si son importantes para la salud pública y el interés público y no hay alternativas disponibles. Para disminuir la presión sobre la salud pública y el medio ambiente, también existe una lista de candidatos para que las sustancias activas sean sustituidas por sustancias activas menos nocivas cuando las sustancias activas antiguas cumplan con los siguientes criterios:
- Cumple con uno de los criterios de exclusión
- Se clasifica como sensibilizador respiratorio
- Sus valores toxicológicos de referencia son significativamente menores que los de la mayoría de las sustancias activas aprobadas para el mismo tipo de producto y uso
- Cumple con dos de los criterios para ser considerado como PBT
- Causa preocupación por la salud humana o animal y por el medio ambiente incluso con medidas de manejo de riesgos muy restrictivas
- Contiene una proporción significativa de isómeros o impurezas no activos
El impacto de la liberación ambiental
La liberación de biocidas en el medio ambiente puede tener enormes consecuencias, ya que estos productos están diseñados para causar daños a los organismos vivos. Un ejemplo clásico es la liberación de tributilestaño desde astilleros, puertos y en rutas de navegación desde la pintura antiincrustante en los cascos de los barcos (De Mora, 1996). El tributilestaño se utilizó en la pintura antiincrustante a partir de la década de 1950 para evitar que los microorganismos se asentaran en los cascos de los barcos, lo que aumentaría los costos de combustible y los costos de reparación. Sin embargo, la liberación de tributilestaño de la pintura resultó en un efecto tóxico en organismos en el fondo de la cadena alimentaria, como algas e invertebrados. El tributilestaño luego se biomagnificó en la red alimentaria, afectando de esta manera a depredadores más grandes, como delfines y nutrias marinas. Eventualmente, el tributilestaño ingresó a la dieta de los humanos. La primera legislación sobre el uso del tributilestaño para buques se remonta a la década de 1980, pero no fue sino hasta el Convenio de Rotterdam de 2008 que se prohibió el uso completo del tributilestaño como biocida activo en pinturas antiincrustantes. Los biocidas también pueden tener un efecto sobre la capacidad del medio ambiente para hacer frente a la contaminación. Los microorganismos se encargan de limpiar las áreas contaminadas mediante el uso del contaminante como fuente de alimento. McLaughlin et al. (2016) estudiaron el efecto de la liberación del biocida glutaraldehído en el agua derramada de la fracturación hidráulica sobre la actividad microbiana y encontraron que la actividad microbiana se veía obstaculizada por el biocida glutaraldehído. De ahí que debido al biocida, el ambiente no fue o más lento capaz de volver a su estado original.
Referencias
De Mora, S.J. (1996). Tributilestaño: estudio de caso de un contaminante ambiental, Vol. 8, Cambridge Univ. Prensa
McLaughlin, M.C., Borch, T., Blotevogel, J. (2016). Derrames de productos químicos de fracturación hidráulica en la capa superior del suelo agrícola: Biodegradación, sorción e interacciones cocontaminantes, Ciencia y Tecnología Ambiental 50, 6071-6078
Explicar la diferencia entre una sustancia activa y un biocida.
¿Cuál es el propósito del uso de cosustancias no activas en un biocida?
Un barco transporta plátanos de Costa Rica a los Países Bajos. Mencione 5 tipos de productos biocidas que podrían usarse en este barco, y su propósito.
Mencionar 3 posibles formas en las que el medio ambiente puede ser dañado como resultado de la liberación (accidental) de biocidas en la práctica diaria común.
2.3.3. Farmacéutica y Veterinaria
(borrador)
Autor: Thomas ter Laak
Crítico: John Parsons, Steven Droge
Objetivos de inclinación:
Deberías ser capaz de:
Palabras clave: emisión, inmisión, tratamiento de aguas residuales, tratamiento de enfermedades
Introducción
Los productos farmacéuticos son consumidos por humanos (productos farmacéuticos humanos) y administrados a animales (productos farmacéuticos veterinarios).
Los principios activos utilizados en medicina humana y veterinaria se superponen parcialmente, sin embargo, la mayor fracción de sustancias farmacéuticas activas en uso se restringe al consumo humano. En la práctica veterinaria la mayoría de los productos farmacéuticos aplicados son antibióticos y agentes antiparasitarios, mientras que en la medicina humana, los productos farmacéuticos para tratar por ejemplo la diabetes, el dolor, las enfermedades cardiovasculares, los trastornos autoinmunes y los trastornos neurológicos constituyen una porción mucho mayor de los productos farmacéuticos en uso. El consumo farmacéutico mundial ha aumentado en el último siglo (aquí se resumen varios números asombrosos). Se espera que el consumo aumente aún más debido a un acceso más amplio a los productos farmacéuticos en los países en desarrollo. Adicionalmente, las tendencias demográficas como el envejecimiento de las poblaciones que a menudo se observan en los países desarrollados también pueden llevar a un mayor consumo de productos farmacéuticos, ya que las generaciones mayores generalmente consumen más productos farmacéuticos que las generaciones más jóvenes (van der Aa et al., 2011). El uso generalizado y creciente y su actividad biológica los hace relevantes para la investigación ambiental. A continuación se ofrece una visión general sobre la emisión, ocurrencia y destino (modelado) de los productos farmacéuticos en el medio ambiente.
Farmacéuticos en el medio ambiente
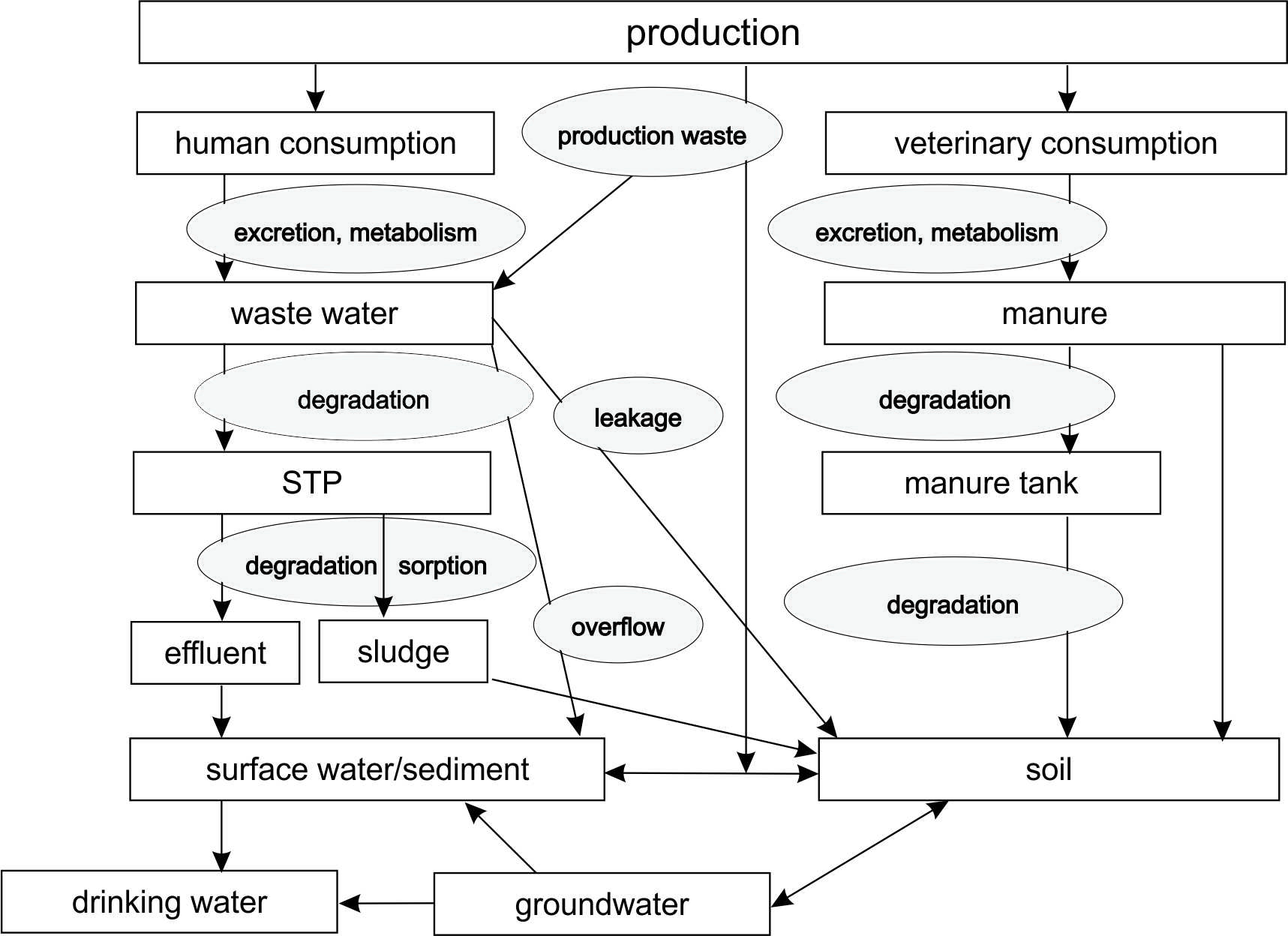
Los productos farmacéuticos pueden ingresar al medio ambiente a través de diversas rutas. La Figura 1 da una visión general de las rutas de emisión de productos farmacéuticos al medio ambiente. Los productos farmacéuticos son producidos, transportados a los usuarios (humanos y/o animales), excretados parcialmente por los usuarios vía orina y heces. Para los humanos, los excrementos son transportados a plantas de tratamiento de aguas residuales, fosas sépticas o emitidos directamente al suelo o aguas superficiales. Para los animales, y especialmente el ganado, el estiércol contiene residuos de los productos farmacéuticos. Estos productos farmacéuticos terminan en el ambiente cuando los animales pastan afuera o cuando el estiércol recolectado centralmente se aplica como fertilizante en tierras cultivables. Al igual que el consumo farmacéutico, el metabolismo en el usuario (un ser humano o un animal), el tratamiento y posterior aplicación de aguas residuales comunales y estiércol varía. Posteriormente, las emisiones también varían entre productos farmacéuticos, países y ubicaciones.
Las concentraciones de productos farmacéuticos en el ambiente varían fuertemente, en la Figura 2 se muestran rangos de concentración de productos farmacéuticos y algunos de sus productos de transformación en el río Mosa y algunos afluentes.
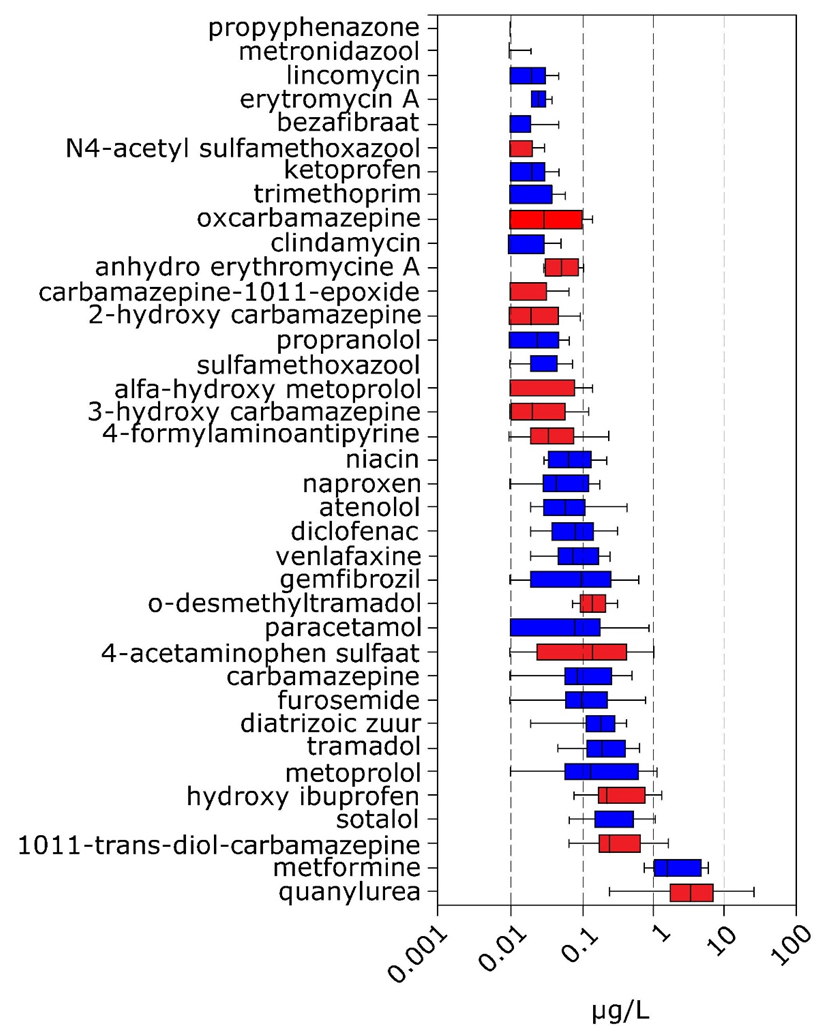
Propiedades de los productos farmacéuticos y su comportamiento y destino en el medio ambiente
Los productos farmacéuticos en uso se desarrollan para una amplia gama de enfermedades y tratamientos terapéuticos. Por lo tanto, las estructuras químicas de estas sustancias también son muy diversas, considerando su tamaño, presencia estructural de átomos específicos y propiedades fisicoquímicas como su hidrofobicidad, solubilidad acuosa e ionización bajo valores de pH ambientalmente relevantes, como se muestra para algunos ejemplos en la Figura 3.
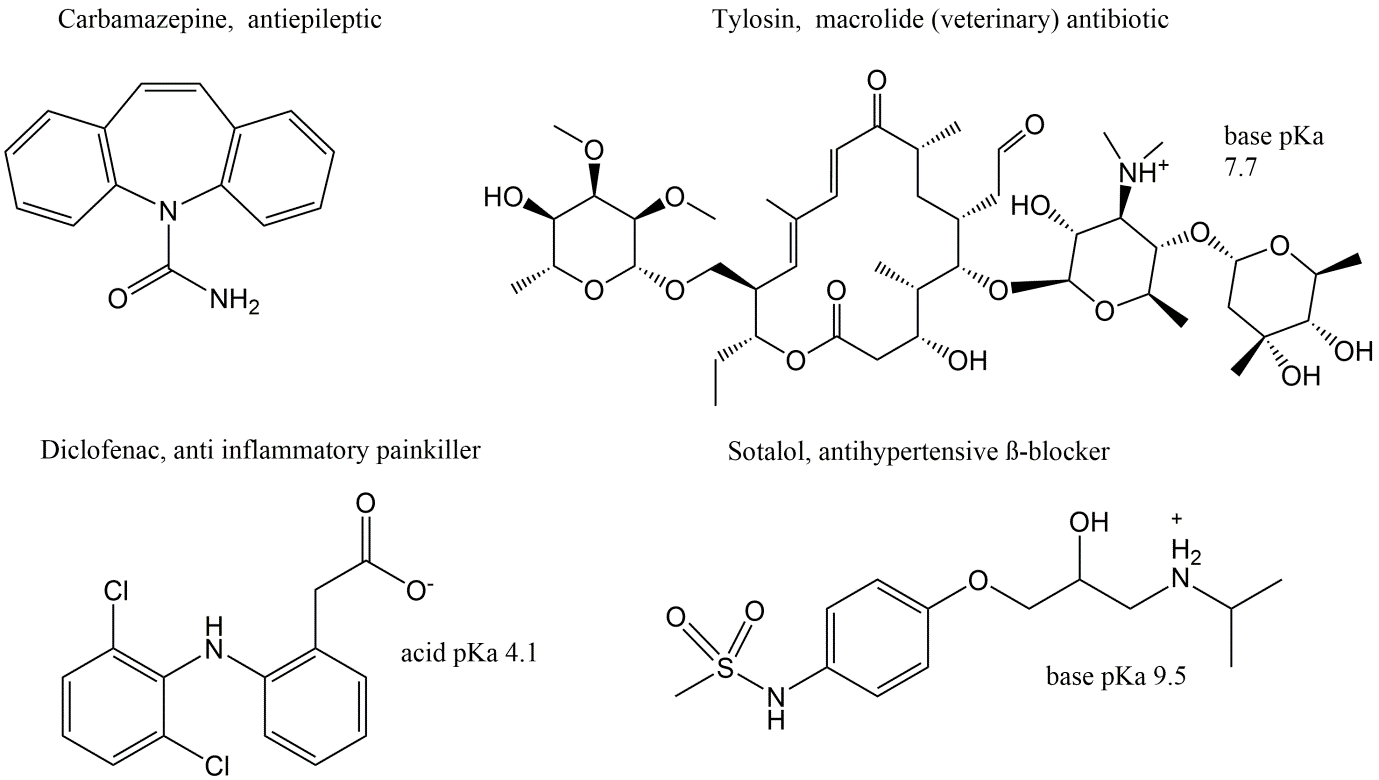
Como consecuencia de su diversidad estructural, su distribución ambiental y destino también es muy variable. Esto dificulta generalizar el comportamiento ambiental y el destino de los productos farmacéuticos. Sin embargo, los productos farmacéuticos tienen generalmente ciertas propiedades en común:
Estas tres propiedades genéricas también las hacen de relevancia ambiental ya que:
Ocurrencia y modelización de productos farmacéuticos humanos y veterinarios en el medio ambiente
Los productos farmacéuticos han sido estudiados en el medio ambiente desde la década de 1990. La mayoría de los estudios se han realizado en aguas superficiales, pero también se estudiaron aguas residuales (efluentes), agua subterránea, agua potable, estiércol, suelo y sedimentos. Se han observado productos farmacéuticos en todas estas matrices en concentraciones que generalmente varían de µg/L a niveles sub ng/L (Aus der Beek et al., 2016, Monteiro y Boxall, 2010). Diversos estudios han relacionado las cargas ambientales y las concentraciones relacionadas con los datos de consumo humano. Básicamente tales -los llamados- estudios de balance de masa o equilibrio de emisión-emisión funcionan de acuerdo con el siguiente principio:
Modelado de productos farmacéuticos en el medio ambiente
Dado que la aplicación de los productos farmacéuticos humanos, el consumo, está relativamente bien documentado. Las concentraciones ambientales pueden estar relacionadas con el consumo. Esta predicción funciona mejor para los productos farmacéuticos más persistentes, ya que las variaciones en los factores de pérdida son marginales para estos productos farmacéuticos. Cuando los factores de pérdida aumentan, generalmente también se vuelven más variables, a través de las variaciones estacionales en el uso, así como la variación en la pérdida durante el tratamiento de aguas residuales y los procesos de pérdida en los ríos receptores, respectivamente. Esto hace que las cargas y concentraciones de productos farmacéuticos más degradables sean más difíciles de predecir (Ter Laak et al., 2010).
Las cargas en un sistema fluvial particular (como un afluente del río Mosa en el siguiente ejemplo) se pueden predecir con un modelo muy simplificado. Aquí el consumo farmacéutico durante un periodo seleccionado se multiplica por el factor de los productos farmacéuticos seleccionados que son excretados sin cambios por el cuerpo humano (que van de 0 a 1) y la fracción que es capaz de pasar por la planta de tratamiento de aguas residuales (EDAR) (que van de 0 a 1):
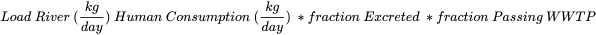
Cuando esto se relaciona con las concentraciones medidas reales y las cargas calculadas a partir de estos números, se puede trazar la correlación entre las cargas predichas y las medidas. Diversos estudios han demostrado que las cargas ambientales pueden predecirse dentro de un factor de 3 para los productos farmacéuticos más comúnmente observados (Ter Laak et al., 2014; Ter Laak et al., 2010; Alder et al., 2010; Oosterhuis et al., 2013).
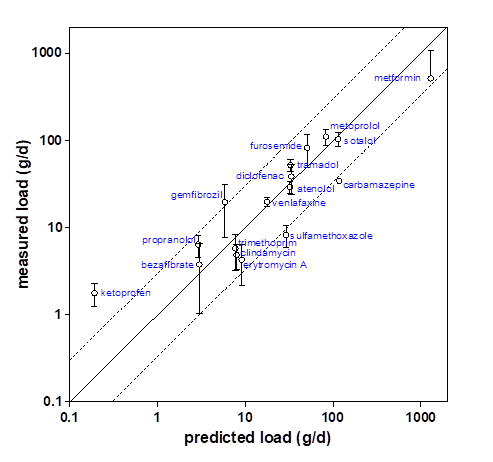
Para los productos farmacéuticos veterinarios este llamado 'equilibrio de emisión' es más difícil debido a una serie de razones:
En cierto modo las emisiones y destino de los productos farmacéuticos veterinarios son similares a las emisiones de pesticidas utilizados en la agricultura, pero luego con una comprensión mucho más pobre sobre las cargas que ingresan al sistema y el destino relacionado con las diversas rutas de emisión y emisiones en combinación con una matriz compleja (orina, estiércol de heces) (Guo et al., 2016). Como consecuencia, los estudios de destino ambiental de los productos farmacéuticos veterinarios a menudo describen casos específicos, o cubren estudios de laboratorio para desentrañar aspectos específicos del destino ambiental de estos productos farmacéuticos (Kaczala y Blum, 2016; Kummerer, 2009).
Observaciones finales
Los productos farmacéuticos se encuentran comúnmente en los compartimentos ambientales como el agua superficial, el suelo, los sedimentos y las aguas subterráneas (Williams et al., 2016). Los productos farmacéuticos consisten en uno o múltiples ingredientes activos que tienen una actividad biológica específica. La aplicación terapéutica y los mecanismos farmacológicos proporcionan información valiosa para evaluar el peligro ambiental de estos químicos. Sus propiedades fisicoquímicas son de mayor relevancia para la evaluación del destino ambiental y la exposición. La ocurrencia en el ambiente y la actividad biológica de este grupo de contaminantes los hace relevantes en la ciencia ambiental.
Referencias
Alder, A.C., Schaffner, C., Majewsky, M., Klasmeier, J., Fenner, K. (2010) Fate of [beta] -blocker human pharmaceuticals in surface water: Comparación de concentraciones medidas y simuladas en la cuenca del Valle de Glatt, Suiza. Investigación del Agua 44, 936-948
Aus der Beek, T., Weber, F., Bergmann, A., Hickmann, S., Ebert, I., Hein, A., Küster, A. (2016) Farmacéuticos en el Medio Ambiente-ocurrencias y perspectivas globales. Medio ambiente. Toxicol. Chem. 35, 823-835.
Guo, X.Y., Hao, L.J., Qiu, P.Z., Chen, R., Xu, J., Kong, X.J., Shan, Z.J., Wang, N. (2016) Características de la contaminación de 23 antibióticos veterinarios en estiércol de ganado y suelos modificados con estiércol en la provincia de Jiangsu, China. J. Environ. Sci. Salud Parte B Pestic. Contamin de alimentos. Agric. Desechos 51 (6), 383-392
Kaczala, F., Blum, S.E. (2016) La ocurrencia de los productos farmacéuticos veterinarios en el medio ambiente: Una revisión. Curr. Anal. Chem., 12 (3), 169-182
Kümmerer, K. (2009) La presencia de productos farmacéuticos en el medio ambiente debido al uso humano - conocimiento presente y retos futuros. J. Environ. Administrar., 90 (8), 2354-2366
Monteiro, S.C., Boxall, A.B.A. (2010) Ocurrencia y destino de los productos farmacéuticos humanos en el medio ambiente. Rev. Environ. Contam. Toxicol., 202, 53-154.
Oosterhuis, M., Sacher, F., ter Laak, T.L. (2013) Predicción de los niveles de concentración de metformina y otros productos farmacéuticos de alto consumo en aguas residuales y aguas superficiales regionales con base en datos de ventas. Sci. Total Environ. 442, 380-388
Ter Laak, T.L., Van der Aa, M., Houtman, C.J., Stoks, P.G., Van Wezel, A.P. (2010) Relacionar las concentraciones ambientales de los productos farmacéuticos con el consumo: Un enfoque de balance de masas para el río Rin. Medio ambiente. Pasante 36, 403-409
Ter Laak, T.L., Kooij, P.J.F., Tolkamp, H., Hofman, J. (2014) Diferentes composiciones de productos farmacéuticos en los ríos holandés y belga explicadas por los patrones de consumo y la eficiencia del tratamiento. Medio ambiente. Sci. Contaminar. Res. 21, 12843-12855
Van der Aa, N.G.F.M., Kommer, G.J., van Montfoort, J.E. y Versteegh, J.F.M. (2011) Proyecciones demográficas del consumo farmacéutico futuro en los Países Bajos. Ciencia y Tecnología del Agua, 825-832.
Williams, M., Backhaus, T., Bowe, C., Choi, K., Connors, K., Hickmann, S., Hunter, W., Kookana, R., Marfil-Vega, R., Verslycke, T. (2016) Farmacéuticos en el medio ambiente: Una introducción al número especial de ET&C. Medio ambiente. Toxicol. Chem. 35, 763-766.
Nombra tres razones por las que los productos farmacéuticos son contaminantes ambientales relevantes?
¿Por qué es más fácil modelar los productos farmacéuticos humanos en el medio ambiente que los veterinarios?
El ibuprofeno (antiinflamatorio) se descarga con las aguas residuales al río. Se conoce la siguiente información sobre el uso y destino de esta droga.
- consumo por cada 1000 habitantes de 1 g/d
- excreción por humanos 10%
- remoción por STP 68%
¿Cuánto iboprufeno se descarga potencialmente al río en g/d?
2.3.4. Drogas de abuso
Autor: Pim de Voogt
Crítico: John Parsons, Félix Hernández
Objetivos de inclinación:
Deberías ser capaz de:
- distinguir entre drogas lícitas e ilícitas
- conocer qué fuentes hacen que las drogas ilícitas aparezcan en el medio ambiente
- entender qué es la epidemiología basada en aguas residuales
Palabras clave: Cocaína, éxtasis, velocidad, cannabis, análisis de aguas residuales
Introducción
Desde poco más de una década, las drogas de abuso (DOA) y sus productos de degradación han sido reconocidos como contaminantes ambientales emergentes. Se encuentran entre el creciente número de químicos que se pueden observar en el medio acuático.
Los residuos de una gran parte de los químicos utilizados en los hogares y la vida diaria terminan en nuestros sistemas de alcantarillado. Entre los muchos químicos se encuentran los agentes de limpieza y detergentes, cosméticos, aditivos alimentarios y contaminantes, pesticidas, productos farmacéuticos, y seguramente también drogas ilícitas. Una vez en el alcantarillado, son transportados a plantas de tratamiento de aguas residuales (EDAR), donde pueden eliminarse por degradación o adsorción a lodos, o terminar en el efluente de la planta cuando la remoción es incompleta.
El consumo tanto de productos farmacéuticos como de DOA ha aumentado sustancialmente en las últimas dos décadas como resultado de varios factores, entre ellos el envejecimiento de la población, la medicalización de la sociedad y los cambios sociales en el estilo de vida. Como resultado, las cargas en aguas residuales de los medicamentos y sus productos de transformación formados en el cuerpo después del consumo han aumentado de manera constante. Más recientemente, se ha observado que los desechos químicos de los sitios de producción de drogas ilícitas se están descargando ocasionalmente a los sistemas de alcantarillado, lo que aumenta drásticamente las cargas de productos químicos de síntesis de drogas ilícitas y productos finales transportados a las EDAR. Como las EDAR no están diseñadas para eliminar drogas, una fracción sustancial de las cargas puede terminar en recibir aguas y, por lo tanto, representar una amenaza para la salud humana y de los ecosistemas.
Drogas de Abuso (DOA)
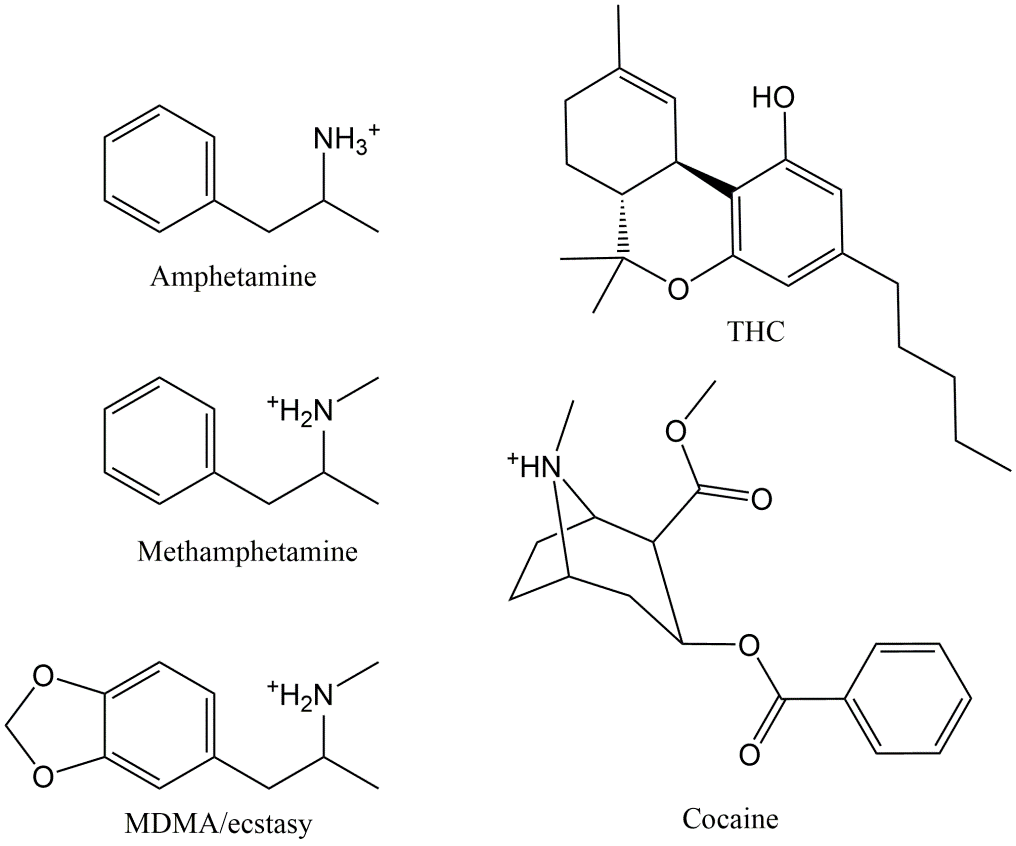
Las drogas ilícitas más utilizadas en Europa son el THC (cannabis), la cocaína, el MDMA (éxtasis) y las anfetaminas. La estructura de estos fármacos se da en la Figura 1. Otros DOA importantes incluyen los opioides como heroína y fentanilo, GHB, Khat y LSD.
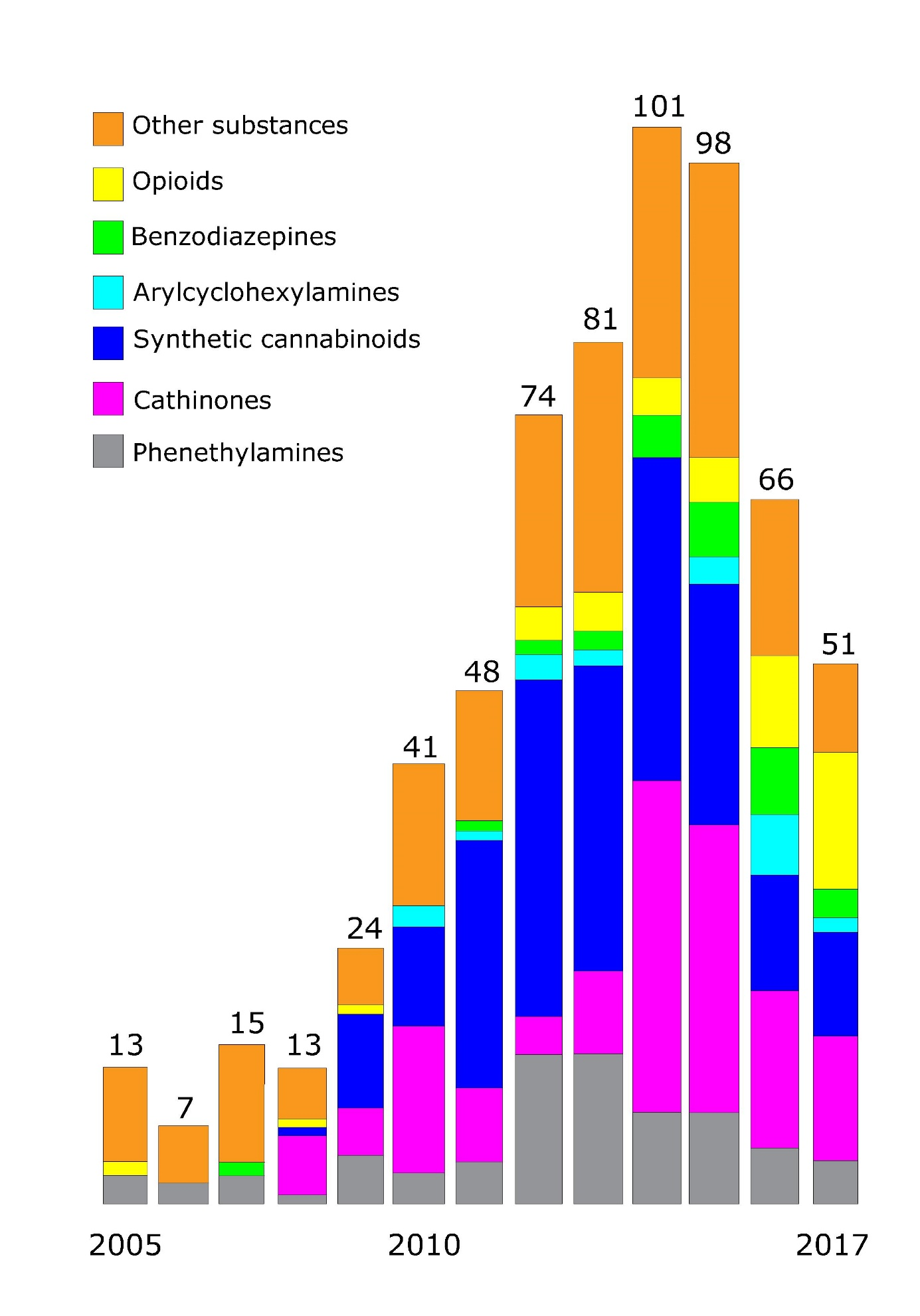
Las drogas de abuso están controladas por la legislación, en los Países Bajos por la Ley del Opio. La Ley del Opio engloba dos listas de sustancias. Los químicos de la lista uno se llaman drogas duras mientras que los químicos de la Lista II se conocen como drogas blandas. Algunos narcóticos también se están utilizando con fines medicinales, por ejemplo, ketamina, diazepinas y uno de los isómeros de la anfetamina. Las nuevas sustancias psicoactivas (NPS), también conocidas como drogas de diseño o máximos legales (porque aún no están controladas ya que no figuran en las listas de la Ley del Opio), se sintetizan cada año y se ponen a disposición en el mercado en números altos (ver Figura 2).
Epidemiología basada en aguas residuales
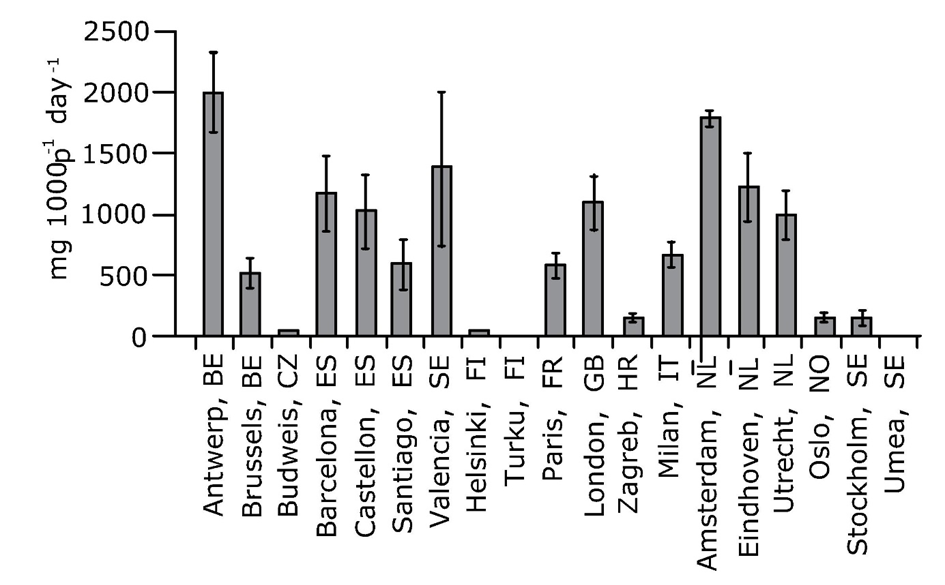
Los sistemas centrales de alcantarillado recolectan y albergan aguas residuales de las actividades de limpieza doméstica y cuidado personal así como productos de excreción resultantes del consumo humano y por lo tanto contienen información química sobre el tipo y cantidad de sustancias utilizadas por la población conectada a la alcantarilla. Los fármacos que se consumen se metabolizan en el organismo y posteriormente se excretan. Los productos de excreción pueden incluir los compuestos intactos así como los productos de transformación, que pueden usarse como biomarcadores. Un ejemplo de esto último es la benzoilecgonina, que es el principal producto de transformación de la cocaína consumida. Las aguas residuales colectivas del sistema de alcantarillado que transportan la carga de productos químicos se dirigen a la EDAR, y este afluente de aguas residuales puede ser muestreado en el punto donde ingresa a la EDAR. Mediante un muestreo apropiado del afluente durante intervalos de tiempo discretos, por ejemplo 24 h, se puede obtener una llamada muestra compuesta y se pueden determinar las concentraciones de los productos químicos. El volumen de afluente que ingresa a la EDAR se registra continuamente. Al multiplicar la concentración promedio observada de 24 h de un compuesto con el volumen total de 24 h se obtiene la carga diaria del químico que ingresa a la EDAR. Esta carga se puede normalizar al número de personas que viven en la cuenca de alcantarillado, resultando en una carga por habitante. Las cargas de fármacos en los afluentes de aguas residuales generalmente se expresan como mg.día -1 .1000 inh -1. Los datos normalizados de carga de medicamento permiten la comparación entre las cuencas de alcantarillado, como se muestra en la Figura 3. La obtención de información química sobre la población a través del análisis de aguas residuales se conoce como Epidemiología basada en aguas residuales, WBE (Ver el video). Si bien el WBE se desarrolló originalmente para obtener datos sobre el consumo de DOA, se ha demostrado que la metodología tiene un potencial mucho más amplio: en el cálculo del consumo de e.g., alcohol, nicotina, NPS, productos farmacéuticos y dopaje, así como para evaluar indicadores de salud comunitaria, como la incidencia de enfermedades o biomarcadores de estrés.
DOA y medio ambiente
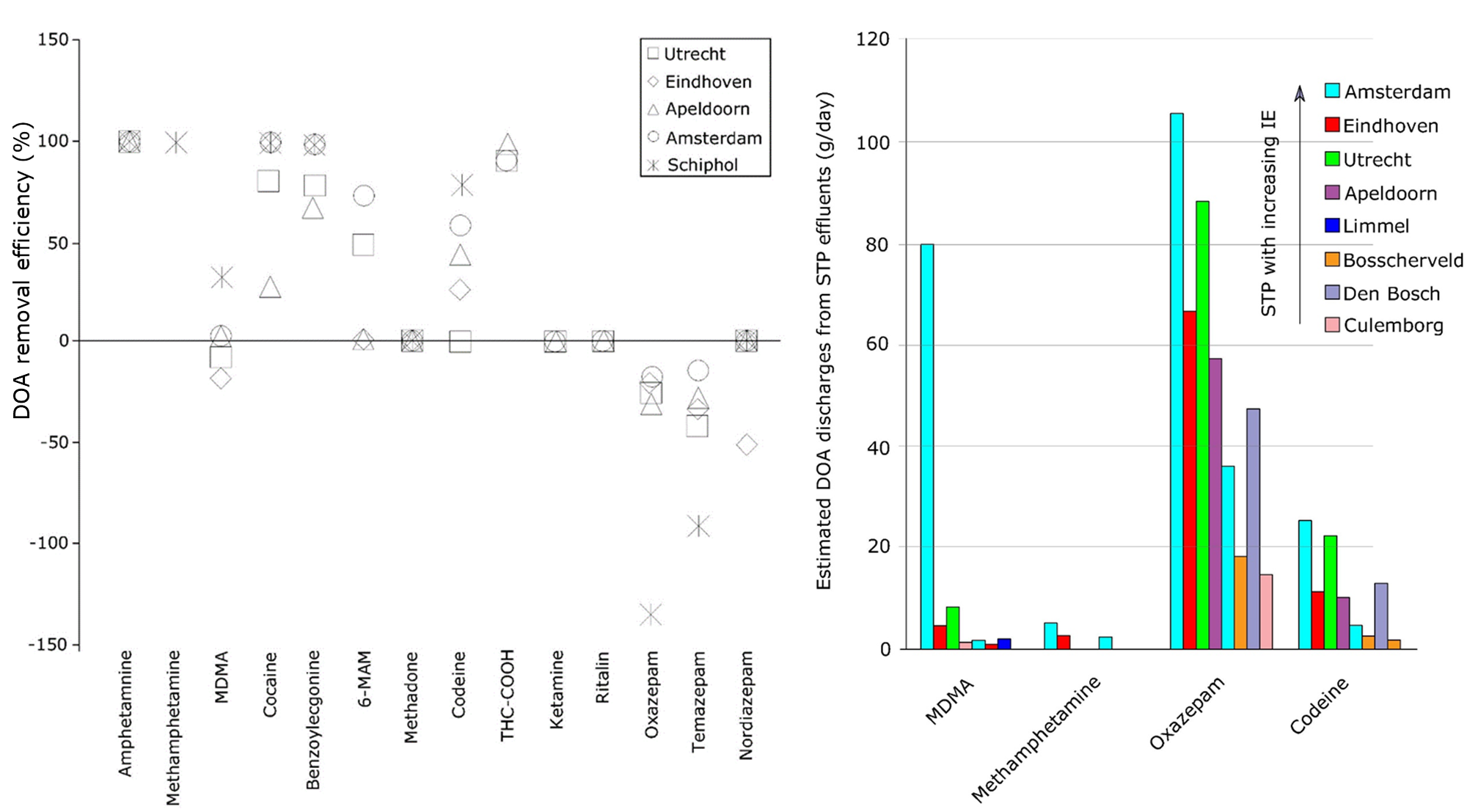
Salvo las descargas directas en aguas superficiales o ambientes terrestres, las principales fuentes de DOA para el medio ambiente son los efluentes de EDAR. El tratamiento convencional en EDAR municipales no ha sido diseñado específicamente para eliminar productos farmacéuticos o DOA. Las tasas de eliminación de DOA varían ampliamente y dependen de las propiedades del compuesto, como la persistencia y la polaridad, así como las condiciones operativas de la EDAR y las configuraciones del proceso. Algunos DOA cruzan las EDAR casi sin obstáculos, terminando así op en las aguas receptoras. Ejemplos de estos últimos son MDMA y algunas diazepinas (ver Figura 4). A pesar de que varios estudios reportan la presencia de DOA o sus productos de transformación en aguas superficiales, hasta ahora hay muy poca información sobre su ecotoxicidad acuática disponible en la literatura científica.
Recientemente, se ha observado que los desechos químicos de la fabricación de DOA sintéticos, incluidos sus precursores y subproductos de síntesis, se descargan directamente a las alcantarillas. Además, los contenedores con desechos químicos de los sitios de producción del DOA han sido arrojados sobre el suelo o las aguas superficiales. Aparte de solventes y ácidos o bases, estos desechos suelen contener restos de los productos de síntesis, que luego pueden disiparse en el medio acuático o filtrarse a través del suelo hacia el agua subterránea.
Considerando que los DOA son altamente activos en el cuerpo humano, se puede esperar que algunos de ellos, en particular los más persistentes, puedan ejercer algunos efectos sobre la biota acuática cuando sus niveles aumentan en el medio acuático.
Referencias
Van der Aa, M., Bijlsma, L., Emke, E., et al. (2013). Evaluación de riesgos por drogas de abuso en el ciclo acuático holandés. Investigación del Agua 47 (5), 1848-1857.
Bijlsma, L., Emke, E., Hernández, F., de Voogt, P. (2012). Investigación de drogas de abuso y metabolitos relevantes en aguas residuales holandesas mediante cromatografía líquida acoplada a espectrometría de masas de alta resolución. Quimosfera 89 (11), 1399-1406.
OEDT, European Drug Report 2018, Lisboa (www.emcdda.europa.eu/publications/edr/trends-developments/2018_es)
Thomas, K. V., Bijlsma, L., Castiglioni, S., et al. (2012). Comparación del consumo de drogas ilícitas en 19 ciudades europeas a través del análisis de aguas residuales. Ciencia del Medio Ambiente Total 432, 432-439.
Una forma de mapear los volúmenes de consumo de sustancias psicoactivas en una ciudad es mediante el análisis químico de residuos de drogas y biomarcadores en aguas residuales. Para evaluar el volumen de consumo de cocaína por una población se determinan las concentraciones en aguas residuales de la sustancia benzoilecgonina (BE). ¿Por qué se usa BE en lugar de la cocaína misma?
¿Qué posibles fuentes pueden llevar a la ocurrencia de una droga ilícita en las aguas residuales?
¿Pueden las drogas ilícitas en las aguas residuales representar una amenaza para el medio ambiente y de ser así, por qué?
2.3.5. Hidrocarburos
Autor: Pim N.H. Wassenaar
Crítico: Emiel Rorije, Eric M.J. Verbruggen, Jonathan Martin
Objetivos de aprendizaje:
Deberías ser capaz de
- explicar la diversidad/variación en las estructuras de hidrocarburos.
- explicar los efectos toxicológicos específicos e inespecíficos de varios hidrocarburos.
Palabras clave: Hidrocarburos, Parafinas, Nafténicos, Aromáticos
Introducción:
Los hidrocarburos son una clase de químicos que solo consisten en átomos de carbono e hidrógeno. Pero a pesar de su simplicidad en los bloques de construcción, este grupo de químicos consiste en una amplia variedad de estructuras, ya que existen diferencias en longitud de cadena, ramificación, tipos de unión y estructuras de anillo. Las principales fuentes de hidrocarburos son el petróleo crudo y el carbón, que se forman a lo largo de millones de años por la descomposición natural de los restos de plantas, animales o madera, y se utilizan para derivar productos que estamos utilizando a diario, incluyendo combustibles y plásticos Otras fuentes naturales incluyen la quema natural (bosque incendios) y fuentes volcánicas
Clasificación de hidrocarburos
Las clases principales de hidrocarburos son parafinas (es decir, alcanos), nafténicos (es decir, cicloalcanos) y aromáticos (Figura 1), y dentro de estas clases, se pueden identificar varias subclases. Las parafinas son hidrocarburos que no contienen ninguna estructura de anillo. Las parafinas se pueden subdividir en parafinas normales (n-), que no contienen ninguna ramificación (cadena lineal), e isoparafinas (i-), que sí contienen una cadena de carbono ramificada. Cuando los alcanos incluyen al menos un doble enlace carbono-carbono, se consideran olefinas (o alquenos).
Tanto los hidrocarburos nafténicos como los aromáticos contienen estructuras anulares pero difieren en la presencia de anillos aromáticos o no aromáticos. Los nafténicos y aromáticos se pueden especificar más en función de su recuento de anillos; a menudo las estructuras de mono-, di- y poli anillos se distinguen entre sí. De todas estas clases, los hidrocarburos aromáticos policíclicos (HAP) son la categoría mejor estudiada en términos de todo tipo de aspectos ambientales.
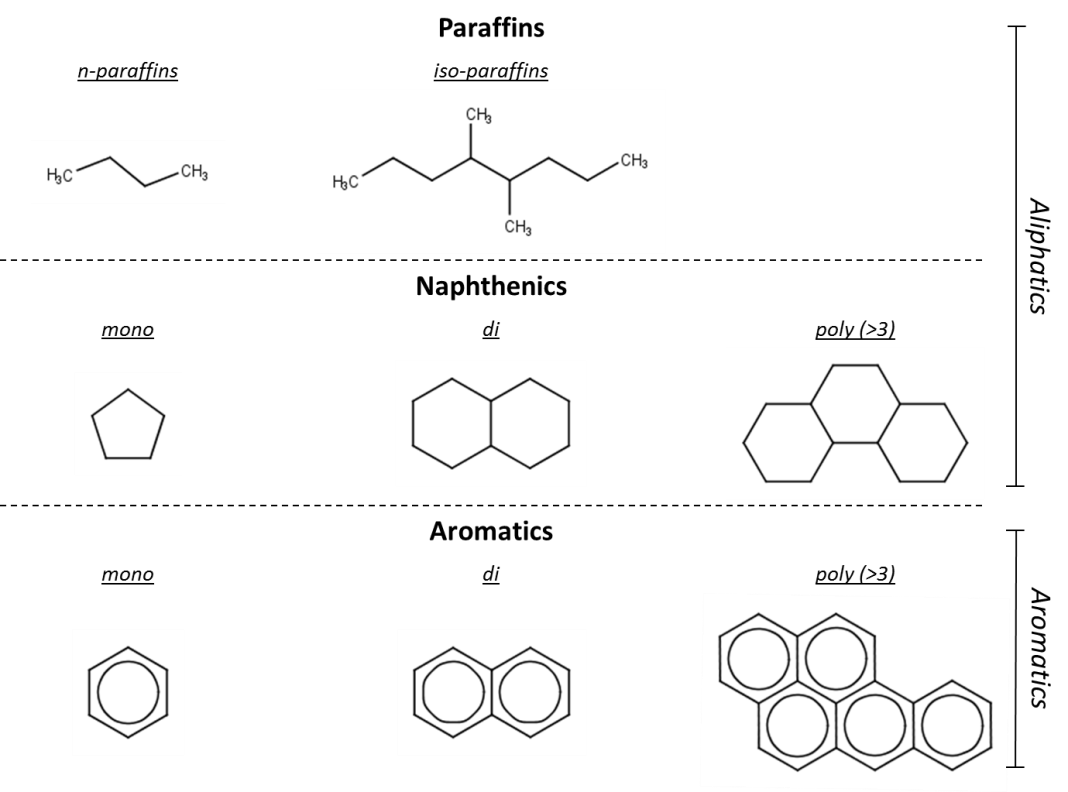
Además de las clases consideradas en la Figura 1., también existen combinaciones de estas clases. Las estructuras nafténicas o aromáticas con cadena lateral alcano se consideran en su mayoría hidrocarburos nafténicos o aromáticos, respectivamente. Sin embargo, cuando un anillo no aromático se fusiona con un anillo aromático, el hidrocarburo se clasifica como una estructura nafténico-aromática. Dependiendo del recuento de anillos se pueden identificar varias subclases, incluyendo nafténico-mono-aromáticos y nafténico-poliaromáticos.
Preocupaciones por la salud humana y el medio ambiente
Debido a su falta de grupos funcionales polares, los hidrocarburos son generalmente hidrófobos y, como consecuencia, muchos son capaces de causar efectos tóxicos agudos en animales acuáticos por un modo de acción inespecífico conocido como narcosis (o toxicidad basal). La narcosis es un estado reversible de actividad inhibida de las estructuras de membrana dentro de las células de los organismos. La toxicidad tipo narcosis se considera la toxicidad mínima que cualquier sustancia podrá tener, solo por alcanzar niveles de concentración en la bicapa fosfolipídica de las membranas celulares que perturban el proceso de transporte de la membrana. De ahí el nombre “basal” o toxicidad mínima. Cuando estos eventos ocurren por encima de cierto umbral, se puede observar toxicidad sistémica en el organismo, como la letalidad. Esta concentración umbral también se conoce como residuo corporal crítico (CBR) (Bradbury et al., 1989; Parkerton et al., 2000; Veith & Broderius, 1990).
Sin embargo, los hidrocarburos también pueden tener mecanismos de acción más específicos, resultando en mayor toxicidad que la toxicidad basal. Por ejemplo, la toxicidad de varios HAP aumenta en combinación con la radiación ultravioleta debido a la toxicidad fotoinducida. La toxicidad fotoinducida puede ser causada por la fotoactivación, en la que una HAP se degrada en un producto oxidado con mayor toxicidad, o más bien por fotosensibilización, en la que se forman especies reactivas de oxígeno (ROS) debido a un estado excitado de los HAP (Figura 2) (Roberts et al., 2017). Los HAP son especialmente vulnerables a la fotodegradación ya que su espectro de absorción se encuentra dentro del rango de longitudes de onda que llegan a la superficie terrestre (> 290 nm), lo que no es el caso de la mayoría de los hidrocarburos monoaromáticos y alifáticos (EMBSI, 2015). Los efectos fotoinducidos son de particular preocupación para las especies acuáticas con cuerpos transparentes, como el zooplancton y las etapas tempranas de la vida, ya que más luz UV puede penetrar en sus órganos y tejidos (Roberts et al., 2017).
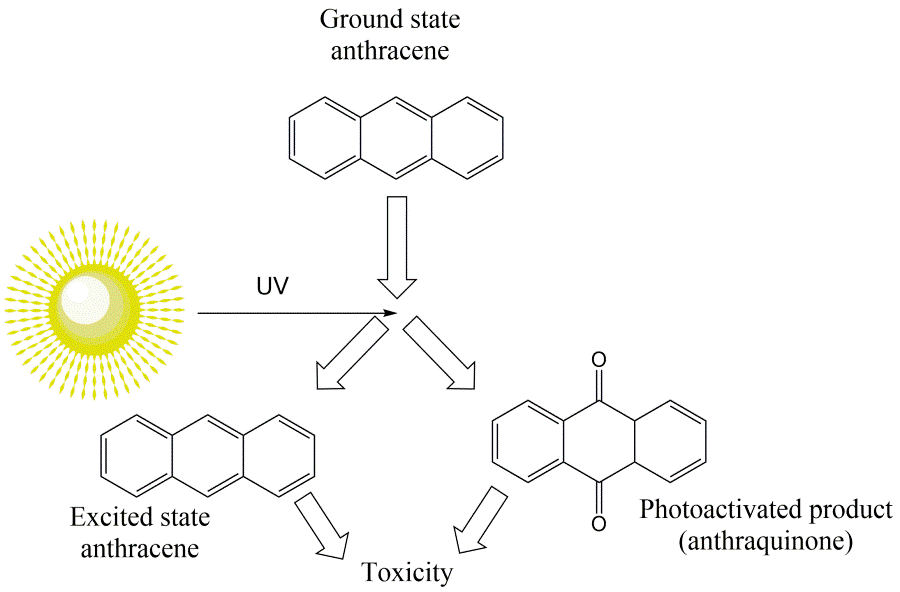
Varios hidrocarburos también son capaces de causar genotoxicidad y cáncer tras la exposición, incluyendo benceno, 1,3-butadieno y algunos HAP. La carcinogenicidad de los HAP es causada por la biotransformación en metabolitos reactivos, específicamente en epóxidos que son el primer paso en la oxidación de estructuras de anillos aromáticos en sistemas de anillos de dihidrodiol (Figura 3). En general, la etapa de biotransformación aumenta la solubilidad en agua de los hidrocarburos (metabolismo de Fase I) y promueve la posterior conjugación y excreción (metabolismo de Fase II). Sin embargo, varios metabolitos epóxidos -más específicamente los epóxidos aromáticos más estables- pueden alcanzar el núcleo celular y reaccionar covalentemente con el ADN, formando aductos de ADN e inducir mutaciones (Figura 3). En última instancia, si no se reparan tales mutaciones pueden acumularse y pueden resultar en la formación de tumores (Ewa & Danuta, 2016). Específicamente, los HAP con una región similar a una bahía son motivo de preocupación ya que la biotransformación da como resultado epóxidos reactivos relativamente estables que no son accesibles a las enzimas epóxido hidrolasa (Figura 3) (Jerina et al. 1980). Similar a los HAP, el 1,3-butadieno y el benceno también son capaces de causar cáncer a través de los efectos de sus respectivos metabolitos reactivos (Kirman et al., 2010; US-EPA 1998).
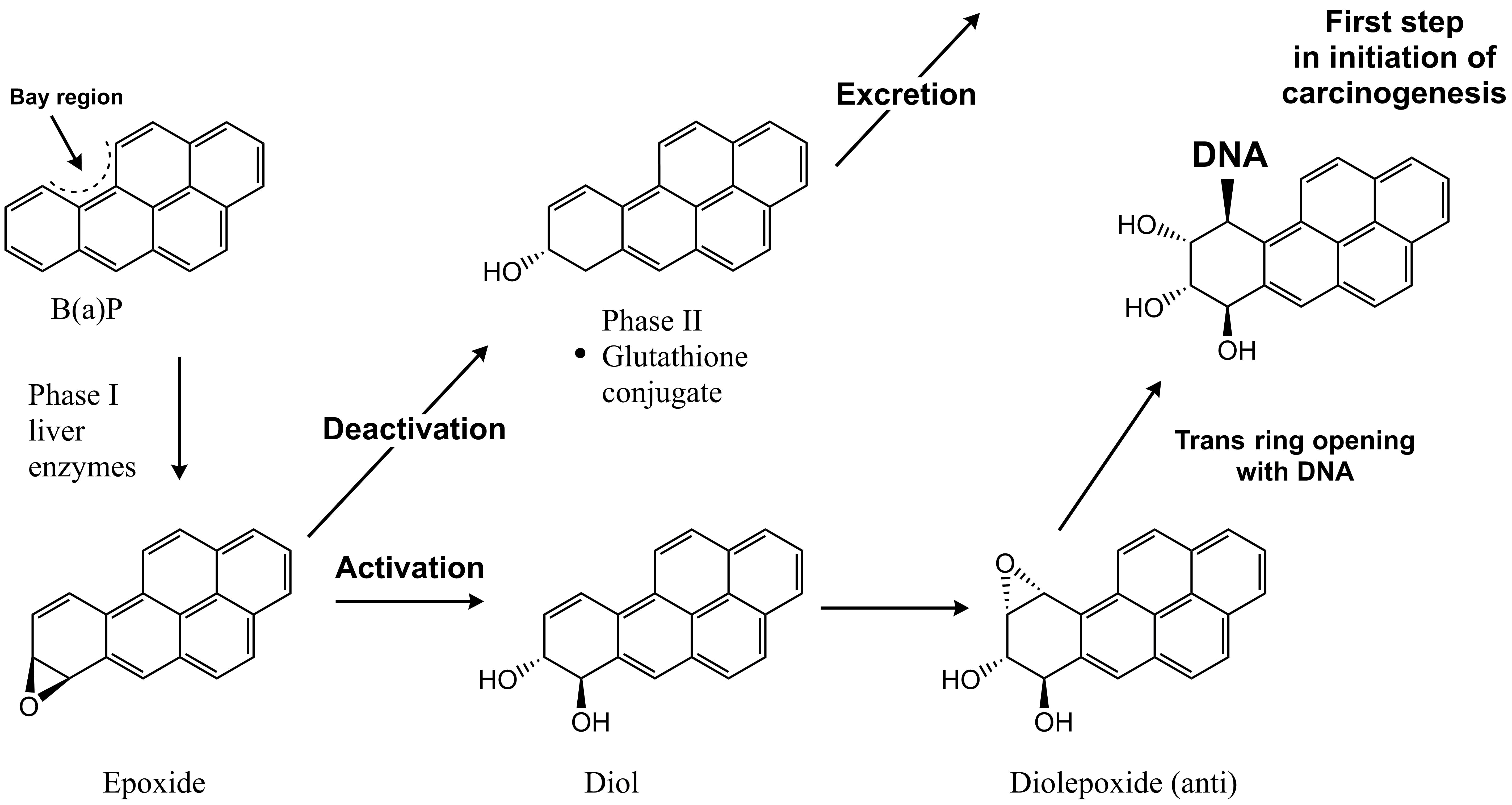
Además de su toxicidad, algunos hidrocarburos como los HAP de alto peso molecular pueden ser persistentes en el ambiente y pueden acumularse en la biota como resultado de su hidrofobicidad. Por lo tanto, se espera que las concentraciones internas sean mayores para dichos hidrocarburos y es interesante que exista así una relación entre la narcosis y el potencial de bioacumulación. En consecuencia, estos hidrocarburos podrían ser de mayor preocupación.
Caracterización de mezclas de hidrocarburos
Como la mayoría de las investigaciones se enfocaron en hidrocarburos específicos, entre ellos varios HAP, es importante señalar que el potencial de biodegradación, bioacumulación y toxicidad de muchos hidrocarburos aún no se conoce del todo, como los HAP alquilados y los nafténicos. Como existe una variedad tan amplia en las estructuras de hidrocarburos, es imposible evaluar los peligros (potenciales) de todos los hidrocarburos por separado. Por lo tanto, se han desarrollado enfoques de agrupación para agilizar la evaluación de riesgos. Dentro de un enfoque de agrupación, los hidrocarburos pueden agruparse en base a similitudes estructurales. El supuesto subyacente es que se espera que todos los productos químicos de un grupo tengan propiedades fisicoquímicas bastante similares, y posteriormente también propiedades de destino y efecto ambiental bastante similares. Como resultado, dicho grupo podría evaluarse potencialmente como si se tratara de un solo hidrocarburo.
Actualmente se está investigando la aplicabilidad de un enfoque de agrupamiento específico de hidrocarburos, conocido como Método de Bloque de Hidrocarburos (King et al., 1996), para evaluar el potencial de biodegradación y bioacumulación de hidrocarburos. Dentro de este enfoque, todos los hidrocarburos se agrupan en función de su clase funcional (por ejemplo, parafina, nafténica, aromática) y el número de átomos de carbono. Se cree que el número de átomos de carbono se correlaciona altamente con el punto de ebullición de los hidrocarburos. En la Figura 4 se presenta una matriz de ejemplo del Método de Bloque de Hidrocarburos. La composición de una sustancia oleosa podría expresarse en dicha matriz después del análisis GC-GC/MS. Posteriormente, las propiedades PBT de los bloques individuales podrían evaluarse potencialmente analizando y extrapolando las propiedades PBT de hidrocarburos representativos para bloques de hidrocarburos variables (ver Figura 4).
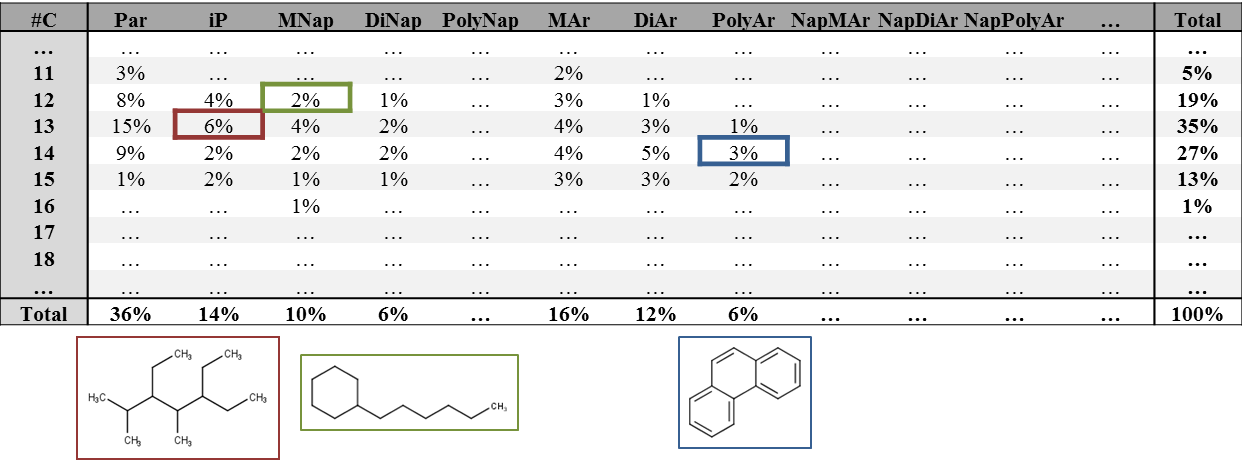
Referencias
Bradbury, S.P., Carlson, R.W., Henry, T R. (1989). Narcosis polar en organismos acuáticos. En Toxicología Acuática y Evaluación de Peligros: Volumen 12. ASTM Internacional.
EMBSI (2015). Evaluación de Procesos Fotoquímicos en la Evaluación de Riesgos Ambientales de HAP
Ewa, B., Danuta, M.Š. (2017). Hidrocarburos aromáticos policíclicos y aductos de ADN relacionados con PAH. Revista de genética aplicada 58, 321-330.
Homburger, F., Hayes, J.A., Pelikanm E.W. (1983). Una Guía de Toxicología General. Karger/Base, Nueva York, NY.
Jerina, D.M., Sayer, J.M., Thakker, D.R., Yagi, H., Levin, W., Wood, A.W., Conney, A.H. (1980). Carcinogenicidad de hidrocarburos aromáticos policíclicos: teoría de la región de la Bahía. En Carcinogénesis: Mecanismos Fundamentales y Efectos Ambientales (pp. 1-12). Springer, Dordrecht.
King, D.J., Lyne, R.L., Girling, A., Peterson, D.R., Stephenson, R., Short, D. (1996). Evaluación del riesgo ambiental de las sustancias petrolíferas: el método del bloque de hidrocarburos. Informe CONCAWE núm. 96/52.
Kirman, C.R., Albertini, R.A., & Gargas, M.L. (2010). 1, 3-Butadieno: III. Evaluación de modos de acción cancerígenos. Revisiones críticas en toxicología 40 (sup1), 74-92.
Parkerton, T.F., Stone, M.A., Letinski, D. J. (2000). Evaluación de la toxicidad acuática de mezclas complejas de hidrocarburos mediante microextracción en fase sólida. Cartas de toxicología 112, 273-282.
Roberts, A.P., Aleación, M.M., Oris, J.T. (2017). Revisión de la toxicidad fotoinducida de contaminantes ambientales. Bioquímica Comparada y Fisiología Parte C: Toxicología y Farmacología 191, 160-167.
US-EPA (1998). Efectos Carcinogénicos del Benceno: Una Actualización. EPA/600/P-97/001F.
Veith, G.D., Broderius, S.J. (1990). Reglas para distinguir sustancias tóxicas que causan síndromes de narcosis tipo I y tipo II. Perspectivas de salud ambiental 87, 207.
¿Mencionar al menos tres aspectos que influyen en la variación en las estructuras de hidrocarburos?
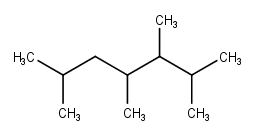
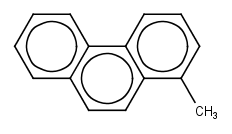
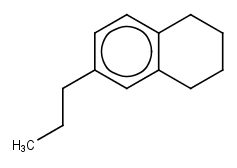
¿A qué clase de hidrocarburos (o Bloque de Hidrocarburos) pertenecen las siguientes estructuras?
1. 
2. 
3. 
¿Qué tipo de efectos tóxicos se pueden observar para los hidrocarburos aromáticos policíclicos?
2.3.6. CFC
(borrador)
Autores: Steven Droge
Crítico: John Parsons
Objetivos de inclinación:
Deberías ser capaz de:
- darse cuenta de lo que se trataba el agotamiento de la capa de ozono
- Entender por qué ciertos productos químicos de reemplazo siguen siendo problemáticos
Palabras clave: Capa de ozono, refrigerador, productos químicos volátiles, botes de aerosol, radicales
Introducción
Los CFC (clorofluorocarbonos) fueron contaminantes atmosféricos muy comunes en el siglo XX porque eran los componentes básicos de refrigerantes y aire acondicionado, propulsores (en aplicaciones de latas de pulverización) y solventes, desde la década de 1930. Siguen siendo contaminantes atmosféricos muy comunes, porque son químicos muy persistentes, y las emisiones aún continúan. En los primeros años como refrigerantes, reemplazaron los componentes mucho más tóxicos amoníaco (NH 3), clorometano (CH 3 Cl) y dióxido de azufre (SO 2). Particularmente, los CFC que se filtran de los viejos sistemas de refrigeración en vertederos y sitios de eliminación de desechos causaron altas emisiones al medio ambiente. Por lo general, estos productos químicos CFC volátiles se basan en las moléculas de carbono más pequeñas metano (CH 4), etano (C 2 H 6) o propano (C 3 H 8). Todos los átomos de hidrógeno en estas moléculas de CFC son reemplazados por una mezcla de átomos de cloro y flúor.
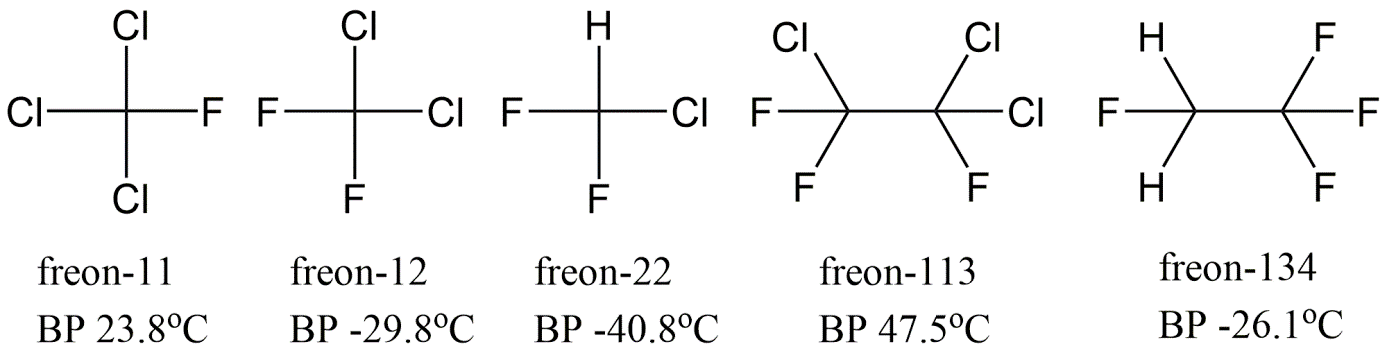
Los CFC son menos volátiles que su análogo hidrocarbonado, debido a que los átomos de halógeno polarizan las moléculas, lo que provoca mayores atractivos intermoleculares. Dependiendo de la sustitución con Cl o F, el punto de ebullición se puede ajustar al punto deseado para los procesos de enfriamiento de refrigeración. Los CFC también son mucho menos inflamables que los análogos de hidrocarburos, lo que los hace mucho más seguros en todo tipo de aplicaciones.
Nombramiento de CFC
Los CFC a menudo eran conocidos por la popular marca Freon. Freón-12 (o R-12) por ejemplo significa diclorodifluorometano (CCl 2 F 2, punto de ebullición -29.8 °C, mientras que el metano tiene -161 °C), como se muestra en la Figura 1. La denominación refleja la cantidad de átomos de flúor como el número más correcto. El siguiente valor a la izquierda es el número de átomos de hidrógeno más 1, y el siguiente valor a la izquierda es el número de átomos de carbono menos uno (no se indican ceros), y los átomos restantes son cloro. En consecuencia, Freón-113 podría aplicarse a 1,1,2-tricloro-1,2,2-trifluoroetano (C 2 Cl 3 F 3, punto de ebullición 47.7 °C, mientras que el etano tiene -161 °C). La estructura de cualquier número Freón-X también se puede derivar de sumar +90 al valor de X, por lo que Freón-113 daría un valor de 203. El primero numérico es el número de C (2), el segundo numérico H (0), el tercer número F (3), y las sustituciones restantes son por cloro (C 2 X 6 da 3 cloros).
La razón por la que el CFC agota la capa de ozono
El tema clave con las emisiones de CFC es la reacción bajo influencia de la luz (“fotodegradación”) que finalmente reduce las concentraciones de ozono (“agotamiento de ozono”) en la atmósfera superior (“estratosfera”). El ozono absorbe la radiación de alta energía del espectro solar UV-B (280-315nm), por lo que la capa de ozono impide que ésta llegue a la superficie de la Tierra. El espectro solar UV-C aún más energético (100-280nm) en realidad está causando la formación de ozono (O 3) al reaccionar con oxígeno (O 2), como se muestra en la Figura 2. Bajo la influencia de la energía lumínica intensa en la atmósfera superior, las moléculas de CFC pueden desintegrarse en dos radicales altamente reactivos (moléculas con un electrón libre . ), para Freón-11:
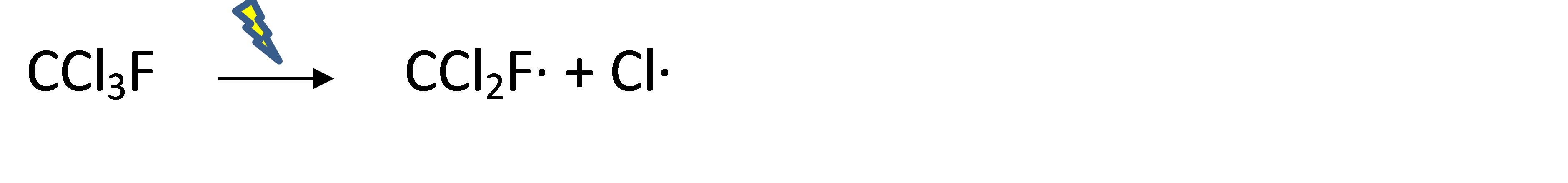
Es el radical Cl . que cataliza la conversión del ozono de nuevo en O 2. El papel ambientalmente relevante de los átomos de flúor en los CFC es que hacen que estos químicos sean muy persistentes después de la emisión, ya que el enlace C-F es uno de los enlaces covalentes más fuertes conocidos. Con vidas medias de hasta >100 años, los niveles altos de CFC pueden llegar a la atmósfera superior. James Lovelock fue el primero en detectar la presencia generalizada de CFC en el aire en la década de 1960, mientras que el daño causado por los CFC fue descubierto solo en 1974. Otro efecto indeseable de los CFC en la estratosfera es que son gases de efecto invernadero mucho más potentes que el CO 2.
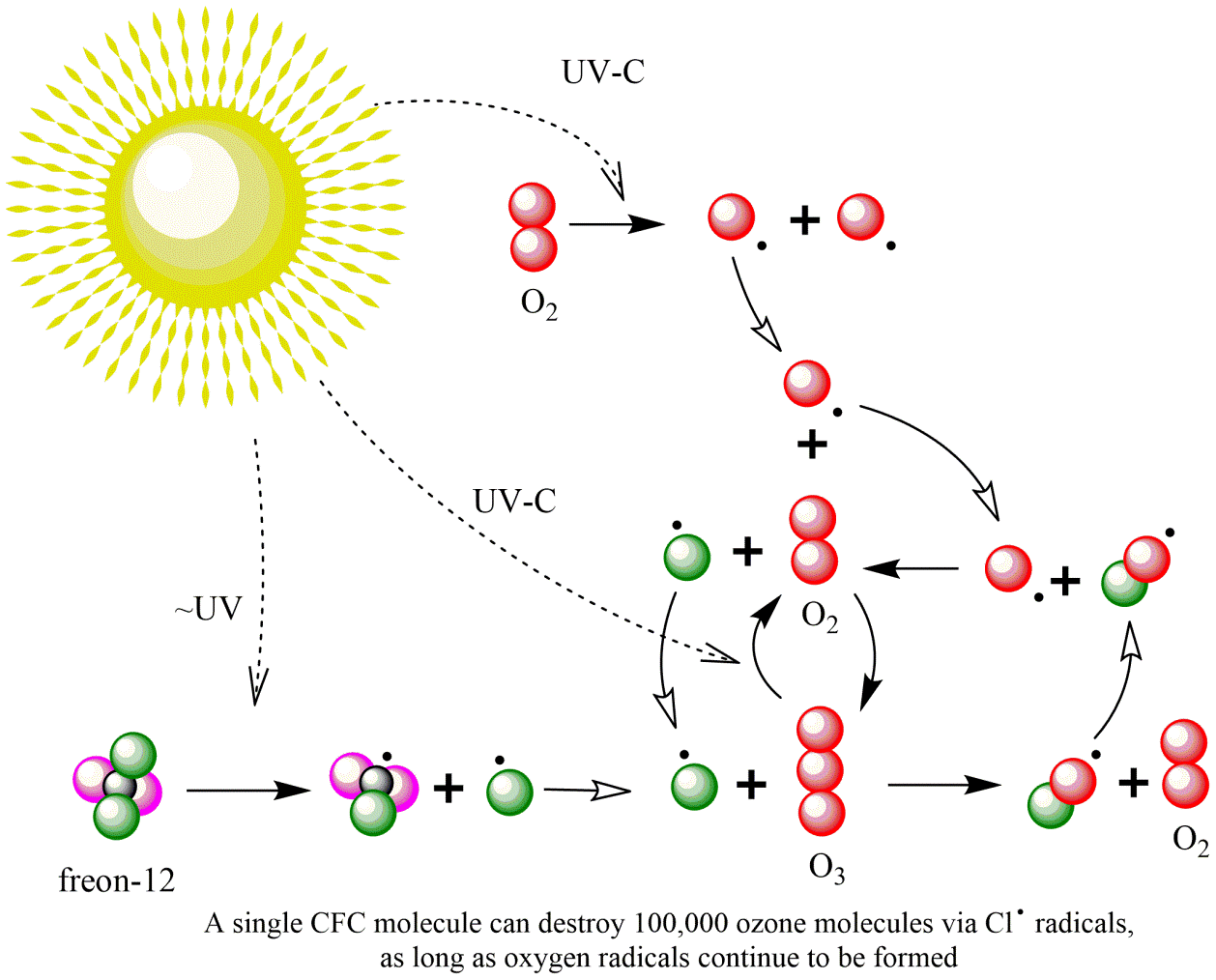
Reemplazos de CFC.
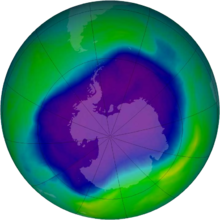
En 1978 Estados Unidos prohibió el uso de CFC como el Freón en latas de aerosol. Después de varios años de observaciones del agotamiento de la capa de ozono a nivel mundial (Figura 3), particularmente por encima de la Antártida, se firmó el Protocolo de Montreal en 1987 para reducir drásticamente las emisiones de CFC a nivel mundial. Los CFC fueron prohibidos a finales de los noventa en la mayoría de los países de la UE, y por ejemplo en Corea del Sur para 2010. Debido a la persistencia de los CFC puede tardar hasta 2050-2070 antes de que la capa de ozono vuelva a los niveles de 1980 (que ya estaban malos).
La característica dañina clave de los CFC en términos de agotamiento del ozono es su persistencia, de manera que las emisiones alcanzan y se acumulan en la estratosfera (a partir de 20km por encima del ecuador, pero sólo a 7km por encima de los polos). Las moléculas de reemplazo de CFC se encontraron inicialmente simplemente agregando más hidrógenos en las estructuras de CFC y algo menos Cl (HCFC), pero las fracciones aún contribuyeron a Cl . radicales. Las alternativas posteriores carecen de los átomos de cloro y tienen vidas aún más cortas en la atmósfera inferior, y simplemente no pueden formar los radicales Cl. Estos “hidrofluorocarbonos” (HFC) son actualmente comunes en los aires acondicionados de automóviles, como el Freón-134 (haz los cálculos para ver que no hay Cl, punto de ebullición -26.1 °C).
Aún así, tanto los HCFC como los HFC siguen siendo gases de efecto invernadero muy potentes, por lo que el uso mundial de tales químicos sigue siendo problemático y da lugar a nuevas legislaciones, regulaciones y búsquedas de alternativas. El R-410A (que contiene solo flúor) es cada vez más utilizado pero es 1700 veces más potente que el CO 2 como gas de efecto invernadero, igual al Freón-22. Las mezclas simples de hidrocarburos como el propano/isobutano ya se utilizan ampliamente en los sistemas de aire acondicionado móviles, ya que tienen las propiedades termodinámicas adecuadas para algunos usos y son relativamente seguras. Desafortunadamente, no teníamos las habilidades tecnológicas, ni la conciencia para aplicar esto allá por la década de 1930.
2.3.7. Cosméticos/productos para el cuidado personal
(borrador)
Autor: Mélanie Douziech
Revisores: John Parsons
Objetivos de aprendizaje:
Deberías ser capaz de:
- Definir qué son los productos de cuidado personal y los cosméticos
- Explicar cómo los químicos de los productos de cuidado personal terminan en el medio ambiente
- Citar y describir algunos de los químicos más comunes que se encuentran en los productos de cuidado personal
Palabras clave: aguas residuales, función química, surfactantes, microperlas
Introducción
Los productos de cuidado personal (PCP) cubren una amplia gama de productos que cumplen con fines de higiene, salud o belleza (por ejemplo, champú, pasta de dientes, esmalte de uñas). Se clasifican en cuidado bucal, cuidado de la piel, cuidado solar, cuidado del cabello, cosmética decorativa, cuidado corporal y perfumes. En general, la mayoría de los PCP se clasifican como cosméticos y se regulan en consecuencia. En la Unión Europea (UE) el Reglamento Cosmético rige la producción, la seguridad de los ingredientes y el etiquetado y comercialización de los productos cosméticos. Los Estados Unidos de América (EE.UU.), por otro lado, tienen una definición más estrecha de cosmética para que los productos que no cumplan con la definición se regulen como farmacéuticos (por ejemplo, protector solar) (Food and Drug Administration, 2016).
Los PCP vienen en una variedad de formatos (por ejemplo, líquidos, barras, aerosoles, polvos) y generalmente contienen una amplia gama de productos químicos, cada uno cumpliendo una función específica dentro del producto. Por ejemplo, un champú puede incluir agentes limpiadores (tensioactivos), productos químicos para asegurar la estabilidad del producto (por ejemplo, conservantes, ajustadores de pH, agentes de control de la viscosidad), diluyente (por ejemplo, agua), productos químicos perfumantes (fragancias) y productos químicos para influir en la apariencia del producto (por ejemplo, colorantes, perlescentes, opacificadores). Los productos químicos presentes en los PCP finalmente ingresan al ambiente ya sea a través del aire durante el uso directo, como los propelentes en los aerosoles, o a través de las aguas residuales a través de la eliminación del drenaje después del uso del producto (por ejemplo, productos de ducha, pasta de dientes). Es necesario monitorear la liberación de químicos PCP al medio ambiente y comprender la seguridad de estos químicos para evitar posibles problemas. En los países desarrollados, el uso de plantas de tratamiento de aguas residuales (EDAR) es clave para eliminar eficazmente los productos químicos PCP y otros contaminantes de las aguas residuales antes de su liberación a los ríos y otros cursos de agua. Los mecanismos de remoción que ocurren en las EDAR incluyen biodegradación, sorción sobre sólidos y volatilización al aire. El grado de remoción está influenciado por las propiedades fisicoquímicas de los químicos y las condiciones operativas de las EDAR. En regiones donde falta tratamiento de aguas residuales, los químicos en los PCP ingresan directamente al medio ambiente.
El uso diario a gran escala de los PCP y los grandes volúmenes asociados de productos químicos liberados explican por qué son examinados por agencias de protección ambiental y organismos reguladores. En las siguientes secciones se revisarán brevemente algunas de las clases de químicos utilizados en los PCP, describiendo su comportamiento en el medio ambiente y su posible efecto en los ecosistemas.
Agentes limpiadores - surfactantes
Los surfactantes son una clase importante y ampliamente utilizada de químicos. Son los componentes clave de muchos agentes de limpieza para el hogar así como los PCP, como champús, jabones, gel de baño y pasta de dientes, debido a su capacidad para eliminar la suciedad. Estas propiedades eliminadoras de suciedad también hacen que los surfactantes sean inherentemente tóxicos para los organismos acuáticos. La biodegradabilidad de los surfactantes es un requisito legal clave para su uso en PCP para minimizar la probabilidad de niveles inseguros en el ambiente. Existen diferentes tipos de surfactantes y a menudo se clasifican en función de su carga superficial. Los tensioactivos aniónicos, que llevan una carga superficial negativa, interactúan y ayudan a eliminar las partículas de suciedad cargadas positivamente de superficies como el cabello y la piel. El lauril sulfato de sodio es un ejemplo típico de un tensioactivo aniónico utilizado en PCP. Los tensioactivos catiónicos, como el cloruro de cetrimonio, están cargados positivamente y pueden usarse como agentes acondicionadores del cabello para hacer que el cabello sea más brillante o más manejable. Los tensioactivos no iónicos (sin carga), como el alcohol cetílico, ayudan a formular productos o aumentar la formación de espuma. Los tensioactivos anfóteros, como el lauriaminodipropionato de sodio, llevan cargas positivas y negativas y se usan comúnmente para contrarrestar las propiedades potencialmente irritantes de los tensioactivos aniónicos.
Fragancias
Las fragancias son mezclas de a menudo más de 20 productos químicos de perfumería utilizados para proporcionar el olor de los PCP. Típicamente, las fragancias están presentes en niveles muy bajos en la mayoría de los PCP (por debajo de 0.01%) de manera que no se divulgan sus composiciones exactas. Sin embargo, se desvela cualquier alérgeno presente en la fragancia para ayudar a los dermatólogos y consumidores a evitar ciertos productos químicos de fragancia. A pesar del deseo de proteger los secretos comerciales, una tendencia reciente ve cada vez más a las empresas revelar las composiciones de fragancias completas de sus productos en sus sitios web (por ejemplo, L'Oréal, Unilever). Ejemplos bien conocidos de fragancias incluyen hexil cinamal, linalol y limoneno. Las posibles preocupaciones sobre el impacto ecotoxicológico de las fragancias han surgido por un lado debido a la falta de divulgación de las formulaciones de fragancias y por otro lado a la detección de ciertas fragancias persistentes en el ambiente (por ejemplo, nitroalmizcle).
Conservantes
Los conservantes generalmente se agregan a los PCP que contienen agua por su capacidad para proteger el producto de la contaminación por bacterias, levaduras y mohos durante el almacenamiento o uso repetido. Dada su acción dirigida contra los organismos vivos, el uso de conservantes en productos químicos, incluidos los PCP, está bajo constante escrutinio. Por ejemplo, en 2016 y 2017, la Comisión Europea endureció la regulación en torno al uso de metilisotiazolinona en productos cosméticos debido a preocupaciones de seguridad humana. Otros conservantes que han sido restringidos en su uso, debido a preocupaciones tanto de seguridad humana como de seguridad ambiental (por ejemplo, efectos de alteración endocrina), incluyen ciertos tipos de parabenos y triclosán.
Filtros UV
Los filtros UV se utilizan en productos de protección solar así como en otros PCP como base, lápiz labial o crema hidratante para proteger a los usuarios de la radiación UV. Los filtros UV pueden ser orgánicos o inorgánicos. Los filtros UV inorgánicos, como el óxido de titanio y el óxido de zinc, forman un límite físico que protege la piel de la radiación UV. Los filtros UV orgánicos, por otro lado, protegen la piel al someterse a una reacción química con la radiación UV entrante. Los filtros UV orgánicos que se encuentran comúnmente en los PCP incluyen metodibenzoilmetano de butilo, metoxicinamato de etilhexilo y octocrileno. Los filtros UV orgánicos son poco biodegradables y tienen el potencial de acumularse en los organismos. Además, varios filtros UV orgánicos han demostrado ser tóxicos para los organismos coralinos en pruebas de laboratorio. Se sospecha que causan blanqueamiento de coral, por ejemplo, promoviendo infecciones virales, pero aún se están investigando para comprender sus posibles efectos ecotoxicológicos a concentraciones ambientales realistas.
Productos químicos volátiles
Ciertos productos químicos utilizados en los PCP son altamente volátiles y pueden terminar en el aire después del uso del producto. Los ejemplos incluyen propelentes, como mezclas de propano butano o aire comprimido/nitrógeno, utilizados en aerosoles para aplicar ingredientes en lacas para el cabello o desodorantes y antitranspirantes. Las fragancias también se volatilizan cuando el producto se aplica sobre la piel o el cabello para proporcionar olor. Las siliconas volátiles, sustancias químicas utilizadas para ayudar a la deposición de ingredientes en líquidos y cremas, son otro ejemplo de sustancias químicas emitidas al aire tras el uso de PCP.
El estuche especial de microperlas de plástico
Microperlas de plástico, con un diámetro menor a 5 mm, se han utilizado en PCP como exfoliantes faciales o geles de ducha por sus propiedades de fregado y limpieza. La creciente preocupación por la contaminación plástica en el agua ha llamado la atención sobre el uso de microperlas en PCPs. Como resultado, se lanzaron una serie de iniciativas tanto para resaltar el uso de microperlas de plástico como para fomentar el reemplazo por alternativas naturales. Un ejemplo de ello es la coalición “Beat the microbead” (https://www.beatthemicrobead.org/) patrocinada por el Programa de las Naciones Unidas para el Medio Ambiente, lanzada para ayudar a los consumidores a identificar y evitar PCP que contienen microperlas. Tales iniciativas junto con los compromisos voluntarios de la industria han llevado a una gran disminución en el uso de microperlas en los productos cosméticos de lavado: En la UE, por ejemplo, el uso de microperlas en productos de lavado se redujo en 97% de 2012 a 2017. Recientemente también se ha promulgado legislación para restringir el uso de microperlas. En Estados Unidos, las microperlas en PCP fueron prohibidas en julio de 2017 y varios países de la UE (por ejemplo, Reino Unido, Italia) también han prohibido su uso en productos de lavado.
Lectura adicional
Para obtener más información sobre los productos químicos PCP y su función en los productos, consulte (Comisión Europea 2009; Asociación de Fabricantes de Abarrotes 2017).
Para mayor información sobre los diferentes tipos de surfactantes, consulte Tolls et al. (2009) y Sección 2.3.8.
Manova et al. (2013) enumeran los diferentes tipos de filtros UV.
El reporte de Scudo et al. (2017) da más información sobre el uso de microplásticos en Europa.
Referencias
Comisión Europea (2019). Cosing. 2009 03.2019]; Disponible en: http://ec.europa.eu/growth/tools-databases/cosing/.
Administración de Alimentos y Medicamentos (2016). ¿Todos los “productos de cuidado personal” están regulados como cosméticos? [citado 2019 03]; Disponible en: https://www.fda.gov/forindustry/fdabasicsforindustry/ucm238796.htm.
Asociación de Fabricantes de Abarrotes (2017). Smartlabel. [citado 2017 11]; Disponible en: http://www.smartlabel.org/.
Manova, E., von Goetz, N., Hauri, U., Bogdal, C., Hungerbuhler, K. (2013). Filtros UV orgánicos en productos de cuidado personal en Suiza: una encuesta de ocurrencia y concentraciones. Revista Internacional de Higiene y Salud Ambiental 216, 508-514.
Scudo, A., Liebmann, B., Corden, C., Tyrer, D., Kreissig, J., Warwick, O. (2017). Microplásticos Agregados Intencionalmente en Productos. en: Limited A.F.W.E.A.I.U., ed. Reino Unido
Peajes, J., Berger, H., Klenk, A., Meyberg, M., Müller, R., Rettinger, K., Steber, J. (2009). Aspectos de seguridad ambiental de los productos de cuidado personal - una perspectiva europea. Toxicología y Química Ambiental 28, 2485-2489.
¿Cómo terminan en el medio ambiente los químicos que se encuentran en los cosméticos?
¿Por qué los surfactantes son una preocupación por la toxicidad ambiental?
¿Cómo contribuyeron los productos de cuidado personal a la contaminación microplástica en el agua?
2.3.8. Detergentes y surfactantes
Autor: Steven Droge
Crítico: Thomas P. Knepper
Objetivos de inclinación:
Deberías ser capaz de:
- explicar por qué los surfactantes eliminan la suciedad
- discutir el progreso histórico en la biodegradabilidad de los tensioactivos
- describir los diferentes tipos de surfactantes comunes.
- describen ejemplos de cómo los surfactantes ingresan al ambiente.
Palabras clave: químicos anfifílicos, formación de micelas, biodegradabilidad
Introducción
Los agentes tensioactivos (“surf-act-ants”) son una amplia variedad de productos químicos producidos en volúmenes a granel (>10.000 toneladas anuales) como ingrediente clave en los productos de limpieza: los detergentes. Lo típico de los surfactantes es que tienen una cola hidrofóbica y un grupo de cabeza hidrófilo (Figura 1).
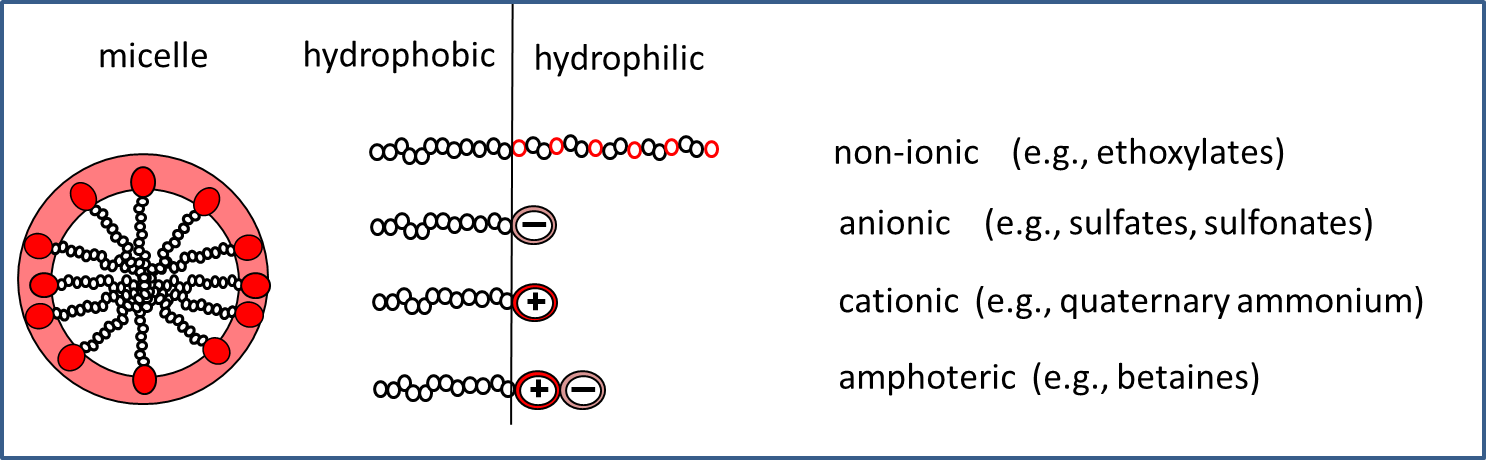
A concentraciones relativamente altas en agua (típicamente >10-100 mg/L), los tensioactivos forman espontáneamente estructuras agregadas llamadas micelas (Figura 1), a menudo en esferas con las colas hidrófobas hacia adentro y los grupos de cabeza hidrófilos hacia las moléculas de agua circundantes. Estas superestructuras micelares permiten que los tensioactivos disuelvan la grasa y la suciedad, por ejemplo, de textiles o platos en agua, que luego se puede lavar. Además de este uso común de surfactantes, sus propiedades anfifílicas (es decir, tanto hidrófilas como lipofílicas) permiten un uso versátil en nuestro mundo moderno:
• Durante el gran derrame de petróleo de 2010 en el Golfo Mexicano, se utilizaron enormes volúmenes (>6700 toneladas) de varios tipos de formulaciones tensioactivas (por ejemplo, "Corexit") para dispersar la corriente constante de petróleo que se escapa del pozo de agua profunda dañado en pequeñas gotas disueltas, en con el fin de facilitar la degradación microbiana y evitar la formación de losas flotantes de petróleo que podrían arruinar hábitats costeros.
• La capacidad de una capa de surfactantes para mantener partículas hidrófobas en solución es un proceso clave en muchos productos, como pinturas y lacas.
• La capacidad de emulsionar partículas de suciedad es una característica clave en los fluidos de proceso durante la perforación profunda en suelo o sedimento.
• Los suavizantes de telas y acondicionadores para el cabello tienen tensioactivos catiónicos como ingredientes clave que se adhieren con los grupos de cabeza cargados positivamente sobre las fibras cargadas negativamente de su toalla o cabello. Después del lavado final, estos tensioactivos catiónicos aún se adhieren a las fibras y debido a los grupos de cabeza hidrófobos que sobresalen hacen que estos materiales se sientan suaves y lisos. A menudo, solo durante el siguiente evento de lavado (con tensioactivos aniónicos o no iónicos) los tensioactivos catiónicos se limpian de las fibras.
• Muchos tensioactivos catiónicos tienen propiedades biocidas a concentraciones relativamente bajas y, por lo tanto, se usan en un poco por ciento en muchos productos cosméticos como conservantes, por ejemplo, en cosméticos, o se usan para matar microbios en el procesamiento de alimentos, toallitas antibacterianas para manos o durante la limpieza de piscinas. Ejemplos son sales de cloruro de benzalconio, bencetonio, cetilpiridinio.
• Los surfactantes disminuyen la tensión superficial del agua, y por lo tanto se utilizan (como “adyuvantes”) en productos pesticidas para facilitar la formación de gotitas durante la pulverización y para mejorar el contacto de las gotitas con las hojas objetivo en caso de herbicidas. Ejemplos son los tensioactivos fluorados, los tensioactivos a base de silicona (Czajka et al. 2015) y la amina de sebo polietoxilada (POEA) utilizados por ejemplo en la formulación de glifosato Roundup.
La cola hidrofóbica de los surfactantes está compuesta principalmente por una cadena de átomos de carbono, aunque también cadenas de carbono fluorado (-CF 2 -) o siloxano (Si (CH 3) 3 -O- [..] -Si (CH 3) 3) también son posibles cadenas.
Los primeros tensioactivos producidos por volumen volumétrico para lavadoras fueron alquilbencenosulfonatos aniónicos ramificados (ABS) y alquilfenoleetoxilatos (APEO), con la fuente de hidrocarburos obtenida del petróleo. Debido a la fuente variable de petróleo, estos químicos suelen ser mezclas complejas. Sin embargo, las cadenas alquílicas ramificadas hidrófobas están poco biodegradadas, y la eliminación constante de estos surfactantes en las aguas residuales causó concentraciones ambientales muy altas, lo que a menudo conduce a ríos espumantes (Figura 2).

Los productores de surfactantes cambiaron 'voluntariamente' a fuentes de carbono como el aceite de palma o la polimerización controlada de etileno a base de petróleo, que podrían ser utilizados para generar surfactantes con cadenas alquílicas lineales: alquilbencenosulfonato lineal (LAS) y etoxilatos de alcohol (AEO). Algunos tensioactivos tienen el grupo de cabeza hidrófilo unido a dos cadenas de carbono, como el docusato aniónico (muy utilizado en el derrame de petróleo BP) y los químicos catiónicos de dialquildimetilamonio. Los tensioactivos detergentes comunes hoy en día están diseñados para pasar pruebas de biodegradabilidad listas (> 60% de mineralización a CO 2 dentro de una ventana de 10 d después de una fase de retraso, en una prueba de 28 d). Los primeros ejemplos de ablandantes de telas son los tensioactivos de doble cadena (dialquil) dimetilamonio, pero la persistencia ambiental de estos compuestos (DODMAC y DHTDMAC, ver por ejemplo EU y RIVM-Reports) ha llevado a un gran reemplazo por diesterquats (DEEDMAC), que se degradan más rápidamente a través de los enlaces éster débiles de las cadenas de ácidos grasos (Giolando et al. 1995). Un cambio a la producción sustentable de las fuentes de carbono está en curso. Mientras que el aceite de etileno a base de petróleo se utilizó principalmente, está siendo reemplazado cada vez más por las cadenas de carbono de ácidos grasos lineales de cualquiera de aceite de palma (principalmente C 16 /C 18), aceite de coco (principalmente C 12 /C 14), pero también tales materias primas deben ser tan derivadas de manera sostenible como sea posible.
Los grupos de cabeza hidrofílicos pueden variar ampliamente. Los tensioactivos no iónicos pueden tener un grupo funcional polar simple (amida), basado en glucosa (poliglicósido), o contener longitudes variables de unidades repetitivas de etoxilado y/o propoxilato. Debido a que el proceso de etoxilación es difícil de controlar, tales tensioactivos suelen ser mezclas complejas. Los tensioactivos aniónicos a menudo se basan en sulfato (SO 4 -) o sulfonato (SO 4 -), pero también son comunes el fosfonato y los carboxilatos. Una diferencia clave entre los tensioactivos aniónicos es que el sulfato y los sulfonatos son completamente aniónicos (pKa ~<0) en todo el rango de pH ambiental (pH4-9), mientras que los carboxilatos son ácidos más débiles que aún son especies parcialmente neutras (pKa ~5). La mayoría de los tensioactivos catiónicos se basan en grupos principales de amonio cuaternario cargados permanentemente (R- (N+) (CH 3) 3), aunque también se aplican varios grupos amina ionizables en tensioactivos catiónicos (por ejemplo, dietanolaminas).
La propiedad de ingrediente clave de la mayoría de los surfactantes es la concentración micelar crítica (CMC), que define la concentración disuelta por encima de la cual comienzan a formarse agregados micelares que pueden eliminar la grasa o emulsionar completamente las partículas. El CMC disminuye proporcionalmente con la longitud de la cola hidrofóbica, y esto significa que con colas más largas, se necesita menos surfactante para comenzar a formar micelas. Sin embargo, al aumentar las colas hidrófobas, los tensioactivos aniónicos precipitan más fácilmente con cationes inorgánicos disueltos como el calcio. Además, la toxicidad del surfactante aumenta proporcionalmente con las longitudes de cola hidrófobas. Si la cadena alquílica es demasiado larga, el surfactante puede unirse fuertemente a todo tipo de superficies y no estar disponible para la formación de micelas. La longitud óptima de la cadena hidrofóbica suele ser, por lo tanto, un equilibrio entre las propiedades deseadas del tensioactivo y varios procesos críticos que influyen en la eficiencia y el riesgo de los tensioactivos.
Referencias
Kümmerer, K. (2007). Sustentable desde el principio: diseño racional de moléculas por ingeniería de ciclo de vida como un enfoque importante para la farmacia verde y la química verde. Química Verde 9, 899-907. DOI: 10.1039/b618298b
Giolando, S.T., Rapaport, R.A., Larson, R.J., Federle, T.W., Stalmans, M., Masscheleyn P. (1995). Destino ambiental y efectos del DEEDMAC: Un nuevo surfactante catiónico rápidamente biodegradable para su uso en suavizantes de telas. Quimosfera 30, 1067-1083. DOI: 10.1016/0045-6535 (95) 00005-S
Czajka, A., Hazell, G., Eastoe, J. (2015). Tensioactivos en el Límite de Diseño. Langmuir 31, 8205−8217. DOI: 10.1021/acs.langmuir.5b00336
Comité Científico de Toxicidad, Toxicidad y Medio Ambiente (CSTEE) (2001). Dictamen sobre los resultados de la Evaluación de Riesgos de: Cloruro de dimetildioctadecilamonio (DODMAC). Informe de la UE C2/JCD/CSTEEOP/DODMACH22022002/d (02) https://ec.europa.eu/health/archive/ph_risk/committees/sct/documents/out143_en.pdf
Van Herwijnen, R. (2009). Límites de riesgo ambiental para DODMAC y DHTDMACRIVM Informe de carta 601782029 - https://www.rivm.nl/bibliotheek/rapporten/601782029.pdf
Intentar buscar literatura de toxicidad para la formulación pesticida Roundup y comparar las toxicidades aparentes del ingrediente activo glifosato y el surfactante adyuvante a organismos no diana. ¿Qué notas?
Los tensioactivos no solo se acumulan en la interfaz aire-agua, sino también en las interfaces agua-disolvente. El coeficiente de partición octanol-agua es una propiedad crítica para la evaluación de riesgos, pero ¿puede aportar razones por las que esta propiedad es problemática para ser derivada y aplicada a surfactantes?
Aunque los detergentes están diseñados para ser fácilmente biodegradables, algunos compuestos parecen ser pseudo-persistentes ya que todavía se encuentran en niveles detectables cerca de la salida de las tuberías de efluentes de tratamiento de aguas residuales. ¿Qué crees que se entiende con esto?
2.3.9. Aditivos para alimentos y piensos
En preparación


