29.1: Propiedades de los Fluidos Supercríticos
- Page ID
- 78674
Como se muestra en la Figura 29.1.1 , un fluido supercrítico es una especie mantenida a una temperatura y una presión que excede su punto crítico. En estas condiciones la especie no es ni un gas ni un líquido. En cambio, es un fluido supercrítico.
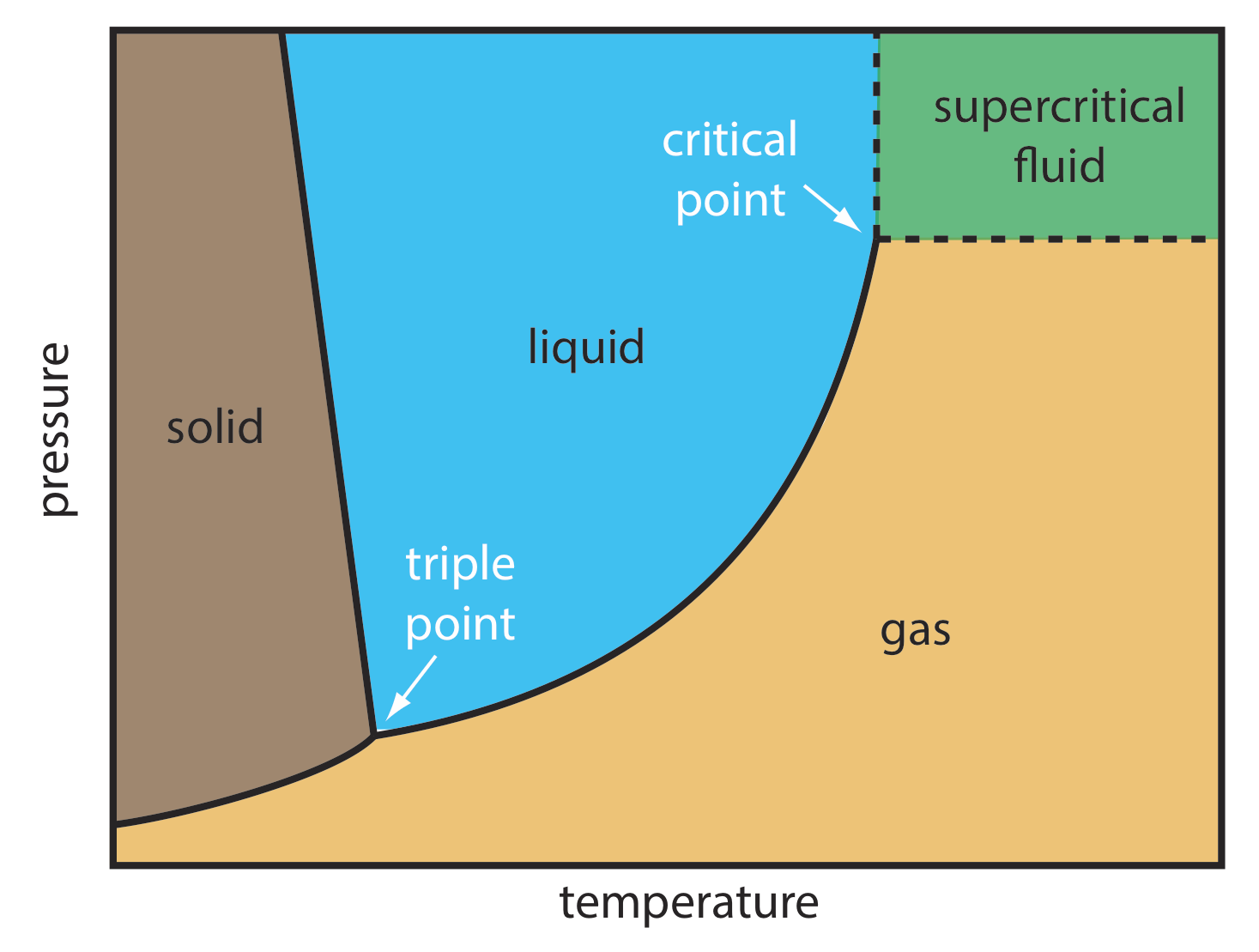
Algunas propiedades de un fluido supercrítico, como se muestra en la Tabla 29.1.1 , son similares a un gas; otras propiedades, sin embargo, son similares a un líquido. La viscosidad de un fluido supercrítico, por ejemplo, es similar a un gas, lo que significa que podemos mover un fluido supercrítico a través de una columna capilar o una columna empaquetada sin necesidad de altas presiones. La densidad de un fluido supercrítico, por otro lado, es mucho más cercana a la de un líquido, lo que explica por qué los fluidos supercríticos son buenos solventes.
| fase | densidad (g/cm 3) | viscosidad (g cm -1 s -1) | coeficiente de difusión (cm 2 s -1) |
|---|---|---|---|
| gas | \(\approx 10^{-3}\) | \(\approx 10^{-4}\) | \(\approx 0.1\) |
| fluido supercrítico | \(\approx 0.1 - 1\) | \(\approx 10^{-4} - 10^{-3}\) | \(\approx 10^{-4} - 10^{-3}\) |
| líquido | \(\approx 1\) | \(\approx 10^{-2}\) | \(\approx 10^{-3}\) |
El fluido supercrítico más utilizado es el CO 2. Su baja temperatura crítica de 31.1 o C y su baja presión crítica de 72.9 atm son relativamente fáciles de lograr y mantener. Aunque el CO 2 supercrítico es un buen disolvente para los orgánicos no polares, es menos útil para los solutos polares. La adición de un modificador orgánico, tal como metanol, mejora la fuerza de elución de la fase móvil. Otras fases móviles comunes y sus temperaturas y presiones críticas se enumeran en la Tabla 29.1.2 .
| compuesto | temperatura crítica (o C) | presión crítica (atm) |
|---|---|---|
| dióxido de carbono | 31.3 | 72.9 |
| etano | 32.4 | 48.3 |
| óxido nitroso | 36.5 | 71.4 |
| amoníaco | 132.3 | 111.3 |
| éter dietílico | 193.6 | 36.3 |
| isopropanol | 235.3 | 47.0 |
| metanol | 240.5 | 78.9 |
| etanol | 243.4 | 63.0 |
| agua | 374.4 | 226.8 |


