3.3: Propiedades Eléctricas del Agua Pura
- Page ID
- 69716
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \) \( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)\(\newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\) \( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\) \( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\) \( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\) \( \newcommand{\Span}{\mathrm{span}}\) \(\newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\) \( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\) \( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\) \( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\) \( \newcommand{\Span}{\mathrm{span}}\)\(\newcommand{\AA}{\unicode[.8,0]{x212B}}\)
Propiedades Eléctricas del Agua Pura
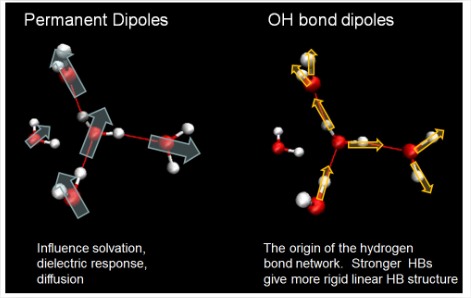
El movimiento de los dipolos del agua guían casi todo lo que sucede en el líquido. Dos contribuciones importantes:
- El momento dipolo permanente de la molécula se encuentra en el eje de simetría.
- Momentos dipolares inducidos (polarización) a lo largo de los enlaces de hidrógeno. El fortalecimiento del enlace de hidrógeno aumenta\(r_{OH}\) y disminuye\(R_{OO}\), lo que aumenta el momento dipolar. El momento dipolar por molécula cambia de 1.7 a 3.0 D pasando de fase gaseosa a líquida.
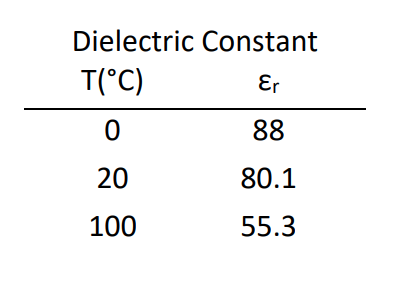
Respuesta dieléctrica de agua
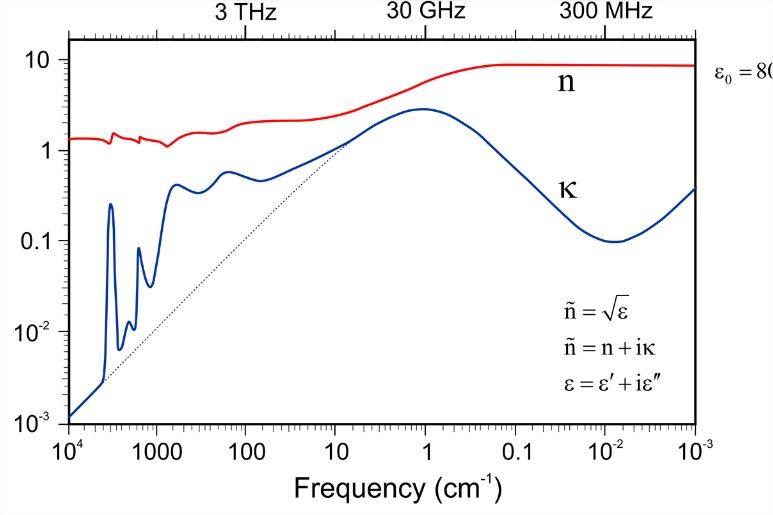
El agua pura es un medio dieléctrico fuerte, lo que significa que las fuerzas electrostáticas de largo alcance que actúan entre dos cargas en el agua se reducen drásticamente. La constante dieléctrica estática es\(\varepsilon = 80\), también conocida como la permitividad relativa\(\varepsilon_r = \varepsilon /\varepsilon_0\). La respuesta dieléctrica depende fuertemente de la frecuencia y la temperatura. Movimiento de cargas de agua codificadas en constante dieléctrica compleja (\(\varepsilon\)) o índice de refracción (\(\tilde{n}\)).
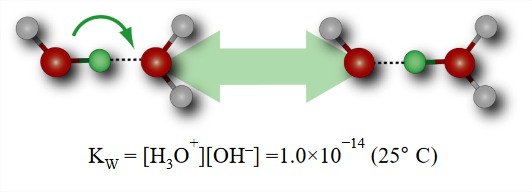
Autoionización de agua y pH
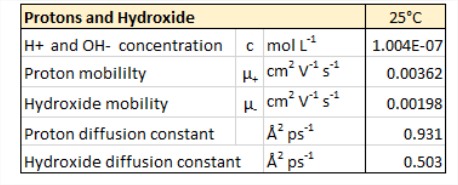
- Los protones y el hidróxido gobiernan la química ácido-base.
- Cualquier molécula de agua a granel vive aproximadamente 10 horas antes de disociarse.
- En un litro, una molécula de agua se disocia cada 30 microsegundos.
Protones en el agua
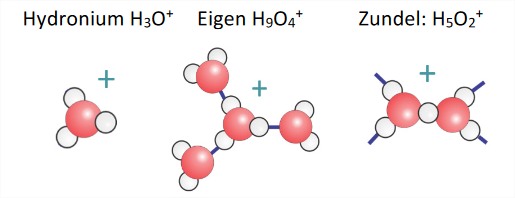
- La estructura del agua y la medida\(H^+\) en que se deslocaliza el exceso de carga sigue sin resolverse. Se asocia lo suficientemente fuerte como para describirse como de interacción covalente, pero su evolución temporal es tan rápida (<1 ps) que es difícil definir una estructura.
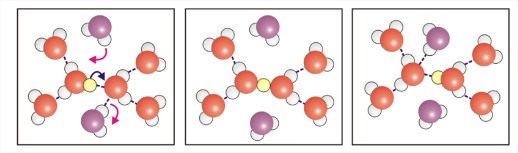
- Movilidad mucho mayor de lo esperado por difusión de un catión de tamaño similar.
- Explicado por Grotthus mecanismo para la transferencia de protones a moléculas de agua vecinas.
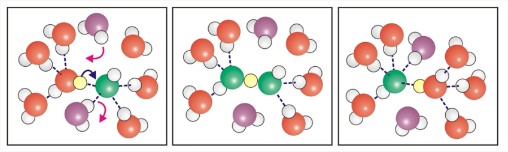
- OH — también es muy móvil y actúa como aceptor de protones del agua.
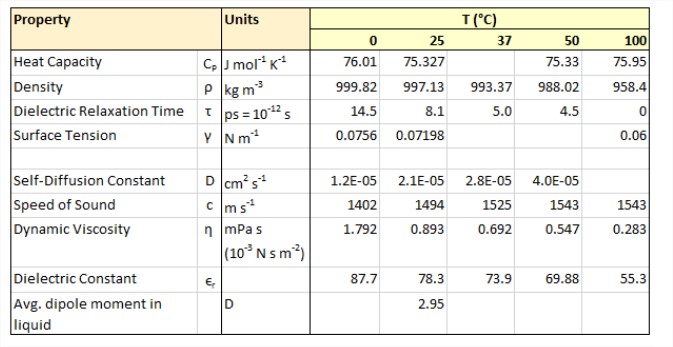
Propiedades Físicas del Agua