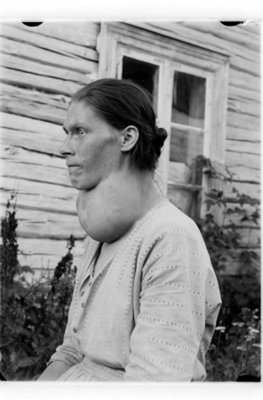
2.4.1: Alimentos- Los Nutrientes Minerales Potasio y Yodo
- Page ID
- 74901
En una sección anterior sobre Dieta elemental observamos minerales esenciales que a veces se llaman “elementos”, pero que en realidad solo son utilizables para nuestros cuerpos cuando se suministran como “compuestos”. Tanto el potasio como el yodo son nutrientes esenciales, pero cada uno debe ser suministrado en un compuesto si va a ser de algún uso (y mucho menos no tóxico) para el organismo. La deficiencia de yodo conduce a disfunción tiroidea y bocio, pero se requiere muy poco yodo, por lo que el bocio es raro. [1] La deficiencia de potasio (hipopotasemia, después de kallium, el nombre alemán para el potasio y fuente del símbolo, K) conduce a debilidad muscular, calambres y estreñimiento [2]. Las dietas recomendadas (RDA) para yodo y potasio son 150 µg y 4700 mg respectivamente, por lo que necesitamos alrededor de 30,000 veces más potasio que yodo. Por suerte, la mayoría de los alimentos (especialmente naranjas, patatas y plátanos) suministran potasio, y el KI solo es necesario como terapia.
|
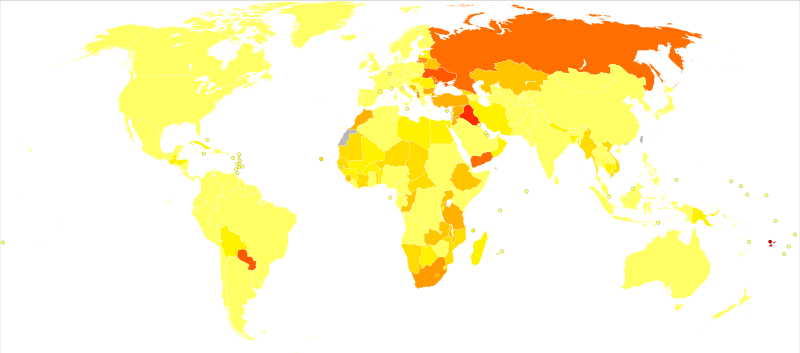
La deficiencia de yodo varía de <50 por 100,000 individuos (amarillo) a más de 800 (rojo) [3]
|
Bocio
|
Como vimos anteriormente, el elemento yodo I 2 es un sólido cristalino tóxico, púrpura, mientras que el nutriente debe ser suministrado como parte de un compuesto, como el yoduro de potasio (KI). El yodo tiene un punto de fusión de tan solo 113 o C, donde también se vaporiza significativamente, y hierve a tan solo 184.3 o C. El yodo tiene una alta densidad de 4.93 g/cc. Veremos a continuación que KI tiene propiedades completamente diferentes.
De igual manera, el elemento potasio (K) es un metal con la menor densidad (0.89 g/cc) de cualquier metal excepto el litio. Corta como mantequilla, tiene un punto de fusión de sólo 63.38 o C y un punto de ebullición de 759 o C. En el sólido, los átomos de K están dispuestos en la red que se muestra a continuación. El potasio reacciona explosivamente con el agua como se muestra en el siguiente video o en YouTube:
Jmol cúbico centrado en el cuerpo: SID10534500
Debido a la toxicidad y reactividad del elemento potasio, las fuentes nutritivas deben contener el potasio en un compuesto como el yoduro de potasio, KI, donde tiene propiedades completamente diferentes. El yoduro de potasio es un sólido cristalino blanco que se ve y sabe a sal de mesa (NaCl), se disuelve en agua, tiene un punto de fusión de 631 o C, y un punto de ebullición de 1330 o C. Se utiliza, junto con yoduro de sodio (NaI) para “yodar” la sal.
|
Potasio metálico, K (el elemento)
|
Yodo, I 2 (el elemento))
|
Yoduro de potasio, KI (el nutriente mineral)
|
| Esta opción no funcionará correctamente. Desafortunadamente, su navegador no admite marcos en línea. |
Violeta, yodo sólido (I 2) |
Yoduro de potasio cristalino blanco |
-
-
- 2 K (s) + I 2 (s) → 2 KI (c)
-
-
-
- Reactivos → Productos
-
Aquí tenemos tres visiones de una misma reacción: En la parte superior, la apariencia macroscópica de los reactivos y productos; debajo de ellos, la representación a nivel microscópico o atómico de los átomos o moléculas; y finalmente, una represenación simbólica en forma de ecuación química. El estado sólido de los reactivos se indica con la “s” entre paréntesis, y el estado cristalino del producto se indica con “(c)”. Los líquidos se designan por (l), los gases por (g) y las soluciones acuosas (agua) como (ac).
Esta ecuación puede interpretarse microscópicamente en el sentido de que 1 átomo de potasio y 1 molécula de yodo reaccionan para formar 2 unidades de yoduro de potasio, pero no existe tal cosa como una unidad KI aislada. Más bien, hay una red extendida de iones K 1+ y iones I 1- alternantes.
Cuando los elementos potasio y yodo se calientan juntos, reaccionan aún más enérgicamente que el potasio y el agua, para dar el compuesto KI de acuerdo con la ecuación anterior.
Esto ilustra el tercer postulado de Dalton, que establece que los átomos son las unidades de los cambios químicos. Observe que hay tantos átomos de potasio después de la reacción como antes de la reacción. Lo mismo se aplica a los átomos de yodo. Los átomos no fueron creados, destruidos, divididos en partes, o cambiados en otros tipos de átomos durante la reacción química. La ecuación química equilibrada refuerza esta idea.
La vista de KI sólida mostrada anteriormente es nuestro primer ejemplo microscópico de un compuesto. Un compuesto se compone de dos (o más) tipos diferentes de átomos. Dado que estos átomos pueden reordenarse durante una reacción química, el compuesto se puede descomponer en dos (o más) elementos diferentes. La relación 1:1 de átomos de K a átomos I implícita en la fórmula KI (se supone el subíndice “1", por lo que KI = K 1 I 1) concuerda con el cuarto postulado de Dalton de que los átomos se combinan en la proporción de números enteros pequeños.
Referencias
- es.wikipedia.org/wiki/Bocio
- es.wikipedia.org/wiki/Hipopotalemia
- es.wikipedia.org/wiki/Bocio