5.4: La naturaleza de onda del electrón
- Page ID
- 75415
Desarrollo Histórico
Al mismo tiempo que Lewis desarrollaba sus teorías sobre la estructura electrónica, el físico Niels Bohr estaba desarrollando una imagen similar, pero más detallada, del átomo.
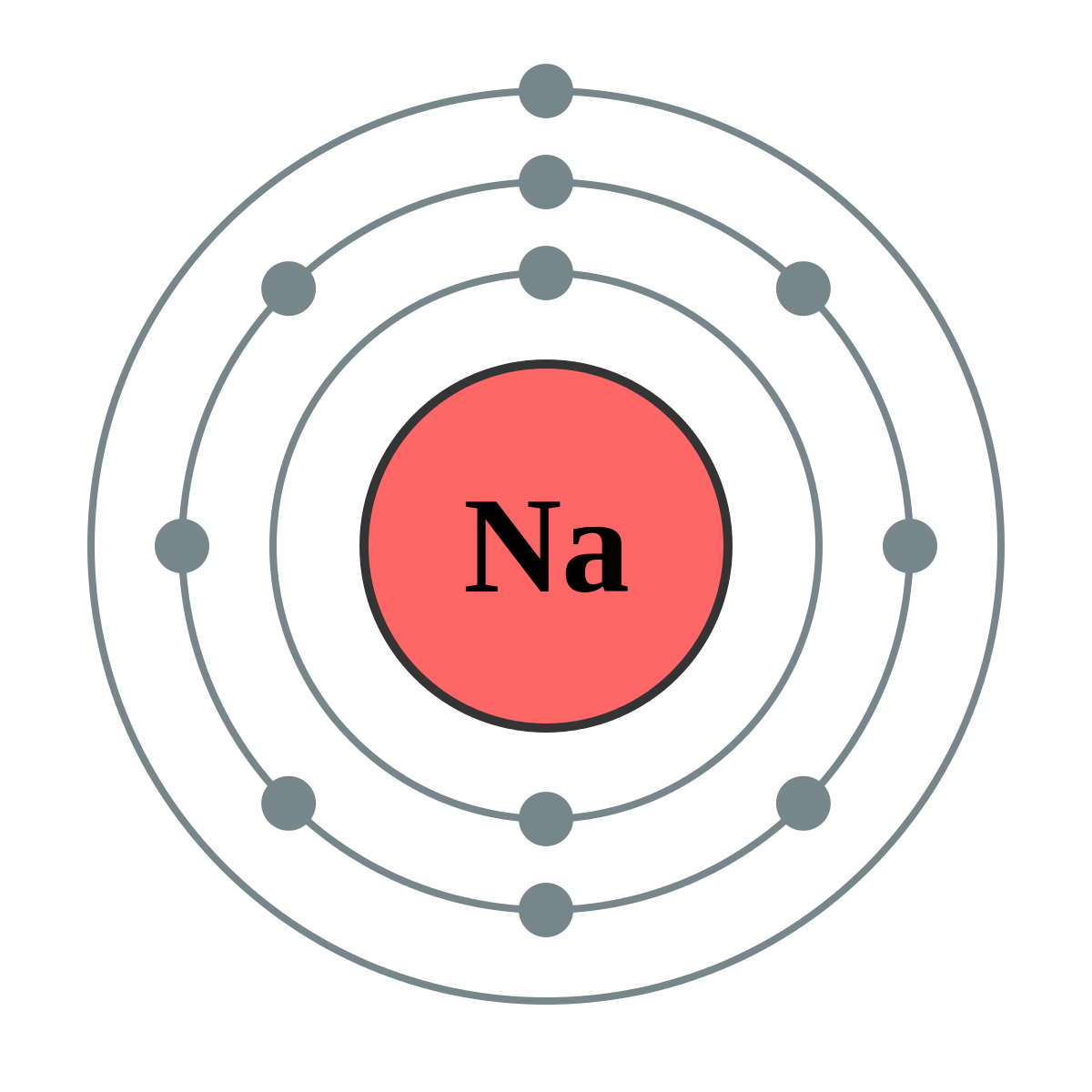
Dado que Bohr estaba interesado en la luz (energía) emitida por los átomos bajo ciertas circunstancias más que en la valencia de los elementos, particularmente quería poder calcular las energías de los electrones. Para ello, necesitaba conocer el camino exacto seguido por cada electrón a medida que se movía alrededor del núcleo. Asumió caminos similares a los de los planetas alrededor del sol. La figura vista arriba ilustra las teorías de Bohr aplicadas al átomo de sodio. Observe cómo el modelo de Bohr, al igual que el de Lewis, asume una estructura de caparazón. Hay dos electrones en la capa más interna, ocho electrones en la siguiente capa y un solo electrón en la capa más externa.
Al igual que el modelo de Lewis, el modelo de Bohr solo tuvo éxito parcial. Explicó algunos resultados experimentales pero fue bastante incapaz de dar cuenta de otros. En particular falló en el nivel matemático cuantitativo. La teoría de Bohr funcionó muy bien para un átomo de hidrógeno con su solo electrón, pero los cálculos sobre átomos con más de un electrón siempre dieron la respuesta equivocada. A nivel químico, también, ciertas características fueron inadecuadas. No hay evidencia que sugiera que los átomos de sodio sean siempre tan alargados o planos como el de la figura. Por el contrario, la forma en que los átomos de sodio se agrupan en un sólido sugiere que se extienden uniformemente en todas las direcciones; es decir, son de forma esférica. Otra debilidad en la teoría era que tenía que asumir una estructura de caparazón en lugar de explicarla. Después de todo, no hay nada en la naturaleza de los planetas que se mueven alrededor del sol que los obligue a orbitar en grupos de dos u ocho. Bohr asumió que los electrones se comportan de manera muy parecida a los planetas; entonces, ¿por qué deberían formar conchas de esta manera?
Una manera de explicar el hecho de que se cuantifican las energías de electrones, o de explicar por qué se puede decir que los electrones existen en conchas particulares, es sugerir que se comportan como ondas estacionarias. Desde la “música de las esferas” de Pitágorus hemos notado que las ondas en una cuerda (como una cuerda de guitarra) producen sólo ciertos tonos o tonos definidos numéricamente. Podemos usar un modelo de onda para explicar por qué es así, para una cuerda que se fija en ambos extremos.
Olas Viajeras
Si mueves una cuerda, una onda viajera se mueve hacia abajo; si haces esto continuamente, digamos una vez por segundo, generas un tren de ondas itinerantes con una frecuencia de 1 s -1, o una longitud de onda por segundo, donde la longitud de onda es la distancia entre picos sucesivos (o cualquier otra característica repetitiva) de la onda:
 Imagen cortesía de Crash Course Physics
Imagen cortesía de Crash Course Physics
Existe una relación entre la frecuencia, generalmente denotada “ν” (“nu”), la longitud de onda, generalmente denotada “λ” (lambda) y la velocidad que la onda se mueve hacia abajo por la cuerda (o a través del espacio, si es una onda de luz). Si denotamos la velocidad “c” (un símbolo utilizado para la velocidad de la luz), la relación es:
\[\lambda =\dfrac{c}{ u} \label{1} \]
Calcular la longitud de onda de un microondas en un horno microondas que viaja a la velocidad de la luz, c = 3.0 x 10 8 m s -1> y tiene una longitud de onda de 2.45 GHz (2.45 x 10 9 s -1) de 12.24 cm.
Solución
Reordenando\(\ref{1}\) tenemos:
\[ u =\dfrac{c}{\lambda} \dfrac{\text{3.0}\times \text{10}^{\text{8}}\text{m s}^{\text{-1}}}{\text{2.45}\times\text{10}^{9}\text{s}^{\text{-1}}} = 0.1224\; m = 12.24\, cm \nonumber \]
Las microondas son ondas como ondas de luz u ondas de radio, pero su longitud de onda es mucho más larga que la luz, y más corta que la radio. Las ondas de esta longitud de onda interactúan con las moléculas de agua hacen que las moléculas giren más rápido y, por lo tanto, calientan los alimentos
Ondas de pie y de viaje
Si la cuerda que estamos moviendo se sostiene en un extremo y se ata en el otro extremo, las ondas se reflejan hacia atrás, y el movimiento hacia atrás interactúa con las ondas hacia adelante para crear un patrón de interferencia constructivo que parece no moverse. Se llama onda estacionaria:
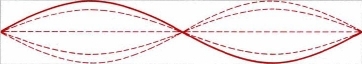 Onda estacionaria 1
Onda estacionaria 1
 Onda estacionaria 2
Onda estacionaria 2
Pero algunas frecuencias no están permitidas (¡no queremos que la guitarra toque todos los tonos a la vez!). Ocurre en situaciones como esta:
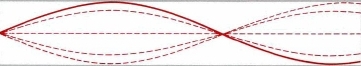
Por lo que el patrón de onda estacionaria va de la onda estacionaria 1 a la onda estacionaria 2, y no puede existir en ninguna parte intermedia. ¡Ese es exactamente el comportamiento que encontramos para los electrones en las conchas! . Los electrones no existen en ninguna parte entre las conchas.
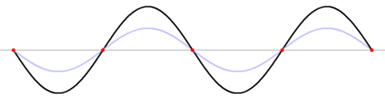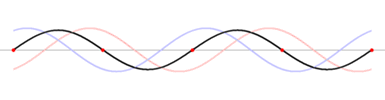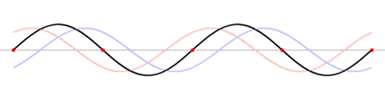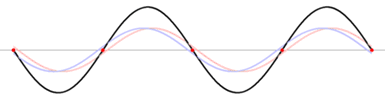
Tenga en cuenta que los “nodos” (donde no hay movimiento) no se mueven, sino que los “antinodos” vibran hacia arriba y hacia abajo, por lo que la posición exacta de la cuerda no es fija. En la siguiente sección se muestran varias ondas estacionarias más; todas ellas tienen frecuencias particulares que dan cuenta de las notas específicas producidas por una cuerda de guitarra de particular longitud, o cuando la cuerda está “trastada”, por ejemplo. Aquí se muestran videos de otra onda estacionaria.
Energía de la Luz
Por lo general, pensamos en las conchas de electrones en términos de su energía. Eso se debe a que la energía luminosa se emite cuando un electrón cae de un caparazón superior a uno inferior, y medir la energía lumínica es la forma más importante de determinar la diferencia de energía entre las conchas. Cuando los electrones cambian de nivel, emiten cuantos de luz llamados “fotones”). La energía de un fotón está directamente relacionada con su frecuencia, o inversamente relacionada con la longitud de onda:
\[\text{E} = \text {h} u =\dfrac{\text{h} \text{c}}{\lambda} \label{2} \]
La constante de proporcionalidad h se conoce como constante de Planck y tiene el valor 6.626 × 10 —34 J s. La luz de mayor frecuencia tiene mayor energía y longitud de onda más corta.
La luz solo puede ser absorbida por los átomos si cada fotón tiene exactamente la cantidad correcta de energía para promover un electrón de una capa inferior a una superior. Si se requiere más energía de la que posee un fotón, no se puede suministrar bombardeando el átomo con más fotones. Por lo que frecuentemente encontramos que la luz de una longitud de onda provocará un cambio fotoquímico por tenue que sea, mientras que la luz de una longitud de onda vecina no provocará un cambio fotoquímico por muy intensa que sea. Eso es porque los fotones deben ser absorbidos para provocar un cambio fotoquímico, y deben tener exactamente la energía necesaria para ser promovidos al siguiente caparazón para ser absorbidos. Si no son absorbidos, no importa cuán intensa sea la luz (cuántos fotones hay por segundo).
¿Qué longitud de onda de luz es emitida por un átomo de hidrógeno cuando un electrón cae de la tercera concha, donde tiene E = -2.42088863 × 10 -19 J, a la segunda concha, donde tiene E = -5.44739997 × 10 -19 J?
Solución
ΔE = E 2 - E 1 = (-5.45 × 10 -19) - (-2.42 × 10 -19 J) = -3.03 × 10 -19 J.
Tenga en cuenta que los niveles de energía se vuelven más negativos (se libera más energía cuando un electrón cae en ellos) cerca del núcleo, y la diferencia aquí es negativa, es decir, se libera energía. Tomando el valor absoluto de la energía para calcular la energía del fotón, y reordenando la ecuación\(\ref{2}\):
\[\lambda =\dfrac{\text{h}\times\text{c}}{E} \nonumber \]
\[λ = \dfrac{(6.626 \times 10^{–34}\; J\; s)(3 \times 10^8)}{3.03 \times 10^{-19}\;J} = 6.56 \times 10^{-7}\; m \nonumber \]
o
\[λ = 656\; nm \nonumber \]
Esta es la longitud de onda de la luz roja.
Ondas estacionarias bidimensionales
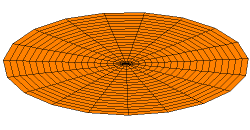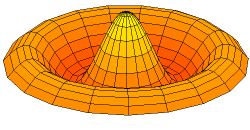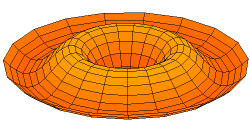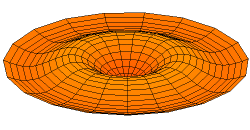
Por supuesto, las conchas para electrones son tridimensionales, no unidimensionales como las cuerdas de guitarra. Podemos comenzar a visualizar ondas estacionarias en más de una dimensión pensando en patrones de onda en una piel de tambor en dos dimensiones. Algunos de los patrones de onda se muestran a continuación. Si miras cuidadosamente, verás nodos circulares que no se mueven en los Modos 2 y 3:
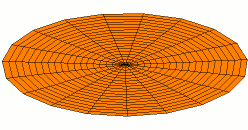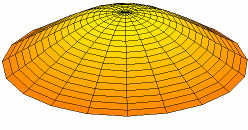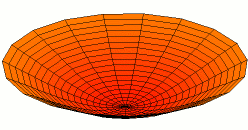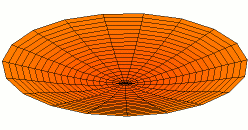
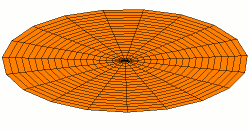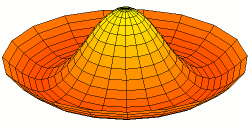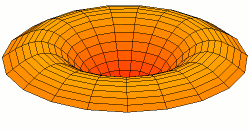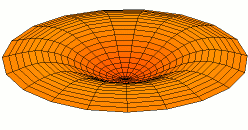
La forma de los orbitales
Los electrones existen alrededor del núcleo en “orbitales”, que son ondas estacionarias tridimensionales. Las ondas estacionarias de electrones son bastante hermosas, y veremos más de ellas en las próximas secciones. Un ejemplo es la flor como “f orbital” a continuación. Aquí las partes rojas de la “función de onda” representan partes matemáticamente positivas (hacia arriba) de la onda estacionaria, mientras que las partes azules son partes matemáticamente negativas (hacia abajo):
![] La representación tridimensional de los orbitales f muestra cuatro sólidos en forma de frijol en el centro. Cuatro sólidos significativamente más grandes en forma de frijol se encuentran en cada esquina. La posición del frijol alterna entre rojo y azul.](https://chem.libretexts.org/@api/deki/files/311701/600px-D4M1.png)


