10.5: Estructuras empaquetadas más cercanas
- Page ID
- 76061
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Una clase importante de estructuras cristalinas se encuentra en muchos metales y también en los gases nobles solidificados donde los átomos (que son todos iguales) se empaquetan lo más cerca posible. La mayoría de nosotros estamos familiarizados con el proceso de empaquetar esferas juntas, ya sea de jugar con canicas o BB de niños o de intentar apilar naranjas u otra fruta redonda en una pirámide. Sobre una superficie nivelada podemos disponer fácilmente una colección de esferas del mismo tamaño en una capa hexagonal muy compacta en la que cada esfera está tocando a seis de sus compañeros, como se ve Figura\(\PageIndex{1}\).

Entonces podemos agregar una segunda capa para que cada esfera agregada se acurruque en una depresión entre tres esferas en la capa de abajo. Dentro de esta segunda capa cada esfera también entra en contacto con seis vecinos, y la capa es idéntica a la primera. Parece que podemos agregar capa tras capa indefinidamente, o hasta que nos quedemos sin esferas. Cada esfera estará tocando a doce de sus compañeros ya que está rodeada por seis en el mismo plano y se anida entre tres en el plano de arriba y tres en el plano de abajo. Decimos que cada esfera tiene un número de coordinación de 12. Es imposible hacer cualquier otra estructura con un número de coordinación mayor, es decir, empacar más esferas dentro de un volumen dado. Por consiguiente, la estructura que se acaba de describir se denomina a menudo una estructura empaquetada más cerca. El níquel, que se muestra a continuación, es un ejemplo de un metal con una estructura empaquetada más cercana.

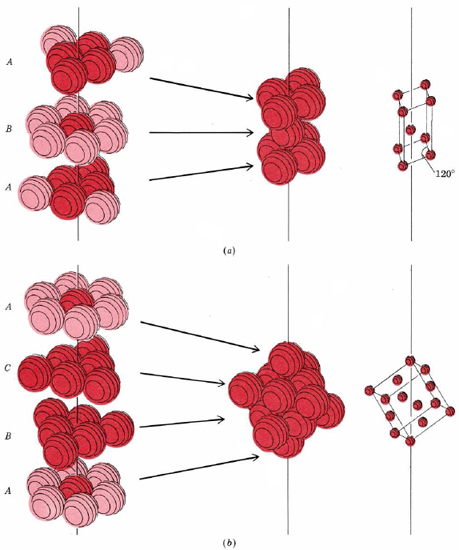
En la parte a de\(\PageIndex{2}\) la Figura la primera capa de esferas ha sido etiquetada A y B para indicar que las esferas de la segunda capa no están directamente por encima de las del puño. La tercera capa se encuentra directamente por encima de la primera, y por lo tanto está etiquetada como A. Si seguimos en la manera mostrada, agregando alternativamente A, luego B, luego A capas, obtenemos una estructura cuya celda unitaria (mostrada en la parte a) tiene dos lados iguales con un ángulo de 120° entre ellos. Otros ángulos son de 90°, por lo que la celda pertenece al sistema de cristales hexagonales. De ahí que esta estructura se llame hexagonal más cercana empaquetada (hpc). Un ejemplo de un metal con una estructura HPC es el Magnesio, que se muestra a continuación.

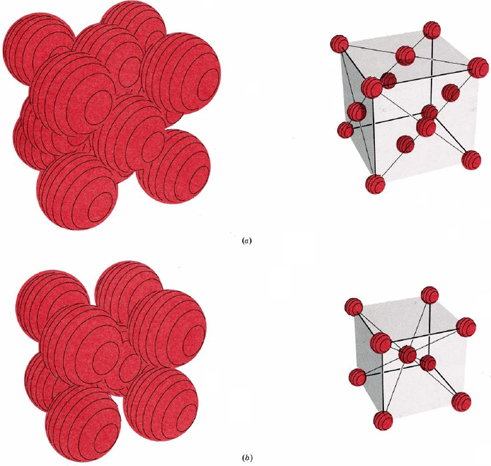
También se muestra en la Figura\(\PageIndex{3}\) la celda unitaria de una estructura llamada cúbica centrada en el cuerpo (bcc). Esto es similar a la estructura fcc excepto que, en lugar de esferas en las caras, hay una sola esfera en el centro del cubo. Esta esfera central está rodeada por ocho vecinos en las esquinas de la celda unitaria, dando un número de coordinación de 8. Por lo tanto, la estructura de bcc no es tan compacta como las estructuras empaquetadas más cercanas que tenían un número de coordinación 12. Sin embargo, se encontró que algunos metales tienen estructuras de bcc.
Cuente el número de esferas en la celda unitaria de (a) una estructura cúbica centrada en la cara y (b) una estructura cúbica centrada en el cuerpo.
Solución
Haciendo referencia a la última figura y usando la ecuación:
\[N=N_{\text{body}}\text{ + }\frac{N_{\text{face}}}{\text{2}}\text{ + }\frac{N_{\text{edge}}}{\text{4}}\text{ + }\frac{N_{\text{corner}}}{\text{8}} \nonumber \]
encontramos
b)\[N=\text{1 + 0 + 0 + }\frac{\text{8}}{\text{8}}=\text{2} \nonumber \]
El silicio tiene la misma estructura cristalina que el diamante. Ahora hay técnicas disponibles para cultivar cristales de este elemento que son prácticamente impecables. El análisis de algunos de estos cristales perfectos encontró que el lado de la celda unitaria tenía 543.102064pm de largo. La celda unitaria es un cubo que contiene ocho átomos de Si, pero es una de las celdas cúbicas simples discutidas ya. A partir de la composición isotópica, masa molar y densidad de los cristales, se determinó que un mol de Si en esta forma cristalina tiene un volumen de 12.0588349×10 -6 m 3. Determine N A partir de estos datos.
Solución Este problema utiliza el conocimiento de la estructura cristalina de silicio para determinar N A. A partir de la longitud del borde, podemos obtener el volumen de la celda unitaria cúbica. Sabemos que la unidad contiene ocho átomos, y como conocemos el volumen de un mol, podemos calcular N A, con la constante Avogadro definida como el número de partículas por unidad de cantidad de sustancia.
\[N_{A}= \frac{N*V_{\text{m}}}{V_{\text{unit cell}}}=\frac{8\times{12.0588349}\times{10}^{-6}\text{m}^{3}}{({ 543.102064}\times{10}^{-12}\text{m})^{3}}={6.02214179}\times{10}^{23} \nonumber \]
Los valores utilizados para determinar este valor fueron tomados de cristales usando Densidad de Cristal de Rayos X (XRCD), para determinar la longitud lateral. Estos valores fueron utilizados en el análisis más reciente publicado por el Comité de Datos para la Ciencia y la Tecnología (CODATA) [1], que estandariza definiciones de constantes y unidades científicas importantes. El valor que acabas de calcular es, por lo tanto, la determinación más precisa de la constante de Avogadro en este momento.
- Mohr, P.J., Taylor, B.N., y D. B. Newell. “CODATA Valores Recomendados de las Constantes Físicas Fundamentales: FCKLR2006.” Instituto Nacional de Estándares y Tecnología. 28 de diciembre de 2007. Constantes [physics.nist.gov]


