7.4: Oligoelementos en sistemas biológicos
- Page ID
- 78297
- Describir algunos de los roles de los oligoelementos en los sistemas biológicos.
De los más de 100 elementos conocidos, se sabe que aproximadamente 28 son esenciales para el crecimiento de al menos una especie biológica, y solo 19 son esenciales para los humanos. ¿Qué hace que algunos elementos sean esenciales para un organismo y el resto no esenciales? Hay al menos dos razones:
- El elemento debe tener alguna propiedad química única que un organismo pueda utilizar en su beneficio y sin la cual no pueda sobrevivir.
- Las cantidades adecuadas del elemento deben estar disponibles en el ambiente en una forma fácilmente accesible.
Como puede ver en el Cuadro 7.6, muchos de los elementos que abundan en la corteza terrestre no se encuentran, sin embargo, en una forma fácilmente accesible (por ejemplo, como iones disueltos en el agua de mar). En cambio, tienden a formar óxidos, hidróxidos o sales de carbonato insolubles. Si bien el silicio es el segundo elemento más abundante en la corteza terrestre, el SiO 2 y muchos minerales de silicato son insolubles, por lo que no son fácilmente absorbidos por los tejidos vivos. Este es también el caso del hierro y el aluminio, que forman hidróxidos insolubles. Por lo tanto, muchos organismos han desarrollado estrategias elaboradas para obtener hierro de su entorno. Por el contrario, el molibdeno y el yodo, aunque no son particularmente abundantes, son altamente solubles—molibdeno como molibdato (MoO 4 2−) y yodo como yoduro (I −) y yodato (IO 3 −) y por lo tanto son más abundantes en agua de mar que en hierro. No es sorprendente que tanto el molibdeno como el yodo sean utilizados por muchos organismos.
Cuadro 7.6 Abundancia relativa de algunos elementos esenciales en la corteza terrestre y los océanos
| Elemento* | Corteza (ppm; promedio) | Agua de mar (mg/L = ppm) |
|---|---|---|
| *Se sabe que los elementos en negrilla son esenciales para los humanos. | ||
| O | 461,000 | 857.000 |
| Si | 282,000 | 2.2 |
| Al | 82,300 | 0.002 |
| Fe | 56,300 | 0.002 |
| Ca | 41,500 | 412 |
| Na | 23,600 | 10,800 |
| Mg | 23,300 | 1290 |
| K | 20,900 | 399 |
| H | 1400 | 108,000 |
| P | 1050 | 0.06 |
| Mn | 950 | 0.0002 |
| F | 585 | 1.3 |
| S | 350 | 905 |
| C | 200 | 28 |
| Cl | 145 | 19,400 |
| V | 120 | 0.0025 |
| Cr | 102 | 0.0003 |
| Ni | 84 | 0.00056 |
| Zn | 70 | 0.0049 |
| Cu | 60 | 0.00025 |
| Co | 25 | 0.00002 |
| Li | 20 | 0.18 |
| N | 19 | 0.5 |
| Br | 2.4 | 67.3 |
| Mo | 1.2 | 0.01 |
| I | 0.45 | 0.06 |
| Se | 0.05 | 0.0002 |
Fuente: Datos de CRC Handbook of Chemistry and Physics (2004).
Afortunadamente, muchos de los elementos esenciales para la vida son necesarios sólo en pequeñas cantidades. (El Cuadro 1.6 enumera los oligoelementos en humanos.) Aun así, los elementos que están presentes en trazas pueden ejercer grandes efectos sobre la salud de un organismo. Dichos elementos funcionan como parte de un mecanismo de amplificación, en el que una molécula que contiene un oligoelemento es una parte esencial de una molécula más grande que actúa a su vez para regular las concentraciones de otras moléculas, y así sucesivamente. El mecanismo de amplificación permite que pequeñas variaciones en la concentración del oligoelemento tengan grandes efectos bioquímicos.
Los oligoelementos esenciales en los mamíferos pueden tener cuatro roles generales: (1) pueden comportarse como macrominerales, (2) pueden participar en la catálisis de reacciones de transferencia de grupos, (3) pueden participar en reacciones de oxidación-reducción, o (4) pueden servir como componentes estructurales.
-
Macrominerales
Los macrominerales—Na, Mg, K, Ca, Cl y P— se encuentran en grandes cantidades en los tejidos biológicos y están presentes como compuestos inorgánicos, ya sea disueltos o precipitados. Todos forman iones monoatómicos (Na +, Mg 2+, K +, Ca 2+, Cl −) excepto el fósforo, que se encuentra como el ion fosfato (PO 4 3−). Recordemos que las sales de calcio son utilizadas por muchos organismos como materiales estructurales, como en el hueso [hidroxiapatita, Ca 5 (PO 4) 3 OH]; las sales de calcio también están en cáscaras de mar y cáscaras de huevo (CaCo 3), y sirven como depósito para Ca 2+ en plantas ( oxalato de calcio).
Los fluidos corporales de todos los organismos multicelulares contienen concentraciones relativamente altas de estos iones. Algunos iones (Na +, Ca 2+ y Cl −) se localizan principalmente en fluidos extracelulares como el plasma sanguíneo, mientras que K +, Mg 2+ y fosfato se localizan principalmente en fluidos intracelulares. Se requieren cantidades sustanciales de energía para transportar selectivamente estos iones a través de las membranas celulares. La selectividad de estas bombas de iones se basa en diferencias en el radio iónico (Sección 7.2) y la carga iónica.
Mantener niveles óptimos de macrominerales es importante porque los cambios temporales en su concentración dentro de una célula afectan las funciones biológicas. Por ejemplo, la transmisión de impulsos nerviosos requiere un aumento repentino y reversible en la cantidad de Na + que fluye hacia la célula nerviosa. De igual manera, cuando las hormonas se unen a una célula, pueden hacer que los iones Ca 2+ entren en esa célula. En una serie compleja de reacciones, los iones Ca 2+ desencadenan eventos como la contracción muscular, la liberación de neurotransmisores o la secreción de hormonas. Cuando las personas que hacen ejercicio vigorosamente durante largos períodos de tiempo se sobrehidratan con agua, los niveles bajos de sal en la sangre pueden resultar en una condición conocida como hiponatremia, que causa náuseas, fatiga, debilidad, convulsiones e incluso la muerte. Por esta razón, los atletas deben hidratarse con una bebida deportiva que contenga sales, no solo agua.
-
Reacciones de transferencia de grupos
Los iones de metales traza también juegan un papel crucial en muchas reacciones biológicas de transferencia de grupos. En estas reacciones, un grupo funcional reconocible, tal como una unidad de fosforilo (−PO 3 −), se transfiere de una molécula a otra. En este ejemplo,
Ecuación 7.18
ROPO 2 − 3 + H 2 O → ROH + HOPO 2 − 3una unidad se transfiere de un alcóxido (RO −) a hidróxido (OH −). Para neutralizar la carga negativa sobre la molécula que está experimentando la reacción, muchas reacciones biológicas de este tipo requieren la presencia de iones metálicos, como Zn 2+, Mn 2+, Ca 2+, o Mg 2+ y ocasionalmente Ni 2+ o Fe 3+. La efectividad del ion metálico depende en gran medida de su carga y radio.
El zinc es un componente importante de las enzimas que catalizan la hidrólisis de proteínas, la adición de agua al CO 2 para producir HCO 3 − y H +, y la mayoría de las reacciones involucradas en la síntesis, reparación y replicación. En consecuencia, la deficiencia de zinc tiene graves efectos adversos, incluyendo crecimiento anormal y desarrollo sexual y una pérdida del sentido del gusto.
-
Reacciones Biológicas de Oxidación-Reducción
Un tercer papel importante de los oligoelementos es transferir electrones en reacciones biológicas de oxidación-reducción. El hierro y el cobre, por ejemplo, se encuentran en proteínas y enzimas que participan en el transporte de O 2, la reducción de O 2, la oxidación de moléculas orgánicas y la conversión de N 2 atmosférico a NH 3. Estos metales suelen transferir un electrón por ión metálico alternando entre estados de oxidación, como 3+/2+ (Fe) o 2+/1+ (Cu).
Debido a que la mayoría de los metales de transición tienen múltiples estados de oxidación separados por un solo electrón, son especialmente adecuados para transferir múltiples electrones uno a la vez. Los ejemplos incluyen molibdeno (+6/+5/+4), que es ampliamente utilizado para reacciones de oxidación-reducción de dos electrones, y cobalto (+3/+2/+1), que se encuentra en la vitamina B 12. Por el contrario, muchos de los elementos del bloque p son muy adecuados para transferir dos electrones a la vez. El selenio (+4/+2), por ejemplo, se encuentra en la enzima que cataliza la oxidación del glutatión (GSH) a su forma disulfuro (GSSG):
\[2 GSH + H_2O_2 \rightarrow 2 H_2O + GSSG\]
-
Componentes Estructurales
Los oligoelementos también actúan como componentes estructurales esenciales de tejidos biológicos o moléculas. En muchos sistemas donde los oligoelementos no cambian los estados de oxidación ni participan directamente en reacciones bioquímicas, a menudo se asume, aunque frecuentemente sin evidencia directa, que el elemento estabiliza una estructura tridimensional particular de la biomolécula en la que se encuentra. Un ejemplo es una proteína de unión a azúcar que contiene Mn 2+ y Ca 2+ que forma parte del sistema de defensa biológica de ciertas plantas. Otros ejemplos incluyen enzimas que requieren Zn 2+ en un sitio para que la actividad ocurra en un sitio diferente en la molécula. Algunos elementos no metálicos, como F −, también parecen tener papeles estructurales. El fluoruro, por ejemplo, desplaza el ion hidróxido de la hidroxiapatita en hueso y dientes para formar fluoroapatita [Ca 5 (PO 4) 3 F]. La fluoroapatita es menos soluble en ácido y proporciona mayor resistencia a la caries dental.

La fluoroapatita (\(Ca_5(PO_4)_3F\)) es menos soluble que la hidroxiapatita (\(Ca_5(PO_4)_3(OH)\))
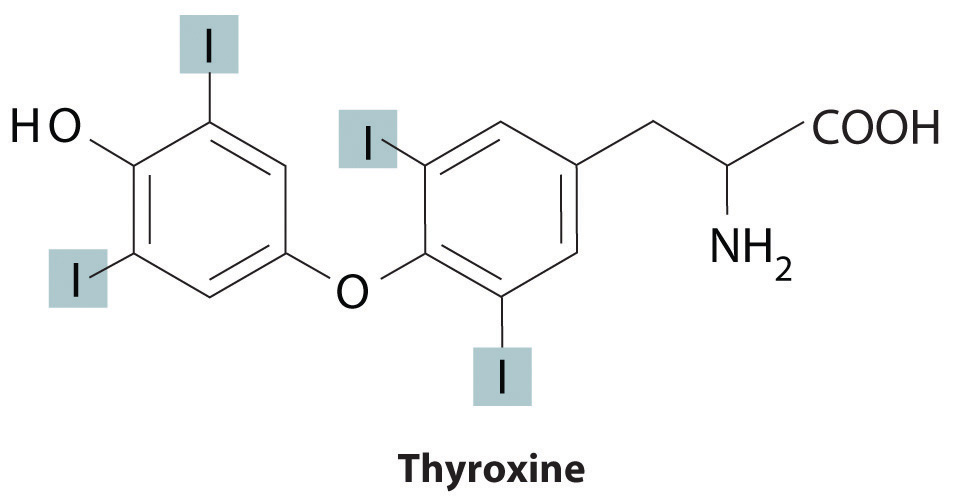
Otro ejemplo de un no metal que juega un papel estructural es el yodo, que en humanos se encuentra en una sola molécula, la hormona tiroidea tiroxina. Cuando la dieta de una persona no contiene suficiente yodo, las glándulas tiroideas en su cuello se agrandan mucho, lo que lleva a una condición llamada bocio. Debido a que el yodo se encuentra principalmente en peces oceánicos y algas marinas, muchos de los colonos originales del Medio Oeste americano desarrollaron bocio debido a la falta de mariscos en su dieta. Hoy en día la mayoría de la sal de mesa contiene pequeñas cantidades de yodo [realmente yoduro de potasio (KI)] para prevenir este problema.

Un individuo con bocio. En Estados Unidos, la “sal yodada” previene la ocurrencia de bocio.
Ejemplo 9
Existe cierta evidencia de que el estaño es un elemento esencial en los mamíferos. Con base únicamente en lo que se sabe sobre la química del estaño y su posición en la tabla periódica, predecir una función biológica probable para el estaño.
Dado: elemento y datos en la Tabla 1.6
Preguntado por: probable función biológica
Estrategia:
A partir de la posición del estaño en la tabla periódica, sus estados de oxidación comunes y los datos de la Tabla 1.6, predicen una función biológica probable para el elemento.
Solución:
Por su posición en la parte inferior del grupo 14, sabemos que el estaño es un elemento metálico cuyos estados de oxidación más comunes son +4 y +2. Dados los bajos niveles de estaño en mamíferos (140 mg/70 kg humanos), es poco probable que el estaño funcione como macromineral. Aunque no se puede descartar un papel en la catalización de reacciones de transferencia de grupos o como componente estructural esencial, el papel más probable para el estaño sería catalizar reacciones de oxidación-reducción que involucran transferencias de dos electrones. Esto aprovecharía la capacidad del estaño para tener dos estados de oxidación separados por dos electrones.
Ejercicio
Con base únicamente en lo que se sabe sobre la química del vanadio y su posición en la tabla periódica, predecir una probable función biológica para el vanadio.
Respuesta: El vanadio probablemente cataliza las reacciones de oxidación-reducción porque es un metal de transición de primera fila y es probable que tenga múltiples estados de oxidación.
Resumen
Muchos de los elementos de la tabla periódica son oligoelementos esenciales que se requieren para el crecimiento de la mayoría de los organismos. Aunque solo están presentes en pequeñas cantidades, tienen importantes efectos biológicos por su participación en un mecanismo de amplificación. Los macrominerales están presentes en mayores cantidades y desempeñan papeles estructurales o actúan como electrolitos cuya distribución en las células está estrechamente controlada. Estos iones son transportados selectivamente a través de las membranas celulares mediante bombas de iones. Otros oligoelementos catalizan reacciones de transferencia de grupos o reacciones biológicas de oxidación-reducción, mientras que otros son componentes estructurales esenciales de moléculas biológicas.
Llave para llevar
- Los oligoelementos esenciales en mamíferos tienen cuatro funciones generales: como macrominerales, como catalizadores en reacciones de transferencia de grupos o reacciones redox, o como componentes estructurales.
Problemas conceptuales
-
Dar al menos un criterio para los elementos esenciales involucrados en reacciones biológicas de oxidación-reducción. ¿Qué región de la tabla periódica contiene elementos que son muy adecuados para este rol? Explica tu razonamiento.
-
¿Cuáles son las funciones biológicas generales de los oligoelementos que no tienen dos o más estados de oxidación accesibles?


