6.1: Preludio a Metales y Aleaciones
- Page ID
- 71976
En la química de los compuestos moleculares, estamos acostumbrados a la idea de que las propiedades dependen fuertemente de la estructura. Por ejemplo podemos racionalizar la polaridad de la molécula de agua en función de su forma. También sabemos que dos moléculas con la misma composición (por ejemplo, etanol y éter dimetílico) tienen propiedades muy diferentes basadas en las disposiciones de unión de los átomos. No debería sorprender que las propiedades de los sólidos extendidos también estén conectadas a sus estructuras, y así para entender lo que hacen debemos comenzar por sus estructuras cristalinas. La mayoría de los metales de la tabla periódica tienen estructuras relativamente simples y por lo que este es un buen lugar para comenzar. Veremos en el Capítulo 8 que las estructuras de compuestos más complejos también están en muchos casos relacionadas con las estructuras simples de metales y aleaciones.
|
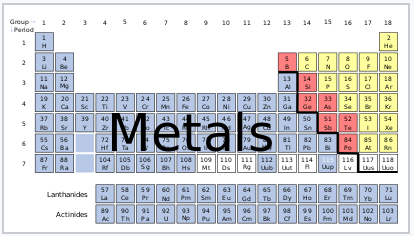
Más de 2/3 de los elementos de la tabla periódica existen en su forma pura como metales. Todos los metales elementales (excepto los tres - Cs, Ga, Hg - que son líquidos) son sólidos cristalinos a temperatura ambiente, y la mayoría tienen una de tres estructuras cristalinas simples. |