12.2.1: Introducción a las reacciones de sustitución
- Page ID
- 81478
La sustitución de ligando se refiere a la sustitución de un ligando en un complejo de coordinación con otro ligando.
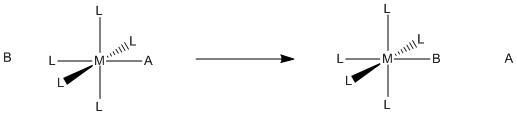
Recuerde, un ligando en la química de coordinación es solo una base de Lewis que se une a un átomo o ion metálico. Lo hace donando un par solitario (u otro par de electrones). En general, esta donación es reversible. El donante siempre puede recuperar sus electrones. Por lo general, puede haber cierto equilibrio entre la necesidad del metal de más electrones y la atracción del donante por sus propios electrones; los átomos donantes suelen ser más electronegativos que el metal.
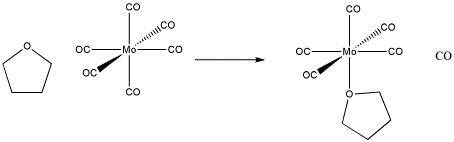
A pesar de que la reacción es bastante simple, puede ocurrir de diferentes maneras.
Es decir, los pasos elementales involucrados en la reacción pueden ocurrir en diferentes órdenes. Las reacciones elementales son los eventos individuales de creación de vínculos o ruptura de vínculos que conducen a un cambio general. A veces el orden de los pasos se conoce como el mecanismo o la vía mecanicista.
- El mecanismo es el orden de los pasos elementales de reacción.
- Las etapas elementales de reacción son etapas individuales de formación de uniones y rotura.
Es posible que hayas visto mecanismos de reacción antes. Por ejemplo, la química de adición de carbonilo puede implicar mecanismos largos, en los que deben ocurrir varias transferencias de protones y otras etapas de formación de enlaces y ruptura de enlaces para pasar de un estado a otro. Debido a que la sustitución de ligandos es más sencilla que eso, es un buen lugar para estudiar el mecanismo con un poco más de profundidad, sin agobiarse por los detalles.
La secuencia de pasos en el mecanismo influye en cómo los diferentes factores impactarán la reacción. Por ejemplo, cambiar las concentraciones de diferentes componentes en una mezcla de reacción puede afectar el tiempo que tarda una reacción en terminar.
- El mecanismo puede tener un impacto dramático en el resultado de la reacción bajo diferentes circunstancias.
Este tipo de consideraciones tienen un impacto dramático en procesos industriales como la producción farmacéutica. En ese entorno, los ingenieros químicos necesitan tomar decisiones sobre cuánto de cada reactivo debe ser admitido en una mezcla de reacción y cuánto tiempo se les debe permitir que reaccionen juntos. Si permiten que la reacción continúe durante demasiado tiempo, puede haber “reacciones secundarias” que comiencen a ocurrir, interfiriendo con la calidad del producto, y perderán un tiempo valioso en la tubería de producción. Si no permiten que reaccione el tiempo suficiente, es posible que la reacción no termine y el producto se contaminará con materiales de partida sobrantes.
En este capítulo, veremos cómo esta simple reacción puede ocurrir de diferentes maneras. Veremos algunos métodos diferentes que se utilizan para decir de qué manera ocurre la reacción (es decir, evidencia de lo que realmente está sucediendo). También veremos algunos factores diferentes que pueden influir en si la reacción es probable que ocurra de una manera u otra (es decir, razones por las que está sucediendo de esa manera, o razones que esperamos que suceda de esa manera).
Algún tipo de sustitución ocurre en cada una de las siguientes reacciones: un átomo o grupo reemplaza a otro. En cada caso, identificar lo que se está reemplazando, y qué lo reemplaza.
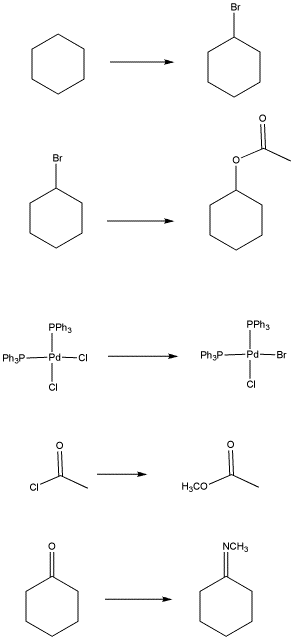
Contestar a-
un átomo de bromo reemplaza a un átomo de hidrógeno
- Respuesta b
-
un grupo acetato (éster etanoílico) reemplaza un átomo de bromo
- Respuesta c
-
un átomo de bromo reemplaza a un átomo de cloro (o iones)
- Respuesta d
-
un grupo metoxi reemplaza a un átomo de cloro
- Respuesta e
-
un grupo metilamino reemplaza un átomo de oxígeno


