14.3.1: Deuteración catalítica
- Page ID
- 81682
Deuteración catalítica de benceno
Las combinaciones de adiciones oxidativas y eliminaciones reductoras tienen muchas aplicaciones en la síntesis de moléculas orgánicas usando un reactivo organometálico.
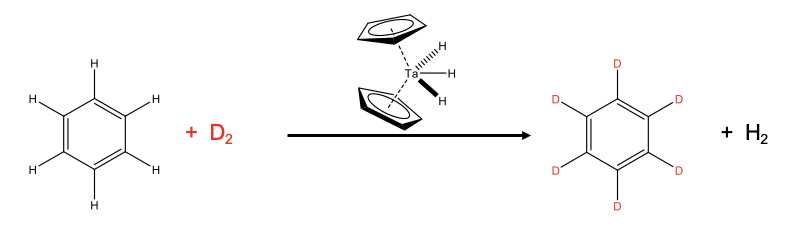
Un ejemplo es la deuteración del benceno (Fig. \(\PageIndex{1}\)). El benceno deuterado es un disolvente importante en la espectroscopía de RMN. Industrialmente, la deuteración se realiza utilizando un catalizador de diciclopentadieniltrihidridotantalio (V) partiendo de benceno y D 2. El D 2 se proporciona en exceso para conducir el equilibrio químico hacia el lado derecho.
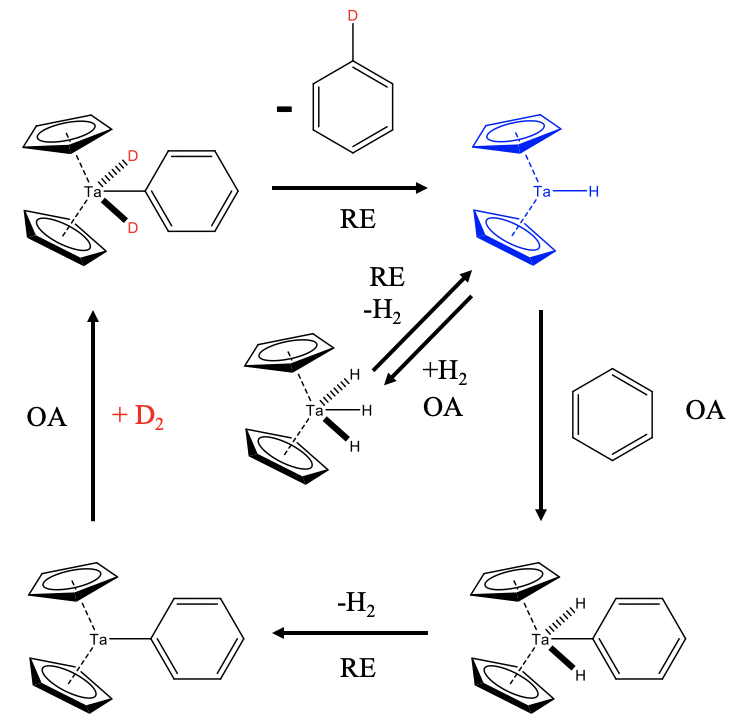
¿Cómo funciona esta reacción mecanísticamente? Este 18e Cp 2 Tah 3 es en realidad un precatalizador que está en equilibrio químico con H 2 y el 16e diciclopentadienilhidrido tántalo (III) que es el catalizador real (Fig. \(\PageIndex{2}\)). La eliminación de H 2 del catalizador de Ta (V) es una eliminación reductiva (RE) y la readición de H 2 a la especie Ta (III) una adición oxidativa (OA). En presencia de benceno, la especie Ta (III) puede agregar oxidativamente benceno para formar un complejo 18e Ta (V). Este complejo puede eliminar reductivamente H 2 para formar un complejo 16e Cp 2 Ta (III) -Ph. En presencia de deuterio este complejo puede agregar D 2 oxidativamente para formar un complejo 18e Cp 2 D 2 Ta (V) -Ph. Esta especie puede entonces eliminar reductivamente una molécula de benceno monodeuterada bajo formación de Cp 2 Ta (III) -D. En presencia de suficiente D 2 este benceno monodeuterado puede deuterarse adicionalmente en ciclos catalíticos posteriores.


