Preguntas de revisión de conceptos Capítulo 10
- Page ID
- 70070
Preguntas sobre la revisión del concepto
Sección 1
1. ¿Cuál es la diferencia entre un compuesto organometálico y un compuesto organometálico?
2. ¿Qué es el kakodilóxido?
3. ¿Qué es la sal de Zeise y qué tiene de inusual su estructura y unión?
4. ¿Qué es el proceso Mond?
5. Explicar por qué las propiedades físicas y químicas del ferroceno son inconsistentes con la coordinación monohapto del Fe por ligandos de ciclopentadienilo.
6. Describir cualitativamente cómo los ligandos de ciclopentadienilo se unen al Fe en ferroceno.
7. ¿Explicar por qué el ciclobutadieno no es plano cuadrado en estado libre sino que es plano cuadrado cuando se coordina a metales de transición en la manera 4?
8. Explique brevemente ¿por qué el ciclooctatetraeno produce complejos sándwich (metalocenos) solo con iones metálicos muy grandes?
Sección 2
1. Explique por qué los carbonilos son interesantes e importantes.
2. ¿Qué orbitales moleculares de CO pueden estar involucrados en la unión con metales de transición? Explique por qué estos orbitales pueden estar involucrados.
3. ¿Qué tipos de unión conoces para los carbonilos en los que el CO actúa como donante de 2 electrones?
4. ¿Qué tipos de unión conoces para los carbonilos en los que el CO actúa como donador de 4 y 6 electrones?
5. ¿Qué tipos de unión conoces para los carbonilos en los que el CO actúa como aceptor de electrones? ¿Cuál de estos tipos de unión conduce a una interacción más fuerte? Explique esto.
6. ¿Cuál es el modelo Chatt-Dewar-Ducanson para carbonilos?
7. ¿Qué se entiende por pi-backbonding en carbonilos?
8. ¿Explicar de qué depende la fuerza del backbonding de la pi-backbonding en los carbonilos?
9. ¿Explicar cómo se puede derivar la estructura de los carbonilos más simples?
10. ¿Cómo se puede medir experimentalmente la fuerza del backbonding pi-backbonding en carbonilos?
11. ¿Qué tiene de inusual la estructura del Co 2 (CO) 8? Explique.
12. ¿Qué tiene de inusual la estructura de V (CO) 6? Explique.
13. ¿Por qué no existen los carbonilos más simples del grupo 4 y del grupo 12?
14. ¿Por qué no existen carbonilos altamente cargados positivamente?
15. ¿Por qué no existen carbonilos diméricos altamente cargados negativamente?
Sección 3
1. ¿Qué se entiende por el concepto de isolobalidad?
2. ¿Explicar cómo el concepto de isolobalidad es útil para la predicción de estructuras estables?
3. Explicar cómo se puede explicar la estructura del Co 4 (CO) 12 utilizando el concepto de isolobalidad.
4. Cuál es la diferencia estructural entre Co 4 (CO) 12 e Ir 4 (CO) 12. Explique esta diferencia.
5. La estabilidad de los carbonilos monoméricos más simples disminuye del grupo 6 al grupo 10. Explique.
6. La estabilidad de los carbonilos monoméricos más simples disminuye del periodo 4 al periodo 6. Explique.
7. Explicar por qué los siguientes complejos se consideran complejos eteno y etino, respectivamente.
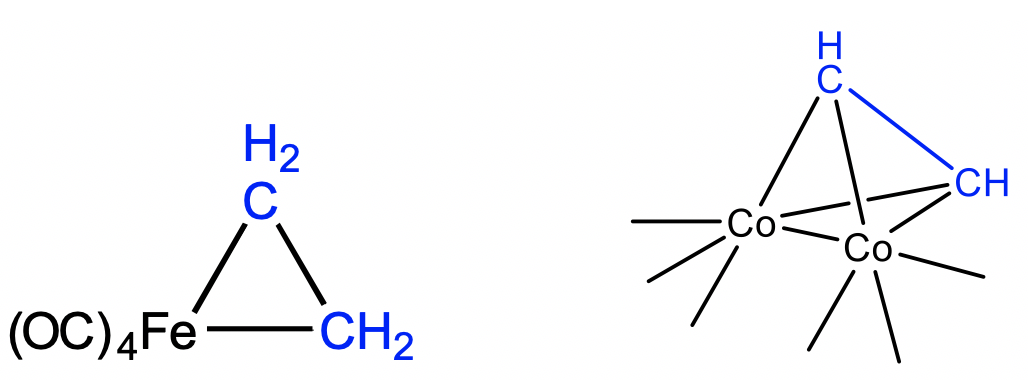
8. ¿Qué es un hidruro de carbonilo?
9. ¿Explicar por qué HCO (CO) 4 es más ácido que HMn (CO) 5?
10. ¿Por qué el ligando CN - es un donante sigma más fuerte y un aceptor de p más débil en comparación con el ligando CO?
11. Explicar por qué el ligando CN tiende a producir cationes complejos, mientras que el ligando CO prefiere hacer aniones complejos.
12. ¿Explicar por qué el átomo de carbono es el extremo reactivo en los complejos de cianuro?
13. ¿Cuáles son los dos modos de unión en los complejos de nitrosil (NO)?
14. ¿Por qué un ligando de NO neutro nunca es un ligando donador de dos electrones?
15. ¿Cómo se pueden explicar los dos modos de unión diferentes en los complejos NO?
16. ¿Por qué la fosfina es un ligando aceptor de pimientras que el amoníaco no lo es
17. ¿Por qué PF 3 es un aceptor pi-más fuerte que PH 3?
18. ¿Por qué PMe 3 es donante sigma más fuerte que PH 3?
19. ¿Por qué H 2 es un ligando aceptor de Pi?
20. Explicar cómo las propiedades aceptoras de pl conducen a la disociación del enlace H-H en la molécula H 2 cuando H 2 actúa como ligando.

